
Диеновый синтез. Реакция Дильса-Альдера
Сопряженные диены реагируют с ненасыщенными соединениями
по схеме:

В реакциях Дильса-Альдера разрываются три -связи и образуются новые связи: одна - и две -связи. Поскольку -связи более стабильны, чем -связи, то эти реакции, как правило, экзотермичны. Однако это не означает, что они обязательно протекают самопроизвольно (спонтанно). Экзотермичность определяется разностью энергий исходных и конечных продуктов, а спонтанность зависит от энергии активации.
Многие из реакций диенового синтеза обратимы, т.е. при высокой температуре аддукт способен распадаться на исходные соединения. Этот процесс называют «ретродиеновый распад».

Реакция между 1,3-бутадиеном и этиленом экзотермична, но температура реакции (600 °С) указывает на то, что энергетический барьер превращения очень высокий.
Для того чтобы диенофил взаимодействовал одновременно с обоими концами диена, диен должен находиться в S-цис-конформации:

Упрощенную схему этого процесса можно себе представить следующим образом. Молекулы диена и диенофила ориентируются так, что оба конца диена одновременно сталкиваются с углеродными атомами диенофила.

Если энергия молекул достаточно велика, т.е. достигается вершина энергетического барьера, начинается электронная перестройка. Это согласованный процесс, в активированном комплексе одновременно завязываются две -связи и одна -связь (они обозначены ' и ') и разрываются три -связи.
Реакция происходит с большой легкостью при наличии электронодонорных групп в диене и электроноакцепторных групп в диенофиле.
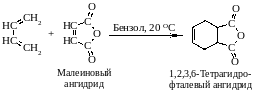
Активность диена возрастает в ряду:
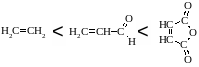
Если для диенового синтеза 1,3-бутадиена с этиленом необходима температура 600 °С, то малеиновый ангидрид мгновенно реагирует с 1,3-бутадиеном при 100 ОC в растворе толуола.
В качестве диенофила можно использовать замещенные алкины.

Реакция Дильса-Альдера стереоспецифична. Конфигурации диена и диенофила сохраняются при образовании аддукта.


Полимеризация
Полимеризация диенов предпочтительно идет по 1,4-положениям через образование наиболее устойчивых частиц.
Механизм:

Натуральный каучук (НК) представляет собой полимер 2-метил-1,3-бутадиена (изопрена). В растениях-каучуконосах он образуется путем биосинтеза. В промышленности полимеризацией изопрена получают аналог натурального каучука - синтетический полиизопреновый каучук (СКИ). Структура НК и СКИ одинакова:

Полимеризация происходит по типу "голова к хвосту". Это обусловлено относительной стабилизацией промежуточных продуктов.
При полимеризации изопрена следует учитывать возможность образования цис- и транс-изомеров. НК и СКИ являются геометрическими цис-изомерами полиизопрена. Цепочки простых С-С-связей, образующих полимерную цепь, расположены по одну сторону от плоскостей -связей.
Гуттаперча - это геометрический транс-изомер полимера изопрена. Полимерные цепочки простых связей С-С находятся по разные стороны от плоскости каждой -связи.

Натуральный каучук при нагревании с серой превращается в эластичный и прочный материал - резину. Этот процесс, называемый вулканизацией, состоит в образовании сульфидных мостиков между различными полимерными цепями.

Аналогично изопрену хлоропрен (2-хлор-1,3-бутадиен) при свободно-радикальной полимеризации дает продукт 1,4-присоединения.

Этот полимер является масло- и бензостойким и устойчив к действию кислорода воздуха.
Большое значение имеют сополимеры диенов с другими мономерами. При сополимеризации 1,3-бутадиена (дивинила) и стирола (винилбензола) C6H5–CH=CH2 получают синтетический каучук дивинилстирольный - СКС. Этот сополимер состоит примерно из трех частей бутадиена и одной части стирола.

Устойчивость сопряженных диенов характеризуются меньшей теплотой гидрирования по сравнению с аналогами они рахактеризуются неотдективностью . Теплоты гидрирования алкенов одинакового строения близки по значениям. Для монозамещенных алкенов с одной алкильной группой при двойной связи эта величина близка к 126 кДж/моль Теплоты гидрирования алкенов и диенов
Соединение |
Теплоты гидрирования, кДж/моль |
CH3–CH=CH2 (Пропен) |
126 |
CH3–CH2–CH2–CH=CH2 (1-Пентен) |
127 |
CH2=CH–CH2–CH=CH2 (1,4-Пентадиен) |
254 |
CH2=CH–CH=CH2 (1,3-Бутадиен) |
239 |
Можно было бы ожидать, что для соединений с большим числом двойных связей теплота гидрирования будет равна сумме теплот гидрирования индивидуальных двойных связей. Для несопряженных диенов эта аддитивность соблюдается, теплота гидрирования 1,4-пентадиена 254 кДж/моль (127∙2 кДж/моль). Однако теплота гидрирования 1,3-бутадиена и других сопряженных диенов несколько меньше, чем удвоенная теплота гидрирования связи >С=СН2.
-
Еп,
кДж
моль

Рис. 6.1. Влияние сопряжения на теплоту гидрирования
При гидрировании сопряженного диена экспериментальная теплота гидрирования на 15 кДж/моль меньше, чем рассчитанная по аддитивной схеме. Это означает, что сопряженный диен устойчивее, чем можно было ожидать, исходя из предположения о независимости двойных связей. Выигрыш энергии называется энергией сопряжения (рис. 6.1).
В чем причина такой устойчивости? Сравним длины простых углерод-углеродных связей, образованных атомами углерода в различных гибридных состояниях (табл. 6.2).
Таблица 6.2
Гибридизация атомов углерода и длины простых углерод-углеродных связей
Соединение |
Связь С–С |
Гибридизация |
Длина связи, нм |
CH3–C2H2–C3H2–CH3 |
C2–C3 |
sp3– sp3 |
15,410-2 |
CH3= C2H–C3H–CH3 |
C2–C3 |
sp2– sp3 |
15,210-2 |
CH2= C2H–C3H=CH2 |
C2–C3 |
sp2– sp2 |
14,810-2 |
Поскольку sp2-орбитали расположены ближе к ядру, чем sp3-орбитали, длина углерод-углеродной связи должна изменяться в следующем порядке: Сsp2–Сsp2 < Сsp3–Сsp2 < Сsp3–Сsp3, что и наблюдается в действительности. Чем короче связь, тем больше ее энергия, т.е. уменьшение длины связи увеличивает устойчивость молекулы.
Вероятно, стабильность сопряженного диена в некоторой степени связана со взаимодействием -электронных облаков соседних -связей, дополнительное электронное взаимодействие уменьшает энергию диена. Возникающая делокализация -электронов делает молекулу более стабильной. На рис. 6.2 показано перекрывание р-орбиталей атомов С2 и С3.

