
- •Билет 1
- •Технический элементарный кремний: методы получения, основные свойства и применение. Получение и применение монокристаллов кремния высокой чистоты.
- •Билет 2
- •Кремнегалогены: классификация кремнегалогенов, методы синтеза простых и комплексных кремнегалогенов, их свойства и применение.
- •Билет 3
- •Билет 4
- •Соединения в системах кремний – азот и кремний – бор: состав, методы синтеза, свойства и применение.
- •Билет 5
- •Билет 6
- •Билет 7
- •Билет 8
- •Билет 9
- •Билет 10
- •Билет 11
- •Билет 12
- •Термодинамическая характеристика твердофазовых реакций: изменение энергии Гиббса и условия, при которых в процессе твердофазовой реакции возможно установление термодинамического равновесия.
- •Билет 13
- •2. Правило фаз Гиббса. Вид уравнения правила фаз для тугоплавких силикатных систем. Понятия: фаза, независимый компонент, степени свободы, вариантность системы, равновесное состояние.
- •Билет 14
- •Билет 15
- •Билет №18
- •Билет №19
- •Вопрос№2
- •Билет № 21
- •Последовательность химических превращений при твердофазовом взаимодействии
- •Билет №22
- •Спекание за счёт процесса испарение- конденсация.
- •Cпекание за счет пластической деформации под давлением/
- •Реакционное спекание
- •Правила определения характера этих точек, процессов, происходящих в них, и дальнейшего пути кристаллизации из точки двойного опускания.
- •Определение характера процесса, происходящего в точке двойного подъема:
- •Определение дальнейшего пути кристаллизации из точки двойного опускания.
- •Билет №23
- •Главный внутр. Фактор – характер и энергия кристалл. Решетки: с увеличением энергии решетки Тпл возрастает у однотипных в-в.
- •Билет №27
- •Диаграмма состояния по Бредигу. Схема превращений.
Билет 1
Технический элементарный кремний: методы получения, основные свойства и применение. Получение и применение монокристаллов кремния высокой чистоты.
Элементарный кремний в природе в чистом виде не встречается. Получение:
- впервые был получен восстановлением фторида кремния металлическим калием
- восстановление галогенидов или кварца SiO2 магнием: SiO2 + 2Mg = Si + 2MgO; Сухие тщательно смешанные SiO2 и Mg нагревают в фарфоровом тигле до красного каления. Кремний загрязнен оксидом магния. Его выделяют обработкой массы соляной и плавиковой кислотами. Получается коричневый порошок – «аморфным кремнием», хотя по структуре он не отличается от кристаллического;
- получение аморфного кремния: термическое разложение монохлорида хремния [SiCl4]x
- получение технически чистого кремния – восстановление (в электрических печах при 1900º) кварца либо углеродом в присутствии железа: SiO2 + 2C = Si + 2CO, Получается сплав железа с кремнием. Продукт, называемый в технике чистым кремнием, обычно содержит 3-5% Fe; либо карборундом: SiO2 + 2SiC = 3Si + 2CO
- алюмотермическое восстановление кремнефтористого калия: 3K2SiF6 + 4Al = 3Si + 2KAlF4 + 2K2AlF5. Получается относительно чистый кремний в виде пластинчатых кристаллов.
- получение монокристаллов особо высокой чистоты. Получают из летучих соединений, например, SiCl4. Его тщательно очищают многократной дистилляцией. Пары восстанавливают водородом в кварцевом реакторе при высокой температуре. Выпадают сростки кристаллов – друзы. Их извлекают, плавят, в расплав опускают затравку (стержень, вырезанный из монокристалла кремния). Медленно, с вращением, вытягивая затравку из расплава, получают монокристаллы в виде стержней.
Основные свойства элементарного кремния:
• атом кремния имеет конфигурацию: 1s22s22p63s23p2 – основная валентность 4. Может быть двухвалентным, но соединения неустойчивы (SiO, SiS).
• может проявлять амфотерные свойства, но, в основном, имеет выраженные неметаллические свойства.
• атомы кремния способны образовывать цепи, но они менее устойчивы, в отличие от –С-С-.
Кремний, полученный различными способами, отличается по реакционной способности. Обусловлено размером частиц, величиной удельной поверхности, содержанием примесей.
• Чистый кремний образует темно-серые кристаллы, расслаивающиеся на пластинки октаэдры. Твердость по Моосу 7. Хрупок. Тпл = 1413С. Обладает электропроводностью, возрастающей с температурой.
• Грубо кристаллический кремний при обычных условиях химически не очень активен. Практически не растворим ни в каких кислотах (даже в HF). Мелко кристаллический и аморфный кремний растворим в HF.
• Реагирует со щелочами во всех формах: Si + 2NaOH + H2O = Na2SiO3 + 2H2
• При высоких температурах взаимодействует со многими элементами. При температуре белого каления реагирует с кислородом и азотом; при температуре электрической дуги – с водородом.
• При нагревании сплавляется с большинством металлов, образуя силициды.
• С галогенами – Кремнегалогены.
• Сильный восстановитель.
Применение:
Применяется при производстве электронагревательных стержней (SiC), в качестве восстановителя. Монокристаллы высокой чистоты – в качестве полупроводникового материала .
Диаграмма состояния системы Na2O-CaO-SiO2. Особенности системы, характеристика тройных соединений, существующих в ней, значение системы для химии и технологии силикатов и использование диаграммы для правильного выбора составов технических стекол.
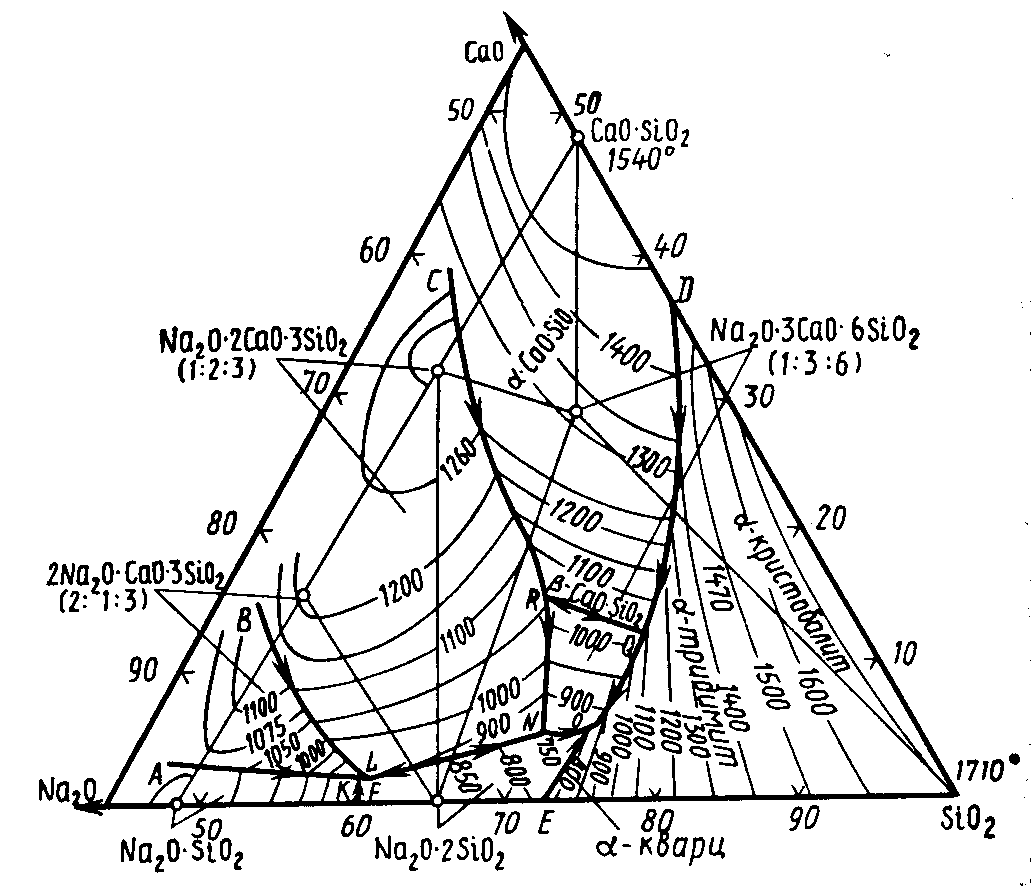
Диаграмма в высокощелочной области ограничена соединением Na2O*SiO2 а в высокоизвестковой – CaO*SiO2. В этой части системы существуют тройные соединения:
Na2O*3CaO*6SiO2 – девитрит. Плавится инконгруэнтно при 1047С, разлагаясь на β-CaO*SiO2 и расплав. В поле девитрита (в верхней части) располагаются составы стекол, наиболее стойких к действию воды и щелочных раствором. Часто выкристаллизовываестся в качестве одной из фаз при расстекловывании.
2Na2O-CaO-3SiO2 плавится инконгруэнтно, разлагаясь при 1140С на кристаллы Na2O*2CaO*3SiO2 и жидкость. Соединение плавится при 1284С без разложения.
Составы системы характеризуются сравнительной легкоплавкостью.
Значение системы для технологии силикатов.
Система включает в себя составы некоторых промышленных стекол, в которых Na2O, CaO и SiO2 – основные компоненты. При кристаллизации этих стекол образуются кристаллические фазы из этой системы (тридимит, кристобалит, волластонит, псевдоволластонит, девитрит). Диаграмма позволяет оценить природу выпадающих фаз, температурные пределы, в которых стекло может закристаллизоваться, скорость кристаллизации, сделать выводы относительно скорости кристаллизации.
Стекла, соответствующие по составу определенным химическим соединения имеют наибольшую скорость кристаллизации.
Составы, образующие при кристаллизации твердую фазу, отличающуюся от состава исходного стекла, будут кристаллизоваться медленнее.
Наиболее трудно при прочих равных условиях кристаллизуются эвтектические составы.
