
2 Методика эксперимента и обработка результатов
2.1 Программа исследований
1. Анализ научно-технической и патентной информации по особенностям нанесения твердых износостойких хромовых покрытий.
2. Выбор составов электролитов.
3. Отработка методик получения хромовых покрытий.
4. Исследование основных параметров нанесения хромовых покрытий и хром – УНМ.
5. Исследование свойств полученных хромовых покрытий.
6. Анализ экспериментальных результатов.
7. Разработка технологической схемы, проведение инженерно-техно-логических расчетов.
8. Оформление расчетно-пояснительной записки и графической части.
2.2 Методика эксперимента
Электрохимические исследования процесса осаждения хромовых покрытий проводились с использованием низкоконцентрированных электролитов хромирования, состав которых приведён в таблице 2.1.
Приготовление электролитов осуществлялось с использованием реактивов марки хч и дистиллированной воды. В химическом стакане на 2/3 рассчитанного объёма заполненного водой, при температуре 30 – 40 °С растворяли хромовый ангидрид. Затем в отдельной емкости в дистиллированной воде растворяли при температуре 30 – 40 °С метиловый фиолетовый. Приготовленные растворы сливались в одну емкость и доводились водой до нужного уровня. После добавления серной кислоты электролит перемешивали и прорабатывали для накопления необходимого количества соединений трёхвалентного хрома. Проработку осуществляли при температуре 40 – 45 °С и катодной плотности тока 25 – 30 А/дм2 в течении 2 – 3 часов.
В процессе электролиза применялись нерастворимые аноды (легированный свинец), контроль активности которых осуществлялся визуально. Темно-коричневый цвет говорил о том, что на поверхности свинца образовался необходимый слой окиси свинца и режим работы анода нормальный. Удаление желтой хроматной пленки с поверхности анодов производилось обработкой в растворе, содержащем NaOH 100 г/л и трилон Б.
Таблица 2.1 – Состав исследуемых электролитов
Электролит |
Компонент |
Содержание, г/л |
1(фон) |
CrO3 H2SO4 |
150 1,5 |
2 |
CrO3 H2SO4 Метиловый фиолетовый (C24 H28 Cl N3) |
150 1,5 1,5 |
3 |
CrO3 H2SO4 Метиловый фиолетовый (C24 H28 Cl N3) Додецилсульфат натрия (C12H25NaO4S) |
150 1,5 1,5 0,2 |
4 |
CrO3 H2SO4 Метиловый фиолетовый (C24 H28 Cl N3) Додецилсульфат натрия (C12H25NaO4S) УНМ |
150 1,5 1,5 0,2 1,0 – 2,5 |
5 |
CrO3 H2SO4 Метиловый фиолетовый (C24 H28 Cl N3) УНМ |
150 1,5 1,5 1,0 - 2,5 |
Проводился контроль пористости, твердости, коррозионной стойкости полученных образцов, а также расчет и сравнение основных характеристик электролитов (рассеивающей способности, распределения по току и по металлу и др.), и подбор оптимальных условий для осаждения хромовых покрытий.
Порядок проведения экспериментов:
- подготовка образцов с рабочей площадью 2 x 2 см2 (материал Ст3, Ст45);
- химическое обезжиривание рабочей поверхности образцов;
- теплая промывка;
- травление рабочей поверхности образцов в растворе соляной кислоты HCl(1:1)
- промывка;
- высушивание;
- сборка экспериментальной установки согласно схеме (рисунки 2.2 и 2.3.).
Все взвешивания образцов производились с помощью аналитических весов модели ВЛР-200г-М.
Для осаждения хромового покрытия использовалась электрохимическая ячейка (рисунок 2.3).В качестве анодов использовался легированный свинец, а в качестве катода листовая сталь марки Ст3 и Ст45. Соотношение площадей катода и анода составляло 1:5.
Методом хроновольтамперомитрии исследован процесс осаждения хрома из низкоконцентрированных электролитов. Все поляризационные измерения проводились с помощью потенциостата марки ПИ-50-1.1(рисунок 2.1). Поляризационные кривые в динамическом режиме получены при скоростях
1
2
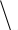
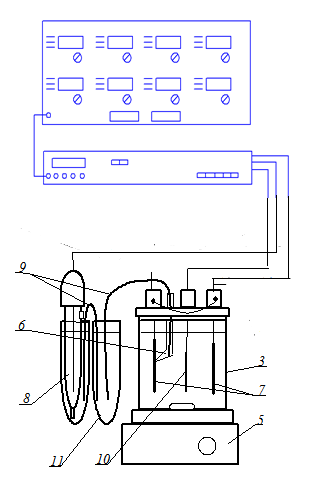
1 – программатор ПР-8; 2 – потенциостат ПИ-50-1.1; 3 – электролизер; 4 – вольтметр; 5 – магнитная мешалка; 6 – капилляр Луггина; 7 – аноды свинцовые; 8 – насыщенный хлорсеребряный электрод ; 9 – солевые мостики; 10 – катод; 11 – промежуточный сосуд.
2.1 – Схема экспериментальной установки для снятия поляризационных кривых.
развертки 50 мВ/с. Потенциалы измерялись относительно насыщенного хлорсеребряного электрода сравнения ЭВЛ-1М3 при температуре опытов. Все
1 – Ячейка Хула; 2 – анод; 3 – разборный катод; 4 – электрод сравнения; 5 – источник тока; 6 – милливольтметр; 7 – вольтметр; 8 – калиброванные сопротивления.
Рисунок 2.2 - Экспериментальная установка для измерения рассеивающей способности

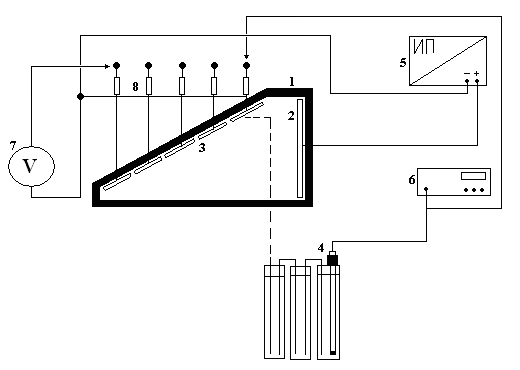
1 – источник питания; 2 – амперметр; 3 – электролизер; 4 – вольтметр; 5 – магнитная мешалка; 6 – капилляр Луггина; 7 – аноды свинцовые; 8 – электрод сравнения; 9 – солевые мостики; 10 – катод; 11 – промежуточный сосуд.
Рисунок 2.3. Схема экспериментальной установки для хромирования
потенциалы в работе, приведены относительно нормальной водородной шкалы.
На основании полученных экспериментальных данных (Ек, ΔUi, Δmi), определялись основные характеристики электролитов и покрытии (ВТi, РСме, РСт).
Расчет электрохимических параметров, рассеивающей способности проводился в соответствии с ГОСТ 9.305-84.
В качестве электродов использовались сталь, противоэлектродом служил легированный свинец. Видимая поверхность электродов 3,0 см2.
Микротвердость покрытия определялась на приборе ПМТ – 3 согласно ГОСТ 9450-76.
Измерение пористости осажденных хромовых покрытий проводилось методом наложения фильтровальной бумаги согласно ГОСТ 9.302 - 88.
Коррозионную стойкость покрытия определяли методом погружения в 3% раствор хлористого натрия (NaCl) с последующим измерением потенциала погружения стального образца с покрытием и без покрытия. На основе изменения потенциала погружения делались выводы о пористости покрытия и его коррозионной стойкости.
В качестве противоэлектродов использовали сталь (Ст-3). Схема установки с внутренней поляризацией приведена на рис. 2.4.
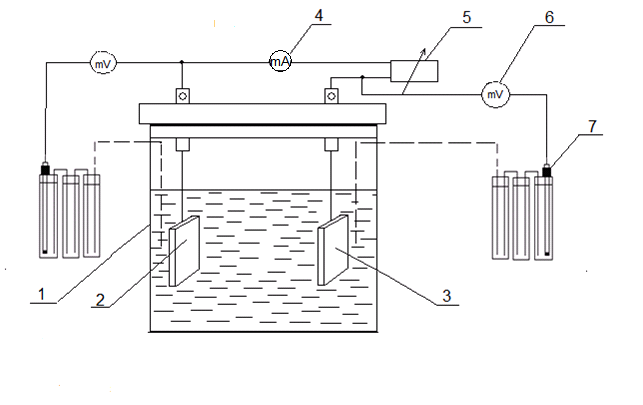
1- электролизёр; 2 - электрод с хромовым покрытием; 3 - противоэлектрод (сталь Ст3); 4 - миллиамперметр; 5 - магазин сопротивлений; 6 - миливольтметр; 7 - электрод сравнения.
Рисунок 2.4. - Экспериментальная установка для коррозионных исследований
