
Учебник Органическая химия Щеголев 2016
.pdf
8.7. СТЕРОИДЫ
Стероиды — важные природные вещества, выполняющие в организме разнообразные функции. В настоящее время известно около 20 000 стероидов. Как уже упоминалось (гл. 6.5.6), стероиды, так же, как и терпены и каротиноиды, относятся к неомыляемым липидам.
В основе стероидов лежит структура, которая имеет тривиальные названия «стеран» и «гонан». Нумерация атомов углерода (принятая в химии стероидов):
|
12 |
17 |
|
|
|
11 |
|
13 |
|
|
1 |
|
|
|
C |
|
D 16 |
||
|
|
|
|
|
|
|
||
2 |
|
10 |
9 |
|
|
14 |
|
|
|
|
|
|
|
15 |
|||
|
A |
|
|
B |
|
8 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
||
3 |
|
|
|
|
|
|
|
|
|
5 |
|
7 |
|
|
|||
|
|
|
|
|
|
|
||
4 6
стеран, гонан, циклопентанопергидрофенантрен
(Циклопентанопергидрофенантрен — название этого углеводорода как производного полициклической ароматической системы фенантрена — гл.
11.4.)
В молекулах стероидов шестичленные кольца имеют преимущественно конформацию кресла, бицикл декалина BC имеет транс-строение, а бицикл декалина AB может иметь как транс-, так и цис-сочленение.
По химической структуре стероиды делятся на несколько групп, наиболее важными из них являются стерины, желчные кислоты, стероидные гормоны и сердечные гликозиды.
Стерины являются производными углеводорода холестана.
|
|
CH3 |
CH2 |
CH2 |
|
|
CH3 |
|
|
CH |
|
|
|||
|
|
|
|
|
|
||
|
CH3 |
|
CH2 |
|
CH |
CH3 |
|
|
|
|
|||||
|
|
|
|
|
|
|
|
CH3
холестан
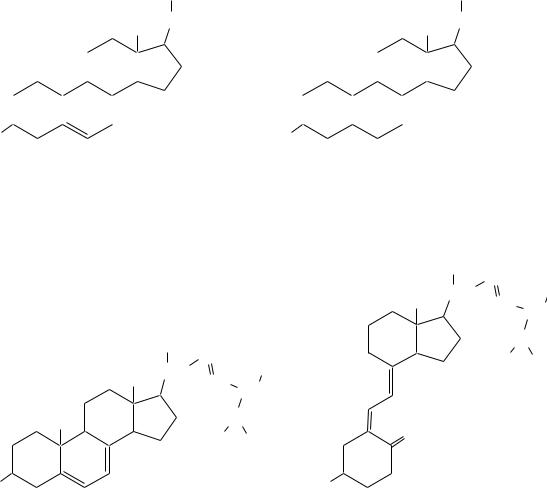
Примерами могут служить холестерин, холестанол, копростанол, эргостерин и витамин D2.
421
|
|
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
CH3 |
|
CH3 |
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
CH-(CH2)3- |
CH |
|
|
|
|
CH-(CH2)3- |
CH |
|||
|
|
|
|
|
CH3 |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
CH3 |
|
|
|
|
CH3 |
|
CH3 |
|
|
|
CH3 |
||
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
HO |
|
|
|
|
|
|
|
||||||
|
холестерин |
|
|
холестанол и копростанол |
|
|
|||||||||
Холестанол и копростанол отличаются друг от друга пространственным расположением циклов A и B: в холестаноле они находятся в транс- конфигурации, а в копростаноле — в цис-конфигурации.
|
|
|
|
|
|
CH3 |
CH |
|
|
|
|
|
|
|
|
CH |
|
CH3 |
|
|
|
|
|
|
CH3 |
|
|
||
|
|
|
|
|
|
CH CH |
|||
|
|
|
|
|
|
|
|
||
|
CH3 |
|
|
|
|
|
CH |
|
|
|
CH |
|
|
|
H3C CH3 |
||||
|
CH3 CH |
|
CH3 |
|
|
||||
|
|
|
|
|
|||||
|
|
CH CH |
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
CH3 |
|
|
CH |
|
CH2 |
|
|
|
|
|
|
H3C CH3 |
|
|
|
|
|||
|
|
|
|
|
|
|
|||
HO |
|
|
|
|
HO |
|
|
|
|
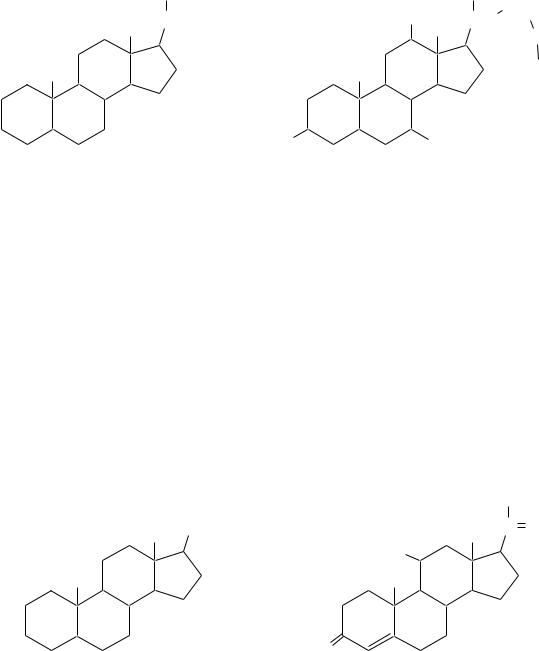
эргостерин |
|
|
|
|
витамин D2 |
|
|
|
|
Холестерин — наиболее распространѐнный представитель стеринов. Он присутствует почти во всех органах животных, особенно в мозге и нервных тканях. Он представляет собой белое кристаллическое вещество с температурой плавления 150 С. Нарушение обмена холестерина приводит к его отложению на стенках артерий и, как следствие, к атеросклерозу. Кроме того, желчные камни обычно содержат в качестве основной составной части холестерин.
Холестанол содержится во многих животных клетках.
Копростанол, или копростерин, образуется из холестерина в кишечнике при действии бактерий и поэтому содержится в фекалиях.
Эргостерин относится к растительным стеринам (фитостеринам). Он встречается в бактериях (особенно много в дрожжевых клетках) и при облучении ультрафиолетом может быть превращѐн в витамин D2 (эргокальциферол).
Витамины группы D — это антирахитические витамины. Кроме витамина D2 существуют близкие по структуре витамины D3 (холекальциферол) и D4. Витамины D содержатся в яичном желтке, сливочном масле, печени жи-
422
вотных, рыбьем жире. Кроме того, провитамин холекальциферола, дегидрохолестерин, содержится в коже человека.
Основная функция витамина D — поддержание в организме постоянной концентрации Са2+ и фосфора, что осуществляется благодаря участию витамина в регуляции всасывания этих элементов в кишечнике.
Желчные кислоты являются производными углеводорода холана. Наиболее распространѐнной из желчных кислот является холевая кислота.
CH3 |
|
CH3 |
CH2 |
CH-CH2CH2CH3 |
OH |
CH |
|
CH3 |
|
||
CH3 |
|
CH2 |
|
|
|
|
|
CH3 |
CH3 |
|
COOH |
HO |
OH |
|
|
холан |
холевая кислота |
|
|
Желчные кислоты образуются в результате расщепления и последующего окисления стеринов в печени. Натриевые и калиевые соли желчных кислот обладают поверхностно-активными свойствами. Они эмульгируют жиры, поступающие с пищей в организм, и тем самым улучшают их усвоение.
Стероидные гормоны. Гормоны — это вещества, образующиеся в железах внутренней секреции и принимающие участие в регулировании обмена веществ и физиологических функций организма. В одних случаях они повышают каталитическую активность ферментов, в других — ускоряют их биосинтез.
Стероидные гормоны могут быть представлены несколькими подгруп-
пами.
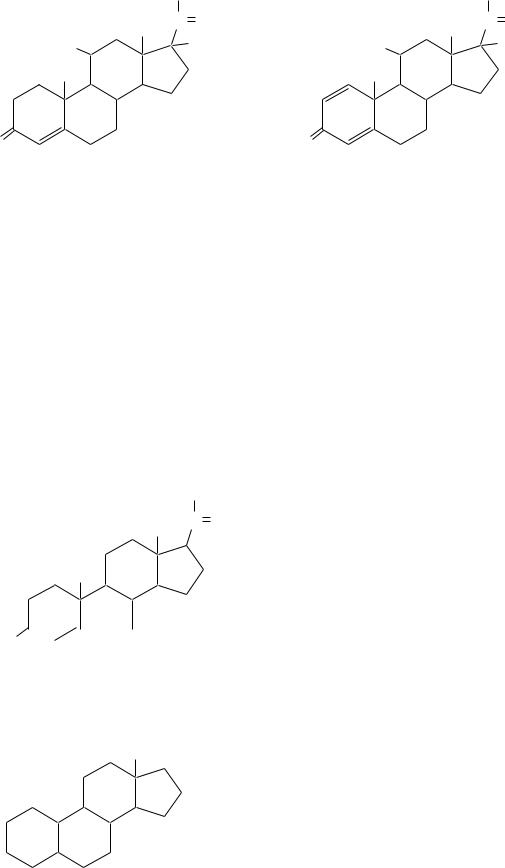
Кортикостероиды — производные углеводорода прегнана. Представителями кортикостероидов являются кортикостерон, гидрокортизон, пред-
низолон.
|
CH2OH |
CH2CH3 |
C O |
CH3 |
CH3 |
|
HO |
CH3 |
CH3 |
|
O |
прегнан |
кортикостерон |
423
|
|
CH2OH |
|
|
CH2OH |
|
CH |
3 |
C O |
CH |
3 |
C O |
|
HO |
OH |
HO |
OH |
|||
|
|
|||||
CH3 |
|
|
CH3 |
|
|
|
O |
|
|
O |
|
|
|
гидрокортизон |
|
|
преднизолон |
|
|
Кортикостероиды образуются в корковом веществе надпочечников и принимают участие в регулировании водного и солевого обмена.
Кортикостерон является антагонистом инсулина и повышает концентрацию глюкозы в крови.
Гидрокортизон способствует накоплению гликогена в печени и также регулирует поступление глюкозы в кровь.
Преднизолон — это синтетический кортикостероид; он обладает бόльшей активностью, чем его природные аналоги. Используется для лечения ревматизма, бронхиальной астмы, воспалительных процессов кожи.
Женские половые гормоны: гестагены и эстрогены. Гестагены, так же,
как и кортикостероиды, являются производными прегнана. Гестагены — это гормоны беременности; они образуются в жѐлтом теле (Corpus luteum) яичников. Наиболее активным гестагеном является прогестерон.
CH3
CH3 C O
CH3
O 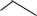
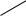
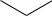
прогестерон
Эстрогены — это производные углеводорода эстрана.
CH3
эстран
424
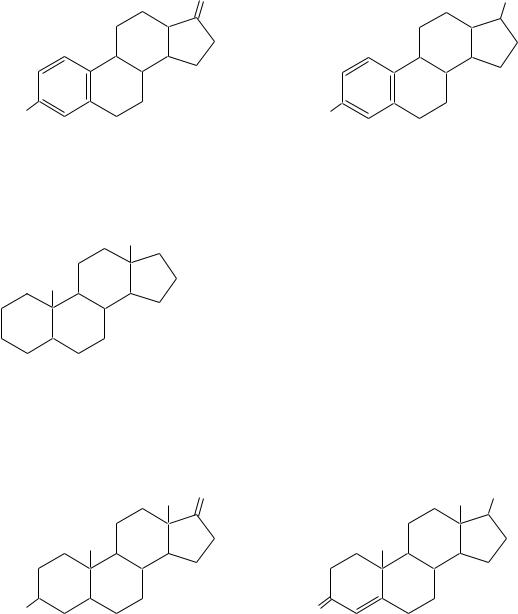
Эстрогены контролируют менструальный цикл у женщин. Наиболее важными эстрогенами являются эстрон и эстрадиол.
CH O |
CH OH |
|||
|
3 |
|
|
3 |
|
|
|||
|
|
|
|
|
|
|
|
|
|
HO |
HO |
эстрон |
эстрадиол |
Мужские половые гормоны (андрогены) — это производные углеводо-
рода андростана.
CH3
CH3
андростан
Они стимулируют развитие вторичных мужских половых признаков и выработку спермы. Важнейшими среди них являются андростерон и тесто-
стерон.
CH |
O |
CH |
OH |
|
3 |
|
3 |
CH3 |
|
CH3 |
|
HO |
|
O |
|
андростерон |
|
тестостерон |
|
Сердечные гликозиды имеют в своѐм составе структурные элементы стероидов и углеводов. Стероидная составляющая, так называемый генин, представляет собой различные производные стерана, в 17-м положении которого имеется ненасыщенное лактонное кольцо (фрагмент - или - лактона). Примерами таких генинов являются дигитоксигенин и сцилларе-
нин.
425
O
|
|
O |
|
O |
|
|
CH2 C O |
|
|
CH |
|
C CH |
CH |
3 |
|
3 |
|
||
CH3 |
|
|
CH3 |
|
OH |
|
OH |
||
HO |
|
|
HO |
|
дигитоксигенин |
сцилларенин |
|
||
Сердечные гликозиды в небольших количествах возбуждают сердечную деятельность и используются в кардиологии. В больших количествах они являются сердечными ядами. Например, гликозид дигитоксин был выделен из листьев наперстянки (дигиталиса, Digitalis purpurea), его стероидная составляющая дигитоксигенин. Сцилларен — один из гликозидов белого морского лука (Scilla maritime L.), обладающих высокой кардиотонической активностью; стероидная часть молекулы сцилларена — сцилларенин.
ВОПРОСЫ И УПРАЖНЕНИЯ
1. Приведите наиболее стабильные конформации соединений: а) цис-1,2- диметилциклогексан, б) транс-1,2-диметилциклогексан, в) транс-1,3-диметилциклогексан, г) транс-1,4-диметилцикло-гексан.
2.Приведите механизмы реакций взаимодействия метилциклопропана со следующими веществами: а) с водородом на никелевом катализаторе, б) с бромом, в) с бромоводородом.
3.Какие соединения будут реагировать с бромоводородом: а) этилциклопропан, б) метилциклобутан, в) 1-метилциклобутен, г) циклогексан, д) циклопентен? Приведите механизмы возможных реакций.
4.Приведите механизм следующего превращения:
CH3 |
H2SO4 |
CH3 |
+ |
CH3 |
CH2OH |
|
OSO3H |
||
|
|
|
5.Из ацетилацетона, 1,2-дибромэтана и других необходимых реагентов получите 1,1-дициклопропилциклопропан.
6.Из бицикло[2.2.1]гепт-2-ена (норборнен), малонового эфира и других необходимых реагентов получите бицикло[3.2.1]октан-3-карбоновую кислоту.
7.Для гераниола приведите схемы реакций: а) окисления диоксидом
426
|
марганца, б) ацетилирования. |
|
|
|
|
|||
8. |
Для |
лимонена |
приведите |
механизмы |
реакций: |
а) |
бромирования, |
|
|
б) гидробромирования, в) гидратации. |
|
|
|
||||
9. |
Приведите схему превращения: |
а) |
гераниола |
в |
терпингидрат, |
|||
|
б) -пинена в терпингидрат. |
|
|
|
|
|
||
10. |
Для |
камфоры |
приведите |
схемы |
реакций: а) |
|
восстановления, |
|
б) взаимодействия с гидроксиламином.
427
Глава 9. БЕНЗОЛ. АРОМАТИЧНОСТЬ. УГЛЕВОДОРОДЫ РЯДА БЕНЗОЛА
Бензол (С6Н6) является родоначальником всех ароматических соединений. В настоящее время к ароматическим соединениям относят большую группу веществ, обладающих определѐнной общностью строения и свойств, но она не является полностью однородной по структурным признакам. Прежде всего, сюда относят вещества, молекулы которых содержат одно или несколько шестичленных полностью сопряжѐнных циклов (бензольных колец). Эти вещества могут быть представлены углеводородами (которые называют аренами) и их функциональными производными.
Вэтой главе рассмотрены углеводороды, молекулы которых содержат
вкачестве ароматического фрагмента одно бензольное кольцо. Это, прежде всего сам бензол, гомологи бензола, а также углеводороды с кратными связями и другими структурными фрагментами в боковых цепях.
9.1. СТРОЕНИЕ БЕНЗОЛА
Впервые циклическую структурную формулу бензола предложил в 1865 году Фридрих Кекуле. Молекула бензола, по мнению Кекуле, представлена шестичленным циклом с чередующимися двойными и ординарными связями. Таким образом, по Кекуле, бензол представлял собой циклогекс- 1,3,5-триен.
|
|
H |
|||
|
|
|
|
||
|
|
C |
|||
H - C |
|
|
C - H |
||
|
|
|
|
|
или |
H - C |
|
|
C - H |
||
|
|
C |
|||
|
|
|
|
|
|
|
|
H |
|||
Недостаток такого изображения молекулы состоит в том, что она предполагает существование двух различных дизамещѐнных производных бензола (относительно ординарной и двойной связей):
X |
|
X |
X |
и |
X |
|
428 |
|
Но такие изомеры обнаружены не были. Эти формулы представляют изображение структуры одного и того же вещества. Кроме того, структура молекулы с локализованными двойными связями не согласуется и с химическими свойствами бензола. Для бензола характерны реакции, не свойственные алкенам и полиенам. Так, он легко вступает в реакции замещения без нарушения сопряжѐнной системы связей. Однако бензол действительно ненасыщен и имеет циклическую структуру. Это соединение может вступать в реакции присоединения, хотя и требует для этого существенно более жѐстких условий, чем алифатические непредельные соединения (табл. 9.1).
Таблица 9.1
Сравнение реакционной способности бензола и гипотетического циклогексатриена
|
Реагенты |
Циклогексатриен |
Бензол |
1 |
Разбавл. раствор |
Быстро реагирует — |
Не реагирует |
|
KMnO4 на холоду |
обесцвечивание |
|
|
|
||
2 |
Раствор Br2 в CCl4 на |
Быстро реагирует — |
Не реагирует |
|
холоду, в темноте |
обесцвечивание |
|
|
|
||
3 |
Н2 на никелевом ка- |
Быстро восстанавлива- |
Восстанавливается при |
|
тализаторе |
ется при 25 С и 0.14 |
100 С и 10.5 МПа |
|
МПа |
||
|
|
|
|
4 |
Катализаторы поли- |
Полимеризуется |
Не полимеризуется |
|
меризации |
||
|
|
|
Для объяснения возникших противоречий Кекуле предложил гипотезу о быстром перемещении (осцилляции) двойных связей в молекуле бензола. И только позже, с развитием электронных представлений, было установлено, что бензол — это не циклогексатриен, а сопряжѐнная система, представляющая собой равносторонний шестиугольник с выравненными связями.
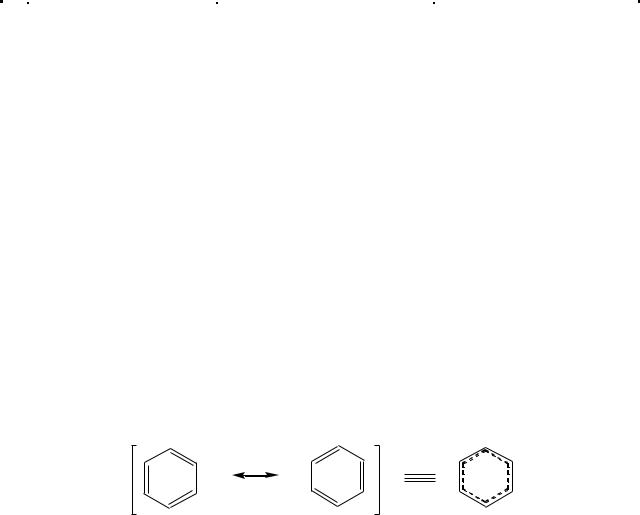
Строение бензола можно представить как промежуточное между двумя структурами Кекуле, имеющими одинаковые длины связей. Такое строение обусловливает устойчивость молекулы и его особые свойства бензола:
Установлено, что молекула бензола планарна, а валентные углы при атоме углерода равны 120 . Каждый атом углерода находится во втором валентном состоянии и образует в плоскости кольца три равноценных -связи за счѐт sp2-гибридных орбиталей. Оставшиеся шесть рz-орбиталей, по одной
429
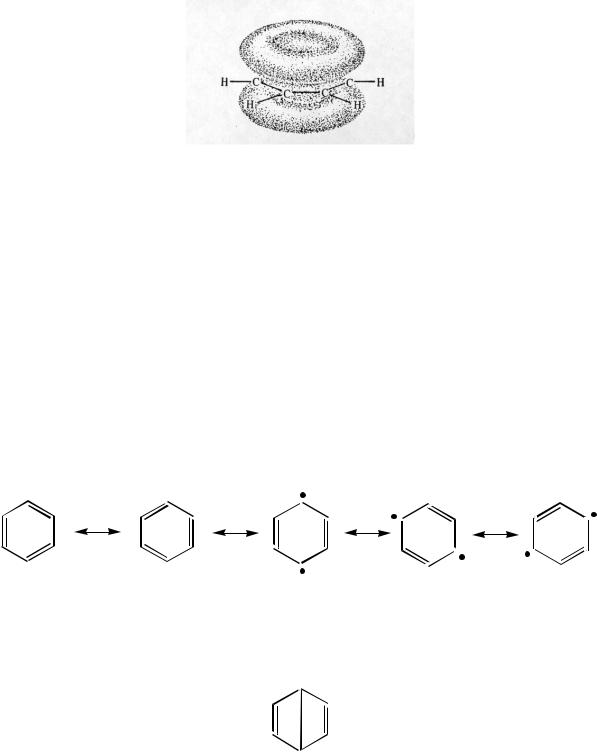
у каждого атома углерода, имеют оси, перпендикулярные плоскости - связей. Каждая рz-орбиталь может одновременно перекрываться с двумя такими же соседними орбиталями так, что образуется замкнутая система шести-электронов.
Роберт Робинсон* связал этот феномен циклической делокализации с ароматической природой бензола и ввѐл термин «ароматический секстет».
Однако бензол и родственные ему соединения являются лишь частным случаем ароматических веществ. В 1930 году Эрих Хюккель* предложил объяснение устойчивости ароматического секстета на основе метода молекулярных орбиталей (правило Хюккеля): плоские моноциклические сопряжѐнные системы с числом -электронов 4n+2 будут ароматическими, тогда как такие же системы с числом -электронов 4n будут неароматическими. При n = 1 число -электронов равно 6 (ароматический секстет).
Для описания -делокализованных систем в органической химии широко привлекают концепцию резонанса (мезомерии), которой отвечает метод валентных связей. Согласно этому подходу истинное строение бензола представляется как промежуточное между пятью граничными структурами: двумя структурами Кекуле (I, II) и тремя структурами Дьюара* (III, IV, V).
I |
II |
III |
IV |
V |
Ранее в структурах Дьюара между двумя противоположными атомами углерода изображали -связь:
430
