
- •Изучение фотодинамического действия света на клеточные структуры
- •1. Введение.
- •2. Краткие сведения из теории.
- •3. Характерные особенности изучаемых в работе фс.
- •4. Выбор длины волны излучения при фдт.
- •5. Экспериментальное моделирование фдэ.
- •6. Экспериментальное оборудование, материалы и расчёты.
- •Выполнение работы.
- •7. Используемое оборудование и материалы.
- •8. Порядок выполнения работы.
- •9. Контрольные вопросы.
- •Математическое описание фдэ.
- •Литература.
Министерство образования Российской Федерации
Московский Государственный технический университет
им. Н.Э. Баумана (МГТУ им. Н.Э. Баумана)
Утверждено Редсоветом
МГТУ им. Н.Э. Баумана
В.П. Жаров, Л.В. Жорина, Г.Н. Змиевской
Изучение фотодинамического действия света на клеточные структуры
Учебное пособие
для выполнения лабораторных работ
по курсу
«Основы взаимодействия физических полей с биообъектами»
Под редакцией И.Н. Спиридонова
Москва 2002 г.
Цель работы: ознакомление с современным методом лечения злокачественных опухолей и других трудноизлечимых заболеваний - методом фотодинамической терапии (ФДТ) на примере наблюдения фотодинамического эффекта (ФДЭ) на взвеси эритроцитов.
1. Введение.
Лазерная фотодинамическая терапия – наиболее современный и наименее травматичный метод лечения онкологических заболеваний.
Суть метода состоит в избирательном воздействии лазерного излучения на патологические клетки, предварительно активированные введением специального вещества – фотосенсибилизатора (ФС). ФС должен обладать рядом специфических свойств, характеризующих его эффективность. Главные из них: селективное накопление в патологических клетках; избирательное и достаточно высокое поглощение излучения на рабочей длине волны лазера; способность с максимальной эффективностью передавать поглощенную энергию внутриклеточному кислороду и тем самым запускать фотохимические реакции, приводящие к гибели патологических клеток при минимальном воздействии на нормальные клетки. В качестве ФС могут выступать естественные (эндогенные) вещества, участвующие в метаболизме клеток (хлорофилл, порфирин). На их основе разработаны лечебные препараты порфиринового ряда, так называемые производные гематопорфирина (ПГП), (ФОТОФРИН в США и Канаде, ФОТОСАН в Германии и Европе, ФОТОГЕМ в России). Исходным веществом для изготовления этих препаратов является кровь. На сегодня в зарубежной практике разрешены к применению только такие препараты. В России, кроме того, разрешен к ограниченному применению синтетический препарат ФОТОСЕНС, представляющий собой металлопорфириновый комплекс с участием цинка или алюминия (относящийся к группе фталоцианинов).
Механизм ФДТ еще не изучен до уровня повседневных методических рекомендаций, поэтому каждый медицинский центр, где применяется ФДТ, является одновременно и научным центром. Идет непрерывный поиск и исследование новых, более эффективных, ФС и постоянное совершенствование технических средств (лазерные источники, средства доставки излучения к объекту, средства дозиметрического контроля процесса и управляющие устройства). Возможности метода не ограничиваются онкологией. Имеются интересные сообщения о применениях ФДТ в кардиологии, микробиологии, дерматологии и ряде других областей.
2. Краткие сведения из теории.
Основным процессом, ответственным за фотодинамический эффект (ФДЭ), можно считать передачу энергии возбуждения от ФС к внутриклеточному кислороду. При поглощении кванта света hν молекула ФС переходит из основного S0 в возбужденное S* состояние (рис.1). Оба эти состояния синглетны, т.е. спины внешних электронов в молекуле ФС антипараллельны, и суммарный спин равен нулю, а спиновое число S = 1 (S = 2s +1, где s – суммарный спин). Переход S0S* вследствие этого наиболее вероятен. Ближайшее к S* возбужденное состояние, расположенное чуть ниже, является триплетным (спины внешних электронов параллельны, s = 1 и S = 2s+1 = 3). Оно не может непосредственно заселяться из основного состояния S0 , поскольку действует правило отбора по спину (переход S0 T* примерно в 104 – 106 раз менее вероятен, чем S0 S*). Но ввиду малой разницы энергий S* и T* состояний возможен переход молекулы ФС из S* в T* состояние за счет спин-орбитального взаимодействия, смешивающего состояния с различной спиновой мультиплетностью. Можно найти ряд ФС, у которых вероятность перехода ик из S* в T* , называемого интеркомбинационной конверсией, близка к единице (ик 0,8). Поскольку из-за тех же правил отбора излучательный переход T* S0 запрещен, время жизни триплетного состояния T* много больше (т* 10-1 10-4 с), чем время жизни синглетного возбуждённого состояния (S* 10-8 10-9 с). Происходит, тем самым, аккумуляция молекул ФС в состоянии T*. Этого не могло бы происходить, если бы отсутствовала интерконверсия, и вся поглощенная энергия высвечивалась бы обратно в виде флуоресценции S* S0 (время жизни состоя ния S* относительно перехода S* S0 + hνфл составляет s* 10-810-9 c). Некоторый, вообще очень слабый, фон флуоресценции всегда присутствует (ик 1) и может быть зарегистрирован достаточно чувствительными приемниками излучения. Поскольку характерной особенностью ФС для ФДТ является преимущественное накопление в опухолевых клетках, повышение интенсивности флуоресценции по сравнению с фоном, характерным для нормальных клеток, является признаком патологии и составляет основу метода люминесцентной диагностики, часто предшествующей ФДТ. Однако легко видеть, что требования к ФС, определяющие его эффективность для терапии и диагностики, противоположны. Для диагностики необходимо, чтобы ик 0, для терапии – наоборот, ик 1. Аккумуляция ФС в Т* состоянии делает возможной эффективную передачу энергии возбуждения другим молекулам с образованием свободных радикалов. В данном случае наиболее вероятна передача энергии возбуждения молекуле кислорода. Основное состояние молекулы кислорода 3О2 является триплетным, тогда как ближайшие возбужденные состояния синглетны (1О2*). Наиболее устойчивым из них является состояние 1g, отстоящее от основного на 0,976 эВ ( = 1,27 мкм). Ввиду различной мультиплетности состояния 1g и основного 3О2 возможна аккумуляция молекул кислорода в состоянии 1g. Характерное время жизни синглетного 1g кислорода (1О2*) в жидкой среде сильно зависит от типа среды и может меняться в пределах 1 10-5 с. При наличии в среде возбужденных молекул ФС в состоянии Т*, энергия которого близка к энергии состояния 1g , весьма вероятно перекрытие электронных оболочек молекул ФС и кислорода с резонансным заселением 1g состояния кислорода. Этот процесс можно схематически изобразить в виде (см. рис. 1):
T*[][] + 3O2[][] S0[][] + 1O2*[][]
т.е. электрон с возбужденной орбитали ФС переходит на возбужденную орбиталь 1g кислорода, а с самой низкой (основной) орбитали кислорода электрон переходит на вакансию в основном состоянии ФС.
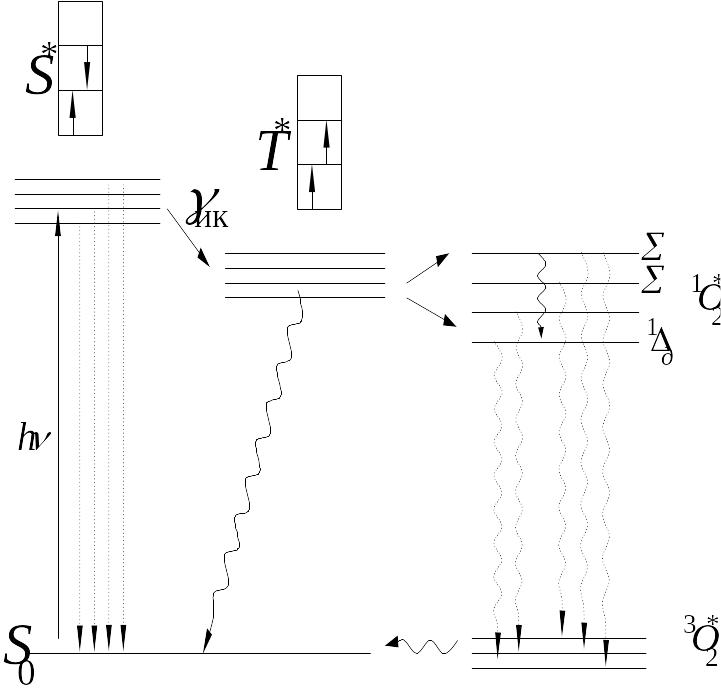
рис.1. Схема передачи энергии возбуждения от ФС к синглетному кислороду.
Синглетный кислород более активен при взаимодействии с внутриклеточными веществами, чем кислород в основном состоянии 3О2. При этом возможен как физический механизм передачи возбуждения, по типу передачи энергии от ФС к самому кислороду без изменения химического состава, так и химический, при котором кислород вступает в реакцию с соответствующим веществом. Поскольку в обоих случаях не происходит радиационных переходов, вещества, принимающие энергию возбуждения от синглетного кислорода, называются тушителями. Вещества-тушители всегда присутствуют в клетках и межклеточной среде, нейтрализуя избыточный синглетный кислород. Преобладание физического механизма тушения означает отсутствие фотодинамического эффекта (ФДЭ). Это имеет место в отсутствие ФС, когда синглетный кислород образуется под влиянием естественных факторов (например, при повышенном солнечном облучении). Для реализации же ФДЭ необходимо включение химического механизма тушения, при котором в реакцию с возбужденным 1О2* вступают ненасыщенные соединения, входящие в состав белков и липидов. Итак, требуемый ФДЭ можно схематически изобразить в виде цепочки реакций:
S0
+ h![]() (1)
(1)
Здесь обозначено:
S0 - невозбужденное (синглетное) состояние ФС;
- эффективное сечение поглощения света молекулой ФС;
I0 - интенсивность падающего излучения [Вт/см2];
S* - возбужденное синглетное состояние ФС;
T* - возбужденное триплетное состояние ФС;
ик – квантовый выход интерконверсии;
3O2 – невозбужденное (триплетное) состояние молекулы кислорода;
1O2* - возбужденное синглетное состояние молекулы кислорода;
RH2 - химический тушитель (субстрат) – внутриклеточное либо входящее в состав мембран или межклеточной среды вещество, активно взаимодействующее с синглетным кислородом и дающее окисленный продукт R , непосредственно воздействующий на метаболизм клетки с летальным для нее исходом.
ФДЭ можно ослабить или усилить в присутствии веществ, либо сильно взаимодействующих с синглетным кислородом и тем самым ослабляющих его реакцию с субстратом (ингибиторы), либо нейтрализующих действие физических тушителей, увеличивающих концентрацию субстрата, влияющих на мембранный транспорт (прооксиданты). Наиболее вероятная схема процессов, приводящих к гибели клетки за счет ФДЭ, приведена на рис. 2.
