
- •Модуль III
- •Номенклатура Обычно ак имеют тривиальное название.
- •Изомерия
- •Классификация
- •Химические свойства
- •I. Кислотно-оснóвные
- •Отношение ак к нагреванию
- •Качественная р-ция на -ак
- •Коричневый Белки
- •Функции белков:
- •Лабораторная работа
- •Тесты для самостоятельной работы студентов Вариант 1.
- •Вариант 2.
- •Вариант 3.
- •Вариант 4.
- •Вариант 5.
Отношение ак к нагреванию
а) a-АК при нагревании могут отщеплять одну или две молекулы воды. При отщеплении одной молекулы воды образуются дипептиды:
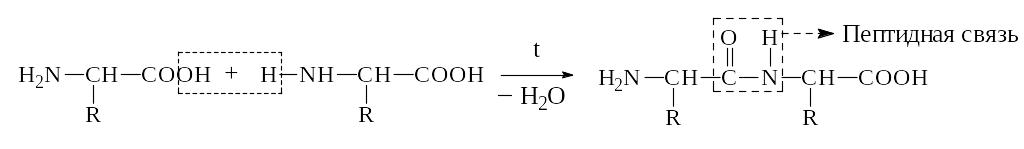
Дипептид обладает способностью взаимодействовать с новой молекулой АК с образованием трипептида, тетрапептида и полипептида. Последний является основой белковых молекул. Название ди– и полипептидов строится по названиям тех к-т, из которых они образуются. Поэтому АК, участвующая в образовании пептида имеет окончание –ИЛ, а концевая АК, сохранившая гр. –СООН – полное название:
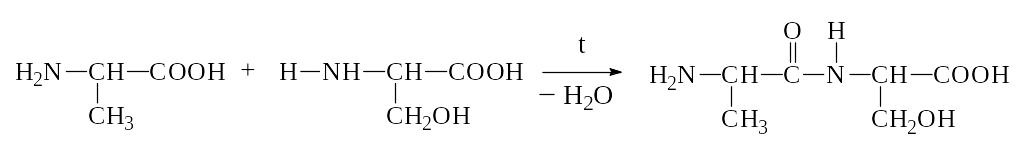
Аланин Серин АланИЛсерин
Используется сокращенная запись полипептида с указанием концевых групп и названий АК первыми тремя буквами русского или латинского алфавита:
Н2N – Ала – Тир – Гли – Глу – СООН
Аla Tyr Gly Glu
При отщеплении двух молекул воды от двух молекул АК образуется дикетопиперазин (циклический амид):

![]()
![]() +
+
![]()
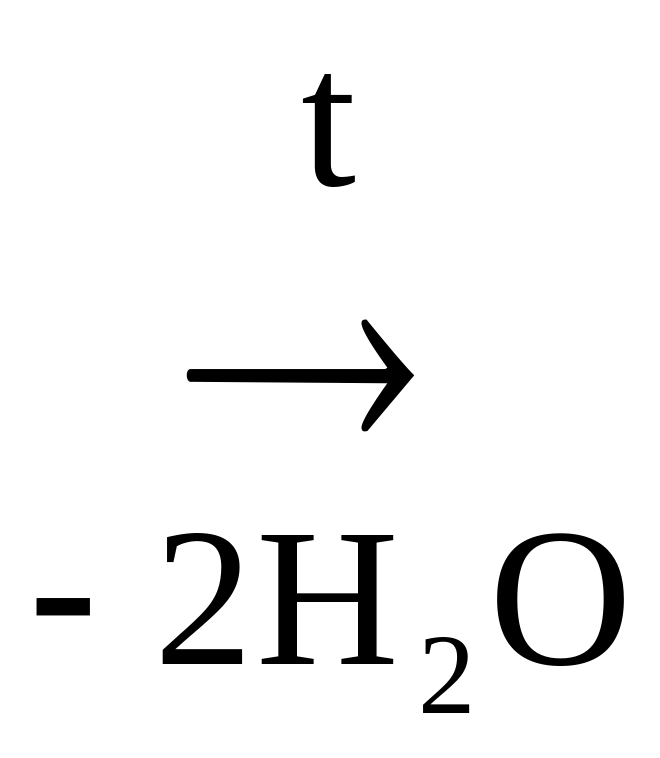
![]()
Глицин Дикетопиперазин
б) -АК выделяют при нагревании NH3 и образуют непредельную к-ту, т.е. идет р-ция дезаминирования:
Кротоновая к-та
СН3–СН=СН–СООН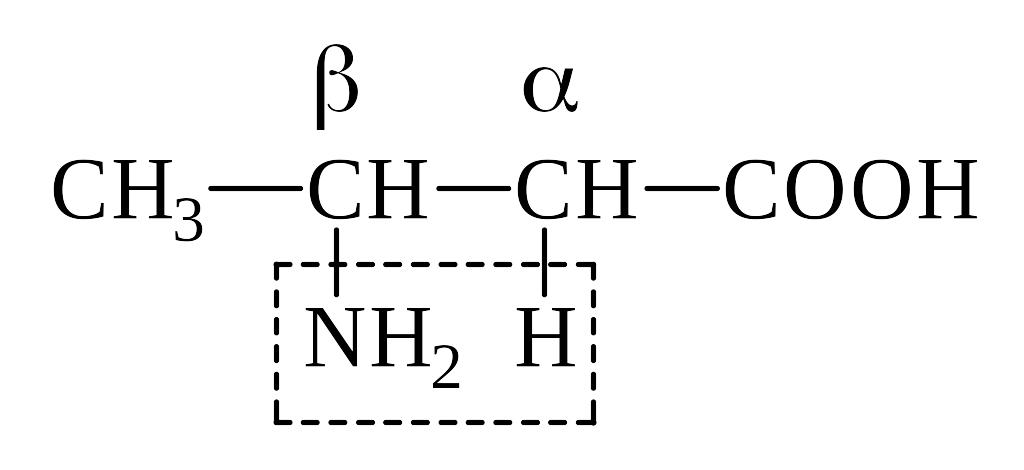
![]()
-Аминомасляная к-та
в) -АК образуют лактамы:
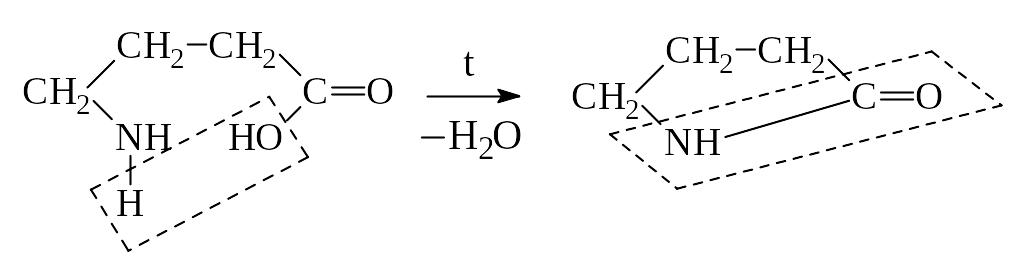
Лактамная
(пептидная) группа
Бутиролактам
-Аминомасляная к-та
Р-ции дезаминирования:
В организме человека и животных под действием различных ферментов происходят процессы дезаминирования. Во всех случаях гр. -NH2 освобождается в виде NH3, а продуктами дезаминирования могут быть жирные к-ты, окси- и кеток-ты. При этом окислительное дезаминирование преобладает:
а) Окислительное дезаминирование
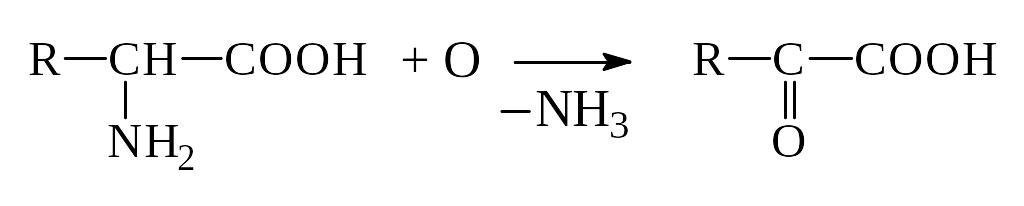
Оксок-та
б) Восстановительное
К-та
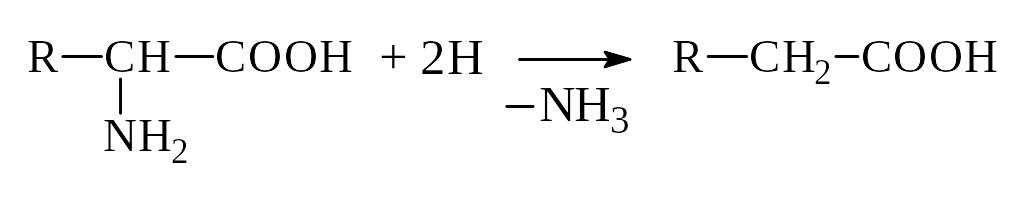
в) Гидролитическое
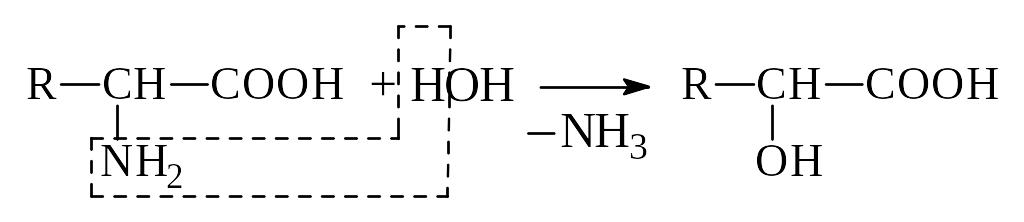
Оксик-та
г) Внутримолекулярное
Непредельная к-та

Р-ции декарбоксилирования
Карбоновые
к-ты in
vitro
декарбоксилируются в очень жестких
условиях. Введение в -положение
ЭА групп -NH2,
![]() ,
–ОН способствует стабилизации карбоаниона
и поэтому такие замещеные к-ты очень
легко декарбоксилируются:
,
–ОН способствует стабилизации карбоаниона
и поэтому такие замещеные к-ты очень
легко декарбоксилируются:
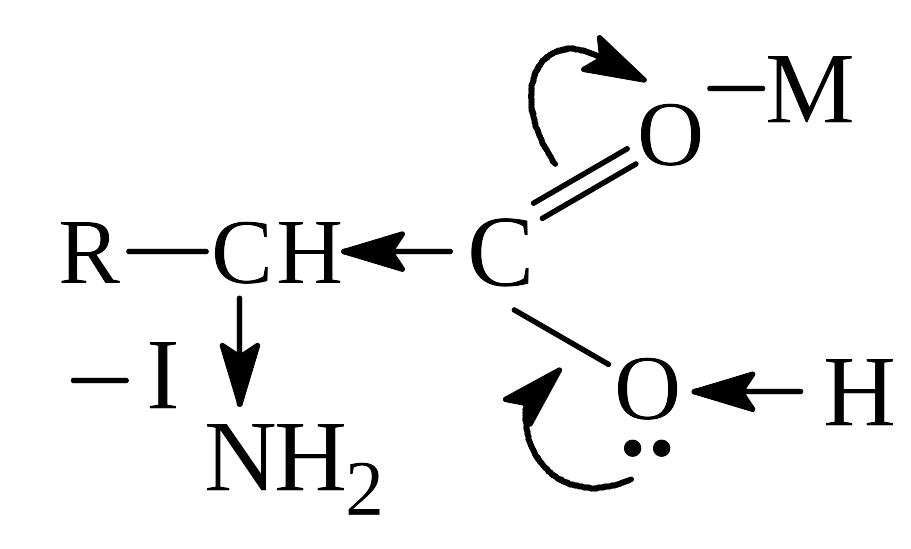
В лабораторных условиях АК легко декарбоксилируются в щелочной среде. В организме -АК декарбоксилируются под действием фермента декарбоксилазы:
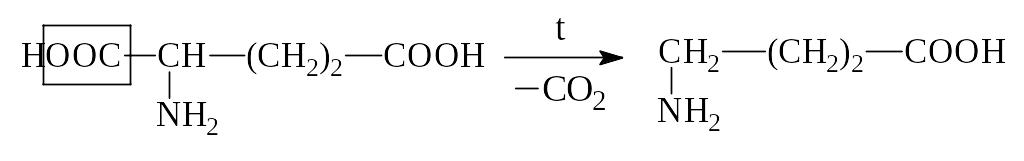
Глутаминовая к-та -Аминомасляная к-та, ГАМК

5-Окситриптофан 5-Окситриптамин,
серотонин

Гистидин, Гистамин,
-амино--[4(5)-имидазолил]- 2-имидозолиламиноэтан,
пропионовая к-та 4(5)-аминоэтилимидазол
Образующиеся амины имеют большое физиологическое значение и наз-ся биогенными аминами. Они участвуют в ряде р-ций обмена нервной и сердечно-сосудистой систем.
К биогенным аминам, образующимся из тирозина в процессе обмена веществ, относится группа катехоламинов: адреналин, норадреналин и дофамин:
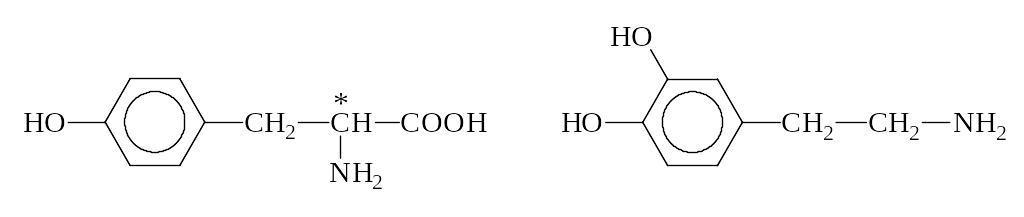
Тирозин Дофамин
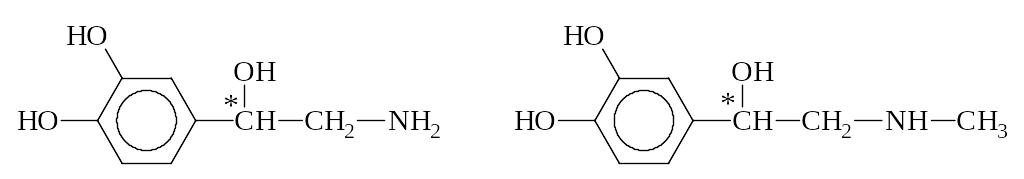
Норадреналин Адреналин
Дофамин, норадреналин и адреналин выполняют роль нейромедиаторов. Из тирозина синтезируются также пигменты кожи, глаз, волос.
Кроме р-ций декарбоксилирования в организме протекают под влиянием ферментов много строго специфических р-ций: переаминирования, трансаминирования и др.
Р-ции по радикалу
Все циклические АК, содержищие бензольное кольцо – триптофан, тирозин, фенилаланин – легко вступают в р-ции замещения по бензольному кольцу с На12, НО–NO2, HO–SO3H.
Путем йодирования тирозина в организме образуется гормон щитовидной железы тироксин:
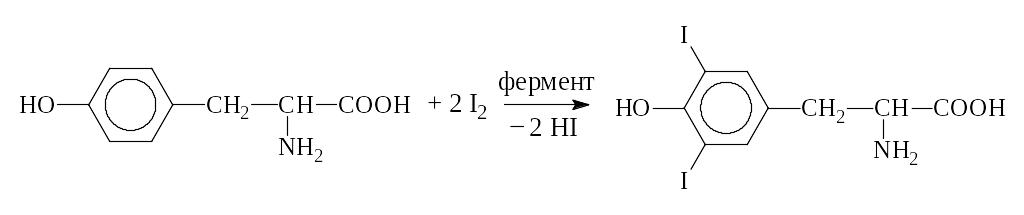
Тирозин Дийодтирозин
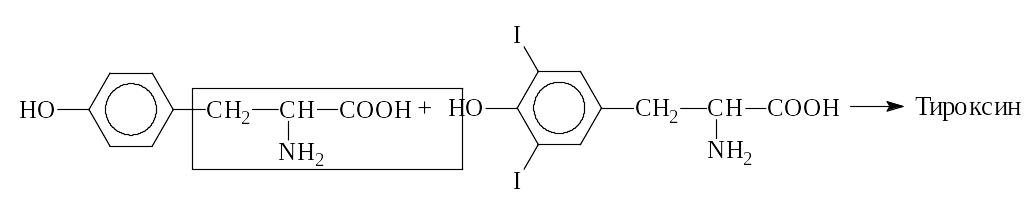
Качественная р-ция на ароматические АК – ксантопротеиновая – обусловлена нитрованием бензольного кольца с образованием нитросоединений желтого цвета. При добавлении к ним щелочи возникает оранжевое окрашивание:

