
- •1. Алкени. Гомологічний ряд алкенів.
- •Електронна будова подвійного зв’язку
- •Ізомерія
- •Одержання
- •Фізичні властивості
- •Хімічні властивості
- •Алкадієни. Реакція полімеризації. Полімери. Одержання, властивості і застосування пластмас.
- •Застосування
- •Дієнові вуглеводні (алкадієни). Типи алкадієнів.
- •Одержання алкадієнів
- •Хімічні властивості алкадієнів
- •Полімеризація дієнових сполук
- •Добування
- •Фізичні властивості алкінів
- •Хімічні властивості
- •I. Реакції приєднання:
- •1) Гідрування:
- •2) Галогенування:
- •Застосування
- •Ароматичні вуглеводні (арени)
- •Будова молекули бензолу (бензену)
- •Гомологи бензолу. Ізомерія. Гомологи бензолу можна розглядати як похідні бензолу, в яких один або декілька атомів вуглецю заміщені різними вуглеводневими радикалами.
- •Фізичні властивості
- •Хімічні властивості
- •І. Реакції заміщення:
- •1) Галогенування
- •Правила орієнтації в бензольному ядрі
Полімеризація дієнових сполук
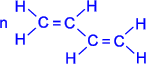
У спрощеному вигляді реакцію полімеризації бутадієну -1,3 по схемі 1,4 приєднання можна представити таким чином:
|
––––► |
|
У полімеризації беруть участь обидва подвійні зв'язки дієну. В процесі реакції вони розриваються, пари електронів, створюючі зв'язки роз'єднуються, після чого кожний неспарений електрон бере участь в утворенні нових зв'язків: електрони другого і третього вуглецевих атомів в результаті узагальнення дають подвійний зв'язок, а електрони крайніх в ланцюзі вуглецевих атомів при узагальненні з електронами відповідних атомів іншої молекули мономера зв'язують мономери в полімерний ланцюжок.
У вільному стані дієнові вуглеводні не існують, але вони входять до складу полімерів природніх канчуків.
Алкіни. Гомологічний ряд алкінів
АЦЕТИЛЕНОВІ ВУГЛЕВОДНІ (АЛКІНИ) – це органічні сполуки, які складаються тільки з вуглецю і водню і містять потрійний (≡)зв'язок. |
Загальна формула алкінів CnH2n-2.
Назви алкінів походять від грецьких та латинських числівників з додаванням суфікса – ін.
Алкіни утворюють гомологічний ряд. Перший член гомологічного ряду алкінів – етин С2Н2 HC≡CH (традиційна назва ацетилен, тому алкінові вуглеводні називають ще ацетиленовими).
Добування
1) піроліз метану (промисловий метод одержання):
2CH4 ––1500°C→ HC≡CH + 3H2
2) з карбіду кальцію при взаємодії з водою:
CaC2 + 2H2O → Ca(OH)2 + HC≡CH Електронна будова потрійного зв’язку
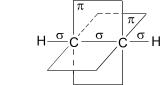
Розглянемо будову ацетилену С2Н2 (НС≡≡СН): у кожного атома вуглецю стають гібридними 2 електронні орбіталі, утворені 1s- і 1p-електронами (sp-гібридизація). Гібридні орбіталі утворюють -зв’язок з атомами водню і між атомами вуглецю. Негібридні орбіталі (два р-електрони) утворюють два π-звязки між атомами вуглецю, вони знаходяться у двох взаємно перпендикулярних площинах:
![]()
Рис. 3 Утворення потрійного зв’язку в ацетилені
Потрійний зв’язок – це ковалентний зв’язок, який складається з одного - і двох π- звязків. Потрійному зв’язку відповідає sp гібридизація. |
Фізичні властивості алкінів
За фізичними властивостями три перші представники гомологічного ряду алкінів за нормальних умов являють собою гази, далі ідуть рідини (С5-С15), а починаючи з вуглеводню С16Н30 алкіни є твердими речовинами. Зміни температур плавлення та кипіння в гомологічному ряді алкінів підпорядковуються основним закономірностям, характерним для алканів і алкенів.
Хімічні властивості
I. Реакції приєднання:
1) Гідрування:
CH3–C≡CH ––t°,Pd;H2•→ CH3–CH=CH2 ––t°,Pd;H2→ CH3–CH2–CH3(пропан)
2) Галогенування:
HC≡CH ––Br2→ CHBr=CHBr ––Br2→ CHBr2–CHBr2 етін 1,2 – диброметен 1,1,2,2- тетраброметан
3) гідрогалогенування: CH3–C≡CH––HBr→CH3–CBr=CH2 ––HBr→ CH3–CBr2–CH3
2-бромпропен-1 2,2-дибромпропан
5) полімеризація (тримеризация ацетилена):
-

+

––600°C,C→
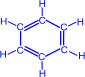
Ацетилен
бензен

 .
.