
- •1. Гранулометрический состав горных пород и методы его определения.
- •2. Седиментационный анализ механического состава горных пород.
- •3. Пористость горных пород. Коэффициент пористости.
- •4. Экстрагирование кернов. Принцип работы аппаратов Сокслета.
- •5. Определение коэффициента открытой пористости методом Преображенского.
- •26. Плотность природного газа и отдельных компонентов смеси.
- •6. Понятие насыщенности. Определение коэффициентов водо-, нефте- и газонасыщенности горных пород.
- •7. Проницаемость горных пород. Коэффициент абсолютной проницаемости.
- •8. Определение коэффициента абсолютной проницаемости по газу.
- •9 . Проницаемость горных пород. Явление проскальзывания газа.
- •8. Фазовые и относительные проницаемости горной породы.
- •9 . Графики относительных проницаемостей для системы «нефть-газ». Капиллярное число.
- •12. Движение смеси нефти, газа и воды в пористой среде.
- •13. Распределение пор по размерам. Функция Леверетта.
- •1 3. Зависимость проницаемости от пористости и размера пор.
- •14. Удельная поверхность горных пород. Связь с проницаемостью, пористостью и размером пор.
- •15. Деформационные свойства горных пород.
- •16. Деформация коллекторов при разработке нефтяных и газовых месторождений.
- •18. Поверхностное натяжение на границе раздела фаз. (17)
- •19. Смачивание и краевой угол смачивания.
- •22. Состав и классификация нефтей.
- •23. Состав и классификация природных газов.
- •24. Смеси газов. Мольная, массовая и объемная концентрации компонентов. Связь между ними.
- •25. Уравнение состояния реальных газов. Коэффициент сверхсжимаемости. (9,8)
- •38. Влагосодержание природных газов.
- •24. Закон соответственных состояний. Монограмма сверхсжимаемости.
- •26. Средняя молекулярная масса природного газа.
- •27. Парциальные давления и объём компонентов в смеси идеальных газов.
- •28. Упругость насыщенных паров.
- •29. Растворимость газов в нефти. Закон Генри.(11)
- •30. Плотность нефти. Зависимость от давления, температуры и состава.
- •34.Схема фазовых превращений бинарной смеси.
- •3 1. Вязкость нефти. Зависимость от давления, температуры и состава.
- •32. Структурно механические свойства аномальновязких нефтей.
- •33. Схема фазовых превращений индивидуальных компонентов углеводородов.(18)
- •35. Закон Рауля-Дальтона.
- •36. Особенности фазовых превращений газоконденсатных углеводородных систем.
- •36. Критическая температура и давление реальных углеводородных систем.
- •38. Уравнения фазовых концентраций и компонентов в смеси углеводородов.
24. Закон соответственных состояний. Монограмма сверхсжимаемости.
26. Средняя молекулярная масса природного газа.
Плотность природного газа в газовой фазе определяют по формуле:
![]()
Плотность газа при нормальных условиях можно определить по его молекулярной массе. Для смеси газов молекулярная масса рассчитывается по компонентному составу газа:
где Мт
— средняя
относительная
![]()
молекулярная масса газа;
М1 ..Мn
- относительные
молекулярные массы соответствующих
компонентов; У1...Уп
— мольные
доли компонентов. В соответствии с
законом Авогадро имеем:![]()
Плотность газов измеряют газовыми пикнометрами или же эффузивным методом, который основан на измерении скорости истечения газов из отверстий (квадраты скоростей истечения газов из малых отверстий обратно пропорциональны их плотностям)
![]()
Относительная плотность газа показывает во сколько раз при одинаковых условиях плотность газа больше или меньше плотности воздуха:
![]()
Плотности многих углеводородных газов больше плотности воздуха. Поэтому эти вещества могут накапливаться в помещениях насосных, в колодцах и т. д., если арматура оборудования негерметична. Это необходимо учитывать при проектировании и проведении работ на промысле.
27. Парциальные давления и объём компонентов в смеси идеальных газов.
Состав нефти и газовых смесей выражается в виде массовой или объемной концентрации компонентов в процентах и мольных долях.
Массовая
концентрация:![]()
где Wi — масса i - го компонента;
∑ Wi — суммарная масса смеси.
Объемная
концентрация какого-либо компонента в
смеси:
![]()
Vi – объем i-го компонента;
∑ Vi - суммарный объем смеси.
Молярная доля
компонента в смеси:![]()
где: ni - число молей i - го компонента в смеси.
З![]() ависимость
между объемной и молярной концентрациями
компонентов смеси газов вытекает из
закона
Авогадро. Так как равные объемы любых
газов при одинаковых температуре и
давлении со-К
держат одинаковое число молекул, то
объем i-го
компонента смеси будет пропорционален
числу молей i-го
компонента:
ависимость
между объемной и молярной концентрациями
компонентов смеси газов вытекает из
закона
Авогадро. Так как равные объемы любых
газов при одинаковых температуре и
давлении со-К
держат одинаковое число молекул, то
объем i-го
компонента смеси будет пропорционален
числу молей i-го
компонента:
т. е. концентрация компонента в процентах по молям (% мол.) в смеси газов при атмосферном давлении практически совпадает с объемной концентрацией этого компонента в процентах (% об.).
28. Упругость насыщенных паров.
Упругость насыщенных паров углеводородов - давление, при котором газ начинает конденсироваться и переходить в жидкое состояние. Она повышается с ростом температуры и она тем выше, чем ниже плотность углеводорода.
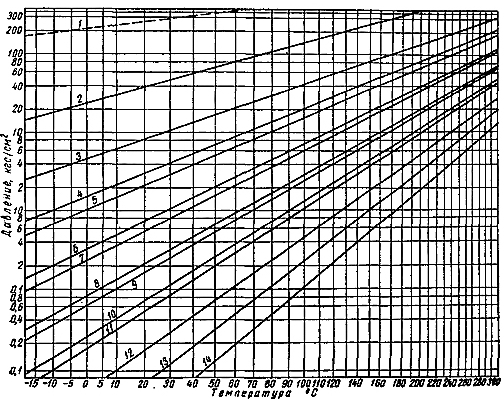
1 — метан; 2 — этан; 3 — пропан; 4 — изобутан; 5 — бутан; в — изопентан; 7 — пентан; 8 — изогексан; 9 — гексан; 10 — изогептан; 11 — гептан; 12 — октан; 13 —нонан; 14 — декан.
29. Растворимость газов в нефти. Закон Генри.(11)
От количества растворённого в пластовой нефти газа зависят все её важнейшие свойства: вязкость, сжимаемость, термическое расширение, плотность и другие.
Распределение компонентов нефтяного газа между жидкой и газообразной фазами определяется закономерностями процессов растворения. Способность газа, растворятся в нефти и воде, имеет большое значение на всех этапах разработки месторождений от добычи нефти до процессов подготовки и транспортировки.
Процесс растворения
для идеального газа при небольших
давлениях и температурах описывается
законом Генри:
![]() или
или
![]() ,
где Vж – объём жидкости-растворителя;
,
где Vж – объём жидкости-растворителя;
a – коэффициент растворимости газа;
Vг – объем газа, растворённого при данной температуре;
Р – давление газа над поверхностью жидкости
К – константа Генри (К=f(a)).
Коэффициент
растворимости газа (a) показывает, какое
количество газа (Vг) астворяется в единице
объёма жидкости (Vж ) при данном давлении:
![]()
Растворимость углеводородов в нефти подчиняется закону Генри. С повышением давления растворимость углеводородного газа растёт, а с повышением температуры – падает, углеводородные газы хуже растворяются в нефти с повышением температуры.
Разные компоненты нефтяного газа обладают разной способностью растворятся в жидкостях, причём с увеличением молекулярной массы газового компонента растёт коэффициент растворимости. Степень растворения углеводородных газов не зависит от молекулярной массы растворителя, а зависит от его природы.
