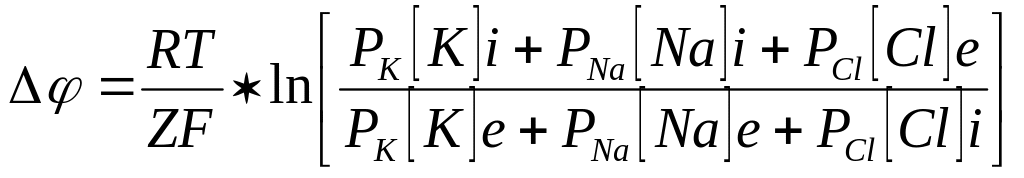- •41. Электрорецепция.
- •42. Как влияет удаление малозначащих признаков из обучающей выборки на процесс обучения нейросети? Пример на эвм.
- •43. Пространственная конфигурация биополимеров. Типы объемных взаимодействий в белковых макромолекулах. Водородные связи.
- •44. Хеморецепция.
- •45. Показать последовательность обучения и тестирования нейронной сети. Что такое внешняя выборка.
- •46. Взаимодействие макромолекул с растворителем. Состояние воды и гидрофобные взаимодействия в биоструктурах.
- •47. Восприятие запахов: пороги, классификация запахов.
- •48. Каким параметром характеризуется быстрота затухания колебаний, и какие процессы в живой природе имеют колебательный характер
- •49. Особенности пространственной организации белков и нуклеиновых кислот. Модели фибрилляторных и глобулярных белков. Качественная структурная теории белка.
- •50. Бактериородопсин как молекулярный фотоэлектрический генератор.
- •51. По каким физическим параметрам классифицируются биопотенциалы и какие требования предъявляются к усилителям биопотенциалов в этой связи.
- •52. Структура и функционирование биологических мембран. Мембрана как универсальный компонент биологических систем.
- •53. Вкус. Вкусовые качества. Строение вкусовых клеток.
- •55. Бислойные мембраны. Протеолипосомы. Поверхностный заряд мембранных систем.
- •56. Фотохимические превращения родопсина. Рецепторные потенциалы.
- •57. Описать методику выполнения измерений длительности сенсомоторных реакций (р-тест).
- •58. Антиоксиданты, механизм их биологического действия. Естественные антиоксиданты тканей и их биологическая роль.
- •59. Закон Вебера-Фехнера.
- •60. Как проверить экспериментально закон Вебера-Фехнера.
50. Бактериородопсин как молекулярный фотоэлектрический генератор.
Бактериородопсины — семейство мембранных светочувствительных белков археот (например, галобактерий). Бактериородопсины осуществляют перенос протона через плазматическую мембрану, по строению сходны с родопсинами млекопитающих.
Пурпурные мембраны (ПМ), локализованные в цитоплазме клеток некоторых экстремально галофильных бактерий, например Halobacterium halobiutn, содержат единственный гидрофобный пигмент — белковый комплекс (ПБК) бактериородопсин, молекулы которого располагаются в пурпурной мембране строго упорядоченно.
Пурпурная мембрана галофильных бактерий представляет собой естественный двумерный кристалл. Молекулы бактериородопсина организованы в мембране в виде тримеров; каждый тример окружён шестью другими так, что образуется правильная гексагональная решётка.
Изучение химического состава пурпурной мембраны показало, что они на 75% состоят из белка и на 25% из липидов. 60% липидов представлено фосфолипидами, подавляющая часть остальных — гликолипидами.
В мембранах клеток галофильных бактерий бактериородопсин выполняет функции светозависимого протонного насоса, создающего градиент ионов водорода, энергия которого используется клеткой для синтеза аденозинтрифосфорной кислоты (АТФ). Этот механизм синтеза АТФ получил название “бесхлорофильный фотосинтез”.
В ответ на поглощение кванта света бактериородопсин обесцвечивается, вступая в цикл фотохимических превращений, в результате которого между внутренней и наружной сторонами мембраны устанавливается градиент концентрации протонов. Образование градиента концентрации протонов приводит к тому, что освещённые клетки синтезируют АТФ. При этом происходит обратимая изомеризация ретиналя в транс-ретиналь, инициирующая каскад фотохимических реакций с последующим отрывом протона из молекулы белка и его присоединением со стороны цитоплазмы. Этот процесс обратим и в темноте протекает в обратном направлении.
Последующий механизм переноса протона посредством бактериородопсина включает цепь водородных связей, образованной боковыми радикалами гидрофильных аминокислот и простирающуюся через всю толщу белка. Перенос протона через цепь может осуществляться в том случае, если она состоит из двух участков и содержит функциональную группировку, способную под воздействием света изменять своё микроокружение и тем самым последовательно “замыкать” и “размыкать” эти участки. Роль такого “челночного” механизма между двумя белковыми проводниками протонов, один из которых сообщается с внешней, а другой – с цитоплазматической поверхностью мембраны клетки, играет альдимин ретиналя при остатке лизина-216.
Бактериородопсин применяют для изучения механизма транспорта протонов в живых организмах. Он перспективен как фотохромное вещество в галографии и вычислительной технике.
51. По каким физическим параметрам классифицируются биопотенциалы и какие требования предъявляются к усилителям биопотенциалов в этой связи.
Между двумя точками живой ткани с помощью чувствительной электроизмерительной аппаратуры можно зарегистрировать постоянную или меняющуюся разность потенциалов, которые связаны с жизненной функцией организма и называются биопотенциалами.
Как бы не были различны биопотенциалы по своим электрическим характеристикам, все они так или иначе обусловлены одной общей причиной - неравномерным распределением ионов в двух различных участках ткани, т.е. асимметрией концентрации ионов. Однако механизмы их образования в клетке могут быть различны:
1. Диффузный потенциал. Для его возникновения необходим контакт электролитов с различной концентрацией и различной подвижностью анионов и катионов (UH+ >> UCl-). Граница раздела одинаково проницаема для обоих ионов. Переход ионов H+ и Cl- будет осуществляться в сторону меньшей концентрации. В силу большей подвижности ионов водорода, будет создаваться их большая концентрация с правой стороны от границы раздела электролитов, возникнет разность потенциалов.
Количественно величина диффузного потенциала определяется уравнением Гендерсона:
![]()
R- универ. Газовая постоянная (8,31); F – число Фарадея (96500); T – темпер. в Кельвинах (273); Z – заряд мембраны; С – концен ионов внутри и снаружи.
2. Равновесный мембранный потенциал. Он возникает на границе раздела двух электролитов, разделенных мембраной, избирательно проницаемой для одного из ионов. Это частный случай диффузного потенциала, когда подвижность одного из ионов равна нулю.
При подвижности ионов Сl равной нулю, ионы Cl остаются по одну сторону мембраны, а ионы Н проходят через мембрану, образуя на другой стороне положительный заряд. Возникающий потенциал описывается уравнением Нернста, частный случай уравнения Гендерсона, когда U cl- = 0:
![]()
3. Стационарный мембранный потенциал. Ходжкин и Катц предположили, что потенциал покоя клетки является не равновесным, а стационарным, т.е. он обусловлен подвижным равновесием потоков ионов: Na, K, Cl.
Суммарный поток по их предположениям обусловлен, с одной стороны, активным транспортом ионов Na+ и K+ за счет энергии, выделяемой при гидролизе АТФ, с другой стороны, пассивным транспортом ионов Na, K и Cl, так как клеточная мембрана проницаема для всех этих ионов. Указанные потоки постоянны, их величины зависят от градиента концентрации ионов по обеим сторонам мембраны и от коэффициента проницаемости через поры и каналы мембраны, согласно уравнению Фика. Возникший за счет этого на мембране потенциал, определяется уравнением Гольдмана-Ходжкина-Катца и называется стационарным: