
- •2. Тематика курсової роботи
- •Вибір технічних розмірностей
- •Вибір компонентів
- •Вибір термодинамічних моделей
- •Побудова технологічної схеми
- •1.1 Математичне моделювання і розрахунок теплообмінних апаратів на еом
- •Рівняння теплового балансу зони ідеального витиснення має вигляд:
- •1.2 Математичний опис прямоточного тоа з двома зонами ідеального витиснення
- •1.3 Моделювання і розрахунок протиточного теплообмінного апарату типу “труба у трубі”
- •1.4 Математичний опис і розрахунок тоа з двома зонами різної гідродинамічної структури
- •1.5 Інженерний розрахунок кожухотрубчастого протиточного теплообмінного апарату на еом з використанням лінійного алгоритму
- •2. Розробка модулів реакторів для автоматизованого розрахунку і проектування складних хіміко-технологічних систем
- •3. Математичне моделювання та розрахунок реакторів витиснення
- •3.1 Побудова математичних моделей реакторів витиснення
- •3.2 Математичний опис ізотермічного реактора витиснення
- •3.3 Математичний опис адіабатичного реактору витиснення
- •3.4 Математичний опис політропічних реакторів витиснення
- •3.5 Моделювання проточного ізотермічного реактора змішування
- •4. Моделювання гетерогено-каталітичних процесів у рамках квазігомогеної моделі
- •4.1 Модель ідеального витиснення
- •4.2 Чисельні методи рішення рівнянь математичного опису каталітичних процесів
- •4.3 Математичне моделювання каталітичного очищення хвостових газів від оксидів азоту
- •4.4 Математичне моделювання конверсії оксиду вуглецю водяною парою
- •4.5 Математичне моделювання реактора з киплячим (псевдозрідженим) шаром
- •5. Побудова математичних моделей експериментально-статистичними методами.
- •5.2 Лінійний регресійний аналіз
- •5.3 Поліноміальний регресійний аналіз
1.5 Інженерний розрахунок кожухотрубчастого протиточного теплообмінного апарату на еом з використанням лінійного алгоритму
Крім описаних у лабораторних роботах 1–3 методів моделювання теплообмінних апаратів з побудовою рівнянь теплового балансу для основного потоку і для холодоагента з урахуванням гідродинаміки їх руху, на практиці широко використовують також інженерні методи розрахунку.
Нижче представлений інженерний метод розрахунку кожухотрубчастого протиточного теплообмінника, працюючого в стаціонарному режимі.
При побудові математичної моделі теплообмінника прийняті наступні допущення:
теплопередача не супроводжується зміною агрегатного стану теплоносіїв;
втрати теплоти не враховуються;
коефіцієнти теплопередачі в трубному і міжтрубному просторах розраховуються при початкових температурах теплоносіїв;
теплоносій, що віддає теплоту («гарячий» поток), направляється у труби, а теплоносій, що сприймає теплоту («холодний» поток) - в міжтрубний простір.
Через те, що в теплообміннику не змінюється склад матеріальних потоків:
GГК = GГН; GХК = GХН CХК = CХН; CГiК = CГiН; i = 1,...,NK.
де G – витрата теплоносія; С – концентрація речовини; індекси К і Н позначають кінцевий і початковий стан, а Г і Х – гарячий і холодний потоки.
Кількість теплоти, передана через стінку, дорівнює:
Q = KTF [(∆t2-∆t1)ln(∆t2/∆t1)], (1.18)
де КТ – коефіцієнт теплопередачі; F – площа поверхні теплообміну.
∆t2 = tHГ - tXK; ∆t1 = tГK – tXН.
Кількість теплоти:
- відданої гарячим теплоносієм:
Q = Г (tГН – tГК); (1.19)
- прийнятої холодним теплоносієм:
Q = X(tXК -tXН) (1.20)
при цьому водяні еквіваленти дорівнюють:
Г = GГНСРГ; X = GXHCPX.
Рівняння теплового балансу теплообмінника має вигляд:
Г(tГH - t ГK) = X(tXK – tXH). (1.21)
З рівняння (1.21) знаходимо:
tГK =tГH – (tXK – tXH)/N; N = Г/X. (1.22)
Через те, що ми зневажаємо втратами теплоти:
Г (tГH – tГK) = KTF [(tГH – tXK) - (tГK – tXH)]/ln[(tГН - tXK)/(tГK – tXH)] (1.23)
Підставивши (1.22) в (1.23) і виконавши прості перетворення, одержуємо:
tXK = (tГH(N.В – N) + tXH(В – N.В))/(В – N),
M = KTF/Г, В = Ехр((1 – N)М).
Коефіцієнт теплопередачі розраховується по формулі:
KT = 1 /(1/TP+∑rCT+1/M), (1.24)
де TP і M – коефіцієнти тепловіддачі в трубному і міжтрубному просторах; ∑rCT – сума термічних опорів стінки.
Теплоємності потоків розраховують по формулі:
![]() . (1.25)
. (1.25)
Додаток 2
2. Розробка модулів реакторів для автоматизованого розрахунку і проектування складних хіміко-технологічних систем
Проектування хіміко-технологічних систем (ХТС), що базується на методі математичного моделювання, припускає наявність математичних моделей окремих елементів ХТС і рівнянь технологічних зв'язків між ними.
Велику актуальність здобуває задача автоматизації проектування ХТС, тобто створення автоматизованих програм моделювання ХТС. Такі програми названі організуючими чи моделюючими, складаються з двох частин: бібліотеки стандартних програм (модулів) елементів ХТС і програми–диспетчера, що здійснює звертання до того чи іншого модуля з одночасним автоматичним вибором оптимального варіанту конструкції апарата.
Програмні модулі оформляються таким чином, щоб їхня робота не залежала від того, відкіля надходить вхідна інформація. Кожен модуль представляється визначеною обчислювальною процедурою і робить розрахунок параметрів вихідних потоків (витрат, концентрацій компонентів, температур) на підставі відомих значень вхідних і керуючих перемінних.
Етап розробки бібліотеки модулів є найменш формалізованим і найбільш трудомістким. У першу чергу це відноситься до хімічних реакторів - одних з важливих та важкостандартизуємих елементів ХТС.
У хімічному реакторі протікає складний технологічний процес: хімічне перетворення, перенесення і перемішування реагуючих речовин і продуктів реакції, передача тепла. У залежності від того, які властивості реактора необхідно досліджувати, для того самого реактора може бути обрано кілька різних моделей.
Нижче наведні лабораторні роботи які призначаються студентам для самостійного розрахунку найбільш розповсюджених у хімічній технології неорганічних речовин хімічних реакторів:
каскаду реакторів ідеального змішування;
змішувача потоків;
проточного ізотермічного реактора витиснення зі складною хімічною реакцією в реакційному обсязі;
ізотермічного реактора ідеального змішування зі складною хімічною реакцією в реакційному обсязі.
Розрахунок каскаду реакторів ідеального змішування (РІЗ) інтераційним методом
Хімічні процеси в безвідходних виробництвах мають самостійне значення для одержання цільових продуктів основного хімічного виробництва і для допоміжних процесів – очищення газових викидів, стічних вод і твердих відходів.
У промисловій практиці з технологічних розумінь нерідко потрібно забезпечити повне перемішування і такий ступінь завершення процесу, що в одиничному реакторі досягти неможливо. У такому випадку використовують ланцюжок послідовно з'єднаних реакторів ідеального змішування чи каскад реакторів. Каскади реакторів широко застосовуються в хімічній технології, зокрема, для окислювання SO2 в SO3, хлорування бензолу, очищення хімстоків та інших процесах.
Розрахунок каскаду реакторів ідеального змішування ітераційним методом на ЕОМ
Для розрахунків каскаду реакторів, у яких швидкість реакції є функцією концентрації вихідної речовини, найбільш зручно використовувати формулу Ньютона:
-
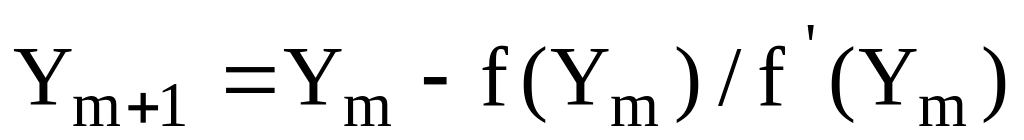 ,
,(2.1)
де m – номер ітерації; Ym – будь-яке наближення кореня функції;
![]() –
наступне, більш
точне, значення шуканого кореня;
–
наступне, більш
точне, значення шуканого кореня;
![]() –
функція, корені
якої визначаються;
–
функція, корені
якої визначаються;
![]() –
її похідна.
–
її похідна.
Загальне рівняння матеріального балансу для i-го реактору ідеального змішування має вигляд:
![]() . (2.2)
. (2.2)
Для стаціонарного режиму час перебування можна визначити по формулі:
![]() , (2.3)
, (2.3)
де Vpі
–
об’єм
i-го
реактору;
– об'ємна
швидкість;
![]() –
швидкість
реакції по
і-ому
компоненту,
яка
розраховується
по рівнянню:
–
швидкість
реакції по
і-ому
компоненту,
яка
розраховується
по рівнянню:
![]() , (2.4)
, (2.4)
де р – порядок реакції.
У випадку каскаду реакторів рівного об’єму τi = τ1 (i = 1, 2, …,n – номер реактора) справедлива рівність:
-
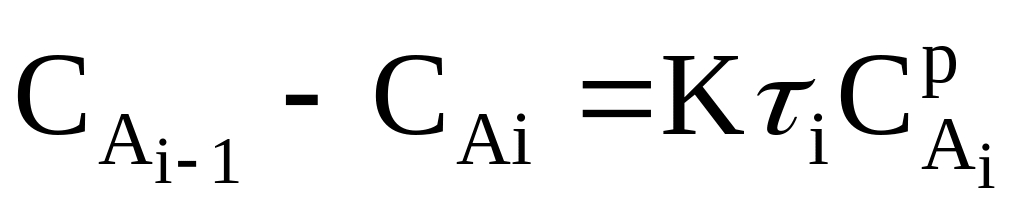 .
.(2.5)
Позначимо частку
непрореагованої
речовини в і-му
реакторі:![]() .
Тоді ступінь перетворення дорівнює:
.
Тоді ступінь перетворення дорівнює:
![]() .
.
У результаті нескладних перетворень рівняння (2.3) приймає вид:
-
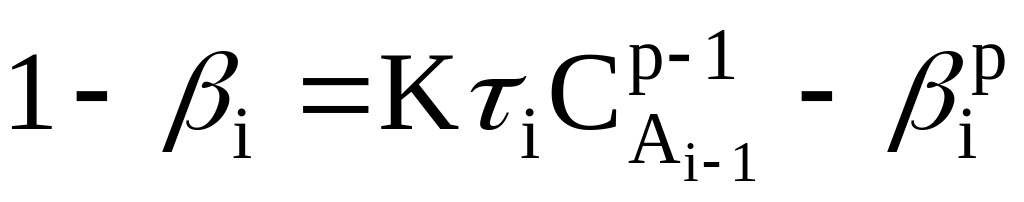 .
.(2.6)
Рівняння (1.6) можна записати у вигляді деякої функції:
-
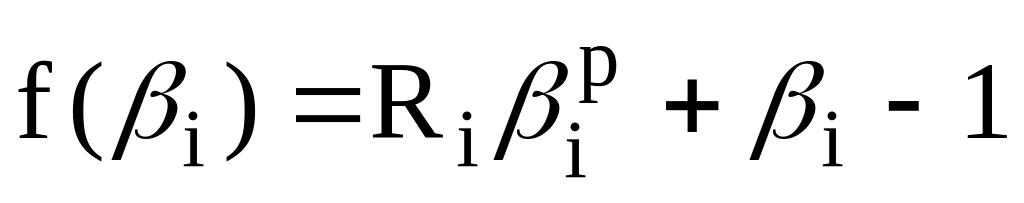 ,
де
,
де
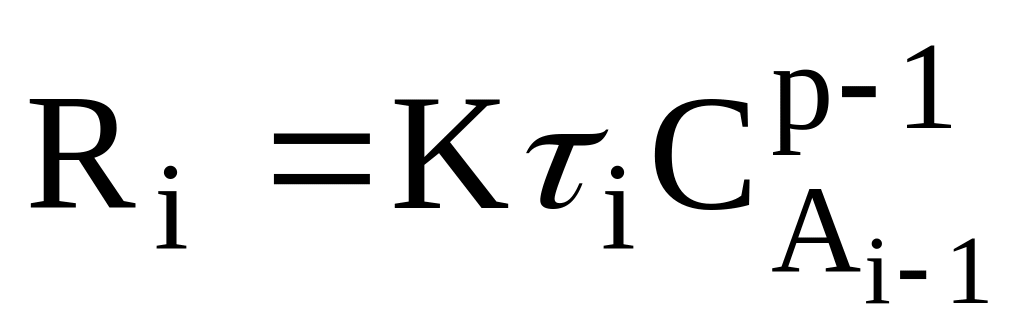 .
.(2.7)
Визначення ступеню
перетворення в реакторах
![]() зводиться,
таким чином, до находження кореня
зводиться,
таким чином, до находження кореня
![]() рівняння (2.7).
рівняння (2.7).
Рішення такої задачі зручно виконувати методом інтерації, використовуючи формулу Ньютона:
-
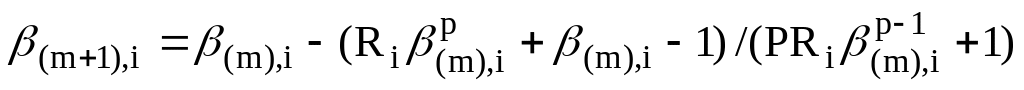
(2.8)
Формула (1.8)
дозволяє обчислити
![]() для будь-якого порядку реакції р.
Як початкове наближення можна прийняти
для будь-якого порядку реакції р.
Як початкове наближення можна прийняти
![]() =1.
Частку
непрореагованої
речовини у вихідному потоці каскаду
РІЗ
розраховуємо по формулі:
=1.
Частку
непрореагованої
речовини у вихідному потоці каскаду
РІЗ
розраховуємо по формулі:
|
(2.9) |
чи к = 1.2.3.....n-1.n.
Формули (2.7 – 2.9) є вихідними при складанні програми на ЕОМ на базі яких проводять обчислення значень і, k, CAi. Точність обчислень і по формулі (2.8) вибирається в залежності від характеру задачі. Для інженерних розрахунків приймаємо, що =0,001.
Розрахунок змішувача потоків ітераційним методом
При складанні математичного опису змішувача потоків (рис.2.1) скористаємося наступними допущеннями:
структура потоку в апараті відповідає режиму ідеального змішування;
режим змішування в апараті – сталий;
в реакційному об’єму апарата відсутні джерела і стоки речовини і теплоти;
число потоків, що змішуються, n = 2; (при необхідності змішування більшого числа потоків у схему можна включити декілька послідовно з'єднаних змішувачів);
теплоємності компонентів i-го потоку розраховується при температурі цього потоку.

Рис.2.1. Схема змішувача потоків
Gj, tj, Cj – витрата, температура і вектор концентрації j-го технологічного потоку.
Загальне рівняння матеріального балансу має вигляд:
![]() ,
,
де G – витрата вихідного потоку; G1, G2, – витрати вхідних потоків.
Рівняння матеріального балансу для i-го компоненту має вигляд:
-
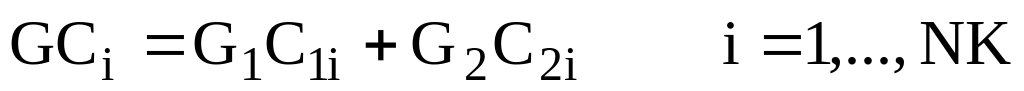 ,
,(2.10)
де C1 – масова частка i-ої речовини у вихідному потоці;
C1i, C2і – масові частки і-ої речовини в першому і в другому вхідних потоках;
NK – число речовин у потоці.
Очевидно, що:
![]() .
.
Рівняння теплового балансу має вигляд:
-
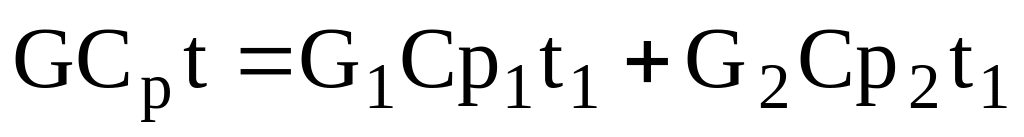 ,
,(2.11)
де Сp – питома теплоємність вихідного потоку; t – температура вихідного потоку; Сp1, Сp2 – питомі теплоєності вхідних потоків; t1, t2 – температури вхідних потоків.
Звідси:
-
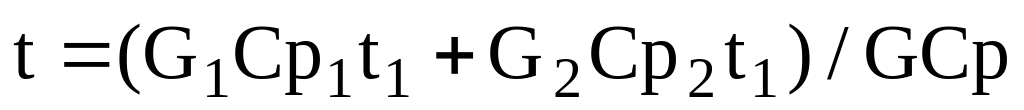 .
.(2.12)
Температурна залежність питомої теплоємності i-ої речовини в j-му потоці може бути представлена як функція температури:
-
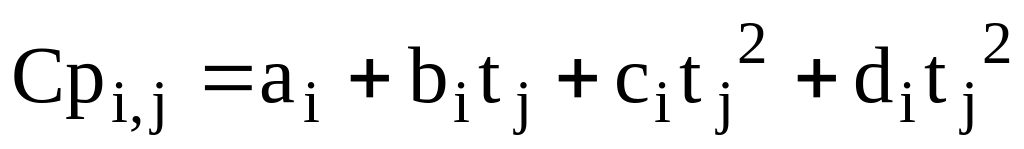
(2.13)
де a, b, c, d – емпірічні коефіцієнти, знайдені для кожної речовини.
Теплоємність j-го потоку обчислюється за правилом адитивності:
-
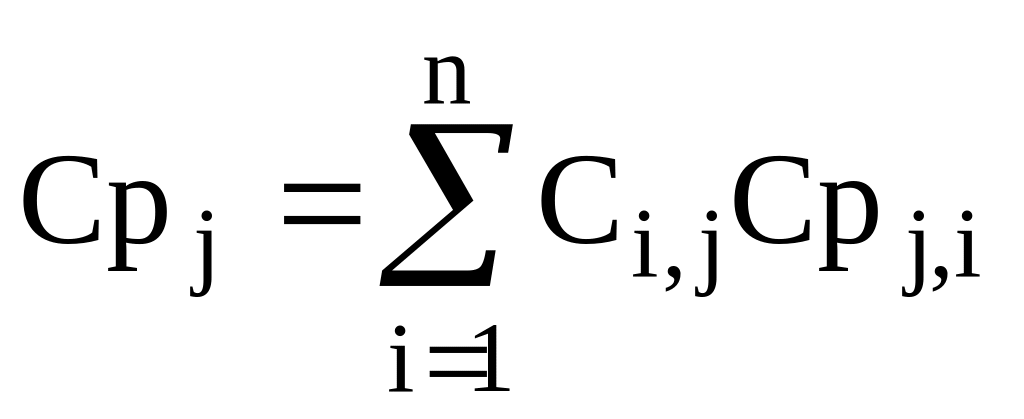
(2.14)
Для вирішення рівняння (2.12) скористуємось методом простої ітерації:
tk+1 = (G1Cp1(t1)t1 + G2Cp2(t2)t2)/(GCp(tk),
де k = 0,1,2,... – номер ітерації.
Умови закінчення розрахунку: |tk-1 - tk| < .
