
- •1. Тепловые эффекты химических реакций. Экзотермические и эндотермические реакции. Теплоты сгорания и образования.
- •Шпаргалки (шпора) по Химии.
- •2. Закон Гесса. Следствия из закона Гесса.
- •Теплота растворения.
- •Энтропия и её изменения при химических процессах и фазовых периодах.
- •Кинетика. Понятие о скорости химических реакций. Гомогенные и гетерогенные системы.
- •Факторы, влияющие на скорость химической реакции
- •Зависимость скорости реакции от концентрации реагирующих веществ. Закон действующих масс в гомогенной и гетерогенной системах.
- •Влияние температуры на скорость реакции. Энергия активации.
- •Катализ. Теория промежуточных соединений
- •Химическое равновесие. Константа химического равновесия.
- •Смещение химического равновесия при изменении концентрации веществ и температуры. Принцип Ле Шателье.
- •Общие понятия о дисперсных системах и растворах. Классификация дисперсных систем.
- •12. Образование растворов. Классификация растворов.
- •Растворы неэлектролитов. 2 закон Рауля.
- •Явление осмоса. Осмотическое давление.
- •16. Основы электролитической диссоциации. Константа диссоциации.
- •17. Растворы электролитов. Степень диссоциации и её зависимость от концентрации растворённого вещества (закон разбавления Оствальда) и температуры.
- •18. Способы выражения концентрации.
- •2 Ответ
- •20. Ионное произведение воды, pH растворов.
- •2 Ответ
- •21. Гидролиз солей.
- •22. Степень гидролиза. Влияние условий на степень полноты гидролиза: природа веществ, температура и концентрация веществ.
- •24. Адсорбция на поверхности раствор-газ. Уравнение Гиббса
- •25. Адсорбция газов и растворенных веществ твердыми сорбентами. Уравнение Френдлиха и Ленгмюра.
- •В некоторых случаях применяется уравнение Ленгмюра вида:
- •2. Уравнение изотермы адсорбции теории бэт
- •В некоторых случаях применяется уравнение Ленгмюра вида:
- •2. Уравнение изотермы адсорбции теории бэт
В некоторых случаях применяется уравнение Ленгмюра вида:
(5)
Здесь Va – адсорбционный объем, V – равновесный объем адсорбата.
2. Уравнение изотермы адсорбции теории бэт
При адсорбции газов и паров на поверхности многих адсорбентов образуется полимолекулярный адсорбционный слой. В этих случаях теория Ленгмюра неприменима и для различного рода расчетов пользуются теорией БЭТ.
Теория БЭТ устанавливает следующую зависимость между A и p :
(6)
Am-адсорбционная емкость насыщенного монослоя, определяющаяся размером “посадочной” площадки молекулы газа, т.е. площадью, которую она занимает в насыщенном монослое;
k-константа, зависящая от энергии взаимодействия молекул в адсорбционном слое;
PS-давление насыщенного пара.
Уравнение (5) можно привести к виду:
(7)
В таком виде уравнение БЭТ является уравнением прямой линии, если функцией считать величину, стоящую слева, а аргументом —P/PS.
Теория БЭТ используется для расчета удельной поверхности адсорбентов (поверхности единицы массы адсорбента) по экспериментально полученной изотерме адсорбции.
Для определения удельной поверхности адсорбента S строят график зависимости P/PS/(1- P/PS)A от P/PS. По угловому коэффициенту прямой, равному, (k-1)/kAm, и, величине отрезка, отсекаемого на оси ординат при P/PS =0 и равного 1/Amk (рис.1), рассчитывают Am.
Удельная поверхность вычисляется по формуле:
(8)
S0-площадь, занимаемая одной молекулой газа в адсорбционном слое;
Na-постоянная Авогадро.
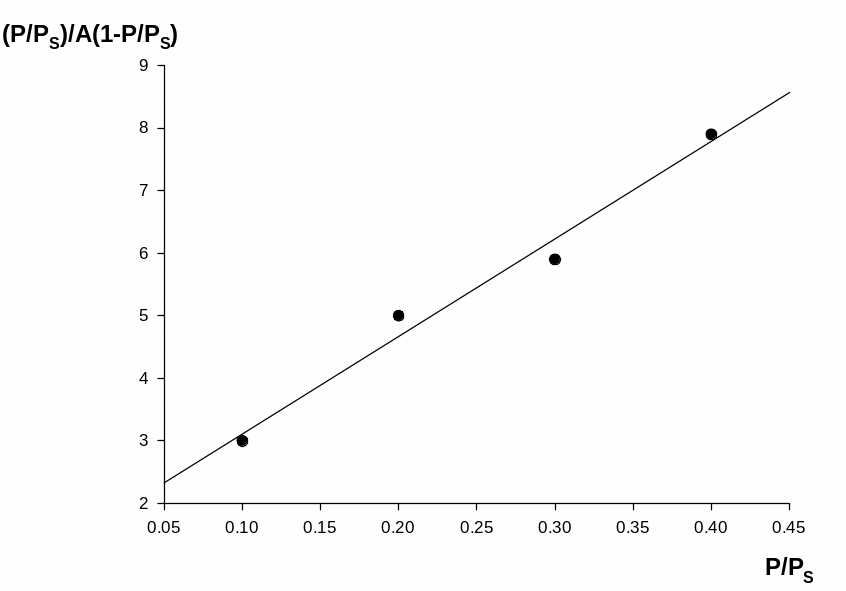
Рис.1.Изотерма адсорбции в координатах линейной формы уравнения БЭТ.
Для адсорбции из растворов линейная форма уравнения БЭТ выглядит таким образом:
(9)
Сs-концентрация насыщенного раствора.
Изотерму адсорбции строим так же, как и в первом случае, в координатах соответствующих этому уравнению. Аналогично вычисляется удельная поверхность:
(10)
3.Уравнение изотермы адсорбции Фрейндлиха
Уравнение Фрейндлиха для адсорбции газа имеет вид:
(11)
K и 1/n –постоянные уравнения Фрейндлиха.
Чаще всего это уравнение применяется в логарифмической форме:
(12)
Уравнение в такой форме позволяет построить линейную зависимость lnA от lnp и графически определить оба постоянных параметра.
Логарифмическое уравнение Фрейндлиха для адсорбции из раствора имеет вид:
(13)
Графически определяем постоянные параметры по линейной зависимости lnA от lnC.(рис.2)
Отрезок, отсекаемый на оси ординат равен lg k, а тангенс угла наклона прямой
равен 1/n.
Р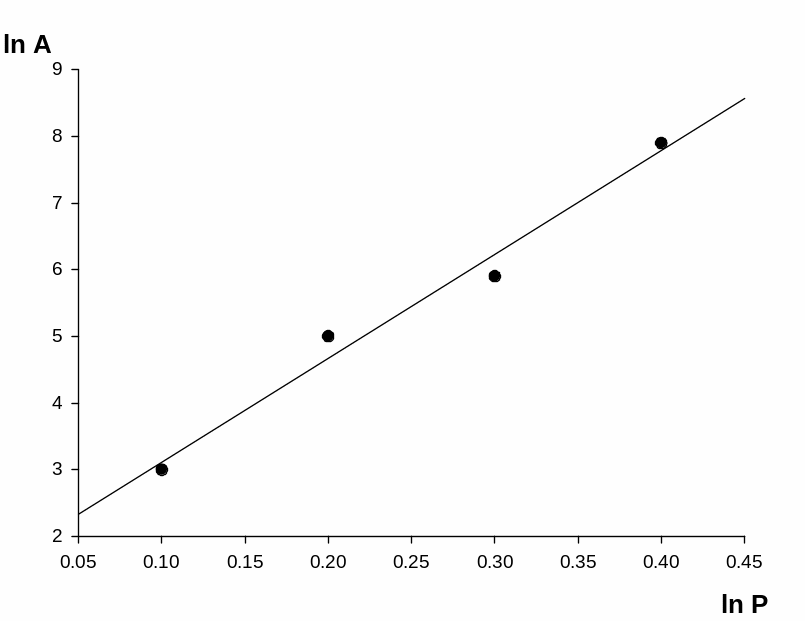 ис.2.
Изотерма адсорбции в координатах
логарифмического уравнения.
ис.2.
Изотерма адсорбции в координатах
логарифмического уравнения.
