
- •§ 27.6. Инфракрасное излучение и его применение в медицине
- •§ 27.7. Ультрафиолетовое излучение
- •§ 27.3. Законы излучения черного тела
- •§ 31.1. Устройство рентгеновской трубки. Тормозное рентгеновское излучение
- •Лучевая терапия
- •§ 29.4. Оптические атомные спектры
- •§ 29.5. Молекулярные спектры
- •§ 13.1. Строение и модели мембран
- •§13.2 Некоторые физические свойства и параметры мембран
- •1.3 Уравнение электродиффузии ионов через мембрану в приближении однородного поля
- •1.3 Уравнение электродиффузии ионов через мембрану в приближении однородного поля
§ 29.4. Оптические атомные спектры
Атомными спектрами называют как спектры испускания, так и спектры поглощения, которые возникают при квантовых перехода* между уровнями свободны* или слабовзаимодействующих атомов.
Под оптическими атомными спек трами будем понимать те, которые обусловлены переходами между уров нями внешних электронов с энергией фотонов ' порядка нескольких
электрон-вольт. Сюда относятся ультрафиолетовая, видимая и близкая инфракрасная (до микрометров) области спектра.
Наибольший интерес представляют оптические атомные спектры испускания, которые получают от возбужденных атомов. Их возбуждение обычно достигается в результате безызлуча-тельных квантовых переходов при электрическом разряде в газе или нагревании вещества пламенем газовых горелок, электрической дугой или искрой.
В § 29.1 были изложены общие соображения о спектрах атомов. Подробные сведения о спектрах конкретных атомов можно найти в специальных справочниках по спектроскопии. В качестве простого примера рас-
смотрим спектр атома водорода и водородоподобных ионов.
Из формул (28.24) и (29.1) можно получить формулу для частоты света, излучаемого (поглощаемого) атомом водорода (Z — 1):
•![]() . (29.15)
. (29.15)
Эта формула была экспериментально найдена И.Я.Бальмером еще задолго до создания квантовой механики и теоретически получена Бором (см. § 28.7); г и * - порядковые номера уровней, между которыми происходит квантовый перевод.
В спектре можно выделить группы линий, называемые спек-тралъными серия. Каждая серия применительно к спектрам испускания соответствует переходам с различных уровней на один и тот же конечный (рис. 29.5).
В ультрафиолетовой области расположена серия Лаймана, которая образуется при переходе с верхних энергетических уровней на самый нижний, основной (п^ = 1). Из формулы (29.15) для серии Лаймана получаем
![]() (я, = 2, 3,4,...), (29.16)
(я, = 2, 3,4,...), (29.16)
т.е. находим частоты всех линий этой серии. Самая длинноволновая линия имеет наибольшую интенсивность. Интенсивности спектральных линий на рис. 29.5 условно показаны толщиной прямых соответствующих переходов.
В видимой и близкой ультрафиолетовой областях спектра расположена серия Балъмера, которая возникает вследствие переходов с верхних энергетических уровней на второй (n/t = 2). Из формулы (29.15) для серии Бальмера получаем
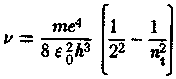 (п, = 3, 4, 5, ...), (29.17)
(п, = 3, 4, 5, ...), (29.17)
т.е. находим частоты всех линий этой серии.
В инфракрасной области расположена серия Ношена, которая возникает при переходах с верхних энергетических уровней на третий (nfc = 3). Из формулы (29.15) для серии Пашена следует
(я, = 4, 5, 6,...). (29.18)
Существуют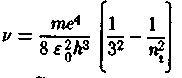 и
другие серии в инфракрасной области.
и
другие серии в инфракрасной области.
Может показаться, что спектр атомарного водорода не ограничен со стороны малых частот, так как энергетические уровни по мере увеличения п становятся сколь угодно близкими. Однако на самом деле вероятность перехода между такими уровнями столь мала, что практически эти переходы не наблюдаются.
Выражение для ионизационного потенциала (15.15) можно получить из (29.15), считая n/t = 1 и п, —» »:
![]() (29.19)
(29.19)
Для атомного спектрального анализа используют как спектры испускания (эмиссионный спектральный анализ), так и спектры поглощения (абсорбционный атомный спектральный анализ).
В медицинских целях эмиссионный анализ служит в основном для определения микроэлементов в тканях организма, небольшого
количества атомов металлов в консервированных продуктах с гигиенической целью, некоторых элементов в трупных тканях для целей судебной медицины и т.п.
