
5.Спектр атома водню
Квантові
числа n, е i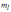 дозволяють повністю описати спектр
випромінювання атома водню, отриманий
в теорії Бора. У квантовій механіці
появляються правила відбору, що обмежують
кількість можливих переходів електронів
в атомі, зв’язаних з випромінюванням
і поглинанням світла. Теоретично доведено
і експериментально підтверджено, що
для дипольного випромінювання електрона,
який рухається в центрально-симетричному
полі ядра атома, можуть здійснюватися
лише такі переходи, для яких: 1) зміна
орбітального квантового числа
дозволяють повністю описати спектр
випромінювання атома водню, отриманий
в теорії Бора. У квантовій механіці
появляються правила відбору, що обмежують
кількість можливих переходів електронів
в атомі, зв’язаних з випромінюванням
і поглинанням світла. Теоретично доведено
і експериментально підтверджено, що
для дипольного випромінювання електрона,
який рухається в центрально-симетричному
полі ядра атома, можуть здійснюватися
лише такі переходи, для яких: 1) зміна
орбітального квантового числа
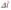 задовольняє
умову
задовольняє
умову ; 2) зміна магнітного квантового числа
; 2) зміна магнітного квантового числа
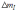 задовольняє
умову
задовольняє
умову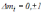 .
.
У
спектральних лініях атома водню серії
Лаймана відповідають переходи np
 1s
(n = 2, 3...), серії Бальмера –
1s
(n = 2, 3...), серії Бальмера –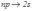 ,
,
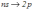 ,
,
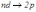 (
(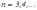 )
(рис. 4).
)
(рис. 4).
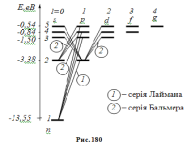
Рис.4
Кожному
значенню енергії електрона в атомі
водню En
(за винятком Е1)
відповідає декілька значень хвильової
функції
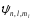 .
Вони відрізняються значеннями квантових
чисел l
i
ml.
Це означає, що атом водню може мати
однакове значення енергії і перебувати
в кількох різних квантових станах.
.
Вони відрізняються значеннями квантових
чисел l
i
ml.
Це означає, що атом водню може мати
однакове значення енергії і перебувати
в кількох різних квантових станах.
6.Порядком виродження
Стани з однаковою енергією називаються виродженими, а число таких станів з одним значенням енергії, називається порядком виродження.
Порядок виродження легко обчислити виходячи з числа можливих значень l i ml. Кожному значенню числа n відповідає 2l+1 значень квантового числа ml. Тому число різних станів для даного значення n, дорівнює
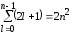 .
.
Таким чином кожен рівень енергії атома водню має порядок виродження 2n2.
У квантовій механіці доводиться, що можливі лише такі переходи електронів між енергетичними рівнями, для яких виконується умова зміни орбітального квантового числа l на одиницю:

 l=
l=
 1
1
Умова,
яка виражена цим співвідношенням
називається правилом
відбору.
Існування цього правила обумовлено
тим, що фотон має власний момент імпульсу,
який називають спіном, рівним наближено
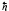 .
При випромінюванні фотон забирає від
атома цей момент, а при поглинанні віддає
атому. Тому правило відбору є відповідним
наслідком закону збереження моменту
імпульсу.
.
При випромінюванні фотон забирає від
атома цей момент, а при поглинанні віддає
атому. Тому правило відбору є відповідним
наслідком закону збереження моменту
імпульсу.
Переходи електронів в атомі водню, які дозволені правилом відбору показані на рис. 5.
Серії
Лаймана відповідають переходи np
 1s,
(n=2,3,4,...).
1s,
(n=2,3,4,...).
Серії
Бальмера відповідають переходи np
 2s,
ns
2s,
ns
 2p
і nd
2p
і nd
 2p,
(n=3,4,5,...).
2p,
(n=3,4,5,...).
Стан 1s є основним станом атома водню. У цьому стані атом має найменшу енергію. Для виведення атома з основного стану йому слід надати необхідну енергію за рахунок зовнішнього джерела. Таким джерелом енергії може бути нагрівання, електричний розряд або опромінення.
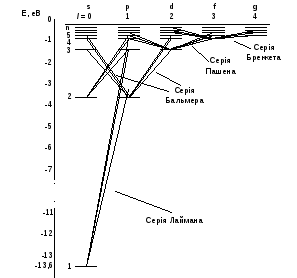
Рис. 5
При опромінені водню фотонами від зовнішнього джерела їх енергія поглинається повністю лише у випадку коли енергія фотонів у точності збігається з різницею енергії двох енергетичних рівнів. У цьому випадку фотон зникає повністю, передаючи атому всю свою енергію. Атом не може поглинути частину фотона, оскільки фотон є неподільним.
7.Модель атома водню
У 1911 Ернест Резерфорд (1871—1937), виходячи з електронної концепції Томсона, запропонував модель атома: в центрі атома знаходиться позитивно заряджене ядро, а навколо нього обертаються негативно заряджені електрони. У 1913 Нільс Бор (1885—1962), використовуючи принципи квантової механіки, показав, що електрони можуть знаходитися не на будь-яких, а на суворо визначених орбітах. Планетарна квантова модель атома Резерфорда примусила вчених по-новому підійти до пояснення будови і властивостей хімічних сполук. Німецький фізик Вальтер Коссель (1888—1956) передбачив, що хімічні властивості атома визначаються числом електронів на його зовнішній оболонці, а утворення хімічних зв'язків зумовлюється в основному силами електростатичної взаємодії. Американські вчені Гілберт Ньютон Льюїс (1875—1946) і Ірвінг Ленгмюр (1881—1957) сформулювали електронну теорію хімічного зв'язку. Відповідно до цих уявлень молекули неорганічних солей стабілізуються електростатичними взаємодіями між іонами, що входять до їх складу, які утворяться при переході електронів від одного елемента до іншого (іонний зв'язок).
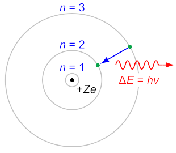

Атомна модель Бора
