
Зміст
-
Постулати Бора
-
Теорія Бора
-
Атомна модель Бора
-
Розв'язок рівняння Шредінгера для атома водню. Енергія атома
-
Спектр атома водню
-
Порядком виродження
-
Модель атома водню
-
Механічний і магнітний моменти атома водню
Вступ
Дослідження Сонця, зірок, міжзоряного простору показують, що найпоширенішим елементом Всесвіту є водень (в космосі у вигляді розжареної плазми він становить 70% маси Сонця і зірок).
За деякими розрахунками, кожну секунду в глибинах Сонця приблизно 564 млн. тонн водню в результаті термоядерного синтезу перетворюються в 560 млн. тонн гелію, а 4 млн. тонн водню перетворюються на потужне випромінювання, яке йде в космічний простір. Немає побоювань, що на Сонці незабаром вичерпаються запаси водню. Воно існує мільярди років, а запас водню в ньому достатній для того, щоб забезпечити ще стільки ж років горіння. Людина живе в воднево-гелієвої всесвіту. Тому водень представляє для нас дуже великий інтерес. Аж до XX ст. Всі були переконані, що за «горючим повітрям» Кавендіш, гідрогеніумом Лавуазьє ховається елемент, що породжує при своєму з'єднанні з киснем звичайну воду. В 1913 році Бор запропонував модель атома водню, в якій електрон обертаються навколо ядра лише по певних строго визначених орбітах. Ця модель отримала назву моделі Бора і стала початком створення квантової теорії атома.
У природі були відкриті три різних водню, три його ізотопу, які були названі відповідно до складності своїх ядер. Найлегший - проти. Водень у звичайній воді в основному складається з протію. Але у воді є і більш важкий водень - дейтерій. На кожні 6700 атомів протію доводиться один атом дейтерію.
Існує і надважкий водень - тритій. Тритій радіоактивний. Він безперервно утворюється в стратосфері під дією космічного випромінювання. Є припущення, що це не межа для існування нових, ще більш важких ізотопів водню, які повинні бути радіоактивн
Моя розповідь про водні і водневої технології був би неповним, якби ми не вказали на ще один лик водню - атомарний водень, переможний хід якого в техніці належить. Справа в тому, що атомарний водень більше перспективне пальне, ніж проти.
Ми будемо розглядати властивості атома водню й воднеподібних атомів, що складаються із позитивно зарядженого ядра, яке для основного ізотопу є просто протоном, і одного електрона: H, He+, Li++... Заряд ядра рівний Ze, де Z - порядковий номер елемента (число протонів у ядрі). Квантово-механічна задача про дозволені енергетичні стани атома водню розв'язується точно. Зважаючи на цю обставину, хвильові функції, отримані як власні функції цієї задачі є базовими для розгляду решти елементів періодичної таблиці. Саме тому атом водню має велике значення для фізики.
1.Постулати Бора
1913 р. Бор опублікував роботу в якій виклав теоріію атома водню. Для пояснення він сформулював такі постулати:
1. Атомна система може перебувати тільки в особливих стаціонарних, або квантових станах, кожному з яких відповідає певна енергія En. У стаціонарному стані атом не випромінює енергію.
2. Перехід атома з одного стаціонарного стану в інший супроводжується випромінюванням чи поглинанням кванту енергії , енергію якого hν визначають за формулою:
hν = Em − En
де m і n - цілі числа (номери стаціонарних станів), якщо Em > En фотон з частотою ν випромінюється, якщо Em < En - поглинається. Який в свою чергу дорівнює різниці енергій різних станів
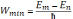
Постулати мають дослідне підтвердження Франка і Герца(підтвердили дискретність енергетичних рівнів).
3. Радіуси rn стаціонарних станів задовольняють умову:
m vn rn = n ħ
де n = 1,2,3,..., m - маса електрона, ħ - зведена стала Планка.
Схеми переходу атома:
1.З основного стаціонарного стану до збудженого,
2. Із збудженого стаціонарного стану до основного.
Рис.
1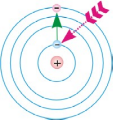 Рис.2
Рис.2 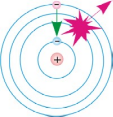
2.Теорія Бора
Теорія Бора — це історично перша теорія, що на основі „квазікласичного підходу” описала „дискретну структуру” енергетичного спектру воднеподібних атомів. Нільс Бор запропонував видозмінити класичну механіку шляхом введення сталої Планка h. Він припустив, що не всі рухи, допустимі в класичній механіці реалізуються в атомних системах, а лише деякі, можна сказати „вибрані”. Стосовно енергії атома гіпотеза Бора означала, що енергія атома E може приймати лише дискретні, квантовані значення.
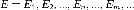
Слід відзначити, що постулат Бора є правильним до сьогодні, не зважаючи на поступ науки, оскільки він є прямим вираженням експериментальних фактів. Постулат Бора суперечив класичній теорії випромінювання, оскільки за нею атом повинен випромінювати неперервно, і тому його енергія може приймати будь-які значення енергії, що лежать між дозволеними рівнями енергії. Таким чином Бор вперше при підході до атомної проблеми став на квантову точку зору, згідно з якою, енергія випромінюється квантами світла. Тоді, шляхом об'єднання закону збереження енергії з постулатом Бора ми отримаємо написаний вперше Бором закон, що зв’язував частоти ωmn, котрі може випромінювати, та поглинати атом (спектр атому), із квантовими рівнями En, властивими для даного атома, тобто
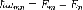
Це рівняння є не що інше, як закон збереження енергії при випромінюванні та поглинанні світла, і в першій теорії Бора виступав, як один із постулатів його теорії („правило частот” Бора). Розділивши останнє рівняння на постійну Планка отримаємо частоти, що поглинаються чи випромінюються квантовими системами.
Недоліки теорії Бора:
1. Внутрішня суперечливість, непослідовність (поєднання класичної фізики та квантово-механічних постулатів).
2. Ніяк не пояснювалося відмінність інтенсивностей спектральних ліній випромінювання, тобто не було пояснення тому, що деякі енергетичні переходи виявляються більш вірогідними, ніж інші.
3. Не дозволяла створити теоретичні моделі більш складних атомних систем, наприклад, гелію всього з двома електронами в атомі.
Теорія Бора була замінена послідовної квантової теорії, що враховує хвильові властивості мікрочастинок, що отримала назву квантова (хвильова) механіка.
