- •Основы биологической химии предисловие
- •Введение Предмет и задачи биохимии
- •Основные признаки живой материи
- •Глава 1. Химический состав организмов
- •Глава 2. Структура и свойства белков
- •2.1. Роль и определение белков.
- •2.2. Функции белков в организме
- •2.3. Элементный состав белков. Содержание белков в органах и тканях
- •2.4. Аминокислотный состав белков
- •2.5. Кислотно-основные свойства аминокислот
- •2.6. Стереохимия аминокислот
- •2.7. Строение белков
- •2.8. Уровни структурной организации белков
- •Первичная структура
- •Вторичная структура белков
- •Третичная структура белков
- •Четвертичная структура белков
- •2.9. Физико-химические свойства белков
- •Кислотно-основные свойства белков
- •Растворимость белков
- •Денатурация и ренатурация
- •2.10. Классификация белков
- •2.11. Методы выделения и очистки белков
- •Очистка белков
Четвертичная структура белков
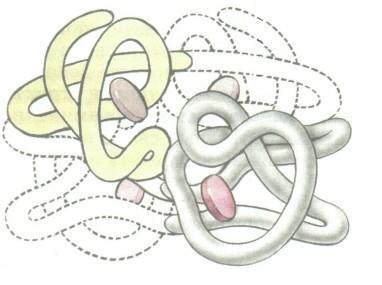
Белки, состоящие из одной полипептидной цепи, имеют только третичную структуру. К ним относятся, например, миоглобин - белок мышечной ткани, ряд ферментов (лизоцим, пепсин, трипсин и так далее). Однако некоторые белки построены из нескольких полипептидных цепей, каждая из которых имеет первичную, вторичную и третичную структуры. Для таких белков введено понятие четвертичной структуры, которая представляет собой организацию нескольких полипептидных цепей в функциональную единую молекулу белка (рис.8б). Такой белок с четвертичной структурой называется олигомером или мультимером, а его полипептидные цепи - протомерами или субъединицами. Стабилизируют четвертичную структуру такие же связи, как и - третичную. Протомеры соединяются в мультимеры по принципу комплементарности - универсальному принципу живой природы. Расположение групп, образующих связи, на одном протомере соответствует их расположению на другом протомере. Принцип комплементарности лежит в основе процесса самосборки олгимерных белков.
|
|
|
|
а |
б |
Рис. 8. Схема третичной (а) и четвертичной (6) структуры белка
При четвертичном уровне организации белки сохраняют основную конфигурацию третичной структуры (глобулярную или фибриллярную). Например, белки волос и шерсти имеют фибриллярную конформацию четвертичной структуры. Примером глобулярного мультимера может служить гемоглобин, состоящий из четырёх субъединиц глобулярного характера: двух α- и двух β-цепей. Его строение кратко можно представить формулой 2α2β. Под действием мочевины происходит обратимая диссоциация гемоглобина:
2α2β = 2α + 2β = α + α + β + β,
либо
2α2β = αβ + αβ = α + α + β + β
димеры протомеры
Отдельные протомеры биологически неактивны, именно четвертичная структура обеспечивает ряду белков их специфические функции. Число протомеров в мультимерах всегда чётное, а молекулярные массы более 1млн. Да. Классическим примером мультимерной молекулы является вирус табачной мозаики с молекулярной массой около 40 млн. Да, состоящий из одной молекулы РНК и 2130 белковых субъединиц.
2.9. Физико-химические свойства белков
Белки имеют различные химические, физические и биологические свойства, которые определяются аминокислотным составом и пространственной организацией каждого белка. Химические реакции белков очень разнообразны, они обусловлены наличием NH2-, СООН-групп и радикалов различной природы. Это реакции нитрования, ацилирования, алкилирования, этерификации, окисления-восстановления и другие. Белки обладают кислотно-основными, буферными, коллоидными и осмотическими свойствами.
Кислотно-основные свойства белков
Белки являются амфотерными полиэлектролитами, т.е. проявляют как кислотные, так и основные свойства. Это обусловлено наличием в молекулах белков аминокислотных радикалов, способных к ионизации, а также свободных α-амино- и α-карбоксильных групп на концах пептидных цепей. Кислотные свойства белку придают кислые аминокислоты (аспарагиновая, глутаминовая), а щелочные свойства - основные аминокислоты (лизин, аргинин, гистидин).
Заряд белковой молекулы зависит от ионизации кислых и основных групп аминокислотных радикалов. В зависимости от соотношения отрицательных и положительных групп молекула белка в целом приобретает суммарный положительный или отрицательный заряд. При подкислении раствора белка степень ионизации анионных групп снижается, а катионных повышается; при подщелачивании - наоборот. При определенном значении рН число положительно и отрицательно заряженных групп становится одинаковым, возникает изоэлектрическое состояние белка (суммарный заряд равен 0). Значение рН, при котором белок находится в изоэлектрическом состоянии, называют изоэлектрической точкой и обозначают pI, аналогично аминокислотам. Для большинства белков pI лежит в пределах 5,5-7,0, что свидетельствует о некотором преобладании в белках кислых аминокислот. Однако есть и щелочные белки, например, сальмин - основной белок из молок семги (pl=12). Кроме того, есть белки, у которых pI имеет очень низкое значение, например, пепсин - фермент желудочного сока (pl=l). В изоэлектрической точке белки очень неустойчивые и легко выпадают в осадок, обладая наименьшей растворимостью.
Если белок не находится в изоэлектрическом состоянии, то в электрическом поле его молекулы будут перемещаться к катоду или аноду, в зависимости от знака суммарного заряда и со скоростью, пропорциональной его величине; в этом заключается сущность метода электрофореза. Этим методом можно разделять белки с различным значением pI.
Белки хотя и обладают свойствами буфера, но емкость их при физиологических значениях рН ограничена. Исключение составляют белки, содержащие много гистидина, так как только радикал гистидина обладает буферными свойствами в интервале рН 6-8. Таких белков очень мало. Например, гемоглобин, содержащий почти 8% гистидина, является мощным внутриклеточным буфером в эритроцитах, поддерживая рН крови на постоянном уровне.