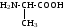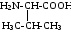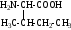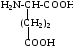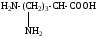- •Основы биологической химии предисловие
- •Введение Предмет и задачи биохимии
- •Основные признаки живой материи
- •Глава 1. Химический состав организмов
- •Глава 2. Структура и свойства белков
- •2.1. Роль и определение белков.
- •2.2. Функции белков в организме
- •2.3. Элементный состав белков. Содержание белков в органах и тканях
- •2.4. Аминокислотный состав белков
- •2.5. Кислотно-основные свойства аминокислот
- •2.6. Стереохимия аминокислот
- •2.7. Строение белков
- •2.8. Уровни структурной организации белков
- •Первичная структура
- •Вторичная структура белков
- •Третичная структура белков
- •Четвертичная структура белков
- •2.9. Физико-химические свойства белков
- •Кислотно-основные свойства белков
- •Растворимость белков
- •Денатурация и ренатурация
- •2.10. Классификация белков
- •2.11. Методы выделения и очистки белков
- •Очистка белков
2.4. Аминокислотный состав белков
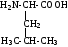
С химической точки зрения белки - это высокомолекулярные азотсодержащие органические соединения (полиамиды), молекулы которых построены из остатков аминокислот. Мономерами белков служат α-аминокислоты, общим признаком которых является наличие карбоксильной группы -СООН и аминогруппы -NH2 у второго углеродного атома (α-углеродный атом):

Аминокислоты классифицируют: - по полярности радикалов на полярные (гидрофильные) и неполярные (гидрофобные);
- по природе радикалов на алифатические (глицин, аланин, валин, лейцин, изолейцин); гидроксиаминокислоты (серии, треонин); дикарбоновые, кислые, (аспарагиновая, глутаминовая и их амиды - аспарагин и глутамин); тиоаминокислоты (цистеин, метионин); диаминомонокарбоновые, щелочные (лизин, аргинин); ароматические (фенилаланин, тирозин); гетероциклические (триптофан, гистидин, пролин).
В настоящее время известно более 200 аминокислот, существующих в природе. В организме человека содержится около 60 различных аминокислот и их производных. В белках же всех видов живых существ - от бактерий до человека - обнаруживают менее 30 из них.
Эти аминокислоты делят на две группы: постоянно встречающиеся в белках (главные) и иногда встречающиеся (редкие). К первой группе относят 20 аминокислот (в том числе и пролин, который, по существу, является иминокислотой) (табл.4).
Таблица 4. Аминокислоты, постоянно встречающиеся в составе белков
|
№ п/п |
Название |
Структура |
Сокращенное обозначение русское, латинское |
pI |
|
1 |
2 |
3 |
4 |
5 |
|
I. Неполярные(гидрофобные) аминокислоты |
||||
|
1. |
Аланин |
|
Ала, Ala |
6,02 |
|
2. |
Валин |
|
Вал, Val |
5,97 |
|
3. |
Лейцин |
|
Лей, Leu |
5,98 |
|
4. |
Изолейцин |
|
Иле, Ile |
6,02 |
|
5. |
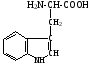
Триптофан |
|
Три, Try |
5,88 |
|
6. |
Пролин (иминокислота) |
|
Про, Pro |
6,10 |
|
7. |
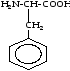
Фенилаланин |
|
Фен, Phe |
5,98 |
|
8. |
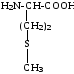
Метионин |
|
Meт, Met |
5,75 |
|
1 |
2 |
3 |
4 |
5 |
|
II. Полярные (гидрофильные) незаряженные аминокислоты |
||||
|
9. |
Глицин |
|
Гли, Gly |
5,97 |
|
10. |
Серин |
|
Сер, Ser |
5,68 |
|
11. |
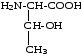
Треонин |
|
Тре, Thr |
6,53 |
|
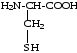
12. |
Цистеин |
|
Цис, Cys |
5,02 |
|
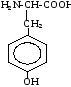
13. |
Тирозин |
|
Тир, Tyr |
5,65 |
|
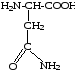
14. |
Аспарагин |
|
Асн, Asn |
5,41 |
|
15. |
Глутамин |
|
Гли,Gln |
5,65 |
|
1 |
2 |
3 |
4 |
5 |
|
III. Отрицательно заряженные (кислые) аминокислоты |
||||
|
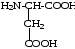
16. |
Аспарагиновая кислота (Аспартат) |
|
Асп, Asp |
2,95 |
|
17. |
Глутаминовая кислота (Глутамат) |
|
Глу, Glu |
3,22 |
|
IV. Положительно заряженные (основные) аминокислоты |
||||
|
18. |
Лизин |
|
Лиз, Lys |
9,74 |
|
19. |
Аргинин |
|
Арг, Arg |
10,76 |
|
20. |
Гистидин |
|
Гис, His |
7,58 |
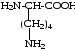
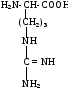
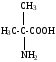
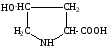
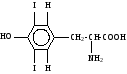
К группе редко встречающихся аминокислот принадлежат, например, гидроксипролин, гидроксилизин, орнитин, йодтирозин, α-аминоизомасляная кислота и некоторые другие. Они имеют следующее строение:
|
|
|
|
|
|
α-аминоизомасляная кислота |
гидроксипролин |
орнитин |
|
|
|
|
||
|
йодтирозин |
гидроксилизин |
||
Эти аминокислоты образуются из главных уже после включения их в состав белковой молекулы.