
- •Электролитическая диссоциация веществ
- •Электролиты. Неэлектролиты.
- •Теория электролитической диссоциации.
- •Свойства ионов
- •Механизм электролитической диссоциации. Гидратация ионов.
- •I. Механизм диссоциации электролитов с ионной связью в водных растворах
- •II. Механизм диссоциации электролитов с ковалентной полярной связью в водных растворах
- •Степень диссоциации.
- •Химическое равновесие. Закон действующих масс. Константа равновесия. Константа диссоциации.
- •Диссоциация кислот, оснований и солей. Амфолиты.
- •Реакции ионного обмена.
- •Правила написания реакций ионного обмена в растворах электролитов
- •Обратимые и необратимые реакции.
- •Свойства кислот, оснований и солей в свете теории электролитической диссоциации.
- •Качественные реакции на катионы и анионы.
- •Качественные реакции на катионы и анионы
- •Гидролиз. Гидролиз солей.
- •I. Понятие о гидролизе.
- •II. Типы солей.
- •III. Типы гидролиза
- •IV. Ступенчатость гидролиза
- •V. Степень гидролиза
- •VI. Практическая значимость гидролиза
- •Электролитическая диссоциация веществ
- •Электролитическая диссоциация веществ
Электролитическая диссоциация веществ
Лекция 1
Электролиты. Неэлектролиты.
Существует две основные причины прохождения электрического тока через проводники:
1) за счёт переноса электронов (характерно для металлов);
2) за счёт переноса ионов.
Ионная проводимость присуща многим химическим соединениям, обладающих ионным строением. По способности проводить электрический ток в водном растворе или расплаве вещества делятся на электролиты и неэлектролиты.
● Электролитами называются вещества, расплавы или растворы которых проводят электрический ток. К электролитам относятся соли, кислоты, основания. В молекулах этих веществ имеются ионные или ковалентные сильно полярные химические связи.
Демонстрационный эксперимент
Опыт 1 Проводимость электрического тока через кристаллический гидроксид натрия
К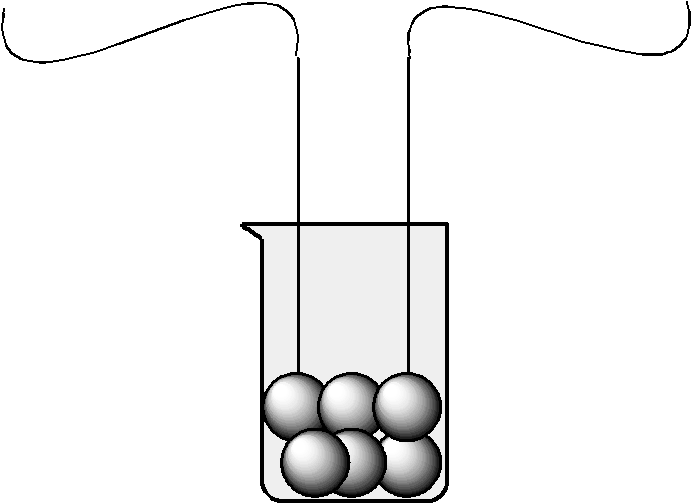 атод
(-) Анод (+)
В химический стакан помещается твёрдый
атод
(-) Анод (+)
В химический стакан помещается твёрдый
гидроксид натрия и от источника постоянного
тока пропускается электрический ток. Индикатором электропроводности служит лампочка, которая должна загореться.
Результат опыта: лампочка не горит
Вывод: кристаллический гидроксид натрия электрический ток не проводит
Рис 1 Проводимость электрического тока
через кристаллический гидроксид натрия
Опыт 2 Проводимость электрического тока через расплав гидроксида натрия
Катод (-) Анод (+) В фарфоровой чашке или ступке расплавляют
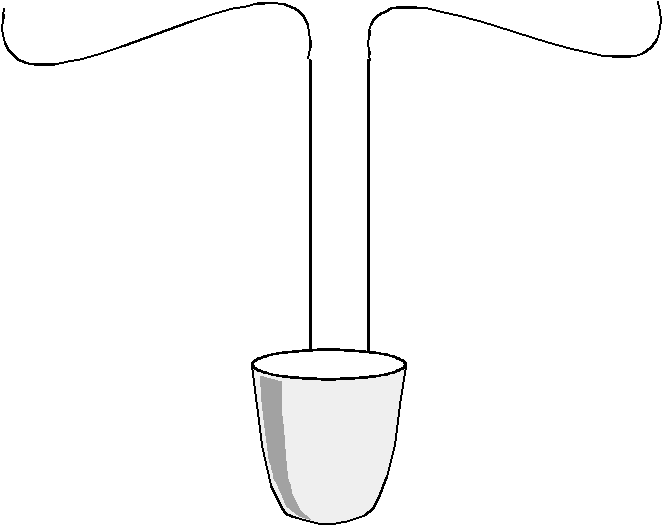 гидроксид натрия и от источника
постоянного
гидроксид натрия и от источника
постоянного
тока пропускаю электрический ток.
Индикатором электропроводности служит
лампочка, которая должна загореться.
Результат опыта: лампочка горит
Вывод: расплав гидроксида натрия
электрический ток проводит
Рис 2 Проводимость электрического тока
через расплав гидроксида натрия
Опыт 3 Проводимость электрического тока через водный раствор гидроксида натрия
К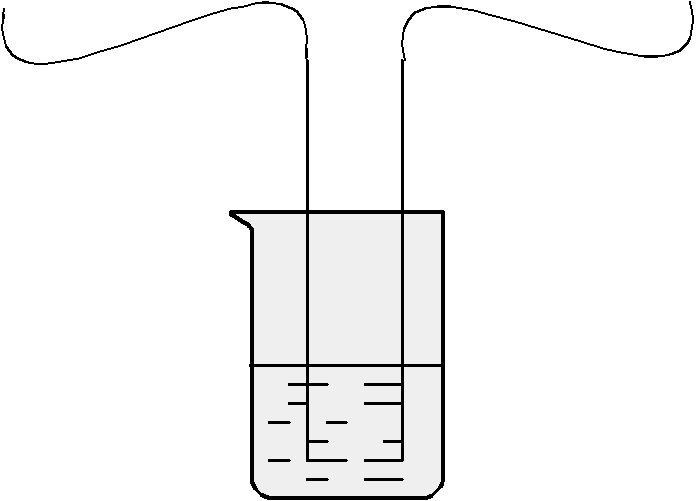 атод
(-) Анод (+) В химический
стакан наливают водный раствор
атод
(-) Анод (+) В химический
стакан наливают водный раствор
гидроксида натрия и от источника постоянного тока пропускают электрический ток. Индикатором электропроводности служит лампочка, которая должна загореться.
Результат опыта: лампочка горит
Вывод: водный раствор гидроксида натрия проводит электрический ток
Рис 3 Проводимость электрического тока
через водный раствор гидроксида натрия
● Неэлектролитами называются вещества, расплавы или растворы которых не проводят электрический ток. К ним относятся: кислород, водород, оксиды, многие органические вещества (сахар, бензол, эфир, спирты и др.). В молекулах этих веществ существуют ковалентные неполярные или малополярные связи.
Демонстрационный эксперимент
Опыт 4 Проводимость электрического тока через бензол
Опыт 5 Проводимость электрического тока через сахар
Опыт 6 Проводимость электрического тока через бутиловый спирт
Результатом всех опытов является отсутствие электропроводности этих веществ
Лекция 2
