
- •Издательство
- •Оглавление
- •Важнейшие классы неорганических соединений
- •Примеры решения задач
- •2. Эквивалент. Закон эквивалентов
- •Примеры решения задач
- •3. Строение атома и Периодическая система
- •Примеры решения задач
- •Степени окисления фосфора, серы, хлора
- •Билет 3.3
- •Билет 3.4
- •Билет 3.5
- •Билет 3.6
- •Билет 3.7
- •Билет 3.8
- •Билет 3.9
- •Билет 3.10
- •Билет 3.11
- •Билет 3.12
- •Билет 3.13
- •Билет 3.14
- •Билет 3.15
- •Билет 3.16
- •Билет 3.17
- •Билет 3.18
- •Билет 3.19
- •Билет 3.20
- •4. Химическая связь и строение молекул
- •5. Энергетика и направление химических процессов
- •Примеры решения задач
- •После подстановки справочных данных из табл.I получаем
- •Таким образом, тепловой эффект реакции равен –853,8 кДж, а DfH 0Fe2o3 составляет –822,2 кДж/моль.
- •Используя справочные данные табл.I получаем:
- •Решение. Вычисляем dh0х.Р. И ds0х.Р.:
- •Энергию Гиббса при соответствующих температурах находим из соотношения
- •При сгорании 1 л с2н4 (н.У.) выделяется 59,06 кДж теплоты. Определите стандартную энтальпию образования этилена. (Ответ: 52,3 кДж/моль).
- •5.3. Сожжены с образованием h2o(г) равные объемы водорода и ацетилена, взятых при одинаковых условиях. В каком случае выделится больше теплоты? Во сколько раз? (Ответ: 5,2).
- •6. Скорость химической реакции
- •Примеры решения задач
- •7. Химическое равновесие
- •Примеры решения задач
- •8. Способы выражения концентрации растворов
- •Примеры решения задач
- •4,37 Моль/кг
- •9. Свойства разбавленных растворов неэлектролитов
- •Примеры решения задач
- •10. Реакции обмена в растворах электролитов
- •Примеры решения задач
- •11. Ионное произведение воды. Водородный показатель. Гидролиз солей.
- •Примеры решения задач
- •12. Коллоидные растворы
- •Примеры решения задач
- •13. Окислительно-восстановительные реакции
- •Примеры решения задач
- •14. Электродные потенциалы. Гальванические элементы Коррозия металлов
- •Примеры решения задач
- •Для первого электрода:
- •Для второго электрода:
- •15 Электролиз
- •Законы электролиза
- •Примеры решения задач
- •Библиографический список
- •Приложение
Примеры решения задач
Пример 3.1. Напишите электронную формулу атома ванадия 23V и: а) подчеркните валентные электроны; б) укажите электронное семейство, период, группу, подгруппу, в которых находится элемент; в) изобразите графически валентные энергетические уровни; г) охарактеризуйте квантовыми числами валентные электроны; д) составьте формулу высшего оксида ванадия и соответствующего ему гидроксида.
Решение. Порядковый номер ванадия (V) в периодической системе 23. Следовательно, положительный заряд ядра равен +23 и столько же электронов в атоме ванадия. Поскольку ванадий находится в 4 периоде, электроны располагаются на 4-х энергетических уровнях следующим образом: 23V 2е, 8е, 11е, 2е. Запись электронной конфигурации атома по уровням и подуровням имеет вид 1s22s22p63s23p63d34s2. Валентные электроны ванадия 3d34s2.
Ванадий отностися к d-электронному семейству и расположен в 4 периоде, VВ группе (побочнаяподгруппа).. Валентные энергитические уровни ванадия 3d и 4s и валентные электроны располагаются на них следующим образом:
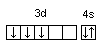
Каждый электрон в атоме характеризуется набором четырех квантовых чисел: n, l, ml, ms. Главное квантовое число n обозначается арабской цифрой и равно номеру уровня, на котором находится электрон. Для 3d электронов главное квантовое число n равно 3, для 4s электронов – n = 4.
В электронных формулах орбитальное квантовое число обозначается буквой l. Напоминаем, что
Орбитальное квантовое число l 0 1 2 3
Обозначение энергетического подуровня s p d f.
Для электронов, находящихся на d-подуровне, l = 2; для электронов s-подуроння l = 0.
Электроны находятся на разных орбиталях, которые ориентированы по разным направлениям. Ориентацию АО в пространстве определяет магнитное квантовое число ml, значение которого зависит от орбитального квантового числа l. Если l=2, ml принимает значение –2, –1, 0, +1, +2; при l = 0 ml = 0.
Спиновое квантовое число ms принимает значения +½ и –½. Таким образом, электроны состояния 3d 3 и 4s2 характеризуются следующими квантовыми числами:
|
N |
n |
l |
ml |
ms |
|
1 |
3 |
2 |
-2 |
+1/2 |
|
2 |
3 |
2 |
-1 |
+1/2 |
|
3 |
3 |
2 |
0 |
+1/2 |
|
4 |
4 |
0 |
0 |
+1/2 |
|
5 |
4 |
0 |
0 |
-1/2 |
Формула высшего оксида ванадия V2O5. Это кислотный оксид и в качестве гидроксида ему соответствует кислота НVO3.
Пример 3.2. Какие орбитали атома заполняются электронами раньше 5d или 6s; 4f или 6p?
Решение. Последовательность заполнения орбиталей осуществляется в соответствии с правилом Клечковского и определяется суммой (n+l). Для подуровня 5d сумма (n+l) равна (5+2) = 7, для подуровня 6s (6+0) = 6. В первую очередь заполняются орбитали с меньшей энергией, следовательно, вначале заполняется 6s, потом 5d. Для подуровней 4f и 6р сумма (n+l) одинакова (4+3) = 7 и (6+1) = 7. При одинаковом значении суммы (n+l) раньше заполняется подуровень с меньшим n, следовательно, 4f.
Пример 3.3. Запишите электронную конфигурацию ионов Fe3+ и S2–.
Решение. Электронная конфигурация атома железа 26Fe 1s22s22p63s23p63d64s2. Если атом железа отдаст три электрона, он превратится в ион: Fe0 – 3e → Fe3+. В первую очередь атом отдает электроны с более высокого энергетического уровня и подуровня. Электронная конфигурация ионов Fe3+ имеет вид 1s22s22p63s23p63d54s0. Электронная конфигурация атома серы 16S 1s22s22p63s2 3p4. Приняв два электрона S0 + 2e → S2–, атом серы превращается в ион S2–, электронная конфигурация которого 1s22s22p63s23p6.
Пример 3.4. Какую высшую и низшую степени окисления проявляют фосфор, сера, хлор? Составьте формулы соединений данных элементов, отвечающих этим степеням окисления.
Решение. Данные элементы находятся соответственно в VA, VIA, VIIA-группах и имеют электронную конфигурацию внешнего энергетического уровня 3s23p3; 3s23p4; 3s23p5.
