
- •Глава 5. Электролиз расплавленных сред [35-39].
- •5.1. Производство алюминия
- •5.1.1. Подготовка сырья
- •5.1.2. Аноды в производстве алюминия
- •5.1.3. Конструкции электролизеров для получения алюминия
- •5.1.4. Электролизеры с непрерывными самообжигающимися
- •5.1.5. Электролизер для получения алюминия с боковым
- •5.1.6. Вспомогательное оборудование Вакуумный ковш для удаления алюминия.
- •5.1.7. Рафинирование алюминия
- •5.1.8. Новые направления в конструировании
- •5.1.9. Ошиновка электролизеров
Глава 5. Электролиз расплавленных сред [35-39].
Электролизом расплавленных сред получают металлы, такие как алюминий, магний, натрий, литий и многие другие. Важнейшими из них являются алюминий и магний, постоянно увеличивается производство лития, используемого в химических источниках тока. С электрохимическими процессами тесно связано получение и рафинирование титана. Будучи наиболее отрицательными металлами в ряду напряжений, легкие металлы не могут быть выделены электролизом водных растворов, так как в этом случае на катоде выделяется водород. Электролитами, не содержащими свободных ионов водорода являются расплавленные соли, электролиз которых и служит основным промышленным способом производства. Рассмотрим основное и вспомогательное оборудование наиболее значимых и характерных производств.
5.1. Производство алюминия
Получение алюминия базируется на трех независимых, но тесно связанных производствах: непосредственно электролизном, подготовки сырья и производстве анодов (или анодной массы).
Алюминий получают электролизом глинозема - мелкодисперсного оксида алюминия Al2O3:
2![]()
В природе в чистом виде глинозем не встречается, наиболее богатыми оксидом алюминия рудами являются бокситы, нефелины и каолин. Однако в состав этих минералов входят также оксиды и гидроксиды железа, кремния, кальция, титана и других более электроположительных элементов, способных восстанавливаться на катоде параллельно алюминию и загрязнять его. Поэтому, на первом этапе подготовки сырья необходимо удаление этих примесей, а на втором - сушка продукта, так как примесь воды резко уменьшает выход по току алюминия и нарушает технологический процесс электролиза.
Анодный материал, применяемый в производстве алюминия, должен иметь высокую электропроводность, стойкость к действию глиноземно-криолитового расплава, инертность по отношению к алюминию, быть механически прочным, дешевым и доступным. В качестве анодного материала в настоящее время используется уголь, отвечающий практически всем выше перечисленным требованиям, кроме одного. Угольный анод интенсивно сгорает при выделении на нем кислорода:
С + О2 = СО2
СО2 + С = СО
Сгорание анода при электролизе (на 2 см в сутки) требует постоянной регулировки межэлектродного расстояния и пополнения массы анода. Все имеющиеся на сегодня конструкции алюминиевых электролизеров определяются именно этими требованиями. Значительно упростить конструкцию и ее обслуживание можно только при условии создания принципиально нового анодного материала. Наиболее перспективным является металлокерамический электрод, спеченный из тугоплавких оксидов металлов, обладающих электронной проводимостью при высоких температурах.
5.1.1. Подготовка сырья
Приготовление сырья и анодной массы не является электрохимическими процессами. Они вообще могут производиться на отдельных специальных заводах. Поэтому в данном курсе они будут рассмотрены схематично.
Способы получения глинозема зависят от выбора исходных материалов и концентрации примесей в них. Поэтому эти способы отличаются большим разнообразием. В качестве примера рассмотрим получение глинозема методом русского ученого Байера, который заключается в обжиге бокситов, выщелачивании, отделении примесей и сушке.
Бокситы - сложная горная порода, в которую входят гидраты окислов алюминия, железа, кремния, титана и др. На первых стадиях боксит проходит обогащение - мойку проточной водой для удаления песка и глины. Следующими стадиями является дробление в молотковых дробилках и измельчение в шаровых мельницах. Обогащенный боксит поступает на очистку от примесей, которая осуществляется выщелачивании и последующем “выкручивании” глинозема.
Для выщелачивания применяют 40% раствор NaOH при температуре 160-170оС, процесс ведут около 3 часов. При выщелачивании протекают реакции растворения оксида алюминия и кремния:
AlOOH + NaOH=NaAlO2 + H2O
SiO2 + NaOH = Na2SiO3 + H2O
Алюминат и силикат натрия взаимодействуют между собой с образованием нерастворимого соединения, окрашенного примесями железа в бурый цвет -“красного шлама” :
2NaAlO2 +2Na2SiO3 + 4H20 = Na2O*Al2O3*SiO2*2H2O + 4NaOH
Красный шлам идет в отвалы, при этом неизбежно теряется часть алюминия и щелочи.
Выщелачивание ведут в автоклавах (см. первую главу) при помощи острого пара. После выщелачивания пульпа подается в испарители, затем промывается водой в агитаторах-осветлителях. При промывке происходит разложение алюминатного раствора (гидролиз) в аппаратах - декомпозерах, так называемое “выкручивание”:
NaAlO2 + 2H2O = NaOH + Al(OH)3
В операции выкручивания могут применяться декомпозеры с воздушным (пачук) и механическим перемешиванием. Аппараты с механическим перемешиванием (рис.5.1.) соединяются последовательно в секции из 9-10 штук. Выкручивание осуществляется непрерывно. В головные аппараты поступает алюминатный раствор и затравка гидроокиси алюминия. Скорость протока выбирается так, чтобы от головного до хвостового декомпозера раствор проходил за время 96-120 час. Гидратная пульпа из хвостового декомпозера направляется в виде готовой затравки в головные декомпозеры (до 75%) , а остальная часть идет на промывку. Процесс продолжается 75-90 часов.
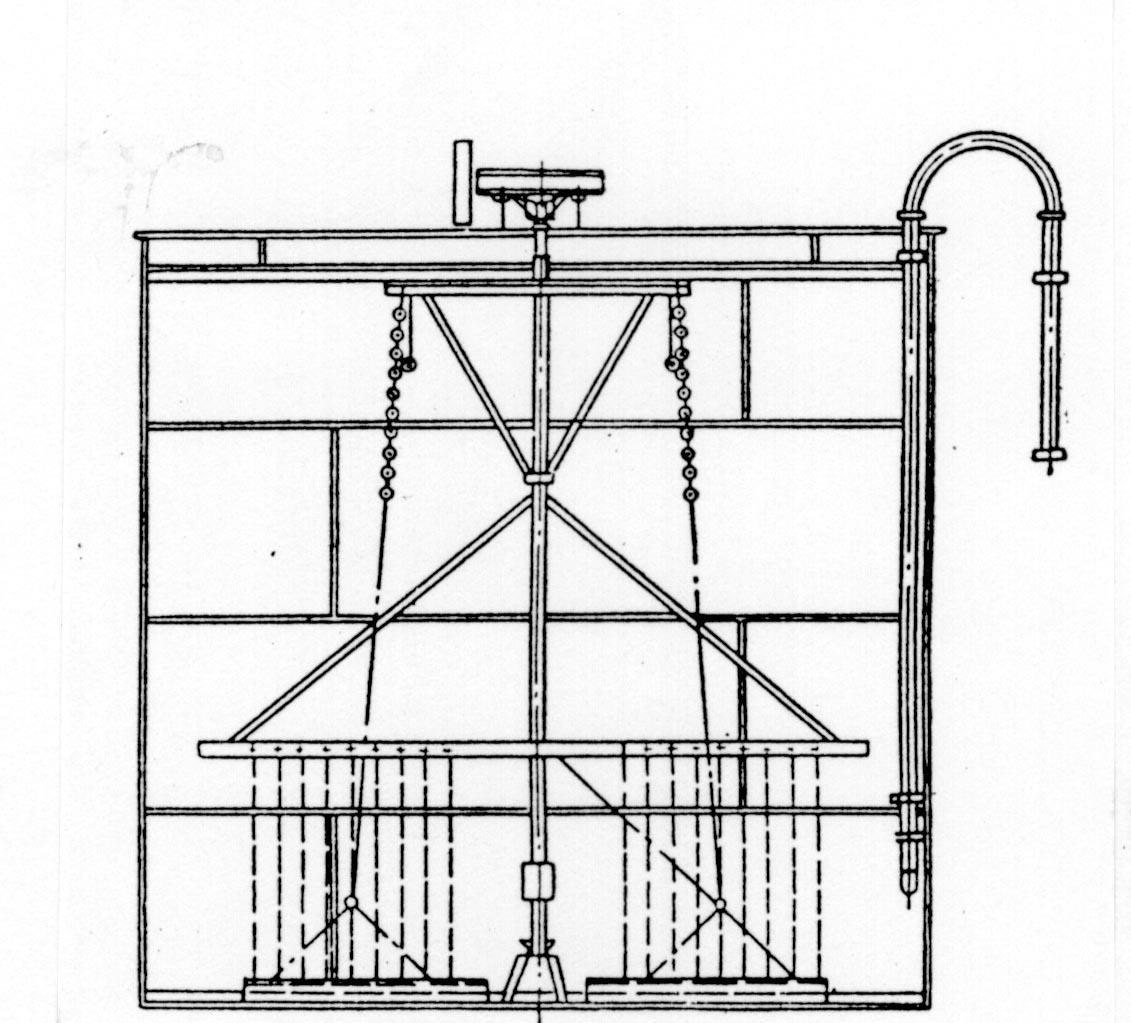
Рис.5.1. Декомпозер с механическим перемешиванием.
Маточный раствор после выкручивания содержит до 140 г/л Na2О и идет на выпаривание, промывные воды - на разбавление пульпы. При выпаривании из раствора выпадают кристаллы карбоната натрия. Для регенерации их обрабатывают гашеной известью Ca(OH)2 и направляют на выщелачивание бокситов.
Полученный гидрат окиси алюминия направляется на сушку-обжиг (кальцинацию) для получения безводного глинозема. Обработку ведут при температуре 1150-1200оС, поскольку процесс превращения Al(OH)3 в Al2O3 завершается именно при этих температурах. Для кальцинации применяют вращающиеся трубчатые печи (см. первую главу).
Чистый глинозем имеет температуру плавления около 2050оС. Для поддержания такой высокой температуры требуются большие энергозатраты, она ограничивает возможность применения многих конструкционных материалов, жидкий алюминий кипит при этой температуре. Поэтому при получении алюминия используется не чистый глинозем, а низкоплавкая эвтектика с криолитом -Na3AlF6, в которой растворяется Al2O3. Природный криолит мало доступен, поэтому обычно применяют криолит искусственного происхождения. Основным сырьем для его получения является плавиковый шпат CaF2. Криолит из плавикового шпата может быть получен двумя методами - кислотным и щелочным. В кислотном методе размолотый и обогащенный плавиковый шпат нагревают в печах до 200оС в присутствии серной кислоты. При этом получают сульфат кальция и плавиковую кислоту. Полученная плавиковая кислота взаимодействует с гидроксидом алюминия и содой:
12HF + 2Al(OH)3 + 3Na2CO3=2Na3AlF6 + 9H2O + 3CO2
Осадок криолита после фильтрации и сушки в барабанных сушилах с паровым обогревом при 150оС является целевым продуктом.
Щелочной способ производства криолита основан на спекании плавикового шпата с содой при 825-875оС с получением фторида натрия. Фторид натрия взаимодействует с алюминатом натрия и при последующей карбонизации получается криолит:
6NaF + NaAlO2 + 2CO2 = Na3AlF6 + 2Na2CO3
Карбонизация продолжается 7 - 8 часов при 70-75 оС . Щелочной метод более экологически чист, менее чувствителен к примесям и менее агрессивен к оборудованию.
