
- •Башкирский государственный аграрный университет
- •Р.И. Галеева, е.В. Тальвинский, и.А. Сагитдинов
- •Практикум
- •По органической химии
- •Оглавление
- •Введение
- •Методика тушения некоторых видов пожаров в химических лабораториях
- •1 Предельные и непредельные углеводороды Алканы
- •Вопросы для контроля
- •Упражнения по теме «Алканы»
- •Вопросы для контроля
- •Упражнения по теме «Алкены»
- •Опыт 1.4 Получение этина и изучение его свойств
- •Вопросы для контроля
- •Упражнения по теме «Алкины»
- •2 Ароматические углеводороды Арены
- •Лабораторная работа
- •Опыт 2.1 Растворимость бензола в воде
- •Опыт 2.2 Окисление боковых цепей гомологов бензола
- •Вопросы для контроля
- •Упражнения по теме «Ароматические углеводороды»
- •3 ГалогенОпроизводные углеводородов
- •Лабораторная работа
- •Опыт 3.1 Получение хлорэтана из этанола
- •Опыт 3.2 Получение хлороформа из хлоральгидрата
- •Опыт 3.3 Получение иодоформа из этанола
- •И в боковой цепи
- •Вопросы для контроля
- •Упражнения по теме «Галогенопроизводные углеводородов»
- •4 Спирты
- •Лабораторная работа
- •Опыт 4.1 Получение этилата натрия
- •Опыт 4.2 Реакция глицерина с гидратом окиси меди в щелочной среде
- •Опыт 4.4 Получение диэтилового эфира
- •Опыт 4.5 Получение этилового эфира этановой кислоты
- •Вопросы для контроля
- •Упражнения по теме «Спирты»
- •5 Фенолы
- •Опыт 5.3 Образование трибромфенола
- •Опыт 5.4 Доказательство кислотного характера фенола
- •Опыт 5.5 Цветные реакции фенолов с хлорным железом
- •Вопросы для контроля
- •Упражнения по теме: «Фенолы»
- •6 Оксосоединения Альдегиды и кетоны
- •Лабораторная работа
- •Опыт 6.1 Окисление метаналя аммиачным раствором окиси
- •Опыт 6.3 Получение ацетона из ацетата натрия
- •Опыт 6.4 Открытие пропанона в виде 2,4-динитрофенилгидрозона
- •Вопросы для контроля
- •Упражнения по теме «Альдегиды и кетоны»
- •7 Карбоновые кислоты и их производные
- •Лабораторная работа №
- •Опыт 7.2 Окисление муравьиной кислоты марганцевокислым калием
- •Опыт 7.4 Получение натриевой соли щавелевой кислоты
- •Образование биурета и циануровой кислоты
- •Вопросы для контроля
- •Упражнения по теме: «Карбоновые кислоты и их производные»
- •8 Амины
- •Лабораторная работа
- •Опыт 8.1 Реакция первичного амина с азотистой кислотой (пример дезаминирования)
- •Вопросы для контроля
- •Упражнения по теме: «Амины»
- •9 Оксикислоты
- •Виннокаменной кислоте.
- •Вопросы для контроля
- •Упражнения по теме «Оксикислоты»
- •10 Углеводы
- •Моносахариды
- •Лабораторная работа
- •В присутствии щелочи
- •Вопросы для контроля
- •Упражнения по теме «Простые сахара»
- •Дисахариды и полисахариды
- •Лабораторная работа
- •(Тростниковом сахаре)
- •Вопросы для контроля.
- •Упражнения по теме «Дисахариды и полисахариды»
- •11 Аминокислоты, белки
- •Лабораторная работа
- •Принцип формольного титрования
- •(Цистин, цистеин)
- •Вопросы для контроля
- •Упражнения по теме «Аминокислоты. Белки»
- •12 Гетероциклические соединения
- •Лабораторная работа
- •С хлоридом железа (III)
- •Натриевой соли в воде
- •(Выделение кристаллической мочевой кислоты)
- •Вопросы для контроля
- •Упражнения по теме «Гетероциклические соединения»
(Цистин, цистеин)
Налить в пробирку 3 капли раствора уксуснокислого свинца и 1-2 капли едкого натра до растворения образовавшегося осадка гидроокиси свинца.
Прибавить 3-4 капли белка и смесь осторожно нагреть. Раствор начинает темнеть (выделяется осадок сернистого свинца).
Вопросы для контроля
1. Классификация аминокислот. Заменимые и незаменимые аминокислоты.
2. Амфотерный характер аминокислот.
3. Химические свойства аминокислот. Отношение их к нагреванию.
4. Получение аминокислот.
5. Получение ди-, три- и полипептидов. Пептидная связь.
6. Классификация белков. Простые и сложные белки.
7. Строение белковой молекулы: первичная, вторичная, третичная и четвертичная структура белка.
Упражнения по теме «Аминокислоты. Белки»
1. Напишите все изомеры аминокислот состава С4Н9О2N (их пять). Назовите их по номенклатуре ИЮПАК.
2. Напишите реакцию изомасляной кислоты с бромом и полученного соединения с избытком аммиака.
3. Напишите уравнения реакций взаимодействия с водным раствором щелочи и с соляной кислотой следующих аминокислот:
а) глицина; б) аланина; в) фенилаланина.
4. Подвергните нагреванию -, β-, γ-аминовалериановые кислоты. Назовите полученные соединения.
5. Напишите уравнения реакций действия азотистой кислоты на:
а) глицин; б) аланин; в) серин.
6. Напишите уравнение реакции декарбоксилирования следующих аминокислот: а) лизин; б) орнитин.
7. Напишите уравнения реакции гидролиза:
а) аланилглицина; б) аланилаланина; в) глицилсерина.
8. Предложите схему синтеза аланина из этилового спирта. Для аминокислоты напишите уравнения реакции:
а) с HCl; б) с NaOH; в) с HNO3.
9. Напишите формулы промежуточных и конечных продуктов в схеме:
![]()
10. Напишите схему следующих превращений:
аланин t0 → дикетопиперазин Н2О → дипептид.
11. Дополните схему следующих превращений:
3-амино-2-метилбутановая кислота t0
→ А
![]() Б
Б
![]() В
В
Назовите конечный продукт.
12. Из ацетилена получите аланин.
13. Из этилена получите аланил-глицин.
14. Напишите формулы следующих трипептидов:
а) аланил-глицил-серин;
б) глицил-фенилаланил-аланин;
в) глицил-лизил-триптофан.
15. С аланином проведите следующие реакции:
а) с этиловым спиртом;
б) с аммиаком;
в) с гидроксидом меди.
12 Гетероциклические соединения
Циклические соединения, у которых циклы образованы не только углеродными атомами, но и атомами других элементов – гетероатомами (О, S, N), - называются гетероциклическими. Гетероциклические соединения делят по размерам цикла и числу гетероатомов в цикле.
Среди этих соединений наибольшее значение имеют пяти- и шестичленные гетероциклические соединения. Типичные гетероциклические соединения обладают ароматическим характером. Однако, наличие гетероатома сказывается на распределении электронной плотности. Например, в пятичленных гетероциклах (в фуране, тиофене, пирроле) электронная плотность смещена от гетероатома в сторону кольца и максимальна в -положениях. Поэтому в -положениях наиболее легко идет реакция электрофильного замещения (SЕ).
В шестичленных циклах (например, пиридине) гетероатом, связанный с углеродом двойной связью, оттягивает на себя -электронную плотность цикла, поэтому электронная плотность в молекуле пиридина понижена в и -положениях. Это согласуется с предпочтительной ориентацией в эти положения реагентов при нуклеофильном замещении (SN). Так как в пиридине электронная плотность больше в - положении, то электрофильный реагент ориентируется в - положение.
При изучении гетероциклов с двумя гетероатомами особо обратить внимание на пиримидин и его производные: урацил, тимин, цитозин. Пиримидиновое ядро встречается в многочисленных природных продуктах: витаминах, коферментах и нуклеиновых кислотах:
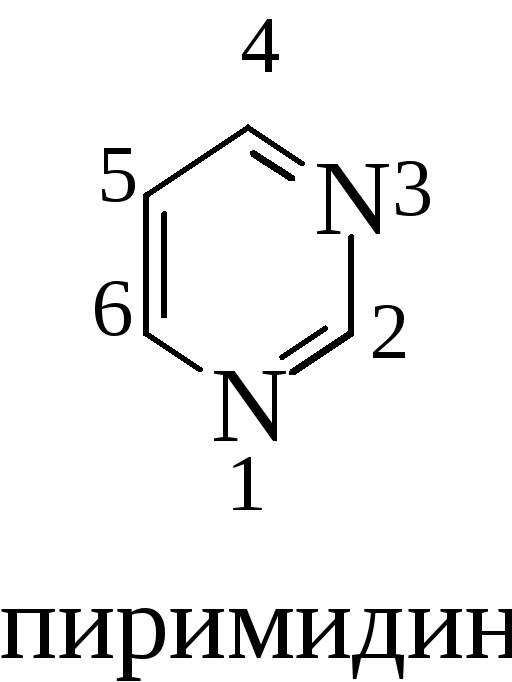
Электрофильное замещение для пиримидина проходит в положении 5; нуклеофильное (как и для пиридина) затруднено и атаке подвергается атом углерода в положениях 4 и 6.
Сложная гетероциклическая система, состоящая из двух конденсированных гетероциклов – пиримидина и имидазола называется ядром пурина.
Пуриновая группировка лежит в основе многих соединений, прежде всего нуклеиновых кислот, в которые она входит в виде пуриновых оснований: аденина (6-аминопурин) и гуанина(2-амино-6-оксипурин).
Интерес представляет кислородное производное пурина - мочевая кислота (2,6,8 – триоксипурин).
