
- •Оглавление
- •Введение
- •Молекулярно-кинетическая теория идеальных газов
- •Которое называется распределением Больцмана. Лабораторная работа 7 Определение постоянной Больцмана
- •Лабораторная работа Определение универсальной газовой постоянной
- •2. Явления переноса в термодинамически неравновесных системах
- •Лабораторная работа 13-1 Определение динамического коэффициента вязкости методом пуазейля
- •Лабораторная работа 13-2 Определение динамического коэффициента вязкости методом Стокса
- •Лабораторная работа Определение средней длины свободного пробега и эффективного диаметра молекул воздуха
- •Лабораторная работа Определение коэффициента теплопроводности твердых тел
- •3. Термодинамика
- •Взаимосвязь между внутренней энергией, работой и теплотой (первый закон термодинамики)
- •Второе начало термодинамики
- •В незамкнутой системе энтропия всегда возрастает. Функция состояния, дифференциалом которой является , называется приведенной теплотой.
- •Основное уравнение термодинамики. Это уравнение объединяет формулы первого и второго начала термодинамики:
- •Подставим уравнение (3.9), выражающее второе начало термодинамики, в равенство (3.10):
- •Лабораторная работа 9 Определение отношения теплоемкостей газов методом клемана - дезорма
- •Лабораторная работа 11 Определение изменения энтропии при изохорическом процессе в газе
- •Лабораторная работа 10 Определение адиабатической постоянной по скорости звука в воздухе
- •4. Свойства жидкостей
- •Лабораторная работа 12 Определение коэффициента поверхностного натяжения жидкости
- •Заключение
- •Библиографический список
- •Фундаментальные физические константы
- •Некоторые внесистемные единицы
- •Постоянные газов (при нормальных условиях)
Лабораторная работа Определение универсальной газовой постоянной
Цель работы: экспериментально определить универсальную газовую постоянную методом откачки.
Методика эксперимента
Универсальную газовую постоянную R можно определить из уравнения (1.7) Менделеева-Клапейрона
![]() , (1.26)
где
p
– давление; V
– объём; m
– масса;
– молярная масса газа.
, (1.26)
где
p
– давление; V
– объём; m
– масса;
– молярная масса газа.
Рассматривая уравнение (1.26) для двух масс m1 и m2 одного и того же газа при одинаковых температурах T и объёме V, получим выражения для универсальной газовой постоянной:
 . (1.27)
. (1.27)
Если определить давление p1 и температуру Т для некоторой массы газа m1, заключенной в сосуде объёмом V, а затем изменить массу газа до m2 (например, откачав газ) и вновь определить давление оставшегося газа p2, то по формуле (1.27) можно рассчитать универсальную газовую постоянную R.
Начальную массу газа m1 можно вычислить по формуле
m1 = V, где – плотность; V – объём газа.
Масса откачанного газа m2 = V0,
где V0 – объем откачанного газа.
Тогда масса оставшегося газа в сосуде
m1 – m2 = (V – V0).
Подставляя последнее выражение в уравнение (1.27), получим:
 . (1.28)
. (1.28)
Э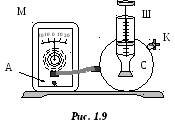 ксперимент
выполняется на установке (рис. 1.9),
состоящей из сосуда С (полый металлический
цилиндр), имеющего три вывода. Один вывод
соединен со шприцем Ш, второй – с
микроманометром М, а в третий впаян кран
К, сообщающий сосуд с атмосферой.
Перемещая поршень шприца, можно откачать
из сосуда С некоторый объем V0
воздуха, меняя массу и давление воздуха
в нем. Изменение давления в сосуде С
фиксируется микроманометром, шкала
которого проградуирована в миллиметрах
водного столба.
ксперимент
выполняется на установке (рис. 1.9),
состоящей из сосуда С (полый металлический
цилиндр), имеющего три вывода. Один вывод
соединен со шприцем Ш, второй – с
микроманометром М, а в третий впаян кран
К, сообщающий сосуд с атмосферой.
Перемещая поршень шприца, можно откачать
из сосуда С некоторый объем V0
воздуха, меняя массу и давление воздуха
в нем. Изменение давления в сосуде С
фиксируется микроманометром, шкала
которого проградуирована в миллиметрах
водного столба.
Порядок выполнения работы
-
Открыв кран К, поставить поршень в шприце в начальное (нулевое) положение. кран закрыть.
-
Арретиром А микроманометра установить стрелку в нулевое положение.
-
Перемещая поршень в шприце, откачать из сосуда С воздух. Объём откаченного воздуха V0 записать в таблицу 1.2.
-
Определить по микроманометру давление р2, записать в таблицу.
-
Повторить три раза п. 1 – 4.
-
Записать в таблицу показания термометра (температура воздуха в лаборатории Т ) и барометра (атмосферное давление p1).
Таблица 1.2
-
V0, см3
p2,
мм вод.ст.
Параметры
постоянные
R

p1 = мм.рт.ст
p1 = Па
Т = К
= 2910-3 кг/моль
= 1, 293 кг/м3
1 мм рт.ст.=133,3 Па
1 мм вод.ст. =9,81 Па
Обработка результатов измерений
-
По формуле (1.28) вычислить универсальную газовую постоянную для каждого эксперимента, переведя все входящие в нее величины в СИ.
-
Рассчитать среднее значение универсальной газовой постоянной
 .
. -
Сравнить полученное значение универсальной газовой постоянной
 с табличным. Сделать вывод по проделанной
работе.
с табличным. Сделать вывод по проделанной
работе.
Контрольные вопросы и задания
-
Какой физический смысл имеет универсальная газовая постоянная R? (используйте первое начало термодинамики для изобарического и изохорического процессов и формулу Майера)
-
Укажите единицы измерения универсальной газовой постоянной R в СИ.
-
Запишите основное уравнение молекулярно-кинетической теории идеальных газов (МКТ) и выведите из него уравнение Клапейрона-Менделеева.
-
Поясните метод определения универсальной газовой постоянной R в данной работе.
