
- •Жидкостная хроматография
- •1. Общая характеристика
- •2. Колоночная жидкостная хроматография
- •2.1. Устройство жидкостного хроматографа
- •Детектор
- •2.2. Сорбенты для жидкостной хроматографии
- •2.2.1 Общая характеристика
- •2.2.2 Материалы для сорбентов
- •2.3. Растворители и подвижные фазы
- •2.3.1 Общая характеристика
- •2.3.2 Характеристика элюирующей способности растворителя
- •3. Характеристика отдельных видов колоночной жидкостной хроматографии
- •3.1. Адсорбционная хроматография
- •3.2. Распределительная хроматография
- •Оптимизация процесса разделения
- •3.3. Ионообменная хроматография как классический и высокоэффективный метод
- •3.3.1. Классическая ионообменная хроматография Неподвижные фазы
- •Подвижные фазы
- •3.3.2. Ионная хроматография
- •Неподвижные фазы
- •Детектирование
- •Варианты ионной хроматографии
- •3.4. Эксклюзионная хроматография
- •4. Практическое применение вэжх
- •5. Плоскостная хроматография
- •5.1. Тонкослойная хроматография
- •5.1.1. Неподвижные и подвижные фазы
- •5.1.2. Методика получения плоскостной хроматограммы
- •5.1.3 Анализ плоскостных хроматограмм
- •5.1.4. Практическое применение
5.1.4. Практическое применение
Тонкослойная хроматография используется как для обнаружения и идентификации веществ (качественный анализ), так и для их количественного определения (количественный анализ).
Качественный анализ

Разделяемые компоненты образуют на хроматографической пластинке или полоске хроматографической бумаги отдельные зоны (пятна). Примерный вид плоскостной хроматограммы показан на рисунке 15.
Рис.
15
Примерный вид плоскостной хроматограммы
Физические методы. Из физических методов для идентификации пятен наиболее часто применяют флуоресценцию. В этом случае пластинку помещают в УФ излучение (обычно флуоресценция вызывается облучением с длиной волны 254 или 365 нм). При обнаружении соединений, обладающих собственной флуоресценцией, они видны на хроматограмме в виде светящихся разным цветом пятен. Для обнаружения нефлуоресцирующих соединений предварительно пропитывают слой сорбента флуоресцентным индикатором (люминофором). Пятна исследуемых соединений можно наблюдать в виде темных зон на желто-зеленом или голубом фоне (в зависимости от люминофора).
Химические методы. При обнаружении соединений химическим методом хроматограмму после окончания разделения обрабатывают различными реагентами. Часто для протекания реакции пластинку необходимо нагревать до определенной температуры. Различают реагенты универсальные, используемые для обнаружения многих соединений, и специфические (групповые), действующие на определенный класс исследуемых соединений. К универсальным реагентам относятся растворы сильных окислителей (например, HNO3, KMnO4 или H2SO4), пары аммиака, брома иода. К специфическим реагентам относится большое количество химических веществ, которые выбирают в зависимости от химических свойств обнаруживаемых веществ. Некоторые из реагентов, используемых для проявления хроматограмм, показаны в таблице 8.
|
Таблица 8 |
Некоторые реагенты-проявители, используемые в плоскостной хроматографии |
|
|
Реагент |
Обнаруживаемые Вещества |
Аналитический эффект |
|
Нингидрин |
Аминокислоты, пептиды, первичные амины |
Синее (пурпурное, коричневое и др.) окрашивание |
|
Реактив Драгендорфа K[BiI4] |
Третичные амины и четвертичные аммониевые соединения |
Тёмно-оранжевые пятна на жёлтом фоне |
|
Раствор SbCl3 в хлороформе |
Стероиды |
Фиолетовое окрашивание |
|
FeCl3 |
Фенолы, легкоокисляющиеся вещества (анальгин, амидопирин и др.) |
Сине-фиолетовое, красно-фиолетовое и др. окрашивание на жёлтом фоне |
|
2,4-Динитрофенилгидразин |
Альдегиды, кетоны |
Жёлтое окрашивание, переходящее в красно-коричневое при обработке 10%-ным NaOH |
Биологические методы. К ним относятся биоавтография и фермент-субстратная реакция. Их используют для анализа биологически активных соединений. Например, при обнаружении стимуляторов роста или витаминов определяется степень роста зон микроорганизмов, а при обнаружении антибиотиков – степень их ингибирования. Биологические методы обладают высокой чувствительностью и избирательность, однако на их проведение требуются большие затраты времени – от нескольких часов до нескольких дней.
Идентификацию соединений в методе ТСХ обычно проводят путем сравнения значений Rf пятен анализируемого и стандартного вещества. При этом растворы стандартных веществ наносятся на пластинку рядом с пятном исследуемого вещества и хроматографируются одновременно в тех же условиях. В случае совпадения величин Rf (Rf ± 0.02) у пятен компонентов исследуемой пробы с пятнами стандартных веществ делают заключение об идентичности соединений. Дополнительным подтверждением идентичности являются одинаковая окраска под воздействием химических реагентов, одинаковая реакция на УФ излучение.
Если состав пробы неизвестен или стандартные вещества недоступны, то идентификацию веществ можно проводить, используя литературные данные, описывающие детектирование пятен веществ и их значения Rf в соответствующих условиях хроматографирования. Однако такой способ весьма не точен, поскольку полное воспроизведение хроматографических условий в ТСХ весьма затруднительно.
Количественный анализ
Методы количественного анализа в ТСХ можно разделить на две группы:
-
методы количественного определения непосредственно на хроматограмме;
-
методы, основанные на извлечении вещества с хроматографической пластинки.
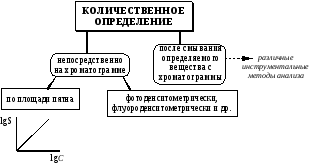
Методы первой группы базируются на том, что площадь пятен и их интенсивность окраски зависят от количества хроматографируемого вещества. Для количественного определения содержания вещества в хроматографических зонах используют два способа.
Первый способ основан на прямо пропорциональной зависимости площади пятна логарифму концентрации при нанесении постоянных объемов раствора анализируемого вещества. Площадь пятен измеряют вручную с помощью миллиметровой бумаги. Погрешность количественного определения таким способом достаточно велика и составляет 5 – 10%.
Полуколичественную оценку содержания вещества можно провести путем визуального сравнения величины окрашенных или флуоресцирующих пятен анализируемых веществ со стандартными растворами.
Второй способ основан на принципах фотометрии с использованием специальных приборов – денситометров. Денситометры позволяют измерять поглощение света веществом непосредственно на хроматограмме в режиме пропускания или отражения, а также флуоресценцию или ее тушение. В настоящее время выделяют два типа денситометров, и соответственно, два типа денситометрии:

Для проведения количественного анализа методом денситометрии необходимо предъявлять более строгие требования к хроматографическим пластинкам и условиям хроматографирования. А именно:
-
использовать специальные пластинки для ВЭТСХ с гомогенным сорбентом, нанесенным равномерным слоем;
-
наносить, одинаковые размеры стартовых пятен точно градуированными микрошприцами или капиллярными пипетками;
-
соблюдать хроматографические условия, обеспечивающие постоянное парциальное давление паров элюента в камере и подбирать состав подвижной фазы, при котором достигается четкое разделение пятен;
-
в случае если для обнаружения веществ используется химическое детектирование, то опрыскивание пластинки реагентом необходимо проводить равномерно с получением контрастных пятен.
Погрешность количественного определения с помощью денситометрии не превышает ± 2%.
Ко второй группе относятся методы, в которых хроматографическую зону переносят с пластинки в подходящую емкость, а затем экстрагируют анализируемое вещество с сорбента подходящим растворителем. Далее осуществляют анализ экстракта с помощью различных инструментальных методов: спектроскопических, электрохимических и др. Этот метод является более трудоемким, хотя при его использовании может быть достигнута большая точность.
