
Первый закон излучения Вина
В 1893 году Вильгельм Вин, воспользовавшись, помимо классической термодинамики, электромагнитной теорией света, вывел следующую формулу:
-
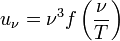 ,
,
где:
-
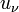 —
плотность энергии излучения
—
плотность энергии излучения -
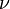 —
частота излучения
—
частота излучения -
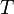 —
температура излучающего тела
—
температура излучающего тела -
 —
функция, зависящая только от частоты
и температуры. Вид этой функции невозможно
установить, исходя только из
термодинамических соображений.
—
функция, зависящая только от частоты
и температуры. Вид этой функции невозможно
установить, исходя только из
термодинамических соображений.
Второй закон излучения Вина
В 1896 году Вин на основе дополнительных предположений вывел второй закон:
-

-
где uν — плотность энергии излучения
-
ν — частота излучения
-
T — температура излучающего тела
-
C1,C2 — константы.
90. Ядерная (Планетарная) Модель Атома
На основании результатов своих экспериментов Э. Резерфорд предложил модель атома, по которой в центре атома расположено положительно заряженное ядро диаметром порядка 1015 м, в котором сосредоточена почти вся масса атома. Вокруг ядра, подобно планетам солнечной системы, обращаются электроны. Так как атом в обычном состоянии электронейтрален, то суммарный заряд электронов равен по модулю заряду ядра.
91.
92. постулаты Бора — основные допущения, сформулированные Нильсом Бором в 1913 году для объяснения закономерностилинейчатого спектра атома водорода и водородоподобных ионов (формула Бальмера-Ридберга) и квантового характера испускания и поглощения света. Бор исходил из планетарной модели атома Резерфорда.
-
Электрон в атоме, не теряя энергии, двигается по определённым дискретным круговым орбитам для которых момент импульса квантуется:
 ,
где n — натуральные
числа,
а
,
где n — натуральные
числа,
а 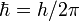 — постоянная
Планка. Пребывание
электрона на орбите определяет энергию
этих стационарных
состояний.
— постоянная
Планка. Пребывание
электрона на орбите определяет энергию
этих стационарных
состояний. -
При переходе электрона с орбиты (энергетический уровень) на орбиту излучается или поглощается квант энергии hν = En − Em, где En;Em — энергетические уровни, между которыми осуществляется переход. При переходе с верхнего уровня на нижний энергия излучается, при переходе с нижнего на верхний — поглощается.
Используя данные постулаты и законы классической механики, Бор предложил модель атома, ныне именуемую Боровской моделью атома[1]. В дальнейшем Зоммерфельд расширил теорию Бора на случай эллиптических орбит. Её называют моделью Бора-Зоммерфельда.
93. Энергетический уровень — собственные значения энергии квантовых систем, то есть систем, состоящих из микрочастиц (электронов, протонов и других элементарных частиц) и подчиняющихся законам квантовой механики. Каждый уровень характеризуется определённым состоянием системы, или подмножеством таковых в случае вырождения. Понятие применимо к атомам (электронные уровни), молекулам (различные уровни, соответствующие колебаниям и вращениям), атомным ядрам(внутриядерные энергетические уровни) и т.д.
94. Рентге́новское излуче́ние — электромагнитные волны, энергия фотонов которых лежит на шкале электромагнитных волн между ультрафиолетовым излучением и гамма-излучением, что соответствует длинам волн от 10−2 до 103 Å (от 10−12 до 10−7 м).
95. Строение Атомного Ядра
Проблему строения атомного ядра удалось решить лишь после того, как в 1932 г. Д. Чэдвиком (1891-1974) была открыта новая частица - нейтрон. В этом же году советский физик Д. Иваненко и немецкий ученый В. Гей-зенберг (1901-1976) предложили протонно-нейтронную модель ядра.
Протон обладает положительным зарядом qp= 1,6-10-19 Кл и массой mр= 1836,2 mе= 1,67 • КГ-27кг = 1,00728 а.е.м.
Нейтрон - электрически нейтральная частица (qn= 0), его масса покоя mn = 1838,7 mе= 1,68 • 10-27 кг = 1,00867 а.е.м. В свободном состоянии он неустойчив: распадается на протон, электрон и антинейтрино. Его время жизни ~ 103 с.
Число протонов в ядре равно атомному номеру химического элемента в периодической таблице Д. Менделеева - z. Число нейтронов в ядре определяется как разность между общим числом А всех частиц в ядре и количеством протонов в нем: N =А - z, где А - массовое число, число нуклонов в ядре.
Нуклонами называются нейтроны и протоны, входящие в состав атомного ядра. Ядро, или атом, обозначается как Azх, где х - химический символ элемента, например 168 О.
ЯДЕРНЫЕ МОДЕЛИ - упрощённые подходы к описанию строения атомных ядер, позволяющие простым образом рассчитывать разл. ядерные характеристики. Как правило, Я. м. основаны на упрощениях, допускающих простое ма-тем. описание. Положенная в основу модели картина всегда отражает лишь отд. черты ядер, а сама модель призвана описывать лишь определ. ядерные свойства. Отд. класс образуют т. н. микроскопич. модели, основанные на ма-тем. приближениях, упрощающих решение ур-ний микроскопич. теории ядра. Особый интерес представляют точно решаемые модели ,к-рые используются для исследования точности разл. приближённых методов.
96. Естественной радиоактивностью называется самопроизвольное превращение ядер неустойчивых изотопов одного химического элемента в ядра других химических элементов. Естественная радиоактивность сопровождается испусканием определенных частиц: альфа-, бета- излучений, антинейтрино, а также электромагнитного излучения(гамма-излучение). Естественная радиоактивность наблюдается у тяжелых ядер элементов, располагающихся в периодческой системе Д.И.Менделеева за свинцом. Существуют и легкие
радиоактивные ядра: изотоп калия 19К40 , изотоп углерода 6С14 и другие
РАДИОАКТИВНОСТЬ ИСКУССТВЕННАЯ -радиоактивность, искусственно создаваемая в устойчивых химических элементах путем их облучения потоками нейтронов в ядерных реакторах или бомбардировки этих элементов тяжелыми частицами — протонами, альфа-частицами и др. Вследствие огромного разнообразия свойств (вид излучения, энергия-, время жизни, масса испускаемых частиц и др.) радиоактивные вещества, получаемые искусственным путем, применяют значительно шире, чем естественные. В связи с открытием искусственной радиоактивности оказалось возможным осуществить мечту средневековых алхимиков — превращать атомы одних химических элементов в атомы других элементов.
97. Закон радиоактивного распада — физический закон, описывающий зависимость интенсивности радиоактивного распада от времени и количества радиоактивных атомов в образце. Открыт Фредериком Содди и Эрнестом Резерфордом. Они обнаружили егоэкспериментальным путём и опубликовали в 1903 году в работах «Сравнительное изучение радиоактивности радия и тория» и «Радиоактивное превращение», сформулировав следующим образом[1]:
Во всех случаях, когда отделяли один из радиоактивных продуктов и исследовали его активность независимо от радиоактивности вещества, из которого он образовался, было обнаружено, что активность при всех исследованиях уменьшается со временем по закону геометрической прогрессии.
![]() которое
означает, что число распадов
которое
означает, что число распадов ![]() ,
произошедшее за короткий интервал
времени
,
произошедшее за короткий интервал
времени ![]() ,
пропорциональнo числу атомов в
образце
,
пропорциональнo числу атомов в
образце ![]() .
.
98. РАДИОАКТИВНЫЕ СЕМЕЙСТВА. Цепочку элементов, самопроизвольно образующихся один из другого в результате радиоактивного распада, называют радиоактивным семейством. Таких семейств существует четыре. Они охватывают все известные радиоактивные элементы. Родоначальником первой цепочки является уран-238, который заканчивает свой распад изотопом обычного свинца-206. Вторая цепочка пачинается торием-232, превращающимся в конечном счете в изотоп свинца-208, третья цепочка — актиния-235 или актиноурана-235 — заканчивается свинцом-207. Процесс распада идет так. При испускании альфа-частицы масса вещества уменьшается на четыре массовые единицы и превращается в новое вещество, стоящее на две клетки раньше в Периодической системе элементов Д. И. Менделеева. При испускании же бета-частицы (электрона) один из нейтронов превращается в протон. Так как в данном случае происходит лишь перераспределение количества нейтронов и протонов в ядре атома, то это влечет за собой превращение его в один из изотопов элемента, стоящего следующим в таблице.
Четвертое радиоактивное семейство начинается с искусственно получаемого радиоактивного сверхтяжелого «зауранового», или «трансуранового», элемента плутония-241, переходит затем в цепочку урана-235 и кончается тоже устойчивым таллием-205
99.
100.
101. Цепна́я я́дерная реа́кция — последовательность единичных ядерных реакций, каждая из которых вызывается частицей, появившейся как продукт реакции на предыдущем шаге последовательности. Примером цепной ядерной реакции является цепная реакция деления ядер тяжёлых элементов, при которой основное число актов деления инициируется нейтронами, полученными при делении ядер в предыдущем поколении.
