
- •1)Основные кинематические величины
- •3) Динамика поступательного движения. Законы Ньютона.
- •5) Понятие работы и мощности. Работа переменной силы.
- •6) Основные понятия динамики вращательного движения. Момент силы и импульса.
- •7) Потенциальная и кинетическая энергия
- •9) Термодинамические и статистические методы исследование термодинамич.
- •10) Первое начало термодинамики, внутренняя энергия ид. Газа. Теплота.Работа.
- •11) Адиабатический процесс. Уравнение Пуассона. 1-е начала термодинамики для Адиабат. Процесса
- •12) Вероятностное описание случайных событий.Функция распределения Максвела по модулю скорости
- •13. Распределение Больцмана. Барометрическая формула.
- •15. Второе начало термодинамики (его формулировки). Принцип работы тепловой машины. Цикл Карно.
- •16. Применение 1-ого начала термодинамики к изопроцессам. Работа расширения газа в изопроцессах.
- •17. Теплоёмкость.
- •18. Характерные скорости движения молекул газа. Вычисление средних скоростей в статической физики.
- •19. Принцип относительности в классической и релятивистской механике. Постулаты Эйнштейна. Преобразования Лоренца.
15. Второе начало термодинамики (его формулировки). Принцип работы тепловой машины. Цикл Карно.
Второе начало термодинамики: в процессах, происходящих в замкнутой системе, энтропия не убывает.
По Кельвину: невозможен круговой процесс единственным результатом которого является превращение теплоты полученной от нагревателя, в эквивалентную ей работу.
По Клаузиусу: невозможен круговой процесс единственным результатом которого является передача теплоты от менее нагретого тела к более нагретому.
Принцип действия тепловой машины: от термостата с более высокой температурой Т1 наз. нагревателем за цикл отнимается кол-во теплоты Q1, а термостату с более низкой температурой Т2 наз. холодильником, за цикл передается кол-во теплоты Q2, при этом совершается работа A=Q1-Q2 .
Принцип действия холодильной машины: за цикл от термостата с более низкой температурой Т2 отнимается кол-во теплоты Q2 и отдаётся термостату с более высокой температурой Т1 кол-во теплоты Q1 .
Без совершения работы нельзя отбирать теплоту от менее нагретого тела и отдавать её более нагретому.
Цикл Карно .
1-2 и 3-4 -изотермическое расширение и сжатие , 2-3 и 4-1 - адиабатическое расширение и сжатие.

Термический
КПД цикла Карно
![]()
Записав для адиабат

16. Применение 1-ого начала термодинамики к изопроцессам. Работа расширения газа в изопроцессах.
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение первого закона термодинамики примет вид: Q=A’, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется. В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы:Q=ΔU+A’. При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. А = 0, и уравнение первого закона имеет вид Q= ΔU, т. е. переданное количество теплоты идет на увеличение внутренней энергии газа. Адиабатным называют процесс, протекающий без теплообмена с окружающей средой. Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается, A’= ΔU Кривая, изображающая адиабатный процесс, называется адиабатой.
1) Изотермическое сжатие
Для вывода 1 закона термодинамики воспользуемся интерактивной моделью изотермического сжатия ( рис.2) и графическим истолкованием работы для процесса ( рис.3)



рис. 2 рис.3 рис.4
Для
изотермического процесса T- const,
![]() T=0,
а значит
T=0,
а значит
![]() U=
3/2 v RT=0 ( внутренняя энергия не изменяется).
Над газом совершается работа А>0, а
тепло выделяется Q<0.
U=
3/2 v RT=0 ( внутренняя энергия не изменяется).
Над газом совершается работа А>0, а
тепло выделяется Q<0.
Первый
закон термодинамики
![]() U=A+Q
выглядит так:
U=A+Q
выглядит так:
0 = -Q + A
Над газом совершается работа, при этом газ выделяет тепло во внешнюю среду ( внутренняя энергия не изменяется)
А блок –схема 1 закона для изотермического сжатия приведена на рис. 4
2) Изотермическое расширение
Для вывода 1 закона термодинамики воспользуемся интерактивной моделью изотермического расширения ( рис.5) и графическим истолкованием работы для процесса( рис.6)


![]()
рис.5 рис.6 рис.7
Для
изотермического процесса T- const,
![]() T=0,
а значит
T=0,
а значит
![]() U=0
( внутренняя энергия не изменяется). Газ
совершает работу А<0, а тепло поглощается
(Q>0).
U=0
( внутренняя энергия не изменяется). Газ
совершает работу А<0, а тепло поглощается
(Q>0).
Первый закон термодинамики выглядит так:
Q = A
Газ совершает работу за счет поглощения тепла из внешней среды ( внутренняя энергия не изменяется)
Блок - схема первый закона термодинамики для изотермического сжатия представлена на рис. 7
3) Изобарное нагревание.
Воспользуемся интерактивной моделью и (пронаблюдаем изобарное нагревание) ( рис. 8) и графическим представлением работы ( рис. 9)


![]()
рис.8 рис.9 рис.10
При
изобарном нагревании температура
увеличивается (
![]() T>0
), внутренняя энергия увеличивается
(
T>0
), внутренняя энергия увеличивается
(![]() U>0),
газ совершает работу , тепло поглощается.
U>0),
газ совершает работу , тепло поглощается.
Первый закон термодинамики выглядит так:
Q
=
![]() U
– A
U
– A
Газ получает тепло из внешней среды. Полученная таким образом энергия тратится на увеличение внешней энергии и на совершение работы.
В итоге блок - схема первого закон термодинамики выглядит как на рис.10
4) Изобарное охлаждение
Пронаблюдав процесс изобарного охлаждения на интерактивной модели ( рис.11) и воспользовавшись рис.12 можем сделать вывод:


![]()
рис.11 рис.12 рис.13
при
изобарном охлаждении температура
уменьшается (
![]() T<0
), внутренняя энергия уменьшается (
T<0
), внутренняя энергия уменьшается (![]() U<0), над газом совершается работа ,
тепло выделяется.
U<0), над газом совершается работа ,
тепло выделяется.
Первый закон термодинамики выглядит так:
![]() U
= -Q + A
U
= -Q + A
Над газом совершается работа, при этом газ выделяет тепло во внешнюю среду, а его внутренняя уменьшается .
Блок – схема для 1 закона термодинамики для этого случая представлен на рис. 13
5) Изохорное нагревание
Изохорное нагревание пронаблюдаем на интерактивной модели ( рис14) и воспользуемся графиком на рис 15. Вывод:


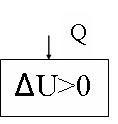
рис. 14 рис. 15 рис. 16
При
изохорном нагревании (![]() T>0 ), внутренняя энергия увеличивается
(
T>0 ), внутренняя энергия увеличивается
(![]() U>0)
, работа A=p
U>0)
, работа A=p![]() V
равна нулю, т.к.
V
равна нулю, т.к.
![]() V=0,
а тепло поглощается (Q>0).
V=0,
а тепло поглощается (Q>0).
Первый закон термодинамики выглядит так:
![]() U=Q
U=Q
Газ увеличивает свою внутреннюю энергию за счет теплоты, полученной из внешней среды.
Интерпретация 1 закона термодинамики для изохорного нагревания представлена на рис. 16
6) Изохорное охлаждение
Изохорное охлаждение пронаблюдаем на интерактивной модели ( рис17) и графиком на рис 18. Вывод:


![]()
рис. 17 рис. 18 рис. 19
При
изохорном охлаждении (![]() T<0 ), внутренняя энергия уменьшается(
T<0 ), внутренняя энергия уменьшается(![]() U<0
, работа A=p
U<0
, работа A=p![]() V
равна нулю, т.к.
V
равна нулю, т.к.
![]() V=0,
а тепло выделяется (Q<0).
V=0,
а тепло выделяется (Q<0).
Первый закон термодинамики выглядит так:
-
![]() U=-Q
U=-Q
Газ выделяет тепло во внешнюю среду; при этом его внутренняя энергия уменьшается.
