
- •3.Абсолютная и относительная истина
- •6. Понятие о структурных уровнях организации материи. Мегамир, макромир, микромир. Микро-, макро- и мегамиры.
- •Микромир.
- •Макромир.
- •Мегамир.
- •Равновесие твердого тела под действием трех сил
- •Силы, действующие на рычаг, и их моменты.
- •9. Законы сохранения количества движения ( импульса), энергии и момента количества движения.
- •11. Концептуальные представления о различиях в строении твердых, жидких и газообразных тел. Роль давления и температуры в агрегатных переходах.
- •12. Концепция атомизма от Демокрита до наших дней. Планетарная модель атома Резерфорда. Постулаты Бора.
- •Значение периодической системы
- •Сущность явления
- •[Править] Пересмотренная последовательность Хаббла
- •[Править] Сила и плотность тока
- •[Править] Мощность
- •27. Гипотезы происхождения жизни на Земле. Гипотезы о возникновении жизни
- •Теория стационарного состояния
- •Самозарождение жизни
11. Концептуальные представления о различиях в строении твердых, жидких и газообразных тел. Роль давления и температуры в агрегатных переходах.
Опыты и примеры показали нам, какие свойства имеют твердые, жидкие и газообразные тела.
Знания о строении вещества помогут объяснить эти свойства.
Лед, вода и водяной пар - три агрегатных состояния одного и того же вещества - воды. Значит, молекулы льда, воды и водяного пара не отличаются друг от друга. А раз так, тоэти три состояния различаются не молекулами, а тем, как эти молекулы расположены и как движутся.
Как же расположены и как движутся молекулы газа, жидкости и твердого тела?
Газ можно сжать так, что его объем уменьшится в несколько раз. Значит, в газах расстояние между молекулами много больше размеров самих молекул.
В среднем расстояния между молекулами газов в десятки раз больше размеров самих молекул. На таких расстояниях молекулы очень слабо притягиваются друг к другу. По этой причине газы не имеют собственной формы и постоянного объема. Нельзя заполнить газом, например, половину бутылки или стакана, так как, двигаясь во всех направлениях и почти не притягиваясь друг к другу, молекулы газа быстро заполнят весь сосуд.
Свойства жидкостей объясняются тем, что промежутки между их молекулами малы: молекулы в жидкостях упакованы так плотно, что расстояние между каждыми двумя молекулами меньше размеров молекул. На таких расстояниях притяжение молекул друг к другу уже значительно. Поэтому молекулы жидкости не расходятся на большие расстояния и жидкость в обычных условиях сохраняет свой объем. Однако притяжение молекул жидкости еще не настолько велико, чтобы жидкость сохраняла свою форму. Этим объясняется то, что жидкости в условиях действия силы тяжести принимают форму сосуда, в котором находятся, и то, что их легко разбрызгать и перелить в другой сосуд.
Сжимая жидкость, мы сближаем ее молекулы настолько, что они начинают отталкиваться друг от друга. Вот почему жидкость так трудно сжать.
Твердые тела в обычных условиях сохраняют и объем, и форму. Это объясняется тем, что притяжение между их частицами еще больше, чем у жидкостей.
Частицы (молекулы или атомы) большинства твердых тел, таких, как лед, соль, алмаз, металлы, расположены в определенном порядке.
Такие твердые тела называют кристаллическими. Хотя частицы этих тел и находятся в движении, но движение это представляет собой колебания около определенных точек (положений равновесия). Частицы не могут уйти далеко от этих точек, поэтому твердое тело сохраняет свою форму и объем.
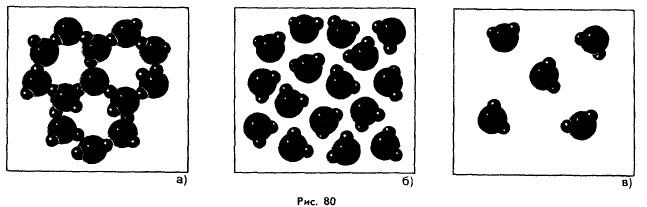
На
рисунке 80 показано расположение молекул
одного и того же вещества - воды в трех
разных состояниях: твердом (а), жидком
(б) и газообразном (в). Различие в
расположении и движении молекул в этих
состояниях объясняет различие в свойствах
льда, воды и водяного пара.
Подведем итоги. Изучение строения вещества показывает, что: 1) все вещества состоят из мельчайших частиц - молекул и атомов; 2) частицы вещества непрерывно и беспорядочно движутся; 3) частицы вещества взаимодействуют друг с другом.
Эти три положения называют основными положениями молекулярно-кинематической1 теории строения вещества.
Фа́зовый перехо́д (фазовое превращение) в термодинамике — переход вещества из одной термодинамической фазы в другую при изменении внешних условий. С точки зрения движения системы по фазовой диаграмме при изменении её интенсивных параметров (температуры, давления и т. п.), фазовый переход происходит, когда система пересекает линию, разделяющую две фазы. Поскольку разные термодинамические фазы описываются различными уравнениями состояния, всегда можно найти величину, которая скачкообразно меняется при фазовом переходе.
Поскольку разделение на термодинамические фазы — более мелкая классификация состояний, чем разделение по агрегатным состояниям вещества, то далеко не каждый фазовый переход сопровождается сменой агрегатного состояния. Однако любая смена агрегатного состояния есть фазовый переход.
Наиболее часто рассматриваются фазовые переходы при изменении температуры, но при постоянном давлении (как правило равном 1 атмосфере). Именно поэтому часто употребляют термины «точка» (а не линия) фазового перехода, температура плавления и т. д. Разумеется, фазовый переход может происходить и при изменении давления, и при постоянных температуре и давлении, но при изменении концентрации компонентов (например, появление кристалликов соли в растворе, который достиг насыщения).
Классификация фазовых переходов
При фазовом переходе первого рода скачкообразно изменяются самые главные, первичные экстенсивные параметры: удельный объём, количество запасённой внутренней энергии, концентрация компонентов и т. п. Подчеркнём: имеется в виду скачкообразное изменение этих величин при изменении температуры, давления и т. п., а не скачкообразное изменение во времени (насчёт последнего см. ниже раздел Динамика фазовых переходов).
Наиболее распространённые примеры фазовых переходов первого рода:
-
плавление и кристаллизация
-
испарение и конденсация
-
сублимация и десублимация
При фазовом переходе второго рода плотность и внутренняя энергия не меняются, так что невооружённым глазом такой фазовый переход может быть незаметен. Скачок же испытывают их производные по температуре и давлению: теплоёмкость, коэффициент теплового расширения, различные восприимчивости и т. д.
Фазовые переходы второго рода происходят в тех случаях, когда меняется симметрия строения вещества (симметрия может полностью исчезнуть или понизиться). Описание фазового перехода второго рода как следствие изменения симметрии даётся теорией Ландау. В настоящее время принято говорить не об изменении симметрии, но о появлении в точке перехода параметра порядка, равного нулю в менее упорядоченной фазе и изменяющегося от нуля (в точке перехода) до ненулевых значений в более упорядоченной фазе.
Наиболее распространённые примеры фазовых переходов второго рода:
-
прохождение системы через критическую точку
-
переход парамагнетик-ферромагнетик или парамагнетик-антиферромагнетик (параметр порядка — намагниченность)
-
переход металлов и сплавов в состояние сверхпроводимости (параметр порядка — плотность сверхпроводящего конденсата)
-
переход жидкого гелия в сверхтекучее состояние (п.п. — плотность сверхтекучей компоненты)
-
переход аморфных материалов в стеклообразное состояние
Современная физика исследует также системы, обладающие фазовыми переходами третьего или более высокого рода.
В последнее время широкое распространение получило понятие квантовый фазовый переход, т.е. фазовый переход, управляемый не классическими тепловыми флуктуациями, а квантовыми, которые существуют даже при абсолютном нуле температур, где классический фазовый переход не может реализоваться вследствие теоремы Нернста.
[править] Динамика фазовых переходов
Как сказано выше, под скачкообразным изменением свойств вещества имеется в виду скачок при изменении температуры и давления. В реальности же, воздействуя на систему, мы изменяем не эти величины, а её объем и её полную внутреннюю энергию. Это изменение всегда происходит с какой-то конечной скоростью, а значит, что для того, чтобы «покрыть» весь разрыв в плотности или удельной внутренней энергии, нам требуется некоторое конечное время. В течение этого времени фазовый переход происходит не сразу во всём объёме вещества, а постепенно. При этом в случае фазового перехода первого рода выделяется (или забирается) определённое количество энергии, которая называется теплотой фазового перехода. Для того, чтобы фазовый переход не останавливался, требуется непрерывно отводить (или подводить) это тепло, либо компенсировать его совершением работы над системой.
В результате, в течение этого времени точка на фазовой диаграмме, описывающая систему, «замирает» (т.е. давление и температура остаются постоянными) до полного завершения процесса.
