
- •Реферат
- •Перелік умовних позначень
- •Огляд літератури розділ 1
- •1.1. Виділення та ідентифікація біотехнологічно-перспективних штамів роду Nocardia
- •1.2. Використання представників роду Nocardia у деградації нафтових забруднень
- •1.2.1. Механізми споживання гідрофобних сполук мікроорганізмами
- •1.2.1.1. Роль поверхнево-активних речовин у асиміляції вуглеводнів
- •1.2.1.2. Гідрофобність клітин мікроорганізмів і споживання вуглеводнів
- •1.2.1.3. Міжфазне споживання гідрофобних сполук, якому сприяють поверхнево-активні речовини
- •1.2.1.4. Генетичні основи деградації вуглеводнів
- •1.2.2. Деградація аліфатичних вуглеводнів
- •1.2.3. Деградація ароматичних вуглеводнів
- •1.2.4. Деградація гетероциклічних сполук
- •1.2.5. Біодеградація складових нафти імобілізованими клітинами бактерій роду Nocardia
- •1.3. Біосинтез практично-важливих метаболітів
- •1.3.1. Представники роду Nocardia як продуценти антимікробних речовин
- •Антибіотичні речовини представників роду Nocardia
- •1.3.2. Біосинтез поверхнево-активних речовин
- •1.4. Використання поверхневого культивування для отримання цільових продуктів
- •1.5. Використання представників роду Nocardia у процесах біотрансформації
- •1.6. Дослідження біосинтезу нокобактину Nocardia farcinica ifm10152
- •Висновки до огляду літератури
- •Експериментальна частина розділ 2 матеріали і методи досліджень
- •2.1. Об’єкти досліджень
- •При рості на агаризованих середовищах штам n. Vaccinii к-8 на 24 год утворює колонії схожої структури та зовнішнього вигляду, зображено у таблиці. Культуральні ознаки штаму Nocardia vaccinii к-8
- •2.2. Культивування Nocardia vacсinii к-8
- •2.3. Визначення параметрів росту і синтезу поверхнево-активних речовин
- •2.3.4. Метод кількісного визначення поверхнево-активних речовин
- •2.4. Визначення хімічного складу пар за допомогою тонкошарової хроматографії
- •2.5. Статистична обробка експериментальних результатів
- •Розділ 3 вплив органічних кислот на синтез поверхнево-активних речовин штамом nocardia vacсinii k-8 за умов росту на гліцерині
- •3.1 Хімічний склад поверхнево-активних речовин Nocardia vaccinii k 8
- •3.2. Вибір попередників та синтез поверхнево-активних речовин залежно від моменту їх внесення
- •Залежність синтезу пар n. Vaccinii k-8 від моменту внесення та концентрації цитрату натрію
- •3.3. Визначення оптимальних концентрацій цитрату й фумарату натрію
- •Залежність синтезу пар n. Vaccinii k-8 від концентрації цитрату
- •Залежність синтезу пар n. Vaccinii k-8 від концентрації фумарату
- •3.4. Синтез поверхнево-активних речовин за спільного внесення органічних кислот
- •Синтез пар штамом n. Vaccinii k-8 під час спільного внесення фумарату й цитрату натрію
- •3.5. Вплив регуляції рН на синтез поверхнево-активних речовин
- •Вплив регуляції рН на вихід поверхнево-активних речовин n. Vaccinii k-8
- •3.6. Вплив якості інокуляту на синтез поверхнево-активних речовин за присутності попередників
- •Вплив якості інокуляту на синтез поверхнево-активних речовин n. Vaccinii k-8
- •Висновки до експериментальної частини
- •Розділ 4 охорона праці
- •4.1 Організація служби охорони праці в лабораторії
- •Аналіз виробничого травматизму
- •Санітарні умови праці на виробництві Мікроклімат
- •Загазованість
- •Запиленість повітря
- •Заходи захисту від шуму та вібрацій
- •Освітлення
- •Випромінювання
- •Висновки по матеріалам аналізу санітарних умов
- •4.2 Розрахунок штучної освітленості для науково-дослідної лабораторії Національного університету харчових технологій Загальне освітлення
- •Місцеве освітлення
- •Список використаної ліератури
- •Ксерокопії публікацій
1.5. Використання представників роду Nocardia у процесах біотрансформації
Мікробна трансформація промислових хімічних відходів та продуктів переробки нафти становить великий інтерес. Прикладом даних процесів є утворення продуктів неповних окиснень під час метаболізму алкілбензенів бактеріями і грибами. Так, у дослідженні, проведеному ще у 1979 р. було встановлено здатність штаму Nocardia tartaricans ATCC 31190 перетворювати етилбензен не до фенілоцтової кислоти, а до 1-фенілетанолу та ацетофенону, що використовуються у органічному синтезі [26]. Після трьохдобового культивування даного штаму на гексадекані (0,5 %) з додавання 0,05 % етилбензену на початку культивуванням та доведенням його концентрації до 0,5 % на початку стаціонарної фази росту, подальшої екстракції хлороформом шляхом тонкошарової хроматографії дані сполуки були виявлені у культуральній рідини. Для того, щоб довести, що дані перетворення відбулися не шляхом звичайних хімічних реакцій, а біотрансформації, було проведено контрольні досліди, де використовували інактивовані клітини, або виключали етилбензен зі складу середовища. В даних реакціях похідних бензену не утворювалося, що свідчить про роль мікроорганізмів у даних реакціях. Щоб підтвердити припущення, що 1-фенілетанол є проміжним продуктом утворення ацетофенону, було проведено культивування N. tartaricans ATCC 31190 на 1-, та 2-фенілетанолі. Ацетофенон утворювався лише у першому випадку. Цікаво, що при заміні гексадекану на ацетат чи глюкозу, синтез ацетофенону значно знижувався, та припинявся зовсім, відповідно. На мою думку, щоб пояснити цю закономірність, необхідно детальніше вивчити шляхи метаболізму даних сполук [26].
У іншому дослідженні вченими з Південної Кореї було проведено дослідження можливості використання цитохрому P154, виділеного з Nocardia farcinica IFM10152, для здійснення трансформації ізофлавоноїдів [41].
Ізофлавоноїди є важливим класом природних сполук, в основі яких лежить 3-фенілхромен-4, який походить від фенілаланіну загальним фенілпропаноїдним шляхом. Залежно від модифікацій виділяють формонетин, даідзен, геністен, біоханін А та гліцитеїн. Так, наприклад, даідзеїну (4’,7-дигідроксиізофлавон) притаманні протипухлинні та естроген-подібні властивості, та здатність попереджувати серцеву недостатність, знижувати ризик захворювання на рак грудей, простати та ін. У природі найбільш поширеним є формонетин (4’-О-метиловий ефір даідзеїну), який є домінуючим ізофлавоном червоної конюшини та відіграє важливу роль у регуляції багатьох фізіологічних процесів у рослин. Антиоксидантні властивості ізофлавоноїдів суттєво підвищуються, якщо їхня структура містить більше гідроксильних груп чи орто-дигідроксильованих часток у α- чи β-кільцях. Порівняно з іншими ізофлавонами, формонетину притаманні слабкі антиоксидантні та протипухлинні властивості, так як у його структурі відсутня 5-гідроксильна група, а 4’-гідроксильна група блокована метальною групою, чим і зумовлене його обмежене застосовування. Таким чином, модифікуючи структуру ізофлавоноїдів використовуючи різні ферменти, наприклад оксидази, пероксидази, та оксигенази можна змінити їх фізіологічні функції, що останнім часом широко використовується на практиці [41].
Серед можливих ферментних систем для здійснення даної біотрансформації проивертає увагу цитохром Р450, що містить гемтіолову групу, яка каталізує більш ніж 40 різних типів хімічних реакцій. Цей фермент зазвичай вводить одну молекулу кисню у субстрат через реакцію гідроксилювання. Також відомо, що він каталізує реакцію О-деалкілування на алкіл-етерових зв’язках, зберігаючи гідроксильну групу. Дане перетворення є цінним біохімічним процесом, так як не лише підвищується гідрофільність та розчинність субстратів, а також їх біологічна та фармакологічна активність. Попри значні успіхи у вивченні каталізу цитохромами процесів окиснення, до сьогодні відомо про здатність каталізувати О-деалкілування лише декількома цитохромами бактерій і ссавців.
У попередніх дослідженнях встановлено, що штам N. farcinica IFM10152 містила 27 цитохромів родини Р450, один з яких згідно філогенетичних досліджень, належить до підродини P107, що каталізує О-деалкілування [41]. Проте, використанням використанням 7-етоксикумарину (індикатора процесів деалкілування) було виявлено дану властивість також у цитохромів підродини P154. Отже, аналізуючи цитохромну активність даним методом було виявлено три цитохроми: дві підродини P154 та один P107, що здатні каталізувати реакції деалкілування. Цитохром P154 (Nfa22930) виявив найвищу О-деалкілуючу активність і тому був вибраний для подальших досліджень з метою практичного використання [41]. Використовуючи даний цитохром та формонетин як субстрат для біотрансформації було проведено перетворення з утворенням важливої біологічно-активної сполуки - 3’,4’,7-тригідроксиізофлавону (Рис. 1.7.).
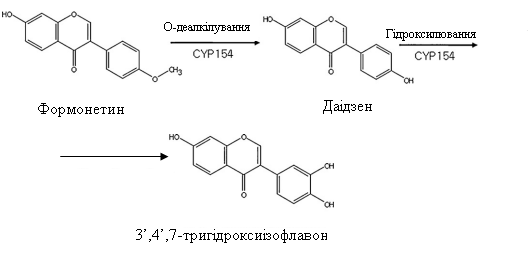
Рис. 1.7. Схема трансформації формонетину
