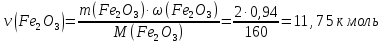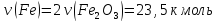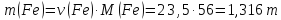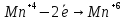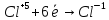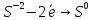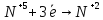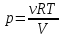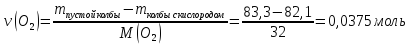- •Основные классы неорганических соединений. Типы оксидов и гидроксидов, их свойства (основные, кислотные, амфотерные) на примере реакций.
- •Понятие эквивалента элемента и закон эквивалентов. Расчет молярной массы эквивалента для элементов и соединений ( кислоты, основания, соли) и в реакциях.
- •Квантовые числа. Атомные орбитали, энергетические уровни и подуровни. Формы s-p-d- орбиталей.
- •Способы выражения концентраций растворов. Перечислить 6 способов.
- •Водородная связь. Условия образования. Примеры водородной связи и свойства веществ с таким типом связи.
- •Металлическая связь. Зонная теория.
- •Газовые законы. Константы Авогадро.
- •Типы кристаллических решеток, свойства соединений с атомной, молекулярной, ионной и металлической связью.
- •1.Что такое ангидрид кислоты? Какими свойствами он обладает? Напишите формулы ангидридов кислот:h2so4, hno3, h3po4, hClO3, hMnO4,
- •2. Определите формулу соединения, содержащего 80% углерода и 20% водорода, относительная плотность которогопо водороду равна 15. Какие законы химии вы используете для рассчетов.
- •5. Какую массу железа можно получить из 2 т руды, содержащей 94% Fe2o3. Составьте уравнение реакции. Как называется такой метод? Какие законы химии вы использовали для расчетов?
- •6. Показать валентные возможности атомов. Рассмотреть на примере хлора.
- •7. У какой группы частиц электронные формулы одинаковые. Ответ поясните.
- •11. Какой тип гибридизации и строение молекулы роCl3?
5. Какую массу железа можно получить из 2 т руды, содержащей 94% Fe2o3. Составьте уравнение реакции. Как называется такой метод? Какие законы химии вы использовали для расчетов?
|
Дано: m (руды) = 2 т ω% (Fe2O3)=94 % Найти: m (Fe) = ? |
Решение 1) Запишем уравнение реакции Fe2O3+3C = 2Fe + 3CO 2) Найдем количество моль Fe2O3
3) По закону эквивалентов
4) Найдем массу Fe
Ответ: m(Fe) = 1,366 т |
Данный метод получения железа из руды называется прямым восстановлением железа.
В расчетах используется закон эквивалентов и закон сохранения массы.
6. Показать валентные возможности атомов. Рассмотреть на примере хлора.
В возбужденном состоянии:
3s2 3p5 3d0 + hν --> 3s2 3p4 3d1
Валентность 3: 3 неспаренных электрона (2 электрона на 3р-подуровне и 1 электрон на 3d-подуровне),
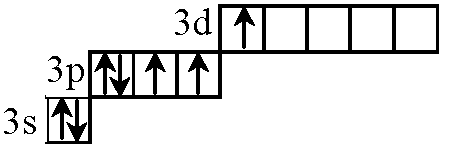
Пример соединения: HClO2, Cl2O3
Валентность 5
3s2 3p4 3d1 + hν --> 3s2 3p3 3d2
5 неспаренных электронов (3 электрона на 3р-подуровне и 2 электрона на 3d-подуровне).
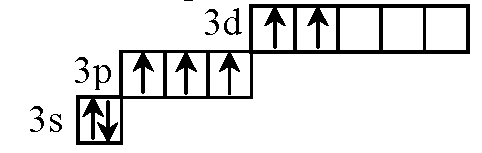
Пример соединения: HClO3, Cl2O5
Валентность 7
3s2 3p3 3d2 + hν --> 3s1 3p3 3d3
7 неспаренных электронов (1 электрон на 3s-подуровне, 3 электрона на 3р-подуровне и 3 электрона на 3d-подуровне).
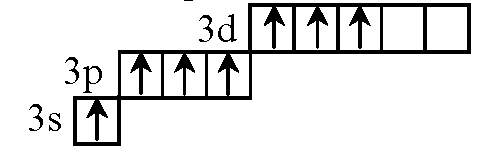
Пример соединения: HClO4, Cl2O7
7. У какой группы частиц электронные формулы одинаковые. Ответ поясните.
1- Sn-Sn2+-Sn4+ 2-F-Cl-Br-I 3- O2--F- Ne-N3- 4-Li+-Na+-K+
У группы 3- O2--F- Ne-N3- электронные формулы одинаковые
O2- : 1s22s22p6
F- : 1s22s22p6
Ne: 1s22s22p6
N3- : 1s22s22p6
8. Уравняйте реакцию MnO2 +KClO3 +KOH = K2MnO4 + KCl + H2O
|
|
2 |
3 |
восстановитель |
|
|
6 |
1 |
окислитель |
3MnO2 +KClO3 +6KOH = 3K2MnO4 + KCl + 3H2O
9. Уравняйте реакцию: HgS + HNO3 + HCl= HgCl2 + S + NO + H2O
|
|
2 |
3 |
восстановитель |
|
|
3 |
2 |
окислитель |
3HgS + 2HNO3 + 6HCl= 3HgCl2 + 3S + 2NO + 4H2O
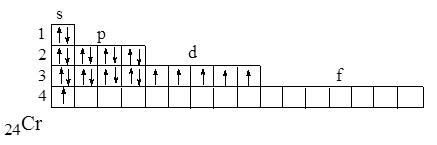
10.Атомный номер элемента 24, атомная масса 51,996. Укажите число протонов, электронов, нейтронов, атомный номер элемента, число неспаренных электронов, семейство элементов. Напишите полную электронную, электронографическую формулу валентных электронов. Какую информацию можно получить еще, зная атомный номер элемента?
Атомный номер элемента 24, атомная масса 51,996 – элемент Cr
Протоны – 24
Электроны – 24
Нейтроны – 28
Атомный номер – 24
Число неспаренных электронов – 6
Семейство элементов – p-элементы
Атомная масса – 52
Полная электронная формула: 1s 22s 22p 63s 23p64s 13d5
11. Какой тип гибридизации и строение молекулы роCl3?
Тип
гибридизации – sp3-гибридизация.
Форма - треугольная пирамида с атомом
P в центре. Говорить , что тетраэдр
(типичная форма для sp3 гибридизации) в
данном случае неверно. Потому как связи
P-O и P-Cl разные, а тетраэдр симметричен
относительно центра.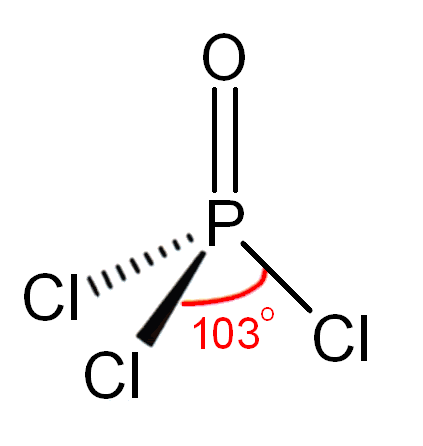
12 Уравнение Менделеева Клапейрона и его применение к решению задач по химии. Колба объемом 750 мл, наполненная при 27оС кислородом имеет массу 83,3г. Масса пустой колбы равна 82,1г. Определить давление кислорода в колбе.
|
Дано: Vколбы=750 мл Т=27 °С mколбы с кислородом=83,3 г mпустой колбы=82,1 г Найти: P=? |
Решение 1) Запишем уравнение Менделеева-Клапейрона
Тогда Р находим по формуле:
2) Количество вещества кислорода равно:
3) Давление в колбе равно
Ответ: давление кислорода в колбе 129,9 кПа
|