
- •Основные классы неорганических соединений. Типы оксидов и гидроксидов, их свойства (основные, кислотные, амфотерные) на примере реакций.
- •Понятие эквивалента элемента и закон эквивалентов. Расчет молярной массы эквивалента для элементов и соединений ( кислоты, основания, соли) и в реакциях.
- •Квантовые числа. Атомные орбитали, энергетические уровни и подуровни. Формы s-p-d- орбиталей.
- •Способы выражения концентраций растворов. Перечислить 6 способов.
- •Водородная связь. Условия образования. Примеры водородной связи и свойства веществ с таким типом связи.
- •Металлическая связь. Зонная теория.
- •Газовые законы. Константы Авогадро.
- •Типы кристаллических решеток, свойства соединений с атомной, молекулярной, ионной и металлической связью.
- •1.Что такое ангидрид кислоты? Какими свойствами он обладает? Напишите формулы ангидридов кислот:h2so4, hno3, h3po4, hClO3, hMnO4,
- •2. Определите формулу соединения, содержащего 80% углерода и 20% водорода, относительная плотность которогопо водороду равна 15. Какие законы химии вы используете для рассчетов.
- •5. Какую массу железа можно получить из 2 т руды, содержащей 94% Fe2o3. Составьте уравнение реакции. Как называется такой метод? Какие законы химии вы использовали для расчетов?
- •6. Показать валентные возможности атомов. Рассмотреть на примере хлора.
- •7. У какой группы частиц электронные формулы одинаковые. Ответ поясните.
- •11. Какой тип гибридизации и строение молекулы роCl3?
-
Понятие эквивалента элемента и закон эквивалентов. Расчет молярной массы эквивалента для элементов и соединений ( кислоты, основания, соли) и в реакциях.
Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н+ или ОН–, в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества. Например, рассмотрим следующую реакцию:
H3PO4 + 2KOH = K2HPO4 + 2H2O.
В ходе этой реакции только два атома водорода замещаются на атомы калия, иначе, в реакцию вступают два иона Н+ (кислота проявляет основность 2). Тогда по определению эквивалентом H3PO4 будет являться условная частица 1/2H3PO4, т.к. если одна молекула H3PO4 предоставляет два иона Н+, то один ион Н+ дает половина молекулы H3PO4.
Эквивалент, как частица, может быть охарактеризован молярной массой (молярным объемом) и определенным количеством вещества νэ. Молярная масса эквивалента (МЭ) – это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности:
МЭ = МfЭ.
Молярная масса эквивалента имеет размерность «г/моль».
Молярная масса эквивалента сложного вещества равна сумме молярных масс эквивалентов образующих его составных частей, например:
МЭ(оксида) = МЭ(элемента) + МЭ(О) = МЭ(элемента) + 8
МЭ(кислоты) = МЭ(Н) + МЭ(кислотного остатка) = 1 + МЭ(кислотного остатка)
МЭ(основания) = МЭ(Ме) + МЭ(ОН) = МЭ(Ме) + 17
МЭ(соли) = МЭ(Ме) + МЭ(кислотного остатка).
Газообразные
вещества помимо молярной массы эквивалента
имеют молярный
объем эквивалента
(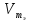 или
VЭ)
– объем, занимаемый молярной массой
эквивалента или объем одного моль
эквивалента.
Размерность
«л/моль».
При
н.у. получаем:
или
VЭ)
– объем, занимаемый молярной массой
эквивалента или объем одного моль
эквивалента.
Размерность
«л/моль».
При
н.у. получаем:
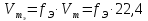
Закон эквивалентов был открыт в 1792 г. И. Рихтером. Современная формулировка закона: вещества реагируют и образуются согласно их эквивалентам. Все вещества в уравнении реакции связаны законом эквивалентов, поэтому:
э(реагента1) = … = э(реагентаn) = э(продукта1) = … = э(продуктаn)
-
Понятие степень окисления, окислитель и восстановитель. Правила расчета степеней окисления. Типы окислительно-восстановительных реакций. Расчет молярной массы эквивалента окислителя и восстановителя в ОВР.
Степень окисления – это условный заряд атома в молекуле или кристалле. Его определяют, условно считая все полярные связи полностью ионнымии.
В окислительно-восстановительных реакциях электроны от одних атомов, молекул или ионов переходят к другим. Процесс отдачи электронов - окисление. При окислении степень окисления повышается:
H20 - 2ē = 2H+
S-2 - 2ē = S0
Al0 - 3ē = Al+3
Fe+2 – ē = Fe+3
2Br - - 2ē = Br20
Процесс присоединения электронов – восстановление. При восстановлении степень окисления понижается.
Mn+4 + 2ē = Mn+2
S0 + 2ē = S-2
Cr+6 +3ē = Cr+3
Cl20 +2ē = 2Cl-
O20 + 4ē = 2O-2
Атомы или ионы, которые в данной реакции присоединяют электроны являются окислителями, а которые отдают электроны - восстановителями.
В зависимости от того, находятся ли атомы, выполняющие в реакции функцию окислителя (акцептора электронов) и восстановителя (донора электронов) в одном или в различных веществах, все окислительно-восстановительные процессы можно разделить на три типа: межмолекулярные, внутримолекулярные и диспропорционирования.
В межмолекулярных (межатомных) реакциях окислительные функции выполняют одни вещества, а восстановительные – другие. Например, в реакции
H2S + Cl2 = S + 2HCl
электроны от восстановителя – молекулы сероводорода – переходят к окислителю – молекуле Cl2.
В реакциях внутримолекулярного окисления-восстановления одна часть молекулы – окислитель, другая – восстановитель. Простейшими примерами могут служить реакции термического разложения вещества:
2NO2=2NO+O2
(NH4)2Cr2O7=N2+Cr2O3+4H2O
Реакции диспропорционирования (самоокисления-самовосстановления) протекают с одновременным уменьшением и увеличением степени окисления атомов одного и того же элемента. Они характерны для соединений или простых веществ, состоящих из промежуточных степеней окисления данного элемента:
Cl2+H2O=HCl+HClO
4KClO3=3KClO4+KCl
3KBrO=KBrO3+2KBr
Эквивалент окислителя или восстановителя – реальная или условная частица вещества, соответствующая одному электрону в данной полуреакции окисления-восстановления. Фактор эквивалентности частиц (молекул, ионов, атомов), участвующих в окислительно-восстановительных реакциях FЭкв=1/n, где n – число принятых или отданных электронов. Молярная масса эквивалента окислителя или восстановителя (Мэ) равна молярной массе, умноженной на фактор эквивалентности:
Мэ = FЭкв · М = М/n
