
- •3. Внутрисердечные механизмы компенсации:
- •Билет 10
- •3.2. Повреждение как начальное звено патогенеза. Уровни повреждения и их проявление
- •I. Анемии, обусловленные острой кровопотерей (постгеморрагические)
- •II. Анемии, возникающие в результате нарушения эритропоэза
- •III. Анемии, возникающие в следствие повышенного разрушения эритроцитов (гемолитические)
- •1) Физиологическая реактивность:
- •2) Патологическая реактивность:
- •1) Физиологическая реактивность:
- •2) Патологическая реактивность:
- •1) Физиологическая реактивность:
- •2) Патологическая реактивность:
- •1) Физиологическая реактивность:
- •3. Патофизиология почек
- •Количественно различают формы реактивности:
- •Качественные характеристики реактивности:
- •Индивидуальная реактивность.
- •1) Физиологическая реактивность:
- •2) Патологическая реактивность:
- •1) Физиологическая реактивность:
- •2) Патологическая реактивность:
Билет 1
1. ПАТОФИЗИОЛОГИЯ .- т.е. наука, изучающая жизнедеятельность
больного организма. Иначе: основные закономерности возникнове-
ния, механизма развития (т.е. патогенез) и исхода болезни (выз-
доровление, реабилитация или смерть). Знание этих общих законо-
мерностей позволяет практическому врачу вести направленный по-
иск специфических признаков болезни, позволяющих поставить пра-
вильный диагноз.
Патофизиологию можно разделить на три части:
1. Нозология - общее учение о болезни.
2. Типические патологические процессы - общие закономер-
ности процессов, лежащих в основе многих заболеваний.
3. Частная патофизиология, изучающая нарушения в отдельных
органах и системах.
Объектом патофизиологических исследований является P-
гический процесс. Основной целью - установление базисных зако-
номерностей патологических процессов, механизмов его развития,
коррекции или ликвидации. Клиническая патофизиология - это пре-
имущественно клинико-диагностическая часть нашей науки. В ее
задачу входит разработка и использование стандартных методов
диагностики продромальных состояний и контроля за течением за-
болевания, а также учет влияния внешних факторов на организм
человека с позиции патофизиологии.
2.ПОВРЕЖДЕНИЕ КЛЕТКИ.
_Повреждение .-типовой патологический процесс,проявляющий-
ся нарушением структурной и функциональной организации живой
системы, вызванным различными причинами
_Физиологическое повреждение - .обусловлено процессами ес-
тественного распада и регенерации клеток (при старении, дли-
тельном бездействии).
Повреждения могут быть:
1) обратимыми и необратимыми;
2) острыми и хроническими.
_Острое повреждение .проявляется преддепрессивной гиперак-
тивностью (усиление функции органелл, прежде всего митохонд-
рий, и повышенная выработка АТФ), парциальным некрозом (унич-
тожение поврежденной части клетки фагоцитами) и тотальным
повреждением ("агония" и смерть клетки).
_"Агония" клетки - .фаза повреждения, когда еще сохраняет-
ся минимальный градиент концентрации электролитов между клет-
кой и внеклеточной средой. При его исчезновении наступает
На уровне клетки повреждающие факторы “включают” несколько патогенетических звеньев. К их числу относят: расстройство процессов энергетического обеспечения клеток (инициальный и ведущий механизм их альтерации);повреждение мембран и ферментных систем ( дисбаланс ионов и жидкости (нарушение генетической программы и/или ее реализации аномального участка ДНК другой клетки, в процессе клеточного деления при митозе или мейозе);расстройство механизмов регуляции функции клеток (
ОСНОВНЫЕ ПРОЯВЛЕНИЯ ПОВРЕЖДЕНИЙ КЛЕТКИ
Дистрофии - нарушения обмена веществ в клетках и тканях, сопровождающиеся расстройствами их функций, пластических проявлений, а также структурными изменениями, ведущими к нарушению их жизнедеятельности.
Дисплазии представляют собой нарушение процесса развития клеток, проявляющееся стойким изменением их структуры и функции, что ведет к расстройству их жизнедеятельности
Изменение структуры и функций клеточных органелл при повреждении клетки.
Некроз и аутолиз.
Некроз (гр. necro – мертвый) – гибель клеток и тканей, сопровождающаяся необратимым прекращением их жизнедеятельности. Основным механизмом аутолиза является гидролиз компонентов клеток и межклеточного вещества под влиянием ферментов лизосом. Этому способствует развитие ацидоза в поврежденных клетках.Под специфическими - изменения свойств клеток, характерные для данного фактора при действии его на различные клетки, либо свойственные лишь данному виду клеток при воздействии на них повреждающих агентов различного характера (нарушением целостности ее мембран. Высокая концентрация в крови альдостерона обуславливает накопление в различных клетках избытка ионов натрия. Повреждение всегда сопровождается комплексом и неспецифических, стереотипных изменений в клетках. Они наблюдаются в различных видах клеток при действии на них разнообразных агентов (ацидоз, чрезмерная активация свободно-радикальных и перекисных реакций, денатурация молекул белка, повышение проницаемости клеточных мембран потенциала, повышение сорбционных свойств клеток).3.Сердечная недостаточность - типовая форма патологии, возникающая вследствие различных причин, при которой ослабляется сократительная функция миокарда и сердце не обеспечивает потребности органов и тканей в адекватном кровоснабжении1. Интракардиальные:поражение миокарда (инфекционный миокардит, токсическая кардиомиопатия, инфаркт миокарда, ИБС, кардиосклероз)- нарушения ритма работы сердца (аритмии) при поражениях миокарда и/или проводящей системы сердца2. Перегрузка сердца сопротивлением (увеличение постнагрузки):артериальные гипертензии- стеноз клапана аорты- стеноз клапана легочной артерии- гидроперикард Перегрузка сердца объемом - увеличение преднагрузки: гиперволемия гемоконцентрация недостаточность аортального клапана едостаточность клапана легочной артерии врожденные пороки сердца синего типа (со сбросом крови справа налево): триада, тетрада, пентада Фалло Общие черты внутрисердечной гемодинамики при серд недостаточности↑ остаточного диастолического объёма вследствие неполной систолы↑ диастолического давления в желудочках дилатация сердца ↓МОК (может быть и ↑)Основные особенности гипертрофированного миокарда:нарушение регуляции гипертрофированного сердца (отставание роста рецепторов и др нервных окончаний от роста миокарда)↓ сосудистой обеспеченности миокарда (отставание роста мелких сосудов от роста мышечных кл-к)развитие относительной коронарной недостаточности↑ массы кардиомиоцитов по сравнению с их поверхностью. Причина – относительный недостаток ферментов, субстратов-белков↓ уровня энергообеспечения кл-к миокарда (отставание ↑ кол-ва митохондрий от роста массы миофибрилл)↓ сократительной способности миокарда
Билет 2
СОВРЕМЕННЫЕ МЕТОДЫ, ИСПОЛЬЗУЕМЫЕ В ЭКСПЕРИМЕНТЕ
В процессе познания _научный эксперимент .выполняет следую-
щие основные функции: 1) посредством вычленения отдельных свойств и сторон предмета дает возможность проникать в его су ность, раскрывать его закономерности; 2) материализуя ту или иную идею, выраженную в теории, гипотезе или предвидении, выс- тупает критерием их истинности, формой проявления общего; 3) выступает в качестве средства получения и накопления новых на- учных данных, является первоисточником новых гипотез и теорий;
4) дает возможность зафиксировать "отклонения" реальных предметов от абстрактно-идеального образа, созданного на основе из вестных законов науки
Для постановки эксперимента необходимо:
I. Формирование рабочей гипотезы.
II. Определение цели и постановка задач исследования.
III. Выбор частных методик, адекватных поставленным зада-
чам.
IY. Проведение эксперимента (серии опытов с контролем).
Y. Фиксация и анализ данных эксперимента.
YI. Обсуждение и выводы.
Экспериментальный метод .: основной метод патофизиологии, основанный на полученных данных в клинику Эксперимент: _острый . - сопровождается вивисекцией воспроизведении болезни у животного, изучение ее, и перенесение например: воспроизведение острой кровопо- тери).хронический . - подразумевает длительное наблю дение за экспериментальным жи вотным введение электродов, трансплантация
-Экспериментальные методики .:
1. Выключения - т.е. удаления какого-либо органа хирурги-
ческим или каким-либо другим воздействием (тепло, холод, радиа-
ция), введение антител, фармакологических препаратов).
2. Раздражения - производится стимуляция первичных струк-
тур для того, чтобы вызвать нарушение функции какого-либо орга-
на.
2Повреждение клеток выражается еще и _нарушением структу-
_ры и функции мембран .. Вообще способность формировать мембра-
ны является решающей в образовании клетки и ее субклеточных
органелл. Любое нарушение сопровождается изменением проница-
емости клеточных мембран и состояния цитоплазмы поврежденной
клетки. Повреждение клеточных мембран, согласно модели Син-
гера, может быть обусловлено деструкцией их липидных или
белковых (ферментных) компонентов.
Повреждение липидных компонентов клеточных и субклеточ-
ных мембран возникает несколькими путями. Важнейшими из них
являются перекисное окисление липидов (ПОЛ), активация мемб-
ранных фосфолипаз, осмотическое растяжение пептидной основы
мембран, повреждающееся воздействие иммунных комплексов.
Суммарным выражением патологии клеточной мембраны может
служить нарушение ее основных функций:
1) мембранного транспорта;
2) изменение проницаемости мембраны;
3) изменение коммуникации клеток и их "узнавания";
4) изменение подвижности мембран и формы клеток;
5) изменение синтеза и обмена мембран.
_Мембранный транспорт . предполагает перенос ионов и дру-
гих субстратов против градиента концентрации. При этом нару-
шается функция клеточных насосов и ингибируются процессы ре-
гуляции обмена веществ между клеткой и окружающей ее средой.
Повреждение Na-K-насоса вызывает освобождение ионов К
из клетки и накопление в ней ионов Na, что характерно для
гипоксических состояний, токсических повреждений клетки (яд
кобры, каракурта), инфекционных поражений, аллергии, сниже-
ния температуры внешней среды. С транспортом ионов Na и К
тесно связан транспорт ионов Са. Интегральное выражение этих
нарушений хорошо иллюстрируется на примере гипоксии миокар-
да, которая прежде всего проявляется патологией митохондрий.
Следует отметить, что повреждение мембран митохондрий
являлется ключом клеточного повреждения. В его прогрессиро-
вании большая роль принадлежит нарушению контроля уровня
кальция в цитоплазме. Ишемическое повреждение митохондрий
приводит к нарушению функции Na-К-АТФазного насоса, посте-
пенному накоплению в клетке Na и потере ею калия, что в со-
вокупности ведет к вытеснению Са из митохондрий. В результа-
те повышается уровень ионизированного кальция в цитоплазме и
увеличивается его связь с кальмодулином, что, в свою оче-
редь, приводит к расхождению клеточных стыков, активации
фосфолипаз. Эндоплазматическая сеть накапливает воду и ионы,
следствием чего является развитие гидропической дистрофии.
Усиление гликолиза сопровождается истощением гликогена, на-
коплением лактата и снижением рН. Таким образом, накопление
Са в клетке можно считать универсальным механизмом клеточной
деструкции.
_Проницаемость мембран . - качество мембраны, позволяющее
поддерживать обмен клетки со средой и осуществлять контроль
"перекрытых каналов", связанный с метаболизмом энергии и
конформацией белка. Проницаемость мембраны позволяет поддер-
живать не только постоянство электролитного состава клетки -
ионный гомеостаз, но и ионный гетерогенитет, т.е. вполне оп-
ределенные, резко выраженные различия ионного состава внут-
риклеточной м внешней среды.
В качестве примера изменения проницаемости для ионов
мембраны эритроцитов при иммунной травме следует указать на
специфический гемолиз. Процесс гемолиза начинается с увели-
чения проницаемости мембраны эритроцитов для ионов К, Na,
Ca. Нарушается функция Na-К-насоса, из эритроцитов выходит
К, а входит Na. Увеличивается проницаемость мембран для мо-
лекул глюкозы, аминокислот и ряда других метаболитов. Тормо-
зится обмен Cl- и HCO3- (феномен Гамбургера) и Cl- и SO4--
за счет фиксации на эритроците гемолизина и комплемента. Подвижность мембран и форма клеток .. Различают два типа изменений; выпячивание мембраны наружу - экзотропия, и выпя чивание мембраны внутрь цитоплазмы - эзотропия. Изменения
формы клеток связаны не только с этими двумя типами измене-
ний, нередко речь идет об упрощении клеточной поверхности,
т.е. потере специфических образований, без которых невозмож-
но нормальное функционирование клетки (например, потеря мик-
роворсинок энтероцитами). Синтез мембран . может усиливаться либо снижаться, также
ак и обмен мембран при некоторых заболеваниях.
Компенсаторная гиперфункция сердца - ↑ работы сердца при длительном воздействии перегрузки.
Стадии:
1. Аварийная стадия - кратковременная, патологические реакции преобладают над компенсаторными.
Характеризуется ↑ нагрузки на сердце, ↓ гликогена в миокарде, ↓ креатинфосфата, ↓ внутриклеточного K и ↑Na, распад гликогена и накопление лактата, гликолиз, активируется анаэробный синтез АТФ, активируется анаэробный ресинтез АТФ, растет масса миофибрилл, растет потребление кислорода, ↑ нагрузки на единицу мышечной массы сердца - ↑ интенсивности функционирования стр-р (ИФС); активация генетического аппарата, ↑ синтеза нукл к-т и белка с нарастанием кол-ва митохондрий → гипертрофия миокарда в течение нескольких недель.
Клинически - острая недостаточность сердца
2. Стадия завершившейся гипертрофии и относительно устойчивой гиперфункции.
Процесс гипертрофии завершён, масса миокарда ↑ и уже не растёт, ИФС нормализована, нормальная активность генетического аппарата, гемодинамика компенсирована.
В эту стадию компенсаторные реакции преобладают.
Клинически - нормализация гемодинамики.
3. Стадия постепенного истощения и прогрессирующего кардиосклероза.
Развивается при прогрессировании процесса с ↑ нагрузки на сердце. Развивается комплекс изнашивания гипертрофированного сердца. Избирательная гибель кардиомиоцитов с замещением их соед тканью. Основная причина комплекса изнашивания – рост митохондрий отстаёт от миофибрилл и часть миокарда остаётся энергетически необеспеченной; энергии не хватает и возникает истощение.
Клинически: недостаточность сердца и кровообращения.
Билет 3
В.В.ПАШУТИН (1845–1901) – один из основоположников патологической физиологии в России, почетный член Лондонского королевского общества, ученик И.М.Сеченова и С.П.Боткина. Он создал первую в России кафедру патофизиологии при Казанском университете в 1874 г., а через 5 лет открыл аналогичную кафедру в Военно-медицинской академии, кардинально переработав курс общей патологии в новом экспериментально–физиологическом направлении. Основные труды Виктора Васильевича посвящены разработке фундаментальных проблем голодания, обмена веществ, теплообмена и кислородной недостаточности. Им написан и издан двухтомник "Лекции по общей патологии (патологической физиологии)".
В.В.ПОДВЫСОЦКИЙ (1857–1913) – крупный отечественный патофизиолог, основоположник Киевской школы патофизиологов. Владимиром Валерьяновичем опубликовано свыше 90 научных работ, посвященных изучению процесса регенерации железистой ткани, проблеме развития опухолей, исследованиям в области микробиологии, иммунитета и патологии инфекций. Учебник В.В.Подвысоцкого "Основы общей и экспериментальной патологии" получил мировую известность. Его учениками были А.А.Богомолец, Д.К.Заболотный, И.Г.Савченко, Л.А.Тарасевич и др.
В.В.ВОРОНИН (1870–1960) – отечественный патофизиолог, профессор, почетный академик АН Грузии. Владимир Васильевич внес значительный вклад в учение о капиллярах, воспалении, а также в разработку проблем физиологии и патологии кровообращения. Им опубликовано около 70 работ, посвященных вопросам патофизиологии, морфологии, микробиологии, эпидемиологии, применению методов статистики и кибернетики в медицине. В числе его многочисленных учеников были А.А.Богомолец (Воронин получил премию имени АА.Богомольца – своего ученика), П.А.Герцен, В.П.Филатов и др.
А.А.БОГОМОЛЕЦ (1881–1946) – отечественный патофизиолог и общественный деятель, академик АН и АМН СССР, Герой Социалистического Труда, лауреат Государственной премии СССР, создатель крупной школы патофизиологов. Основное направление исследований Александра Александровича – изучение реактивности организма в нормальных и патологических состояниях. Его учение о трофической функции соединительной ткани является основой современных представлений о коллагенозах. Он был организатором и руководителем научной разработки консервирования крови.
А.Д.СПЕРАНСКИЙ (1888–1961) – российский патолог, академик АН и АМН СССР, лауреат Государственной премии СССР, заслуженный деятель науки РСФСР, ученик И.П.Павлова. Алексей Дмитриевич, развивая идеи нервизма И.П.Павлова, создал оригинальное направление в патологии, выявил общие закономерности развития нервно–дистрофических процессов и их генерализации, выдвинул концепцию о нервной системе как ведущем звене в механизмах заболевания, выздоровления и компенсации.
И.Р.ПЕТРОВ (1893–1970) – российский патофизиолог, академик АМН СССР, генерал–майор медицинской службы. Иоакимом Романовичем успешно разрабатывались проблемы кислородного голодания, кровопотери, шока и терминальных состояний, посттрансфузионных осложнений, электротравмы, профессиональной патологии. Всеобщее признание получили его научные работы по проблеме гипоксии. Им разработана плазмозамещающая жидкость (жидкость Петрова), которая широко использовалась во время Великой Отечественной войны, и принципы терапии шока.
А.М.ЧЕРНУХ (1916–1982) – академик АМН СССР, лауреат Государственной премии СССР. Всемирную известность получили работы Алексея Михайловича в области физиологии и патологии микроциркуляции и воспаления. В его трудах большое место занимает анализ механизмов заболевания и выздоровления, а также вопросы методологии общей патологии и учения о болезни. Им создан Институт общей патологии и патологической физиологии АМН СССР.
А.Д.АДО (род. в 1909 г.) – российский патофизиолог–аллерголог, академик АМН СССР, заслуженный деятель науки РСФСР. Основное направление трудов – вопросы патофизиологии аллергии, воспаления и иммунитета. Им впервые были проведены исследования по аутоаллергии, а совместно с П.К.Булатовым предложена клинико-патогенетическая классификация форм бронхиальной астмы. Он является автором учебника "Патологическая физиология". Андрей Дмитриевич много внимания уделяет вопросам общего учения о болезни, этиологии и патогенезе. По его инициативе в России создана аллергологическая служба.
П.Д.ГОРИЗОНТОВ (1902–1987)–выдающийся российский патофизиолог, академик АМН СССР, лауреат Ленинской и Государственной премий СССР, крупный организатор медицинской науки. Петр Дмитриевич окончил Омский медицинский институт и работал ассистентом на кафедре патофизиологии последнего в 30-х годах. Он активно разрабатывал наиболее актуальные проблемы теоретической патологии (этиология, патогенез, роль внешней среды в возникновении заболеваний), изучал патогенез лучевой болезни, стресс, разрабатывал методологические аспекты экспериментальной медицины.
3.Экстракардиальные ри снижении сердечного выброса у больных с сердечной недостаточностью активируются барорецепторы синокаротидной зоны и дуги аорты, происходит активация САС, при этом увеличивается концентрПация адреналина и особенно норадреналина в крови. Гиперактивация САС является одним из наиболее рано включающихся факторов компенсации при сердечной недостаточности. Активация САС на начальном этапе хронической сердечной недостаточности оказывает определенное положительное адаптивно-компенсаторное влияние на сердечно-сосудистую систему (ССС). Основными эффектами активации САС на этом этапе являются: увеличение частоты сердечных сокращений (ЧСС) и повышение сократительной функции миокарда вследствие стимуляции b1-адренорецепторов миокарда, что приводит к увеличению минутного объема крови;развитие компенсаторной концентрической гипертрофии миокарда;тимуляция a1-адренорецепторов и повышение венозного тонуса, что приводит к увеличению венозного возврата крови к сердцу и увеличению преднагрузки;тимуляция a1-адренорецепторов артерий и артериол, что вызывает повышение общего периферического сосудистого сопротивления• активация РААС вследствие стимуляции a1-адренорецепторов юкстагломерулярного аппарата почек. • увеличения объема циркулирующей крови в связи с чрезмерной активацией РААС и выраженной задержкой натрия и воды в организме; значительного повышения потребности миокарда в кислороде вследствие избытка катехоламинов и возросшей нагрузки на миокард;развития тяжелых нарушений сердечного ритма (мерцательной аритмии, желудочковой тахикардии, частой политопной желудочковой экстрасистолии и даже фатальных аритмий — трепетания и фибрилляции желудочков);непосредственного кардиотоксического эффекта (выраженная дистрофия миокарда, возможны даже некротические изменения);развития гибернации части кардиомиоцитов;
повышение потребности миокарда в кислороде под влиянием возрастающих постнагрузки и преднагрузки и продолжающейся активации САС;развитие гипертрофии, ремоделирования, апоптоза и фиброза миокарда с последующим снижением сократительной функции миокарда (гипертрофия миокарда и апоптоз кардиомиоцитов стимулируются ангиотензином - П, в развитии фиброза миокарда вследствие стимуляции синтеза коллагена огромную роль играет гиперпродукция альдостерона);Гиперсекреция антидиуретического гормона приводит к резкому усилению реабсорбции воды в почечных канальцах, увеличению объема циркулирующей крови, отекам.
Антидиуретический гормон обладает также вазоконстрикторным и вазопрессорным действием, повышает тонус вен, артерий, артериол, в результате чего увеличивается преднагрузка и постнагрузка, что резко повышает потребность миокарда в кислороде, способствует прогрессированию хронической сердечной недостаточности.
Кардиальные адаптационно-компенсаторные механизмы имеют большое патогенетическое значение при хронической сердечной недостаточности. Под влиянием нейрогуморальных воздействий, а также нередко вследствие влияния самого этиологического фактора (например, препятствия для выброса крови из левого желудочка при аортальном стенозе и т. д.) развивается концентрическая или эксцентрическая гипертрофия миокарда. Длительное существование увеличенной постнагрузки приводит к развитию концентрической гипертрофии миокарда — то есть к утолщению мышечной стенки без расширения полости желудочка. Увеличение толщины миокарда при концентрической гипертрофии позволяет развивать достаточное внутрижелудочковое давление в систолу и преодолеть значительно увеличенную постнагрузку и обеспечить адекватную перфузию органов и тканей. При увеличении преднагрузки постепенно развивается эксцентрическая гипертрофия, то есть умеренная гипертрофия миокарда, сопровождающаяся тоногенной дилатацией полости желудочка.
Гипертрофия миокарда и умеренная тоногенная дилатация ЛЖ в течение определенного времени обеспечивают сохранение достаточной величины сердечного выброса, что происходит в соответствии с законом Стерлинга - увеличение исходного конечного диастолического объема желудочка приводит к усилению его сокращения, что позволяет преодолеть увеличенную преднагрузку и постнагрузку.
Однако с течением времени в условиях продолжающейся гемодинамической
перегрузки или непосредственного повреждения миокарда компенсаторная реакция сердца становится недостаточной, эффективность механизма Стерлинга резко уменьшается, сердечный выброс снижается. Уменьшение насосной функции сердца запускает процессы ремоделирования сердца, которые происходят под влиянием всех вышеуказанных патогенетических механизмов сердечной недостаточности, прежде всего, высокой активности нейрогуморальных систем.
Ремоделирование — это структурно-геометрические изменения ЛЖ, включающие в себя процессы гипертрофии миокарда и дилатации сердца, приводящие к изменению его геометрии и нарушению систолической и диастолической функции.
4 билет
1.Патологическая реакция - неадекватный и биологически нецеле-
сообразный (вредный или бесполезный) ответ организма или отдельных
его систем на воздействие обычных или чрезвычайных (патогенных)
раздражителей.
Патологический процесс - закономерная последовательность
явлений, возникающих в организме при воздействии патогенного
фактора и включающая (в различных соотношениях) нарушения нор-
мального течения жизненных процессов и защитно-приспособитель-
ные реакции.
Патологическое состояние - стойкое отклонение от нормы, имею-
щее биологически отрицательное значение для организма.
Патологическое состояние - болезненные расстройства с ма-
лой динамичностью, медленно развивающийся процесс или его
последствия. При этом собственно болезни может и не быть в свя-
зи с полной компенсацией имеющихся нарушений (например, врож-
денные уродства - косолапость, гипоплазия органа, состояние
после ампутации конечности).
Патологическое состояние - это интегральное выражение па-
тологического процесса в каждый конкретный момент.
Типическим (типовым) является такой патологический про-
цесс, который развивается по общим закономерностям независимо
от вызвавших его причин, локализации и вида живого. Они эволю-
ционно закреплены. К типовым патологическим процессам относятся
воспаление, отек, лихорадка, нарушения микроциркуляции, гипок-
сия и другие процессы.
3. Внутрисердечные механизмы компенсации:
1) Срочные:
1. Гетерогенный механизм (обусловлен свойствами миокарда) включается при перегрузке объемом крови (по закону Франка-Старлинга) - линейная зависимость между степенью растяжения мышечного волокна и силой сокращения постоянно становится нелинейной (мышца не сокращается сильнее при увеличении ее растяжения).
2. Гомеометрический механизм при повышении сопротивления оттоку. Повышается напряжение миокарда при сокращении, Феномен мышцы - каждое последующее сокращение сильнее предыдущего.
Наиболее полезен гетерометрический механизм - меньше потребляется О2, меньше расходуется энергии.
При гомеометрическом механизме сокращается период диастолы - период восстановления миокарда.
Участвует внутрисердечная нервная система.
2) Долгосрочный механизм:
Компенсаторная гипертрофия сердца.
При физиологической гиперфункции прирост мышечной массы сердца идет параллельно с ростом мышечной массы скелетной мускулатуры.
При компенсаторной гипертрофии сердца увеличение массы миокарда идет независимо от роста мышечной массы.
Билет 5
ОПРЕДЕЛЕНИЕ ПОНЯТИЙ "ЗДОРОВЬЕ, БОЛЕЗНЬ, ПРЕДБОЛЕЗНЬ"
Здоровье - это состояние полного физического, психического
и социального благополучия, а не только отсутствие болезней или
физических дефектов (из преамбулы ВОЗ).
Здоровье - это не только отсутствие болезни и инвалид-
ности, но и наличие полноценного, гармонически развитого физи-
ческого, психического и нравственного состояния человека
(Б.В.Петровский).
Здоровье - это высокоустойчивое состояние саногенетических
механизмов, это выражение не только биологической сущности, но
и социальной стороны...(С.М. Павленко).
Здоровье - биологическая полноценность трудоспособного ин-
дивидуума (О.С. Глозман).
Здоровье - жизнь трудоспособного человека, приспособленного
к изменениям окружающей среды (И.Р. Петров).
Для здорового состояния человека характерно:
1. поддержание устойчивой неравновесности организма и сре-
ды;
2. сохранение целостности организма человека;
3. сохранение трудоспособности.
Норма здоровья - оптимальное состояние живой системы, при ко-
тором обеспечивается максимальная адаптивность, т.е. приспособляе-
мость к условиям жизни.
Норма здоровья - такая форма жизнедеятельности организма, ко-
торая обеспечивает ему наиболее совершенную деятельность и
адекватные условия существования.
Болезнь . - это особый вид страдания, вызванный поражением
организма, отдельных его систем различными повреждающими факто-
рами, характеризующийся нарушением системы регуляции и адапта-
ции и снижением трудоспособности(ВОЗ).
Предболезнь - это состояние организма, являющееся следс-
твием ослабления некоторых саногенетических механизмов и их
комплексов (С.М.Павленко).
Предболезнь (т.е. переход от здоровья к болезни) - это
снижение функциональной активности некоторых саногенетических
механизмов или их комплексов, ведущее к расстройству саморегу-
ляции и ослаблению резистентности организма.
Предболезнь формируется под действием факторов внешней
среды, но, в ряде случаев, с опосредованием через внутреннюю
среду организма.
В развитии предболезни можно выделить некоторые общие па-
тогенетические варианты:
1) наследственное (врожденное) состояние предболезни;
2) в ряде случаев на организм начинает действовать пато-
генный фактор, не способный (из-за малой интенсивности) и (или)
достаточности защитных сил организма вызвать развитие болезни.
Однако, при длительном воздействии он постепенно может приво-
дить к снижению саногенетических механизмов - например, запы-
ленность, загазованность, вибрация;
3) чаще встречается иная ситуация, когда состояние предбо-
лезни обусловлено действием одного причинного фактора (N1),
вызвавшего в организме ограничение возможности компенсатор-
но-приспособительных реакций, и на этом фоне может действовать
какой-то другой фактор (N2), который приведет к развитию опре-
деленного заболевания.
Хронический стресс может привести к снижению активности
или дезинтеграции системы иммунного надзора - состояние предбо-
лезни - и на этой основе возможно развитие различных заболева-
ний - инфекции, опухоли, аутоиммунные болезни.
_Преморбидная стадия . отличается возникновением специфичес-
ких, обычно единичных, симптомов, предопределяющих общую нап-
равленность развивающейся патологии - кардиологическую, пульмо-
нологическую, гастроэнтерологическую.
_Донозологическое состояние . проявляется усугублением расс-
тройств поражаемого органа, что приводит к нарастанию числа
специфических синдромов, сочетание которых позволяет определить
возможный нозологический диагноз.
_Факторы риска:
I. По принадлежности:
1. Социально-производственные (материальное обеспечение,
социальный дискомфорт, шум, вибрация, физическое и психическое пере-
напряжение, монотонность и однообразность выполняемых операций, запы-
ленность, микроклимат рабочих помещений, ночные смены и т.д.).
2. Семейно-бытовые (жилищные условия, межличностные взаи-
моотношения в семье, религиозно-воспитательные и санитарно-гигиеничес-
кие критерии, вредные привычки, нарушения режима отдыха, особенности
питания и т.д.).
3. Экологические (загрязнение окружающей среды, радиоак-
тивный фон, метеорологические и геомагнитные воздействия).
II. По механизму действия:
1. Неврогенные.
2. Алиментарные.
3. Инфекционно-токсические.
2.Одной из важнейших причин таких изменений являются свободно-радикальные реакции (СРР) и перекисное окисление липидов (ПОЛ). Эти реакции протекают в клетках и в норме, являясь необходимым звеном таких жизненноважных процессов, как транспорт электронов в цепи дыхательных ферментов, синтез простагландинов и лейкотриенов, пролиферация и созревание клеток, фагоцитоз, метаболизм катехоламинов.
Интенсивность ПОЛ регулируется соотношение факторов, активирующих (прооксиданты) и ингибирующих (антиоксиданты) этот процесс. К числу наиболее активных прооксидантов относятся легко окисляющиеся соединения, индуцирующие свободные радикалы, в частности, нафтохиноны, витамины А и Д, восстановители - НАДФН2, НАДН2, липоевая кислота, продукты метаболизма простагландинов и катехоламинов.
Процесс ПОЛ условно можно разделить на следующие этапы:
1) кислородной инициации (“кислородный” этап), 2) образование свободных радикалов (”свободнорадикальный” этап), 3) продукции перекисей липидов (“перекисный” этап) Инициальным звеном свободнорадикальных перекисных реакций при повреждении клетки является образование в процесса оксигеназных реакций активных форм кислорода: супероксидного радикала кислорода (О2-), гидроксильного радикала (ОН-), перекиси водорода (Н2О2), которые взаимодействуют с различными компонентами структур клеток, главным образом с липидами, белками и нуклеиновыми кислотами. В результате образуются активные радикалы, в частности липидов, а также их перекиси. Реакция может приобрести цепной “лавинообразный” характер. Однако, в клетках действуют факторы, ограничивающие свободнорадикальные и перекисные реакции, т.е. оказывают антиоксидантный эффект. В нижеприведенной таблице представлены ферментные и неферментные механизмы антиоксидантной защиты.
ЗВЕНЬЯ АНТИОКСИДАНТНОЙ СИСТЕМЫ И ЕЕ НЕКОТОРЫЕ ФАКТОРЫ
Чрезмерная активация свободнорадикальных и перекисных реакций, а также несостоятельность системы антиоксидантной защиты является одним из главных факторов повреждения мембран и ферментов клеток. Ведущее значение при этом имеют следующие процессы:
1) изменение физико-химических свойств липидов мембран, что обуславливает нарушение конформации их липопротеидных комплексов и соответственно снижение активности ферментных систем, обеспечивающих рецепцию гуморальных воздействий, трансмембранный перенос ионов и молекул, структурную целостность мембран;
2) изменение физико-химических свойств белковых мицелл, выполняющих структурную и ферментативную функции в клетке; 3) образование структурных дефектов в мембране - простейших каналов (кластеров) вследствие внедрения в них продуктов ПОЛ. Так накопление липидных гидроперекисей в мембране приводит к их объединению в мицеллы, создающие трансмембранные каналы проницаемости, по которым возможен неконтролируемый ток катионов и молекул в клетку и из нее, что сопровождается нарушением процессов возбудимости, генерации регулирующих воздействий, межклеточного взаимодействия и др. вплоть до фрагментации мембраны и гибели клетки.
В норме состав и состояние мембран и ферментов модифицируется не только свободнорадикальными и липоперекисными процессами, но также и лизосомальными ферментами, как свободными (солюбилизированными) так и мембраносвязанными: липазами, фосфолипазами, протеазами. Под действием различных патогенных факторов их активность или содержание в гиалоплазме может резко возрасти (например: вследствие ацидоза, способствующего повышению проницаемости лизосомальных мембран). В результате этого глицерофосфолипиды и белки мембран, а также ферменты клеток подвергаются интенсивному гидролизу. Это сопровождается значительным повышением проницаемости мембран и снижением кинетических свойств ферментов.
В результате действия гидролаз (главным образом липаз и фосфолипаз) в клетке накапливаются свободные жирные кислоты и лизофосфолипиды, в частности, глицерофосфолипиды: фосфатидилхолины, фосфатидилэтаноламины, фосфатидилсерины. Эти амфифильные соединения способны проникать и фиксироваться как в гидрофобной, так и в гидрофильной средах мембран. Внедряясь в биомембраны, они изменяют нормальную структуру липопротеиновых комплексов, увеличивают проницаемость, а также меняют конфигурацию мембран в связи с “клинообразной” формой липидных молекул. Накопление в большом количестве амфифильных соединений ведет к формированию в мембранах кластеров и появлению микроразрывов.
3. Повышение функции сердца в условиях перегрузки миокарда давлением или объемом связаны с активацией миокардиальных (локальных) нейрогормональных систем.
Существует миокардиальная ренин-ангиотензиновая система (РАС). Основным действующим компонентом РАС является ангиотензин II (АТ II)
АТ II миокардиальной РАС
оказывает как прямое пролиферативное действие на кардиомиоциты и гладкомышечные клетки сосудов, вызывая их гипертрофию, так и опосредованное действие - путем стимуляции или потенцирования действия факторов роста
Эндотелин - вазоконстрикторный пептид, синтезируется в сосудах и миокарде разными клетками: эндотелиоциты сосудов, миоциты желудочков сердца, фибробласты.
Увеличение эндотелина способствует ремоделированию миокарда, вызывает гипертрофию миоцитов и изменения в экстрацеллюлярном матриксе в виде увеличения фиброза.
В ответ на эти факторы активизируется генетический аппарат мышечных и соединительно-тканных клеток (c-myc, c-fos), увеличивается синтез ДНК и РНК, числа рибосом, усиливается синтез белков, что ведет к быстрому увеличению объема мышечного волокна, его внутриклеточной гиперплазии и гипертрофии
Развитие гипертрофии миокарда приводит к увеличению площади поперечного сечения миокарда, при этом показатель А удельная работа вновь возвращается к нормальным величинам (в пределах ~1)
Билет 6
Болезнь . - это особый вид страдания, вызванный поражением
организма, отдельных его систем различными повреждающими факто-
рами, характеризующийся нарушением системы регуляции и адапта-
ции и снижением трудоспособности(ВОЗ).
Болезнь - это сложная реакция организма на действие болезнет-
ворного агента, качественно новый процесс, возникающий в результа-
те расстройства взаимоотношения организма с окружающей средой и
характеризующийся нарушением его функций и приспособляемости, ог-
раничением работоспособности и социально полезной деятельности
(Д.Е.Альперн).
Болезнь - качественно новый процесс жизнедеятельности,
возникающий в результате воздействия на организм чрезвычайного
раздражителя, характеризующийся, с одной стороны нарушением
функции отдельных звеньев нервно-регуляторного аппарата, а с
другой - рефлекторным включением защитно-приспособительных ме-
ханизмов, направленных на выздоровление (С.М.Павленко).
Болезнь - это сложная качественно новая реакция организма
на действие чрезвычайного раздражителя, возникающая вследствии
расстройства взаимодействия его с окружающей средой и характе-
ризуется:
- нарушением функций и морфологических структур организма,
регуляции функций и жизнедеятельности;
- расстройством взаимодействия организма с окружающей сре-
дой, т.е. снижением приспосабливаемости;
- ограничением работоспособности и социально-полезной дея-
тельности.
Наиболее общие формы возникновения заболеваний:
Острое (внезапное) без скрытого периода и с инкубационным периодом, что характерно для действия ионизирующей радиации, инфекций, химических факторов.
Постепенное (хроническое), характерное для болезней обмена веществ (подагра), эндокринных заболеваний (сахарный диабет, микседема и др.).
Формы течения заболеваний:
Ациклическое или прямолинейное, характеризующееся интенсивным нарастанием сдвигов.
Циклическое, протекающее в несколько стадий. Циклически протекают лучевая болезнь, инфекционные заболевания. Выделяют следующие периоды:
латентный,
продромальный период (неспецифические симптомы),
разгар болезни,
период выздоровления.
Течение заболеваний может быть типическим и атипическим. Типическим считается заболевание в том случае, если обнаруживаются симптомы, характерные для данной нозологической формы. Атипическое течение характеризуется отклонением от обычного течения и может проявляться в виде стертой формы (с невыраженной или слабо выраженной симптоматикой), абортивной (с укороченным течением, быстрым исчезновением всех болезненных проявлений и внезапным выздоровлением). Молниеносные формы характеризуются быстро нарастающим и тяжелым течением заболевания.
Рецидивирующее течение заболевания. Рецидив (лат. recidivus – возобновляющийся) – возобновление или усугубление проявлений болезни после их временного исчезновения, ослабления или приостановки болезненного процесса (ремиссии). Рецидивирующее течение характерно для некоторых инфекционных заболеваний: брюшной и возвратный тиф, малярия, бруцеллез, а также наблюдается и при таких соматических заболеваниях как подагра, ревматизм, язвенная болезнь желудка, шизофрения и др. Симптомы рецидива могут повторять первичную картину болезни, но могут и отличаться по своим проявлениям.
Рецидивирующее течение болезни предполагает наличие ремиссий (от лат. remissio – уменьшение, ослабление) – временное улучшение состояния больного, связанное с замедлением или прекращением прогрессирования болезни, частичным обратным развитием. Клинически это выражается временным ослаблением или исчезновением видимых проявлений болезни. Ремиссия является в ряде случаев характерным этапом болезни, но отнюдь не выздоровлением, так как вновь сменяется рецидивом, т.е. обострением патологии.
Латентное течение – внешне не проявляющееся течение заболевания (малярия).
Если к основному заболеванию присоединяется другой патологический процесс или другое заболевание, не обязательные для данной болезни, но возникшие в связи с ним, то говорят об осложнении (корь – воспаление легких).
Обострение – стадия течения хронического заболевания, характеризующаяся усилением имеющихся симптомов или появлением новых. Возможен также переход острого заболевания в хроническое.
По продолжительности течения заболевания различают:
острое (до 2 недель),
подострое (от 2 до 6 недель),
хроническое (свыше 6–8 недель).
Окончание заболевания может быть двояким:
Критическим – резкое изменение течения заболевания (как правило, к лучшему). Например, при инфекционном заболевании может внезапно нормализоваться температура тела, что сопровождается усиленным потоотделением, слабостью и сонливостью (возможен коллапс – острая сосудистая недостаточность).
Литическим – медленное исчезновение симптомов заболевания.
Возможно три исхода болезней:
а) полное выздоровление,
б) неполное выздоровление или переход в патологическое состояние,
в) смерть.
Выздоровление – один из исходов болезни, заключающийся в восстановлении нормальной жизнедеятельности организма после болезни. О выздоровлении судят по морфологическим, функциональным и социальным критериям. Ведущими являются функциональные и социальные критерии. Когда нет морфологического и функционального восстановления, то очень важна социальная реабилитация. Следует помнить о том, что выздоровление не является возвратом к исходному состоянию (аппендэктомия).
Полное выздоровление характеризуется практически полным восстановлением нарушенных во время болезни функций организма, приспособительных возможностей и трудоспособности.
Неполное выздоровление или переход в патологическое состояние – это исход патологического процесса или болезни, это устойчивый малодинамичный процесс. Неполное выздоровление характеризуется неполным восстановлением нарушенных во время болезни функций, с ограничением приспособительных возможностей организма и трудоспособности.
Смерть – это самый неблагоприятный исход заболевания. Она может быть естественной (физиологическая от дряхлости, старения) и преждевременной, которая может быть насильственной (убийство) и от заболевания. Кроме того, выделяют смерть мозговую (внезапная гибель головного мозга на фоне всех здоровых органов, поддерживаемых искусственной вентиляцией легких) и соматическую, наступающую в результате необратимого, несовместимого с жизнью поражения какого–либо органа, органов или систем. Она чаще встречается при хронических заболеваниях, когда одновременно, но медленно погибают кора головного мозга и внутренние органы.
23.Гипертрофия - компенсаторно-приспособительное увеличение массы органа за счет возрастание массы каждой его структурной единицы, сопровождающееся усилением функции
Гипертрофия имеет приобретенный характер и является обратимым процессом. В этой стадии масса увеличивается на 100 – 120 % и больше не прибавляется, что позволяет сердцу адекватно выполнять свою функцию
В миокарде новообразования клеток не происходит и в основе гипертрофии лежит усиление анаболических процессов и гиперплазия клеточных органелл (митохондрий, мышечных белков, рибосом…)
В эту стадию патологические изменения в обмене и структуре миокарда не выявляются, потребление кислорода, образование энергетических соединений не отличаются от нормы.
Нормализуются гемодинамические нарушения. Гипертрофированное сердце приспособилось к новым условиям нагрузки и в течение длительного времени компенсирует их
Гипертрофия миокарда может быть реализована по концентрическому или эксцентрическому типу. Увеличение напряжения миокарда во время систолы при перегрузке сопротивлением является основным фактором, стимулирующим развитие концентрической гипертрофии миокарда (параллельное добавление миофибрилл) - утолщению мышечной стенки без расширения полости желудочка. перегрузке объемом во время диастолы развивается эксцентрическая гипертрофия (последовательное добавление миофибрилл), при которой утолщение стенки сопровождается расширением полости органа и сохранением его функции. Это явление носит название тоногенная дилятация, подразумевая в данном случае под этим термином как степень растяжения мускулатуры сердца, так и степень сокращения к концу диастолы.
В условиях достигнутого предела функциональных нагрузок, гиперплазия и гиперфункция компенсирующих структур относительно стабилизируются по степени, что соответствует стадии устойчивой компенсации.
Термин "ремоделирование сердца" был предложен N. Sharp в конце 70-х годов прошлого века .
В клинике структурные изменения желудочков, характеризующиеся гипертрофией, дилатацией, увеличением массы миокарда, изменением геометрии и формы левого желудочка
называют ремоделированием
миокарда
Структурно–геометрические изменения в сердце:
- гипертрофия, гиперплазия, нарушение взаимного расположения миофибрилл
- дистрофия, фиброз, замена коллагена типа I на тип III
- снижение относительной плотности капилляров
- увеличение капилляро–мышечного пространства
Последствия:
- изменение геометрии полостей сердца и его контуров
- дилатация полостей его желудочков и предсердий
- снижение сократительной функции миокарда
Стадия истощения характеризуется глубокими нарушениями обмена веществ, что проявляется в нарушении энергообразования и, как следствие, сократительной функции миокарда.
В результате дефицита кислорода в кардиомиоцитах происходит накопление промежуточных продуктов обмена СЖК – ацилкарнитина, ацил-КоА, НАД·Н, угнетается пируватдегидрогеназа, соответственно устраняется возможность утилизации пирувата, в результате чего он практически полностью превращается в лактат.
Лактат накапливается в клетке вместе с ионами Н+, что приводит к снижению внутриклеточного рН и развитию внутриклеточного ацидоза
Промежуточные продукты обмена СЖК угнетают адениннуклеотидтранслоказу митохондрий и затрудняют перенос макроэргических фосфатов через их мембрану, что нарушается процесс образования энергии в миокарде
Формирующийся тканевый лактатацидоз вызывает разобщение окислительного фосфорилирования, вызывая перегрузку кардиомиоцитов ионами кальция, который активирует фосфолипазу А2 с последующим инициированием процессов ПОЛ и повреждением мембран-
ных структур.
Нарушается работа гипоксантин-ксантиновой системы. При дефиците кислорода ксантиндегидрогеназа функционирует как оксидаза, которая приводит к образованию активных форм кислорода и активации
СРО
Начинают преобладать отрицательные биологические эффекты механизмов, которые ранее способствовали компенсации, формируются так называемые «порочные круги».
Под влиянием ангиотензина II стимулируется рост фибробластов, повышается содержание коллагена. Это способствует снижению плотности капилляров, нарушению диффузии кислорода и ишемии миокарда
Повышенное содержание коллагена приводит к снижению эластичности миокарда и повышению его ригидности
Чрезмерная гипертрофия миокарда и воздействие на него повышенного количества катехоламинов сопровождается увеличением потребности миокарда в кислороде.
В результате гипертрофии миокарда возникает также относительная недостаточность его кровоснабжения
На уровне органа: увеличение массы сердца опережает рост иннервирующих его аксонов симпатических нейронов. В результате концентрация норадреналина в миокарде падает, что приводит к снижению инотропного и расслабляющего эффекта
На уровне тканей: рост артериол и капилляров отстает от увеличения размеров мышечных клеток, что приводит к локальной гипоксии и ишемии, снижению коронарного резерва
На уровне клетки: масса клетки увеличивается в большей степени, чем ее поверхность, покрытая сарколемной мембраной. Снижается мощность локализованных в мембране K-Na, Na-Ca насосов, что нарушает ионный транспорт, сопряжение сокращения и
расслабления сердечной
мышцы.
На уровне органелл:
при значительном увеличении массы миофибрилл, становится мало митохондрий, что приводит к снижению энергообеспечения гипертрофированного сердца
На уровне молекул: увеличения соотношения между легкими и тяжелыми цепями в головках молекул миозина (тяжелые цепи - носители АТФ-азной активности), что приводит к снижению скорости сокращения сердечной мышцы
Билет 7
Этиология – это учение о причинах и условиях возникновения и развития болезней. общую, изучающую общие закономерности происхождения целых групп заболеваний (инфекционных, аллергических, онкологических, сердечно–сосудистых и др.);
частную, изучающую причины возникновения отдельных заболеваний (нозологических форм) – сахарного диабета, пневмонии, инфаркта миокарда. Частную этиологию изучают клиницисты.
2.2. Характеристика и классификация причинных факторов и условий
Под причиной или этиологическим фактором понимают такой предмет или явление, которые, непосредственно воздействуя на организм, вызывают при определенных условиях то или иное следствие, т.е. болезнь и сообщают ей специфические черты.
Классификация причин (принципы).
По происхождению все этиологические факторы делят на две группы:
Внешние (экзогенные) этиологические факторы:
механические – воздействие явлений или предметов, обладающих большим запасом кинетической энергии, способных в момент соприкосновения с организмом вызвать перелом, растяжение, размозжение и т.д.);
физические – воздействие различных видов энергии:
электрической (ожоги, электрошок, фибрилляция сердца), ионизирующего излучения (лучевые ожоги, лучевая болезнь), термических факторов (высокой и низкой температуры – ожоги, отморожения);
химические – воздействие кислот, щелочей, ядов органической и неорганической природы, солей тяжелых металлов, гормонов и т.д.;
биологические – вирусы, бактерии, гельминты;
психогенные – точкой приложения этих факторов является кора головного мозга. Они вызывают ятрогенные заболевания (iatros – врач; gennao – создавать). Эти заболевания развиваются вследствие неправильного поведения медицинских работников ("исчезла печень" вместо того, чтобы сказать "печень сократилась до нормальных размеров"; "не сердце, а тряпка" вместо "слабые, вялые сокращения сердца" и т.д.). Иногда неправильное поведение медработников ухудшает течение имеющегося заболевания.
К "внутренним" относят наследственные и конституциональные факторы. 2. По интенсивности действия (классификация И.П.Павлова) различают следующие этиологические факторы:
чрезвычайные, или необычные, экстремальные этиологические факторы (большие дозы яда, воздействие молнии,
обычные, но действующие в необычных количествах и размерах, т.е. обычные по своей природе, но выходящие по интенсивности за пределы диапазона физиологических приспособительных возможностей организма (недостаточное содержание кислорода в воздухе,
индифферентные – факторы, которые у большинства людей не вызывают заболеваний, но у некоторых при определенных условиях могут стать причиной заболевания. К ним относятся аллергены: пыльца растений,
Условие (лат. – conditio) – это такой фактор, обстоятельство или их комплекс, которые воздействуя на организм, сами по себе вызвать заболевание не могут, но они влияют на возникновение, развитие и течение заболевания. Например, микобактерии туберкулеза вызывают заболевание не у всех людей, а лишь при наличии неблагоприятных условий.
Неблагоприятные условия углубляют связь между причиной и следствием и способствуют возникновению заболевания.
Внешние условия делят на бытовые, социальные, природные. К внешним неблагоприятным условиям можно отнести неполноценное питание, неправильную организацию режима дня, жару, сырость, холод и т.д.
К внутренним, т.е. связанным с самим организмом, неблагоприятным условиям относят: наследственную предрасположенность, ранний детский возраст, старческий возраст, патологическую конституцию.
Роль причинного фактора в возникновении заболевания:
а) причинный фактор необходим . Всякое заболевание имеет свою причину, без нее болезнь не может возникнуть ни при каких условиях. б) причинный фактор незаменим, т.е. не может быть заменен совокупностью неблагоприятных условий;
в) причина действует непосредственно на организм, вызывая то или иное следствие – заболевание, патологический процессг) причинный фактор обусловливает основные специфические черты заболевания (клинические проявления вирусного гепатита существенно отличаются, точнее, абсолютно не похожи на клинические проявления стенокардии, эпилепсии, пневмонии и т.д.).
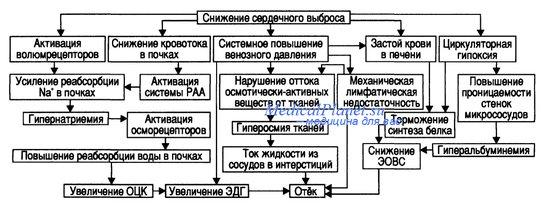
3. Центральным патогенетическим звеном хронической сердечной недостаточности является снижение сердечного выброса, а также дисбаланс вазоконстрикторных и вазодилатирующих нейрогуморальных систем
Для поддержания на должном уровне артериального давления активизируется симпатоадреналовая система. Выброс катехоламинов приводит к вазоконстрикции сосудов и усугублению снижения кровоснабжения
органов и тканей
Уменьшение кровоснабжения почек активизирует ренин-ангиотензиновую систему, действие которой также направлено на поддержание нормальных величин артериального давления
Ангиотензин II, синтезируемый ренин-ангиотензиновой системой, стимулирует синтез альдостерона, который повышает реабсорбцию в почках натрия и способствует активации антидиуретического гормона. Это приводит задержке в организме воды, увеличению объема циркулирующей крови и формированию застойной сердечной недостаточности.
Билет 8
Монокаузализм (mono – один, causa – причина) – механистическое учение, признающее значимость только причин и отрицающее роль условий в возникновении заболевания. Его возникновение связано с бурным развитием микробиологии и разработкой представлений об инфекционном процессе. Сторонники этого направления в медицине утверждали, что для возникновения инфекционных болезней вполне достаточно проникновения инфекционного возбудителя в организм, а реактивность организма, его индивидуальная восприимчивость, условия жизни не имеют никакого значения. Это учение материалистическое, но механистическое, так как слишком упрощенно толкуется роль этиологического фактора. Сторонники этого направления в медицине считали причинную связь единственной связью, а она, как известно, является только частицей всеобщей связи. Они не признавали значимость условий, а саму каузальную связь превращали в простую механическую связь, утверждая, что то, что содержится в причинном факторе, то и содержится в следствии. Такого, как известно, не бывает: при воздействии на живой организм какого–либо причинного фактора на последствиях этого воздействия обязательно скажется и роль условий.
Сторонники это направления в понимании этиологии сводят на нет роль врача и возможность, улучшая условия жизни человека, влиять на возникновение и развитие заболевания.
Кондиционализм (лат. conditio – условие) – субъективно–идеалистическое направление в медицине, отрицающее объективную причинность возникновения болезней и подменяющее категорию причины понятием суммы равноценных по значению условий. Появление этого направления в медицине было связано с дальнейшим развитием естествознания, и в частности микробиологии, сторонники которого попытались опровергнуть монокаузализм. Их утверждения базировались на тех наблюдениях, когда проникновение патогенных микробов в организм человека не всегда сопровождалось развитием заболевания: нужны были определенные условия, которые, по их мнению, играли решающую роль. Ферворн и Ганземан утверждали, что принцип каузальности устарел. Они отвергали существование причины, выбросив таким образом из всеобщей связи причинный фактор и тем самым обезоружив практическую медицину. Кондиционалисты нивелируют значение конкретной причины той или иной болезни, полностью приравнивая ее к прочим условиям и игнорируют принцип причинности.
Это учение идеалистично (так как отрицает причину), антинаучно (всякое явление можно понять только на основе знания причины), реакционно (если болезнь случайное стечение обстоятельств, то, следовательно, нет радикального лечения и профилактики).
Конституционализм – направление в медицине, согласно которому решающее значение для возникновения и течения болезни имеют определенные особенности конституции организма, обусловленные неполноценностью его генотипа и передающиеся из поколения в поколение. Это учение базируется на формальной генетике: если есть дефект в генах, то болезнь проявится обязательно. С позиций формальной генетики признавалась фатальность – неизбежность заболевания при генных изменениях. Это учение антинаучно, реакционно. На этом учении базируется фашизм, расизм. Оно оправдывает многие неэтические действия врачей (стерилизацию неполноценных людей). Конституционалисты считали, что медицина сохраняет жизнь неполноценных людей и увеличивает банк патологических генов. Конституционалисты недооценивают роль окружающей среды в возникновении болезней.
Монокаузализм и кондиционализм в их первоначальном виде уже нигде не встречается. Однако, современные варианты кондиционализма в виде "полиэтиологизма", "теории факторов", "факторов риска" широко бытуют не только за рубежом, но и в отечественной медицине. Пропагандируются концепции "болезней цивилизации", "социальной дезадаптации", "холизм". Под предлогом социальных проблем медицины формируются субъективно–идеалистические и биологизаторские установки в понимании здоровья и болезни человека.
2. Воспаление – типовой патологический процесс, сформировавшийся в эволюции как защитно-приспособительная реакция организма на воздействие патогенных (флогогенных) факторов, направленная на локализацию, уничтожение и удаление флогогенного агента, а также на устранение последствий его действия и характеризующийся альтерацией, экссудацией и пролиферацией.
Этиология воспаления:
Воспаление возникает как реакция организма на патогенный раздражитель и на вызываемое им повреждение. Патогенные, называемые в данном случае флогогенными, раздражители, т.е. причины воспаления, могут быть разнообразные: биологические, физические, химические как экзогенного, так и эндогенного происхождения.
Этиогенные факторы: Тромб, эмбол, отложение солей, кровоизлияние, опухоль
Экзогенные факторы: механические, физические, химические, биологические.
Главная роль - рефлекторного механизма.
Классификация:
Различают три основных формы воспаления:
интерстициальное диффузное;
гранулематозное;
воспалительные гиперпластические (гиперрегенераторные) разрастания
Местные признаки воспаления.
Покраснение – яркий клинический признак воспаления, связано с расширением артериол, развитием артериальной гиперемии и “артериализацией” венозной крови в очаге воспаления.
Припухлость из-за образованием инфильтрата, вследствие развития экссудации и отека, набухания тканевых элементов.
Жар, повышение температуры, развивается из-за усиленного притока теплой артериальной крови, в результате активации метаболизма, повышения теплопродукции и теплоотдачи в очаге воспаления.
Боль – возникает в результате раздражения окончаний чувствительных нервов различными биологически активными веществами (гистамин, серотонин, брадикинин и др.), сдвига рН внутренней среды в кислую сторону, возникновения дисионии, повышения осмотического давления в очаге повреждения, вызванного усиленным распадом тканей, механическим сдавлением тканей, вышедшей из кровеносного русла в окружающую ткань жидкостью.
Нарушение функции на почве воспаления возникает, как правило всегда; иногда это может ограничиваться расстройством функций пораженной ткани, но чаще страдает весь организм, особенно когда воспаление возникает в жизненно важных органах.
Признаки общего характера: I. Изменение количества лейкоцитов в периферической крови.
Подавляющее большинство воспалительных процессов сопровождается лейкоцитозом, значительно реже, при воспалении вирусного происхождения – лейкопенией. По своей природе лейкоцитоз является, в основным перераспределительным, т.е. обусловлен перераспределением лейкоцитов в организме, выходом их в кровеное русло.
2. Лихорадка развивается под влиянием поступающих из очага воспаления пирогенных факторов: первичных пирогенов экзо- и эндогенного происхождения и вторичных пирогенов и вторичных пирогенов
3. Изменение количества и качественного состава белков плазмы крови. При остром воспалительном процессе в крови накапливаются синтезируемые гепатоцитами, макрофаками и др. Клетками так называемые “белки острой фазы” воспаления. Для хронического течения воспаления характерно увеличение в крови содержания - и особенно -глобулинов.
4. Увеличение скорости оседания эритроцитов (СОЭ), что особенно имеет место при хронических воспалительных процессах, обусловлено повышением вязкости крови, снижением отрицательного заряда и агломерацией эритроцитов, изменениями состава белков крови, подъем температуры.
5. Изменения содержания гормонов в крови заключаются, как правило, в увеличении концентрации катехоламинов, кортикостероидов.
Билет 9
Термин "патогенез" происходит от двух слов: греч. pathos –страдание (по Аристотелю, pathos – повреждение) и genesis – происхождение, развитие. Патогенез – это учение о механизмах развития, течения и исхода болезней, патологических процессов и патологических состояний. Изучая патогенез, мы отвечаем на вопрос: как, каким образом возникло заболевание, т.е. выясняем механизмы развития болезни и имеем дело преимущественно с внутренними факторами.
а) частный патогенез, который изучает механизмы отдельных патологических реакций, процессов, состояний и заболеваний (нозологических единиц). б) общий патогенез предполагает изучение механизмов, наиболее общих закономерностей, лежащих в основе типовых патологических процессов или отдельных категорий болезней (наследственных, онкологических, инфекционных, эндокринных и т.д.). Общий патогенез занимается изучением механизмов, приводящих к функциональной недостаточности какого–либо органа или системы. Например, общий патогенез изучает механизмы развития сердечной недостаточности у больных с патологией сердечно–сосудистой системы: при пороках сердца, инфаркте миокарда, ишемической болезни сердца, заболеваниях легких с легочной гипертензией.
Общий и частный патогенез тесно связаны друг с другом, так как вскрытие и обобщение общих закономерностей возможно только на основе анализа частных форм патологии, а созданное на этой основе учение об общем патогенезе используется при раскрытии механизмов конкретных заболеваний и индивидуальных форм их течения.
Изучение патогенеза сводится к изучению так называемых патогенетических факторов, т.е. тех изменений в организме, которые возникают в ответ на воздействие этиологического фактора и в дальнейшем играют роль причины в развитии болезни. Патогенетический фактор вызывает появление новых расстройств жизнедеятельности в развитии патологического процесса, болезни.
2. Динамика сосудистых реакций и изменения кровообращения при развитии В. стереотипа: вначале возникает кратковременный рефлекторный спазм ортериол и прекапилляров с замедлением кровотока, затем, сменяя друг друга, развивается артериальная и венозная гиперемия, престаз и стаз – остановка кровотока.
Артериальная гиперемия является результатом образования в очаге В. большого количества вазоактивных веществ – медиаторов В., которые подавляя автоматию гладкомышечных элементов стенки артериол и прекапилляров, вызывают их расслабление. Это приводит к увеличение притока артериальной крови, ускоряет ее движение, открывает ранее не функционировавшие капилляры, повышает в них давление. Кроме того, приводящие сосуды расширяются в результате “паралича” вазоконстрикторов и доминирования парасимпатических влияний на стенку сосудов, ацидоза, гиперкалийионии, снижения эластичности окружающей сосуды соединительной ткани.
Венозная гиперемия возникает вследствие действия ряда факторов, которые можно разделить на три группы: 1) факторы крови, 2) факторы сосудистой стенки, 3) факторы окружающих тканей. К факторам, связанным с кровью, относится краевое расположение лейкоцитов, набухание эритроцитов, выход жидкой части крови в воспаленную ткань и сгущение крови, образование микротромбов вследствие активации фактора Хагемана и уменьшении содержания гепарина.
Влияние факторов сосудистой стенки на венозную гиперемию проявляется набуханием эндотелия, в результате чего просвет мелких сосудов еще больше суживается. Измененные венулы теряют эластичность и становятся более податливыми сдавливающему действию инфильтрата. И, наконец, проявление тканевого факторов состоит в том, сто отечная ткань, сдавливая вены и лимфатические сосуды, способствует развитию венозной гиперемии.
С развитием престатического состояния наблюдается маятникообразное движение крови – во время систолы она движется от артерий к венам, во время дистолы – в противоположном направлении. Наконец, движение крови может полностью прекратиться и развивается стаз, следствием которого могут быть необратимые изменения клеток крови и тканей.
