
Вариант №4.
1.Выражение ∆G0= -RTlnKназывают уравнением:
1) первого закона термодинамики;
2) второго закона термодинамики;
3) закона Гесса;
4) изотермы;
5) изобары.
2. Данная диаграмма есть диаграмма
1) Системы с неограниченной растворимостью компонентов в жидком состоянии. В твердом состоянии компоненты образуют химические соединения, которые плавятся конгурэнтно;
2) Системы с неограниченной растворимостью в жидком и твердом состояниях;
3) Системы с неограниченной растворимостью компонентов в жидком и взаимной нерастворимостью в твердом состоянии.
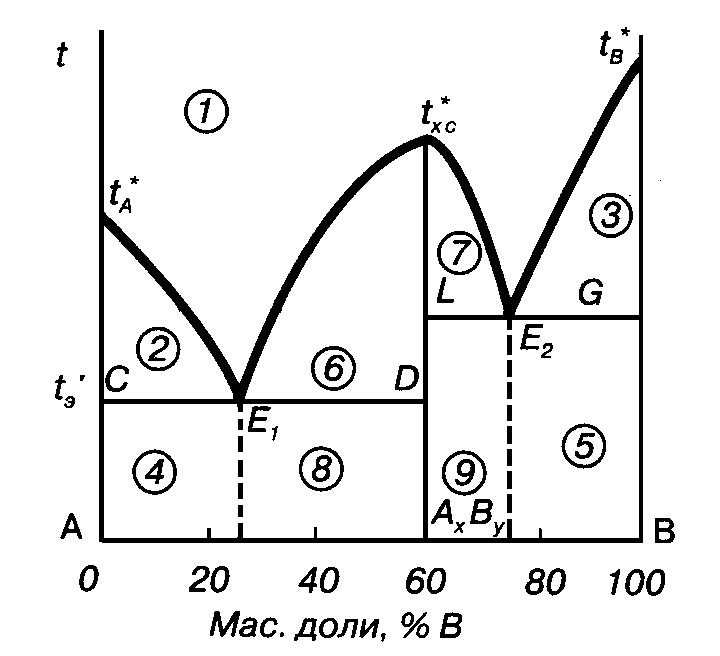
3. В фигуративной точке "а" система обладает числом степеней свободы, равным:
1) 2; 2) 1; 3) 0.
4.Температурой кипения жидкости является температура, при которой давление насыщенного пара над ней становится:
равным внешнему давлению;
больше внешнего давления;
меньше внешнего давления;
температура кипения жидкости не зависит от внешнего давления;
температура кипения является постоянной величиной.
5.При одинаковой ли температуре:
а) закипают 0,1- ный растворNaCIи 0,1- ный растворKCI
б) замерзают 0,1- ный растворNaCIи 0,1- ный растворKCI
да, да;
нет, нет;
да, нет;
нет, да;
для ответов не хватает данных.
6. К достоинствам потенциометрического титрования можно
отнести:
1) возможность определения в мутных и окрашенных средах;
2) определение с погрешностью < 0,1%;
3) использование электродных систем;
4) использование аппаратуры;
5) компенсационный метод измерения.
7. Электродвижущая сила гальванического элемента -связана с энергией Гиббса зависимостью:
1) rG = -zF;
2) rG = -(zF/RT);
3) rH +T rS = -zF;
4) rH -T rS = +zF;
5) E(-) –E(+) =rG.
8 Поверхностная активность пропанола будет больше поверхностной активности этанола в растворах одинаковой концентрации в
а). 34,33 раза
б). 9,75 раза
в).3,2 раза
9. Особенности строения ПАВ, обуславливающие их высокую адсорбционную способность
а) наличие полярной группы
б) наличие неполярного радикала
в) дифильная природа
10. В системе полярный адсорбент – неполярный растворитель
а) неполярная часть молекулы ПАВ обращена к поверхности адсорбента, а полярная часть погружена в растворитель
б) молекулы растворителя выигрывают конкуренцию за активные центры адсорбента
в) полярная часть молекулы ПАВ обращена к поверхности адсорбента, неполярная часть погружена в растворитель
11. Характеристика коллоидных систем по степени дисперсности:
а) гомогенные
б) гетерогенные;
в) ультрамикрогетерогенные
12. Конденсационный метод получения коллоидных систем заключается в
а) механическом, физическом или физико-химическом измельчении крупных частиц
+б) укрупнении частиц при агрегации молекул или ионов химическим или физическим способом
в) образовании малорастворимых в данной среде веществ
13. Электрокинетический ξ -потенциал возникает на границе
а) агрегат – адсорбционный слой ионов
б) адсорбционный слой – диффузный слой
в) потенциалопределяющие ионы – диффузный слой
14. При взаимодействии избытка сульфата меди (II) с гексацианоферратом (II) калия образовался золь, в диффузном слое которого находятся ионы
а) К+
б) SO42-
в)Cu2+
15. Строение мицеллы золя гидроксида алюминия, полученного гидролизом AlCl3:
а)
![]()
б)
![]()
+в)
![]()
16. Ионы Al3+являются эффективным коагулянтом для золя
а) {[mAs2S3]·nS2-(2n-x)H+}x-·xH+
б) {[mFe(OH)3]·nFe3+3(n-x)Cl-}3x+·3xCl
в) {[mBaSO4]·nBa2+2(n-x)SO42-}2x+·2xSO42
17. Лиотропный ряд ионов металлов по увеличению порога коагуляции выглядит как
а) Cs+>Rb+>K+>Na+>Li+
б) Li+>Na+>K+> Rb+> Cs+
в) Cs+ > Ba2+> Rb+> Sr2+> K+> Ca2+> Na+> Li+
18. Порядок реакции 2Ств+О2=2СО равен:
а) 0;
б) 2;
в) 1;
г) 3
