
Вариант №3.
1.Первый закон термодинамики выражает формула:
Q = ∆E + W;
W = Q + E;
∆E = Q - W;
2. Уменьшение вероятности самопроизвольного протекания реакций при увеличении температуры выполняется для
а) 3С2Н2(г) → С6Н6(ж); ΔНº < 0, ΔSº < 0
б) FeO(т) + Н2(г) →Fe(т) +H2O(г); ΔНº > 0, ΔSº > 0
в) обеих реакций
3.Суточное потребление энергии ребёнком в возрасте 1 год составляет 3352 кДж. Питание такого ребёнка только молоком
а) невозможно, так как энергетическая ценность 100 г молока 0,28 кДж
б) возможно при условии частого приёма молока
в) данных для вывода недостаточно
4. Данная диаграмма есть диаграмма
1) Системы с неограниченной растворимостью компонентов в жидком состоянии. В твердом состоянии компоненты образуют химические соединения, которые плавятся конгурэнтно;
2) Системы с неограниченной растворимостью в жидком и твердом состояниях;
3) Системы с неограниченной растворимостью компонентов в жидком и взаимной нерастворимостью в твердом состоянии.
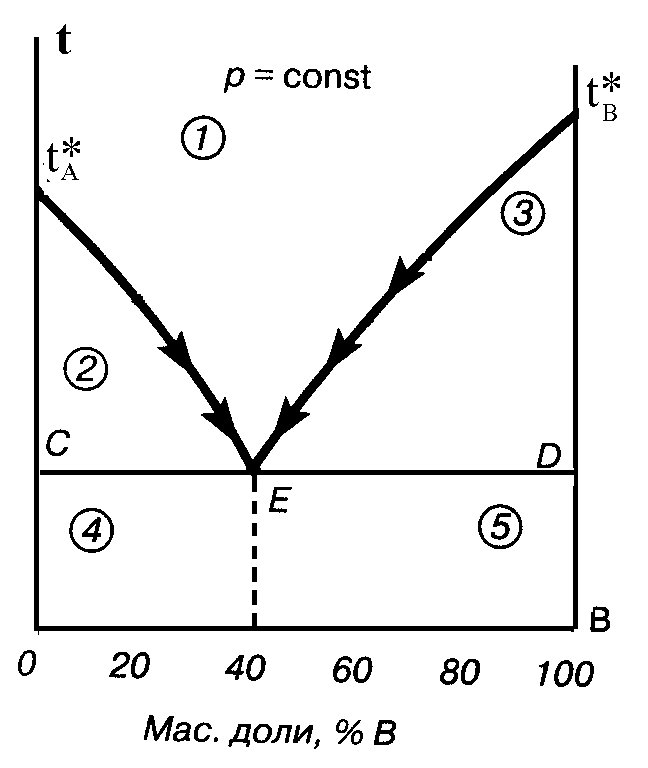
5. В фигуративной точке "а" система обладает числом степеней свободы, равным:
1) 2; 2) 1; 3) 0.
6. Количество твердой фазы, которое выпадет из расплава, содержащего 80% компонента В при Т= 400С (m= 2 кг) равно:
а) 1,1
б) 0,9
в) 0,7
7.При добавленииNaCIк воде температура замерзания раствора по сравнению с растворителем:
понизится, т.к. повышается концентрация солей;
повысится, т.к. понижается концентрация солей;
не изменится, т.к. NaCI– нелетучее вещество;
.
8.Раствор, содержащий 11,6г вещества в 400г воды, замерзает при температуре0,93С (Kk(H2O) = 1,86). Молярная масса растворенного вещества равна:
58;
29;
116;
9. Поверхностная активность бутанола будет больше поверхностной активности этанола в растворах одинаковой концентрации в
а) 34,33 раза
б) 10,56 раза
в)3,25 раза
10.Уравнение определения площадиSo, занимаемой одной молекулой в монослое с площадьюSx
2) So = Sx∙nNA;
3) So / Sx = nNA;
5) So = Sx∙n/NA.
11.Мерой способности веществ изменять поверхностное натяжение является величина, называемая:
а) поверхностным натяжением
б) свободной энергией поверхности
в) поверхностной активностью
12.Предельный одноатомный спирт, имеющий максимальную поверхностную активность:
а) этанол
б) бутанол
в) гексанол.
13. Функциональные группы анионитов
а) –NH3Cl, –Cl-, –SO3Na
б) –NH2, ═NH, ≡N, –NH3OH, –OH
в) –PO3H2, –SH, –CO2H, –SO3H
14.В медицинском эфире и хлороформе недопустимы следы влаги. Для осушки этих жидкостей целесообразно использовать
а) Р2O5
б) активированный уголь
в) цеолит
15.Частицы коллоидных систем
а) отражают свет; не проходят через бумажный фильтр, задерживаются ультрафильтрами (целлофан, пергамент), наблюдаются в оптический микроскоп
б) опалесцируют (рассеивают свет); проходят через бумажный фильтр, задерживаются ультрафильтрами, наблюдаются в ультрамикроскоп
в) опалесцируют, проходят через бумажный фильтр и ультрафильтры, кинетически и термодинамически устойчивы
16. Электроосмос – перемещение в электрическом поле
а) дисперсионной среды относительно неподвижной дисперсной фазы
б) дисперсной фазы относительно неподвижной дисперсионной среды
в) дисперсной фазы и дисперсионной среды одновременно
17.Коллоидная частица была получена в результате взаимодействияBaCl2(изб) сH2SO4. Знак заряда частицы
а) положительный
б) отрицательный
в) частица незаряжена
18.Строение мицеллы золя, образованного при сливании равных объёмов растворовAlCl3 с С(1/3AlCl3)=0,1 моль/дм3 иNaOHС(1/1NaOH) = 0,05 моль/дм3
а)
![]()
б)
![]()
в)
![]()
19.Электролит, обладающий максимальной коагулирующей способностью для положительно заряженных гранул золя
а) SnCl4
б) Na3PO4
в) K4[Fe(CN)6]
20. Действие электролитов-коагулянтов вызывает
а) сжатие диффузного слоя частиц
б) увеличение электростатического заряда частиц
в) упрочнение адсорбционно-сольватных оболочек
ИТОГОВЫЙ ТЕСТ ПО ФИЗИЧЕСКОЙ И КОЛЛОИДНОЙ ХИМИИ
