
- •2. Трансаминирование аминокислот: химизм, значение. Характери-стика трансаминаз. Непрямое дезаминирование аминокислот.
- •3. Окислительное дезаминирование аминокислот: химизм, характери-стика ферментов. Восстановительное аминирование альфакетоглу-тарата, значение.
- •4. Декарбоксилирование аминокислот. Образование биогенных ами-нов, их роль в регуляции метаболизма и функции.
- •6.Трансметилирование. Метионин и s-аденозилметионин (участие в синтезе креатина, адреналина, фосфатидилхолина, метилировании чужеродных соединений). Участие тетрагидрофолиевой кислоты в метилировании.
- •10. Активация и окисление высших жирных кислот: химизм, энергети-ка, физиологическая роль.
- •2. Окисление глицерина
- •11. Биосинтез и использование кетоновых тел.
- •Реакции 3 этапа
- •13. Биосинтез триацилглицеринов, лицерофосфолипидов.
- •14. Обмен и функции холестерина. Прямой и обратный транспорт хо-лестерина. Биосинтез холестерина: химизм, регуляция.
Реакции 3 этапа


13. Биосинтез триацилглицеринов, лицерофосфолипидов.
Триацилглицерины синтезируются во многих органах и тканях, но наиболее важную роль в их синтезе играют печень, стенка кишечника, лактирующая молочная железа и жировая ткань. Для синтеза необходима активная форма глицерина – a-глицерофосфат и активная форма жирной кислоты – ацил-КоА. Активация глицерина может происходить двумя способами:1. В стенке кишечника и почках, печени есть активная глицерол-
киназа:

2. В жировой ткани и мышцах активность этого фермента очень
низкая и образование a-глицерофосфата связано с гликолизом:
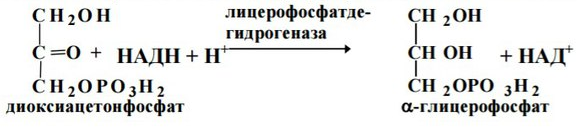
a-Глицерофосфат, образованный любым из этих путей, взаимо-
действует с двумя молекулами активированных жирных кислот (ацил-
КоА) с образованием фосфатидной кислоты:

6. Синтез глицерофосфолипидов
Биосинтез глицерофосфолипидов наиболее интенсивно происходит в печени, стенке кишечника, семенниках, молочной железе. Реакции синтеза локализованы в эндоплазматической сети. Синтез до образования фосфатидной кислоты происходит также, как и синтез триацилглицеринов.

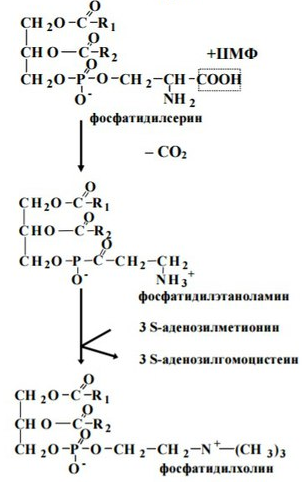
14. Обмен и функции холестерина. Прямой и обратный транспорт хо-лестерина. Биосинтез холестерина: химизм, регуляция.
Обмен холестерина. Транспорт холестерина
1. Обмен холестерина
Функции холестерина: 1) входит в состав клеточных мембран, 2) из него образуются другие физиологически важные соединения: желчные кислоты, кортикостероидные и половые гормоны, витамин Д. Условно в организме человека можно выделить три пула холестерина:
А – быстрообменивающийся (около 30 г холестерина);
В – медленнообменивающийся (около 50 г холестерина);
С – очень медленнообменивающийся (около 60 г холестерина).
К первому пулу А следует отнести холестерин печени и других паренхиматозных органов, а также холестерин кишечной стенки и плазмы крови. Обновление холестерина этого пула происходит в среднем за 30 сут (1 г/сут). К третьему пулу (пул С) можно отнести холестерин головного и спинного мозга, нервов и холестерин соединительной ткани. Скорость обновления холестерина в белом веществе мозга исчисляется годами. Холестерин остальных органов и тканей составляет промежуточный медленнообменивающийся пул В. За сутки в организме человека около 500 мг холестерина окисляется в желчные кислоты, примерно такое же количество экскретируется с фекалиями, около 100 мг удаляется со слущивающимся эпителием кожи и секретом сальных желез и менее 100 мг используется на образование стероидных (половых и кортикоидных) гормонов. Таким образом, ежесуточный расход холестерина составляет около 1,2 г, и он черпается из быстрообменивающегося пула А. Для того, чтобы восполнить эту потерю, организм синтезирует в сутки около 800 мг холестерина и примерно 400 мг получает с пищей.
2. Транспорт холестерина
Прямой транспорт холестерина Это транспорт холестерина в клетку в составе ЛПНП. Основное место синтеза холестерина – печень, в остальные органы и ткани он поступает в составе ЛПНП. В 1985 году американцы Браун и Гольдстейн за раскрытие механизма захвата ЛПНП клетками получили Нобелевскую премию. Они открыли на поверхности клеток рецепторы, высокоспецифичные к апопротеину В, а это – основной белок ЛПНП. Поступление холестерина в клетку включает следующие этапы: 1. Связывание ЛПНП с рецепторами. 2. Эндоцитоз комплекса ЛПНП – рецептор в клетку. 3. Расщепление лизосомальными ферментами апоВ до аминокислот, эфиров холестерина до холестерина и жирной кислоты. 4. Возвращение молекулы рецептора на поверхность клетки.
Рецепторы захвата ЛПНП
Поступивший холестерин клетка использует для построения мембран. Такой рецепторно-опосредованный путь поступления холестерина в клетку предохраняет ее от перегрузки холестерином, т.к.: 1) ингибируется фермент синтеза холестерина – ГМГ-КоА-редуктаза; 2) подавляется синтез рецепторов для ЛПНП. 3) активируется ацил-КоАхолестеринацилтрансфераза (АХАТ), которая переводит свободный холестерин в запасную форму – эфиры холестерина; Нерегулируемые пути поступления холестерина в клетку: 1) неспецифический эндоцитоз через скэвенджер рецепторы; 2) рецепторный путь с помощью рецепторов, не имеющих высокой специфичности к отдельным апопротеинам; 3) путь физико-химического обмена холестерином между мембраной клетки и ЛПНП. Эти пути транспорта холестерина могут привести к накоплению холестерина в клетке. Обратный транспорт холестерина Это транспорт холестерина из клеток периферических тканей (в том числе и из сосудистой стенки) в составе ЛПВП в печень. ЛПВП синтезируются в печени в виде дисков, богатых лецитином и апопротеинами АI, АII (насцентные ЛПВП). Кроме того, подобные частицы образуются в капиллярах во время липолиза ХМ и ЛПОНП. Перенос холестерина из клеток на дисковидные частицы ЛПВП (насцентные ЛПВП) происходит по градиенту концентрации. При контакте ЛПВП с клеткой апоАI связывает свободный холестерин мембраны клетки. Фермент лецитинхолестеринацилтрансфераза (ЛХАТ), находящийся на поверхности ЛПВП, присоединяет остаток жирной кислоты из лецитина (в составе ЛПВП) к свободному холестерину. Образуется гидрофобная молекула эфира холестерина, которая перемещается в центр диска ЛПВП. При этом освобождаются участки поверхности апоАI для связывания новых молекул свободного холестерина из мембраны клетки. Вновь происходит эстерификация холестерина, в результате частица ЛПВП из диска превращается в сферическую молекулу и в такой форме захватывается рецепторным путем печенью. В печени холестерин, поступивший в составе ЛПВП, используется для биосинтеза желчных кислот и в конечном итоге выводится из организма. Вывод: холестерин в клетку поступает с ЛПНП (прямой транспорт), а удаляется с ЛПВП – обратный транспорт холестерина.
Синтез холестерина
Ланостерин превращается в мембранах гладкого эндоплазматического ретикулума в холестерин. Метильная группа при С14 окисляется, и образуется 14-десметилланостерин.
2. Затем удаляются ещё два метила при С4, и образуется зимостерол.
3. Далее двойная связь C8=С9 перемещается в положение С8=С7 и образуется Δ7,24-холестадиенол.
4. Двойная связь далее перемещается в положение С5=С6,образуется десмостерол.
5. После чего в боковой цепи восстанавливается двойная связь, и образуется холестерин.
(Восстановление
двойной связи в боковой цепи может,
однако, происходить и на предшествующих
стадиях биосинтеза холестерола.) 
