
- •Правило Клечковского
- •Билет №11 Химическая связь и строение молекул.
- •Билет №13-14 Кратность связи. Сигма и пи связи, схемы перекрывания ао и прочность связей. Полярные связи и мол-лы.
- •Билет №15 Энергетические диаграммы обр. Молекул n2 и о2. Кратность связи и магнитные св-ва.
- •Билет №16 Ионная связь и её св-ва. Строение ионных кристаллов типа СsCl , NaCl , ZnS (сфалерит) и CaF2 (флюорит)
- •Свойства ZnS (сфалерит)
- •Билет №17 Металлическая связь и её св-ва.Кристаллические структуры металлов типа вольфрама, меди и магния. Координационные числа и плотность упаковки атомов.
- •Билет №19 Агрегатные состояния вещества и их характеристика. Плазма. Стекла и аморфные вещества. Понятие о ближнем и дальнем порядках.
- •Формы плазмы
- •Билет №20 Энергетический (тепловой) эффект изохорного и изобарного химических процессов. Стандартная энтальпия образования химического соединения. Закон Гесса и следствие из него.
- •Билет №23 Направление химической реакции. Понятие о свободной энергии Гиббса и её изменении как движущей силы изобарного процесса. Стандартное изменение энергии Гиббса при хим. Реакции.
- •Билет №24 Скорость гомогенной реакции. Средняя и истинная скорость реакции. Закон действия масс. Константа скорости реакции. Понятие о молекулярности и порядке реакции.
- •Порядок химической реакции
- •Билет №27 Катализаторы химических реакций. Представление о механизме катализа. Специфичность катализа. Примеры и роль каталитических процессов при химической переработке древесного сырья.
- •Билет №28 Растворы. Процессы при образовании растворов. Идеальные и реальные растворы. Гидраты и сольваты.
- •Билет №30 Растворимость газов, жидкостей и твердых веществ в жидкостях. Закон Генри. Ненасыщенные, насыщенные и перенасыщенные растворы.
- •Растворение как физико-химический процес
- •Растворимость
- •Растворы неэлектролитов. Понятие об осмосе и осмотическом давлении. Закон Вант-Гоффа. Изотонические растворы. Роль осмоса в жизни растений.
- •Билет №32 Давление насыщенного пара растворителя над раствором нелетучего растворённого вещества. Закон Рауля. Температура замерзания и кипения растворов (влияние концентрации)
- •Билет №33 Растворы электролитов. Сильные и слабые электролиты. Связь кажущейся степени диссоциации и изотоническим коэффициентом(см. Конспект). Понятие об активности и ионной силе раствора.
- •Билет №34 Обменные реакции между ионами. Молекулярные и ионные уравнения реакций. Условия необратимости ионных реакций.
- •Билет №35 Степень и константа диссоциации слабого электролита. Закон разбавления Оствальда. Ступенчатая диссоциация электролита. Влияние общих ионов на диссоциацию слабых электролитов.
- •Вывод значения pH
- •Билет №37 Растворимость малорастворимых твердых электролитов в воде. Произведение растворимости (пр). Влияние общих ионов на растворимость. Амфотерные гидроксиды и оксиды.
- •Билет №38 Гидролиз солей по катиону, аниону, катиону и аниону. Ступенчатый гидролиз. Необратимый совместный гидролиз солей.
Билет №3
Классы химических соединений
Химические соединения делят на классы: неорганические и органические. Последние в широком смысле включают в себя элементоорганические соединения: борорганические, кремнийорганические, фосфорорганические и др.
Некоторые виды cложных неорганических соединений:
оксиды (H2O, CaO, CO2, P2O5 (P4O10) и др.)
гидроксиды:
основания (Na(OH), Ca(OH)2 и др.)
кислородосодержащие кислоты (HNO3, H2SO4, H3PO4 и др.)
амфотерные гидроксиды (Al(OH)3, Fe(OH)3 и др.)
безкислородные кислоты (HCl, HCN и др.)
нитриды (NH3, Si3N4 и др.)
соли (NaCl, KNO3, Fe2(SO4)3, LiBr и др.)
кристаллогидраты: (CuSO4·5H2O и др.)
комплексные соединения: (K3[Fe(CN)6] и др.)
Структурная формула — это разновидность химической формулы, графически описывающая расположение и порядок связи атомов в соединении, выраженное на плоскости. Связи в структурных формулах обозначаются валентными черточками.
Часто используются структурные формулы, где связи с атомами водорода не обозначаются валентными черточками (тип 2). В другом типе структурных формул (скелетных), применяемых для крупных молекул в органической химии, не указываются атомы водорода связанные с углеродными атомами и не обозначаются атомы углерода (тип 3).
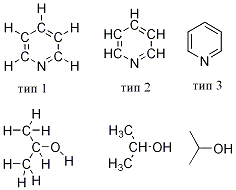
С помощью разных типов условных обозначений, используемых в структурных формулах, указываются также координационные связи, водородные связи, стереохимия молекул, делокализованные связи, локализация зарядов и т. д.
Оксиды
Простое вещество + кислород = оксид S + O2 = SO2 4P + 5O2 = 2P2O5 2Zn + O2 = 2ZnO
Разложение некоторых солей и нерастворимых оснований MgCO3 = MgO + CO2 2Cu(NO3)2 = 2CuO + 4NO2 + O2 2Fe(OH)3 = Fe2O3 + 3H2O
Кислоты
Кислотный оксид + H2O = кислота (SiO2 с водой не реагирует) Cl2O7 + H2O = 2HClO4 SO3 + H2O = H2SO4
H2 + простое вещество =
Сильная кислота + соль слабой кислоты = слабая кислота + соль сильной кислоты 2HNO3 + Na2SiO3 = H2SiO3 + 2NaNO3 H2SO4 + MgSO3 = H2SO3 (H2O + SO2) + MgSO4
Нерастворимые гидроксиды
Растворимая соль + щелочь = соль + нерастворимое основание Ni(NO3)2 + 2KOH = 2KNO3 + Ni(OH)2 FeCl2 + Ca(OH)2 = CaCl2 + Fe(OH)2
Щелочи
Основный оксид + вода = щелочь (в реакцию вступают оксиды щелочных и щелочноземельных металлов) BaO + H2O = Ba(OH)2 K2O + H2O = 2KOH
Активный металл + вода = щелочь + H2 2Na + 2H2O = 2NaOH + H2 Ca + 2H2O = Ca(OH)2 + H2
Соли
Кислотный оксид + основный оксид = соль SO3 + CaO = CaSO4 N2O5 + K2O = 2KNO3
Кислотный оксид + щелочь = соль + вода CO2 + 2NaOH = Na2CO3 + H2O Cl2O7 + 2KOH = 2KClO4 + H2O
Основный оксид + кислота = соль + вода CuO + H2SO4 = CuSO4 + H2O Fe2O3 + 6HBr = 2FeBr3 + 3H2O
Кислота + основание = соль + вода H3PO4 + 3KOH = K3PO4 + 3H2O 3H2SO4 + 2Fe(OH)3 = Fe2(SO4)3 + 6H2O
Соль слабой кислоты + сильная кислота = соль сильной кислоты + слабая кислота K2SO3 + 2HCl = 2KCl + H2O + SO2 (H2SO3) NaCl + H2SO4 = NaHSO4 + HCl
Растворимая соль + растворимая соль = нерастворимая соль + соль CuCl2 + Na2S = CuS + 2NaCl Ba(NO3)2 + K2SO4 = BaSO4 + 2KNO3
Растворимая соль + щелочь = соль + нерастворимое основание Fe(NO3)3 + 3NaOH = 3NaNO3 + Fe(OH)3 MnCl2 + Ca(OH)2 = CaCl2 + Mn(OH)2
Кислота + металл (находящийся в ряду напряжений левее водорода) = соль + водород 2HCl + Fe = FeCl2 + H2 2H3PO4 + 6K = 2K3PO4 + 3H2 Важно: кислоты-окислители (HNO3, конц. H2SO4) реагируют с металлами по-другому.
Растворимая соль металла (*) + металл (**) = соль металла (**) + металл (*) Fe + CuCl2 = FeCl2 + Cu Ni + 2AgNO3 = Ni(NO3)2 + 2Ag Важно: 1) металл (**) должен находиться в ряду напряжений левее металла (*), 2) металл (**) НЕ должен реагировать с водой.
Металл + неметалл = соль 2Fe + 3Cl2 = 2FeCl3 Ca + Se = CaSe
Билет №4
Стехиометрические законы. Их современное толкование.
Основные законы стехиометрии, включающие законы количественных соотношений между реагирующими веществами с помощью уравнений химических реакций, вывод формул химических соединений, составляют раздел химии, называемый стехиометрией. Стехиометрия включает в себя законы Авогадро, постоянства состава, кратных отношений,Гей-Люссака, эквивалентов и сохранения массы.
В основу составления химических уравнений положен метод материального баланса, основанный на законе сохранения массы (М. В. Ломоносов, 1748,А. Лавуазье, 1789).
Закон сохранения массы веществ:
Масса реагирующих веществ равна массе продуктов реакции.
В химической реакции число взаимодействующих атомов остается неизменным, происходит только их перегруппировка с разрушением исходных веществ. Взаимодействие водорода и кислорода с образованием воды может быть записано с помощью уравнения химической реакции
|
|
|
|
Коэффициенты перед формулами химических соединений называются стехиометрическими.
Закон постоянства состава (Ж. Пруст):
Химическое соединение, имеющее молекулярное строение, независимо от метода получения характеризуется постоянным составом.
Такие соединения называют дальтонидами или стехиометрическими в отличие от бертолидов, состав которых зависит от способа получения. Такие соединения состоят не из молекул, а из атомов или ионов.
Закон кратных отношений (Д. Дальтон):
Если два элемента образуют между собой несколько молекулярных соединений, то масса одного элемента, приходящаяся на одну и ту же массу другого, относятся между собой как небольшие целые числа.
При взаимодействии азота с кислородом образуются пять оксидов. На 1 грамм азота в образующихся молекулах приходится 0,57, 1,14, 1,71, 2,28, 2,85 грамм кислорода, что соответствует отношением 2:1, 1:1, 2:3, 1:2, 2:5 в этих оксидах; их составы N2O, NO, N2O3, NO2, N2O5.
Закон эквивалентов (И. Рихтер):
В молекулярных соединениях массы составляющих их элементов относятся между собой как их эквиваленты.
Химический эквивалент – реальная или условная частица вещества, способная соединиться и заместить 1 моль атомов водорода в реакциях присоединения и замещения или принять (отдать) 1 моль электронов в окислительно-восстановительных реакциях.
Химический эквивалент
|
|
|
|
![]()
![]()
Закон простых объемных отношений (Ж. Гей-Люссак):
При равных условиях объемы вступающих в реакцию газов относятся друг к другу и к объемам образующихся газообразных продуктов, как небольшие целые числа.
Так, в реакции образования аммиака из простых веществ отношение объемов водорода, азота и аммиака составляет 3 : 1 : 2.
Закон Авогадро: В равных объемах любых газов, взятых при одинаковых условиях, содержится одинаковое число молекул.
Из закона Авогадро вытекают два следствия:
Одинаковое количество молекул любых газов при одинаковых условиях занимают одинаковый объем.
Относительная плотность одного газа по другому равна отношению их молярных масс.
Число Авогадро – число частиц в моле любого вещества; NA = 6,02∙1023 моль–1.
Молярный объем – объем моля любого газа при нормальных условиях(температура 273 К, давление 101,3 кПа); равен 22,4 л∙моль–1.
Молярная масса (M) – масса одного моля вещества, численно совпадающая с относительными массами атомов, ионов, молекул, радикалов и других частиц, выраженных в г∙моль–1.
Билет№5
Химический эквив. Элемента,оксида,гидроксида и соли. Эквивалент – это реальная или условная частица, которая в кислотно-основных реакциях присоединяет (или отдает) один ион Н+ или ОН–, в окислительно-восстановительных реакциях принимает (или отдает) один электрон, реагирует с одним атомом водорода или с одним эквивалентом другого вещества.
МЭ(оксида) = МЭ(элемента) + МЭ(О) = МЭ(элемента) + 8
МЭ(кислоты) = МЭ(Н) + МЭ(кислотного остатка) = 1 + МЭ(кислотного остатка)
МЭ(основания) = МЭ(Ме) + МЭ(ОН) = МЭ(Ме) + 17
МЭ(соли) = МЭ(Ме) + МЭ(кислотного остатка).
Газообразные
вещества помимо молярной массы
эквивалента имеют молярный
объем эквивалента
(![]() или
VЭ)
– объем, занимаемый молярной массой
эквивалента или объем одного моль
эквивалента.
Размерность
«л/моль».
При
н.у. получаем:
или
VЭ)
– объем, занимаемый молярной массой
эквивалента или объем одного моль
эквивалента.
Размерность
«л/моль».
При
н.у. получаем:
|
|
Из закона эквивалентов следует, что массы (или объемы) реагирующих и образующихся веществ пропорциональны молярным массам (молярным объемам) их эквивалентов. Для любых двух веществ, связанных законом эквивалентов, можно записать:
|
|
где m1 и m2 – массы реагентов и (или) продуктов реакции, г;
![]() ,
,
![]() –
молярные массы эквивалентов реагентов
и (или) продуктов реакции,
г/моль;
–
молярные массы эквивалентов реагентов
и (или) продуктов реакции,
г/моль;
V1, V2 – объемы реагентов и (или) продуктов реакции, л;
![]() ,
,![]() –
молярные объемы эквивалентов реагентов
и (или) продуктов реакции,
л/моль.
–
молярные объемы эквивалентов реагентов
и (или) продуктов реакции,
л/моль.
Следует учитывать, что эквивалент одного и того же вещества может меняться в зависимости от того, в какую реакцию оно вступает. Эквивалент элемента также может быть различным в зависимости от вида соединения, в состав которого он входит. Эквивалентом может являться как сама молекула или какая-либо другая формульная единица вещества, так и ее часть.
Эквивалент, как частица, может быть охарактеризован молярной массой (молярным объемом) и определенным количеством вещества э. Молярная масса эквивалента (МЭ) – это масса одного моль эквивалента. Она равна произведению молярной массы вещества на фактор эквивалентности:
|
МЭ = МfЭ. |
Таблица 1.1 – Расчет фактора эквивалентности
|
Частица |
Фактор эквивалентности |
Примеры |
|
Элемент |
где В(Э) – валентность элемента |
|
|
Простое вещество |
где n(Э) – число атомов элемента (индекс в химической формуле), В(Э) – валентность элемента |
fЭ(H2) = 1/(21) = 1/2; fЭ(O2) = 1/(22) = 1/4; fЭ(Cl2) = 1/(21) = 1/2; fЭ(O3) = 1/(32) = 1/6 |
|
Оксид |
где n(Э) – число атомов элемента (индекс в химической формуле оксида), В(Э) – валентность элемента |
fЭ(Cr2O3) = 1/(23) = 1/6; fЭ(CrO) = 1/(12) = 1/2; fЭ(H2O) = 1/(21) = 1/2; fЭ(P2O5) = 1/(25) = 1/10 |
|
Кислота |
где n(H+) – число отданных в ходе реакции ионов водорода (основность кислоты) |
fЭ(H2SO4) = 1/1 = 1 (основность равна 1) или fЭ(H2SO4) = 1/2 (основность равна 2) |
|
Основание |
где n(ОH–) – число отданных в ходе реакции гидроксид-ионов (кислотность основания) |
fЭ(Cu(OH)2) = 1/1 = 1 (кислотность равна 1) или fЭ(Cu(OH)2) = 1/2 (кислотность равна 2) |
|
Соль |
где n(Ме) – число атомов металла (индекс в химической формуле соли), В(Ме) – валентность металла; n(А) – число кислотных остатков, В(А) – валентность кислотного остатка |
fЭ(Cr2(SO4)3) = 1/(23) = 1/6 (расчет по металлу) или fЭ(Cr2(SO4)3) = 1/(32) = 1/6 (расчет по кислотному остатку)
|
|
Частица в окислительно-восстановительных реакциях |
где
|
Fe2+
+ 2 fЭ(Fe2+) =1/2;
MnO4–
+ 8H+
+ 5 fЭ(MnO4–) = 1/5 |
|
Ион |
где z – заряд иона |
fЭ(SO42–) = 1/2 |
Билет №6
Субатомные частицы
Основная статья: Субатомная частица
Хотя слово атом в первоначальном значении обозначало частицу, которая не делится на меньшие части, согласно научным представлениям он состоит из более мелких частиц, называемых субатомными частицами. Атом состоит из электронов, протонов, все атомы, кроме водорода-1, содержат также нейтроны.
Электрон является самой лёгкой из составляющих атом частиц с массой 9,11·10−31 кг, отрицательным зарядом и размером, слишком малым для измерения современными методами.[4] Протоны обладают положительным зарядом и в 1836 раз тяжелее электрона (1,6726·10−27 кг). Нейтроны не обладают электрическим зарядом и в 1839 раз тяжелее электрона (1,6929·10−27 кг).[5]
При этом масса ядра меньше суммы масс составляющих его протонов и нейтронов из-за эффекта дефекта массы. Нейтроны и протоны имеют сравнимый размер, около 2,5·10−15 м, хотя размеры этих частиц определены плохо.[6]
В стандартной модели элементарных частиц как протоны, так и нейтроны состоят из элементарных частиц, называемых кварками. Наряду с лептонами, кварки являются одной из основных составляющих материи. И первые и вторые являются фермионами. Существует шесть типов кварков, каждый из которых имеет дробный электрический заряд, равный +2⁄3 или −1⁄3 элементарного. Протоны состоят из двух u-кварков и одного d-кварка, а нейтрон — из одного u-кварка и двух d-кварков. Это различие объясняет разницу в массах и зарядах протона и нейтрона. Кварки связаны между собой сильными ядерными взаимодействиями, которые передаются глюонами.[7][8]
Электроны в атоме
Основная статья: Атомная орбиталь
При описании электронов в атоме в рамках квантовой механики, обычно рассматривают распределение вероятности в 3n-мерном пространстве для системы n электронов.
Электроны в атоме притягиваются к ядру, между электронами также действует кулоновское взаимодействие. Эти же силы удерживают электроны внутри потенциального барьера, окружающего ядро. Для того, чтобы электрон смог преодолеть притяжение ядра, ему необходимо получить энергию от внешнего источника. Чем ближе электрон находится к ядру, тем больше энергии для этого необходимо.
Электронам, как и другим частицам, свойственен корпускулярно-волновой дуализм. Иногда говорят, что электрон движется по орбитали, что неверно. Состояние электронов описывается волновой функцией, квадрат модуля которой характеризует плотность вероятности нахождения частиц в данной точке пространства в данный момент времени, или, в общем случае, оператором плотности. Существует дискретный набор атомных орбиталей, которым соответствуют стационарные чистые состояния электронов в атоме.
Каждой орбитали соответствует свой уровень энергии. Электрон может перейти на уровень с большей энергией, поглотив фотон. При этом он окажется в новом квантовом состоянии с большей энергией. Аналогично, он может перейти на уровень с меньшей энергией, излучив фотон. Энергия фотона при этом будет равна разности энергий электрона на этих уровнях (см.: постулаты Бора).
Свойства атома
По определению, любые два атома с одним и тем же числом протонов в их ядрах относятся к одному химическому элементу. Атомы с одним и тем же количеством протонов, но разным количеством нейтронов называют изотопами данного элемента. Например, атомы водорода всегда содержат один протон, но существуют изотопы без нейтронов (водород-1, иногда также называемый протием — наиболее распространённая форма), с одним нейтроном (дейтерий) и двумя нейтронами (тритий).[9] Известные элементы составляют непрерывный натуральный ряд по числу протонов в ядре, начиная с атома водорода с одним протоном и заканчивая атомом унуноктия, в ядре которого 118 протонов.[10] Все изотопы элементов периодической системы, начиная с номера 83 (висмут), радиоактивны.[11][12]
Размер
Основная статья: Радиус атома
Атомы не имеют отчётливо выраженной внешней границы, поэтому их размеры определяются по расстоянию между ядрами соседних атомов, которые образовали химическую связь (Ковалентный радиус) или по расстоянию до самой дальней из стабильных орбит электронов в электронной оболочке этого атома (Радиус атома). Радиус зависит от положения атома в периодической системе, вида химической связи, числа ближайших атомов (координационного числа) и квантово-механического свойства, известного как спин.[17] В периодической системе элементов размер атома увеличивается при движении сверху вниз по столбцу и уменьшается при движении по строке слева направо.[18] Соответственно, самый маленький атом — это атом гелия, имеющий радиус 32 пм, а самый большой — атом цезия (225 пм).[19] Эти размеры в тысячи раз меньше длины волны видимого света (400—700 нм), поэтому атомы нельзя увидеть в оптический микроскоп. Однако отдельные атомы можно наблюдать с помощью сканирующего туннельного микроскопа.
Малость атомов демонстрируют следующие примеры. Человеческий волос по толщине в миллион раз больше атома углерода.[20] Одна капля воды содержит 2 секстиллиона (2·1021) атомов кислорода, и в два раза больше атомов водорода.[21] Один карат алмаза с массой 0,2 г состоит из 10 секстиллионов атомов углерода.[22] Если бы яблоко можно было увеличить до размеров Земли, то атомы достигли бы исходных размеров яблока.[23]
Учёные из Харьковского физико-технического института представили первые в истории науки снимки атома. Для получения снимков учёные использовали электронный микроскоп, фиксирующий излучения и поля (field-emission electron microscope, FEEM). Физики последовательно разместили десятки атомов углерода в вакуумной камере и пропустили через них электрический разряд в 425 вольт. Излучение последнего атома в цепочке на фосфорный экран позволило получить изображение облака электронов вокруг ядра.[24]
Эмиссионный спектр, спектризлучения, спектр испускания — относительная[1] интенсивностьэлектромагнитного излученияобъекта исследования по шкалечастот.
Обычно изучается излучение в инфракрасном,видимомиультрафиолетовомдиапазонеот сильно нагретоговещества. Спектр излучения вещества представляют либо в виде горизонтальной цветовой полосы — результат расщепления света от объектапризмой— либо в видеграфикаотносительной интенсивности, либо в виде таблицы.
Билет №7
В
1924 году[1]
французский физик Луи
де Бройльвысказал гипотезу о том,
что установленный ранее[1]
для фотоновкорпускулярно-волновой
дуализмприсущ всем частицам —электронам,протонам,атомами так далее, причём количественные
соотношения между волновыми и
корпускулярными свойствами частиц те
же, что и для фотонов. Таким образом,
если частица имеет энергию![]() и
импульс, абсолютное значение которого
равно
и
импульс, абсолютное значение которого
равно![]() ,
то с ней связана волна, частота которой
,
то с ней связана волна, частота которой![]() и
длина волны
и
длина волны![]() (Уравнение
Де Бройля), где
(Уравнение
Де Бройля), где![]() —постоянная
Планка.[1]
Эти волны и получили название волн
де Бройля.[1]
—постоянная
Планка.[1]
Эти волны и получили название волн
де Бройля.[1]
Корпускуля́рно-волново́й дуали́зм — принцип, согласно которому любой объект может проявлять какволновые, так икорпускулярныесвойства.
Как классический пример, светможно трактовать как поток корпускул (фотонов), которые во многих физических эффектах проявляют свойстваэлектромагнитных волн. Свет демонстрирует свойства волны в явленияхдифракциииинтерференциипри масштабах, сравнимых с длиной световой волны. Например, дажеодиночные фотоны, проходящие через двойную щель, создают на экране интерференционную картину, определяемуюуравнениями Максвелла
Билет №8
Распределение электронов в атоме по энергетическим уровням, подуровням, орбиталям и квантовым ячейкам.
Атомная орбиталь — одноэлектронная волновая функция, полученная решениемуравнения Шрёдингерадля данного атома, задаетсяглавнымn, орбитальнымl и магнитнымm квантовыми числами.
Квантовые числа и номенклатура орбиталей
Радиальное распределение плотности вероятности для атомных орбиталей при различных n и l.
Главное квантовое число n может принимать любые целые положительные значения, начиная с единицы (n = 1,2,3, … ∞) и определяет общую энергию электрона на данной орбитали (энергетический уровень) :
![]()
Энергия для n = ∞ соответствует энергии одноэлектронной ионизации для данного энергетического уровня.
Орбитальное квантовое число (называемое также азимутальным или дополнительным квантовым числом) определяет момент импульса электрона и может принимать целые значения от 0 до n — 1 (l = 0,1, …, n — 1). Момент импульса при этом задаётся соотношением
![]()
Атомные орбитали принято называть по буквенному обозначению их орбитального числа:
|
Значение орбитального квантового числа |
0 |
1 |
2 |
3 |
4 |
|
Буквенное обозначение |
s |
p |
d |
f |
g |
Буквенные обозначения атомных орбиталей произошли от описания спектральных линий в атомных спектрах: s (sharp) — резкая серия в атомных спектрах, p (principal)— главная, d (diffuse) — диффузная, f (fundamental) — фундаментальная.
Магнитное квантовое число ml определяет проекцию орбитального момента импульса на направление магнитного поля и может принимать целые значения в диапазоне от -l до l, включая 0 (ml = -l … 0 … l):
![]()
Принцип Паули
в пределах одной квантовой системы в данном квантовом состоянии может находиться только одна частица, состояние другой должно отличаться хотя бы одним квантовым числом.
Правило Хунда
Правило Хунда определяет порядок заполнения орбиталейопределённого подслоя и формулируется следующим образом: модуль суммарного значенияспиновогоквантового числаэлектроновданного подслоя должен быть максимальным. Это означает, что в каждой из орбиталей подслоя заполняется сначала один электрон, а только после исчерпания незаполненных орбиталей на эту орбиталь добавляется второй электрон. При этом на одной орбитали находятся два электрона с полуцелымиспинамипротивоположного знака, которые спариваются (образуют двухэлектронное облако) и, в результате, суммарный спин орбитали становится равным нулю.
Правило Клечковского
эмпирическое правило, описывающее энергетическое распределение орбиталей в многоэлектронных атомах.
Правило Клечковского гласит:
|
Заполнение
электронами орбиталей в атоме
происходит в порядке возрастания
суммы главного
и орбитального
квантовых
чисел
|
![]()
|
Таблица 1. Энергетическая последовательность орбиталей в изолированных атомах | ||||
|
(n+l) |
n |
l |
Атомные орбитали | |
|
1 |
1 |
0 |
1s |
Первый период |
|
2 |
2 |
0 |
2s |
Второй период |
|
3 |
2 |
1 |
2p | |
|
3 |
0 |
3s |
Третий период | |
|
4 |
3 |
1 |
3p | |
|
4 |
0 |
4s |
Четвёртый период | |
|
5 |
3 |
2 |
3d | |
|
4 |
1 |
4p | ||
|
5 |
0 |
5s |
Пятый период | |
|
6 |
4 |
2 |
4d | |
|
5 |
1 |
5p | ||
|
6 |
0 |
6s |
Шестой период | |
|
7 |
4 |
3 |
4f | |
|
5 |
2 |
5d | ||
|
6 |
1 |
6p | ||
|
7 |
0 |
7s |
Седьмой период | |
|
8 |
5 |
3 |
5f | |
|
6 |
2 |
6d | ||
|
7 |
1 |
7p | ||
|
8 |
0 |
8s |
Начало восьмого периода | |
Электронные формулы атомов элементов (Z<56).
|
№ эл-та |
химический знак |
Название элемента |
Электронная формула |
|
1 |
H |
водород |
1s 1 |
|
2 |
He |
гелий |
1s 2 |
|
II период | |||
|
3 |
Li |
литий |
1s 22s 1 |
|
4 |
Be |
бериллий |
1s 22s 2 |
|
5 |
B |
бор |
1s 22s 22p 1 |
|
6 |
C |
углерод |
1s 22s 22p 2 |
|
7 |
N |
азот |
1s 22s 22p 3 |
|
8 |
O |
кислород |
1s 22s 22p 4 |
|
9 |
F |
фтор |
1s 22s 22p 5 |
|
10 |
Ne |
неон |
1s 22s 22p 6 |
|
III период | |||
|
11 |
Na |
натрий |
1s 22s 22p 63s 1 |
|
12 |
Mg |
магний |
1s 22s 22p 63s 2 |
|
13 |
Al |
алюминий |
1s 22s 22p 63s 23p1 |
|
14 |
Si |
кремний |
1s 22s 22p 63s 23p2 |
|
15 |
P |
фосфор |
1s 22s 22p 63s 23p3 |
|
16 |
S |
сера |
1s 22s 22p 63s 23p4 |
|
17 |
Cl |
хлор |
1s 22s 22p 63s 23p5 |
|
18 |
Ar |
аргон |
1s 22s 22p 63s 23p6 |
|
IV период | |||
|
19 |
K |
калий |
1s 22s 22p 63s 23p64s 1 |
|
20 |
Ca |
кальций |
1s 22s 22p 63s 23p64s 2 |
|
21 |
Sc |
скандий |
1s 22s 22p 63s 23p64s 23d1 |
|
22 |
Ti |
титан |
1s 22s 22p 63s 23p64s 23d2 |
|
23 |
V |
ванадий |
1s 22s 22p 63s 23p64s 23d3 |
|
24 |
Cr |
хром |
1s 22s 22p 63s 23p64s 13d5 |
|
25 |
Mn |
марганец |
1s 22s 22p 63s 23p64s 23d5 |
|
26 |
Fe |
железо |
1s 22s 22p 63s 23p64s 23d6 |
|
27 |
Co |
кобальт |
1s 22s 22p 63s 23p64s 23d7 |
|
28 |
Ni |
никель |
1s 22s 22p 63s 23p64s 23d8 |
|
29 |
Cu |
медь |
1s 22s 22p 63s 23p64s 13d10 |
|
30 |
Zn |
цинк |
1s 22s 22p 63s 23p64s 23d10 |
|
31 |
Ga |
галлий |
1s 22s 22p 63s 23p64s 23d104p1 |
|
32 |
Ge |
германий |
1s 22s 22p 63s 23p64s 23d104p2 |
|
33 |
As |
мышьяк |
1s 22s 22p 63s 23p64s 23d104p3 |
|
34 |
Se |
селен |
1s 22s 22p 63s 23p64s 23d104p4 |
|
35 |
Br |
бром |
1s 22s 22p 63s 23p64s 23d104p5 |
|
36 |
Kr |
криптон |
1s 22s 22p 63s 23p64s 23d104p6 |
|
V период | |||
|
37 |
Rb |
рубидий |
1s 22s 22p 63s 23p64s 23d104p65s1 |
|
38 |
Sr |
стронций |
1s 22s 22p 63s 23p64s 23d104p65s2 |
|
39 |
Y |
иттрий |
1s 22s 22p 63s 23p64s 23d104p65s24d1 |
|
40 |
Zr |
цирконий |
1s 22s 22p 63s 23p64s 23d104p65s24d2 |
|
41 |
Nb |
ниобий |
1s 22s 22p 63s 23p64s 23d104p65s14d4 |
|
42 |
Mo |
молибден |
1s 22s 22p 63s 23p64s 23d104p65s14d5 |
|
43 |
Tc |
технеций |
1s 22s 22p 63s 23p64s 23d104p65s24d5 |
|
44 |
Ru |
рутений |
1s 22s 22p 63s 23p64s 23d104p65s14d7 |
|
45 |
Rh |
родий |
1s 22s 22p 63s 23p64s 23d104p65s14d8 |
|
46 |
Pd |
палладий |
1s 22s 22p 63s 23p64s 23d104p65s04d10 |
|
47 |
Ag |
серебро |
1s 22s 22p 63s 23p64s 23d104p65s14d10 |
|
48 |
Cd |
кадмий |
1s 22s 22p 63s 23p64s 23d104p65s24d10 |
|
49 |
In |
индий |
1s 22s 22p 63s 23p64s 23d104p65s24d105p1 |
|
50 |
Sn |
олово |
1s 22s 22p 63s 23p64s 23d104p65s24d105p2 |
|
51 |
Sb |
сурьма |
1s 22s 22p 63s 23p64s 23d104p65s24d105p3 |
|
52 |
Te |
теллур |
1s 22s 22p 63s 23p64s 23d104p65s24d105p4 |
|
53 |
I |
йод |
1s 22s 22p 63s 23p64s 23d104p65s24d105p5 |
|
54 |
Xe |
ксенон |
1s 22s 22p 63s 23p64s 23d104p65s24d105p6 |
|
VI период | |||
|
55 |
Cs |
цезий |
1s 22s 22p 63s 23p64s 23d104p65s24d105p66s1 |
|
56 |
Ba |
барий |
1s 22s 22p 63s 23p64s 23d104p65s24d105p66s2 |
Билет №9-10
Периодический закон и система элементов Д.И.Менделеева
«свойства химических элементов, а также формы и свойства образуемых ими простых веществ и соединений находятся в периодической зависимости от величины зарядов ядер их атомов».
С развитием атомной физикииквантовой химииПериодический закон получил строгое теоретическое обоснование. Благодаря классическим работамЙ. Ридберга(1897),А. Ван-ден-Брука(1911),Г. Мозли(1913) был раскрыт физический смысл порядкового (атомного) номера элемента. Позднее была создана квантово-механическая модель периодического изменения электронного строения атомов химических элементов по мере возрастания зарядов их ядер (Н. Бор,В. Паули,Э. Шрёдингер,В. Гейзенберги др.).
Закон Мозли — закон, связывающий частоту спектральных линийхарактеристическогорентгеновского излученияатомахимического элементас его порядковым номером. Экспериментально установлен английским физикомГенри Мозлив1913 году.
Согласно
Закону Мозли, корень
квадратный
из частоты
![]() спектральной
линии
характеристического излучения элемента
есть линейная
функция его
порядкового номера
спектральной
линии
характеристического излучения элемента
есть линейная
функция его
порядкового номера
![]() :
:![]()
где
![]() —постоянная
Ридберга,
—постоянная
Ридберга,
![]() —постоянная
экранирования,
—постоянная
экранирования,
![]() —главное
квантовое число.
На диаграмме Мозли зависимость от
—главное
квантовое число.
На диаграмме Мозли зависимость от
![]() представляет
собой ряд прямых (К-, L-, М- и т. д. серии,
соответствующие значениям n = 1, 2, 3,...).
представляет
собой ряд прямых (К-, L-, М- и т. д. серии,
соответствующие значениям n = 1, 2, 3,...).
Закон
Мозли явился неопровержимым доказательством
правильности размещения элементов в
периодической
системе элементов
Д.
И. Менделеева
и содействовал выяснению физического
смысла
![]() .
.
В соответствии с Законом Мозли, рентгеновские характеристические спектры не обнаруживают периодических закономерностей, присущих оптическим спектрам. Это указывает на то, что проявляющиеся в характеристических рентгеновских спектрах внутренние электронные оболочки атомов всех элементов имеют аналогичное строение
Проявления периодического закона в отношении энергии ионизации
Зависимость энергии ионизации атома от порядкового номера элемента (рис. 1) носит отчетливо периодический характер. Легче всего удалить электрон из атомов щелочных металлов, включающих по одному валентному электрону, труднее всего — из атомов благородных газов, обладающих замкнутой электронной оболочкой. Поэтому периодичность изменения энергии ионизации атомов характеризуется минимумами, отвечающими щелочным металлам, и максимумами, приходящимися на благородные газы. Наряду с этими резко выраженными минимумами и максимумами на кривой энергии ионизации атомов наблюдаются слабо выраженные минимумы и максимумы, которые по-прежнему нетрудно объяснить с учетом упомянутых эффектов экранирования и проникновения, эффектов межэлектронных взаимодействий и т. д[10].
Проявления периодического закона в отношении энергии сродства к электрону
Периодичность значений энергий сродства атомов к электрону объясняется, естественно, теми же самыми факторами, которые уже были отмечены при обсуждении ионизационных потенциалов (см. определение энергии сродства к электрону).
Наибольшим сродством к электрону обладают p-элементы VII группы. Наименьшее сродство к электрону у атомов с конфигурацией s² (Be, Mg, Zn) и s²p6 (Ne, Ar) или с наполовину заполненными p-орбиталями (N, P, As)[11]:
|
|
Li |
Be |
B |
C |
N |
O |
F |
Ne |
|
Электронная конфигурация |
s1 |
s² |
s²p1 |
s²p² |
s²p³ |
s²p4 |
s²p5 |
s²p6 |
|
ε, эВ |
-0,59 |
0,19 |
-0,30 |
-1,27 |
0,21 |
-1,47 |
-3,45 |
0,22 |
Проявления периодического закона в отношении электроотрицательности
Строго говоря, элементу нельзя приписать постоянную электроотрицательность. Электроотрицательность атома зависит от многих факторов, в частности от валентного состояния атома, формальной степени окисления, координационного числа, природы лигандов, составляющих окружение атома в молекулярной системе, и от некоторых других. В последнее время все чаще для характеристики электроотрицательности используют так называемую орбитальную электроотрицательность, зависящую от типа атомной орбитали, участвующей в образовании связи, и от её электронной заселенности, т. е. от того, занята атомная орбиталь неподелённой электронной парой, однократно заселена неспаренным электроном или является вакантной. Но, несмотря на известные трудности в интерпретации и определении электроотрицательности, она всегда остается необходимой для качественного описания и предсказания природы связей в молекулярной системе, включая энергию связи, распределение электронного заряда и степень ионности, силовую постоянную и т. д.
Периодичность атомной электроотрицательности является важной составной частью периодического закона и легко может быть объяснена, исходя из непреложной, хотя и не совсем однозначной, зависимости значений электроотрицательности от соответствующих значений энергий ионизации и сродства к электрону[12].
В периодах наблюдается общая тенденция роста электроотрицательности, а в подгруппах — её падение. Наименьшая электроотрицательность у s-элементов I группы, наибольшая — у p-элементов VII группы.
Проявления периодического закона в отношении атомных и ионных радиусов
![]()
Рис. 4 Зависимость орбитальных радиусов атомов от порядкового номера элемента.
Периодический характер изменения размеров атомов и ионов известен давно. Сложность здесь состоит в том, что из-за волновой природы электронного движения атомы не имеют строго определенных размеров. Так как непосредственное определение абсолютных размеров (радиусов) изолированных атомов невозможно, в данном случае часто используют их эмпирические значения. Их получают из измеренных межъядерных расстояний в кристаллах и свободных молекулах, разбивая каждое межъядерное расстояние на две части и приравнивая одну из них к радиусу первого (из двух связанных соответствующей химической связью) атома, а другую — к радиусу второго атома. При таком разделении учитывают различные факторы, включая природу химической связи, степени окисления двух связанных атомов, характер координации каждого из них и т. д[13]. Таким способом получают так называемые металлические, ковалентные, ионные и ван-дер-ваальсовы радиусы. Ван-дер-ваальсовы радиусы следует рассматривать как радиусы несвязанных атомов; их находят по межъядерным расстояниям в твердых или жидких веществах, где атомы находятся в непосредственной близости друг от друга (например, атомы Ar в твердом аргоне или атомы N из двух соседних молекул N2 в твердом азоте), но не связаны между собой какой-либо химической связью.
Но, очевидно, лучшим описанием эффективных размеров изолированного атома является теоретически рассчитанное положение (расстояние от ядра) главного максимума зарядовой плотности его наружных электронов. Это так называемый орбитальный радиус атома. Периодичность в изменении значений орбитальных атомных радиусов в зависимости от порядкового номера элемента проявляется довольно отчетливо (см. рис. 4), и основные моменты здесь состоят в наличии очень ярко выраженных максимумов, приходящихся на атомы щелочных металлов, и таких же минимумов, отвечающих благородным газам. Уменьшение значений орбитальных атомных радиусов при переходе от щелочного металла к соответствующему (ближайшему) благородному газу носит, за исключением ряда Li—Ne, немонотонный характер, особенно при появлении между щелочным металлом и благородным газом семейств переходных элементов (металлов) и лантаноидов или актиноидов. В больших периодах в семействах d- и f-элементов наблюдается менее резкое уменьшение радиусов, так как заполнение орбиталей электронами происходит в пред- предвнешнем слое. В подгруппах элементов радиусы атомов и однотипных ионов в общем увеличиваются.
Проявления периодического закона в отношении энергии атомизации
Энергия атомизации простых веществ является характеристикой, которая во многом определяет их реакционную способность[14]. Зависимость энергии атомизации простых веществ от порядкового номера элемента имеет периодический характер. Основные моменты такой периодической зависимости состоят в следующем: энергия атомизации растет при переходе от щелочного металла (для них эти значения сравнительно невелики и близки 84 кДж/моль) к следующим за ним элементам, достигает максимума, затем убывает, становясь очень небольшой для галогена (63—126 кДж/моль) и, наконец, превращается в нуль в случае примыкающего к галогену благородного газа, который, как известно, при стандартных условиях существует в виде практически не взаимодействующих атомов. Положение максимума энергии атомизации в ряду элементов от щелочного металла до соответствующего (ближайшего) благородного газа зависит от многих факторов, выходящих за рамки настоящего изложения. Так, в ряду Li—Ne наибольшей энергией атомизации характеризуется углерод (718,2 кДж/моль), а в рядах K—Kr и Cs—Rn наибольшими энергиями атомизации обладают переходные металлы: ванадий (516,6 кДж/моль) и вольфрам (844,2 кДж/моль). Неравномерное изменение энергии атомизации в пределах одного ряда элементов от щелочного металла до благородного газа оказывается довольно сложным, особенно если этот ряд включает семейство переходных металлов.
Проявления периодического закона в отношении степени окисления
Одним из основных понятий в химии было и остается понятие степени окисления (степень окисления, состояние окисления, окислительное состояние). Несмотря на то что степень окисления представляется во многом формальной и более искусственной относительно других традиционных химических понятий, она до сих пор остается широко распространенной и сохраняет свою значимость для обобщения и более глубокого понимания основных принципов образования химических соединений[15].
Следует подчеркнуть, что степень окисления элемента, будучи формальной характеристикой, не дает представления ни об эффективных зарядах атомов этого элемента в соединении, ни о валентности атомов, хотя степень окисления часто называют формальной валентностью. Многие элементы способны проявлять не одну, а несколько различных степеней окисления. Например, для хлора известны все степени окисления от −1 до +7, хотя четные очень неустойчивы, а для марганца — от +2 до +7. Высшие значения степени окисления изменяются в зависимости от порядкового номера элемента периодически, но эта периодичность имеет сложный характер. В простейшем случае в ряду элементов от щелочного металла до благородного газа высшая степень окисления возрастает от +1 (RbF) до +8 (XeО4). В других случаях высшая степень окисления благородного газа оказывается меньше (Kr+4F4), чем для предшествующего галогена (Br+7О4−). Поэтому на кривой периодической зависимости высшей, степени окисления от порядкового номера элемента максимумы приходятся или на благородный газ, или на предшествующий ему галоген (минимумы — всегда на щелочной металл). Исключение составляет ряд Li—Ne, в котором ни для галогена (F), ни для благородного газа (Ne) вообще неизвестны высокие степени окисления, а наибольшим значением высшей степени окисления обладает средний член ряда — азот; поэтому в ряду Li—Ne изменение высшей степени окисления оказывается проходящим через максимум. В общем случае возрастание высшей степени окисления в ряду элементов от щелочного металла до галогена или до благородного газа происходит отнюдь не монотонно, главным образом по причине проявления высоких степеней окисления переходными металлами. Например, возрастание высшей степени окисления в ряду Rb—Xe от +1 до +8 «осложняется» тем, что для молибдена, технеция и рутения известны такие высокие степени окисления, как +6 (MoО3), +7 (Tc2О7), +8 (RuO4).
Проявления периодического закона в отношении окислительного потенциала
Одной из очень важных характеристик простого вещества является его окислительный потенциал, отражающий принципиальную способность простого вещества к взаимодействию с водными растворами, а также проявляемые им окислительно-восстановительные свойства[16]. Изменение окислительных потенциалов простых веществ в зависимости от порядкового номера элемента также носит периодический характер. Но при этом следует иметь в виду, что на окислительный потенциал простого вещества оказывают влияние различные факторы, которые иногда нужно рассматривать индивидуально. Поэтому периодичность в изменении окислительных потенциалов следует интерпретировать очень осторожно.
|
Na/Na+(aq) |
Mg/Mg2+(aq) |
Al/Al3+(aq) |
|
2,71В |
2,37В |
1,66В |
|
K/K+(aq) |
Ca/Ca2+(aq) |
Sc/Sc3+(aq) |
|
2,93В |
2,87В |
2,08В |
Можно обнаружить некоторые определенные последовательности в изменении окислительных потенциалов простых веществ. В частности, в ряду металлов при переходе от щелочного к следующим за ним элементам происходит уменьшение окислительных потенциалов (Na+(aq) и т. д. — гидратированный катион):
Это легко объясняется увеличением энергии ионизации атомов с увеличением числа удаляемых валентных электронов. Поэтому на кривой зависимости окислительных потенциалов простых веществ от порядкового номера элемента имеются максимумы, отвечающие щелочным металлам. Но это не единственная причина изменения окислительных потенциалов простых веществ.

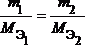 или
или
 или
или
 ,
,