
- •Тесты для самоподготовки к экзамену Вариант №1
- •1. Главное квантовое число (n) характеризует:
- •3. После 5 s – подуровня, согласно правилу Клечковского заполняется подуровень:
- •18. Укажите номер правильного ответа.
- •Дополните
- •42. С уменьшением концентрации соли степень диссоциации
- •76. Виды коррозии: Примеры:
- •77. Для защиты металла от коррозии
- •78. Вид коррозионных процессов: При контакте фаз:
- •79. Алюминий склёпан медью
- •90.При электролизе раствора соли
- •4. Реакция восстановления оксида меди (II) алюминием возможна
- •5. При взаимодействии 1 моль ортофосфорной кислоты с 1 моль гидроксидом натрия образуется:
- •6. Метилоранж становится желтым при растворении в воде каждой из двух солей:
- •7. При взаимодействии водных растворов солей сульфата алюминия и карбоната натрия, сумма коэффициентов в кратком ионном уравнении равна:
- •13.При электролизе раствора сульфата цинка с графитовым анодом и катодом на катоде выделится:
- •14. Рассмотрите электролиз раствора нитрата серебра, если:
- •15. Протектором для железа может быть:
Дополните
Теория электролитической диссоциации:
а) В растворе сильных электролитов больше частиц - ионов
б) Слабые электролиты количественно отличаются по величине степень диссоциации
в) рН = -lg[ H+]
г![]() )
рН + рОН = 14
)
рН + рОН = 14
д) Математическое выражение закона разбавления Оствальда …
е) [Н+] = 10-3, а [ОН-] = 10-11
ж) [ОН-] = 10-2, рН = 12
Установите соответствие
34. Класс формула
средняя соль в) Fe2(SO4)3 е) CaOCl2
двойная соль г) KAl(SO4)2
кислая соль б) KH2PO4
комплексная соль д) K3[Fe(CN)6]
кислота ж) H2CO3
основание и) Fe(OH)2
лишний в списке — это основная соль а) PbOHNO3
35.Среда раствора индикатор
кислая г) метилоранж (красн)
нейтральная б) метилоранж (оранж)
щелочная а) фенолфталеин (б/ц) в) метилоранж (желт)
36.Диссоциация электролиты
1
 .
ступенчато ( ) б)Fe(OH)3
а)
FeOHCl2
в) KHCO3
.
ступенчато ( ) б)Fe(OH)3
а)
FeOHCl2
в) KHCO3
2 .
в одну ступень ( )
г) ZnCl2
.
в одну ступень ( )
г) ZnCl2
3 .
ступенчато ( первичная ) д)
Na[Al(OH)4]
.
ступенчато ( первичная ) д)
Na[Al(OH)4]

 ( вторичная )
( вторичная )
При диссоциации электролитов образуется число ионов
электролиты число ионов
KAl(SO4)2 в) 4 иона
Fe2(SO4)3 г) 5 ионов
CrBr3 в) 4 иона
AlCl3 в) 4 иона
лишние ответы б) 2 иона а) 3 иона д) 6 ионов
38. Среда раствора рН
нейтральная б) рН = 7
кислая а) рН = 4
щелочная в) рН = 9 г) рН = 11
Установление правильную последовательность действий
39. При составлении ионных уравнений реакций необходимо:
записать схему реакции
определить силу электролита
расписать сильные электролиты на ионы
уравнять атомы
сократить одинаковые ионы
з
 аписать
кратное ионное уравнение
аписать
кратное ионное уравнениев
 виде молекул записать ( (осадки);
(газы); слаб.эл-ты)
виде молекул записать ( (осадки);
(газы); слаб.эл-ты)
1, 4, 7, 2, 3, 5, 6
Выберите правильный вариант
4 0.
Краткое ионное уравнение имеет вид:
2H+
+ CO2-3
CO2
+ H2O
при взаимодействии:
0.
Краткое ионное уравнение имеет вид:
2H+
+ CO2-3
CO2
+ H2O
при взаимодействии:
(
 NH4)2CO3
+ HBr
NH4)2CO3
+ HBr L
 i2CO3
+ H2SiO3
i2CO3
+ H2SiO3C
 aCO3
+ H2SO4
aCO3
+ H2SO4B
 aCO3
+ HCl
aCO3
+ HCl
4 1.
Уравнению реакцииCu(OH)2
+ H2SO4
CuSO4
+ 2H2O
1.
Уравнению реакцииCu(OH)2
+ H2SO4
CuSO4
+ 2H2O
соответствует сокращенное ионное уравнение
1 .
2H+
+ 2OH-
2H2O
.
2H+
+ 2OH-
2H2O
2 .
Cu(OH)2
+ 2H+
Cu2+
+ 2H2O
.
Cu(OH)2
+ 2H+
Cu2+
+ 2H2O
3 .
Cu2+
+ SO42-
CuSO4
.
Cu2+
+ SO42-
CuSO4
4 .
Cu2+
+ H2SO4
CuSO4
+ 2H+
.
Cu2+
+ H2SO4
CuSO4
+ 2H+
42. С уменьшением концентрации соли степень диссоциации
1) возрастает 3) не изменится
2) уменьшается
Дополните:
В результате гидролиза соли образуется электролит слабый
Гидролиз соли протекает по катиону, если соль образована слабым основанием, сильной кислотой и рН = меньше 7 (кислая)
Гидролизу не подвергаются соли, образованные сильным основанием и сильной кислотой
Выберите правильный ответ:
Полному гидролизу подвергается:
1) AlCl3 3)KCl
2) ZnCl2 4) Al2S3
Гидролизу не подвергается:
1) Na2CO3 3) Na3PO4
2) NaBr 4) Na2SiO3
Дополните:
Степень окисления – это условная величина, с помощью которой принято описывать окислительно-восстановительные реакции. Численно она равна количеству электронов, которое отдает атом приобретающий положительный заряд, или количеству электронов, которое присоединяет к себе атом, приобретающий отрицательный заряд.
Окисление – процесс отдачи электронов
Если алгебраическая величина (С.О.) уменьшается, то протекает процесс восстановления
Восстановитель в ходе окислительно-восстановительной реакции отдает электроны
Сложное вещество, содержащее элемент в высшей степени окисления играет роль окислителя
Ме – простые вещества являются восстановителями
Чем меньше величина
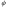 о,
тем сильнее выражены свойства окислителя
о,
тем сильнее выражены свойства окислителя
ЭДС рассчитывают по формуле ЭДС=φ катода — φ анода ( ЭДС=φ окислителя — φ восстановителя); ЭДС > 0, то реакция возможна
Установите соответствие:
Окислительно-восстановительная реакция Тип
1 )
2KNO3
2KNO2
+ O2
a)
сопропорционирования
)
2KNO3
2KNO2
+ O2
a)
сопропорционирования
2 )
2NO2
+ H2O
HNO3
+ HNO2
б)
внутримолекулярная
)
2NO2
+ H2O
HNO3
+ HNO2
б)
внутримолекулярная
3 )
4NH3
+ 5O2
4NO
+ 6H2O
в) диспропорционирования
)
4NH3
+ 5O2
4NO
+ 6H2O
в) диспропорционирования
4 )
2Na2S
+ Na2SO3
+ 3H2SO4
3S + 3Na2SO4
+ 3H2O
г)
межмолекулярная
)
2Na2S
+ Na2SO3
+ 3H2SO4
3S + 3Na2SO4
+ 3H2O
г)
межмолекулярная
1- б 2-в 3- г 4- а
Выберите правильный вариант:
В кислой среде (С.О.) марганца в KMnO4 изменяется до:
1) Mn0 3) Mn+4
2) Mn+2 4) Mn+6
Вещество проявляет только окислительные свойства:
1) Сr2(SO4)3 3) СrSO4
2) Сr0 4) K2Сr2O7
Окислительно-восстановительную двойственность проявляет:
1) H2SO4 3) Na2SO4
2) Na2SO3 4) H2S
Дополните:
Анод – электрод, на котором протекает процесс окисления
На границе Металл – раствор возникает электростатическое притяжение прилегающий слой жидкости заряжается положительно
Полуэлементом называют электрод, погруженный в подходящий электролит, разработанный для измерения электродного потенциала.
Стандартный (нормальный) электродный потенциал металла – это это потенциал металла, определенный относительно стандартного (нормального) водородного электрода, при условии, что концентрация ионов водорода Н+ и ионов испытуемого металла Men+ равны 1 моль-ион/л при стандартных условиях (298К, 101кП)
В цинковом полуэлементе – условно-графическая схема, которого
Zn2+ | Zn0 (2+ и 0 это заряды, наверху пишите)
процесс возникновения электродного потенциала отражает x уравнение Zn-2e = Zn 2+ (2+ это заряд напишите сверху)
Если возрастает концентрация ионов металла в растворе, то электродный потенциал уменьшается
Уравнение Нернста при Т = 298 К имеет вид ….
![]()
катода больше анода.
Установите соответствие:
В Г.Э.: Sn | SnSO4 | | NiSO4 | Ni
|
Электроды
|
Металлы и заряды
д) 0 лишнее |
68. В Г. Э.: Сu | CuCl2 | | ZnCl2| Zn
|
ЭДС (н.у.) равно:
|
3.– 1,1 В 4.– 0,42 В |
Выберите правильный вариант:
Если в гальвоническом элементе Анод – железный электрод, тогда Катод в Г.Э.:
|
1.Zn 2.Mg |
3.Sn 4.Cr |
Составьте условно- графическую схему.
Sn | SnCl2 | | FeCl2| Fe
pH =5, p H2/н+ равно:
|
|
Ответ 3
Дополните:
71.Электрохимическая коррозия – это процесс разрушения металлов в среде различных электролитов, который сопровождается возникновением внутри системы электрического тока.
72.На анодных участках протекает процесс называемый окислением а с электронной точки зрения – это процесс отдачи электронов
73.Деполяризаторы – вещества, которые служат для поглощения водорода, выделяющегося на положительном электроде гальванического элемента к ним относятся: 1) Деполяризаторы первого типа
2) Деполяризаторы второго типа
74. В кислой среде на катоде протекают два процесса – химизм:
1) а) в нейтральных или щелочных средах -
2Н2О + О2+ 4е- = 4ОН-
2) в кислых средах -
О20+ 4Н+ = 2Н2О
75.Электрохимическая коррозия возможна, если электродный потенциал анодного процесса меньше электродного потенциала катода
Установите соответствие:
