
- •Тесты для самоподготовки к экзамену Вариант №1
- •1. Главное квантовое число (n) характеризует:
- •3. После 5 s – подуровня, согласно правилу Клечковского заполняется подуровень:
- •18. Укажите номер правильного ответа.
- •Дополните
- •42. С уменьшением концентрации соли степень диссоциации
- •76. Виды коррозии: Примеры:
- •77. Для защиты металла от коррозии
- •78. Вид коррозионных процессов: При контакте фаз:
- •79. Алюминий склёпан медью
- •90.При электролизе раствора соли
- •4. Реакция восстановления оксида меди (II) алюминием возможна
- •5. При взаимодействии 1 моль ортофосфорной кислоты с 1 моль гидроксидом натрия образуется:
- •6. Метилоранж становится желтым при растворении в воде каждой из двух солей:
- •7. При взаимодействии водных растворов солей сульфата алюминия и карбоната натрия, сумма коэффициентов в кратком ионном уравнении равна:
- •13.При электролизе раствора сульфата цинка с графитовым анодом и катодом на катоде выделится:
- •14. Рассмотрите электролиз раствора нитрата серебра, если:
- •15. Протектором для железа может быть:
Тесты для самоподготовки к экзамену Вариант №1
Часть А
Укажите номер правильного ответа:
1. Главное квантовое число (n) характеризует:
Вращение А.О. вокруг собственной оси;
Энергию электрона (номер Э.У.);
Форму А.О. (подуровень);
Расположение А.О. в магнитных осях атома.
2. Если n = 1, то l принимает значение:
О (s), 1(p);
O (s);
O (s), 1 (p), 2 (d);
O (s), 1 (p), 2 (d,) 3 (f)/
3. После 5 s – подуровня, согласно правилу Клечковского заполняется подуровень:
4 p 3) 3 p
3 d 4) 4 d
Электронная формула 4 s23 d6 соответствует атому:
1) Mn 3) Fe
2) Co 4) Ni
Две свободные 3 d – А.О. имеет атом:
V 3) Sc
Ti 4) Fe
Атому Fe в возбужденном состоянии соответствует электронная формула:
4 s14 p1 3) 3 d54 s14 p1
3 d54 s1 4) 3 d64 s14 p1
Электронная формула иона Э2+… 4 s03 d8 соответствует атому:
Sc 3) Mn
Fe 4) Ni
Явление провала (проскока) электронов у элементов IV n. наблюдаются:
1) Zn и Mn 3) Cr и Cu
2) Co и Ni 4) V и Ti
Высшая степень окисления атома элемента с электронной формулой … 4 s23 d5 равна:
(+6) 3) (+5)
(+7) 4) (+4)
Низшая степень окисления атома азота равна:
1) (-1) 3) (-2)
2) (-3) 4) (0)
Дополните:
Ковалентная связь – это связь за счет образования общих электронных пар образуется между атомами элементов неметаллов
Связь, образованная по линии, связывающей ядра атомов называется Сигма-связь (σ) связью, эта связь имеет особенности:
1 σ -Связь прочнее p-связи
2 По s-связям возможно внутримолекулярное вращение атомов
3 поляризуемость s-связи ниже чем p-связи
Число
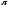 связей
в молекуле SO2Cl2
равно 2
связей
в молекуле SO2Cl2
равно 2Укажите номер правильного ответа. Вещества с ковалентной полярной связью – это:
фтор 2) алмаз 3) кобальт 4) аммиак
Полярность ковалентной связи уменьшается в ряду:
HBr, HCl, HJ
CO2, CCL4, CF4
NH3, PH3, AsH3
ScO2, TeO2, SO2
Химическая связь в молекулах аммиака и брома соответственно:
Ковалентная полярная и ковалентная неполярная
Ионная и ковалентная полярная
Ковалентная неполярная и ковалентная полярная
Водородная и ковалентная неполярная
18. Укажите номер правильного ответа.
К гомогенной реакции относится:
С
+ О2
![]() СО2
СО2
S
+ O2
![]() SO2
SO2
N2
+ O2
![]() 2NO
2NO
2Al
+ 3Cl3![]() 2AlCl3
2AlCl3
Математическое
выражение средней скорости химической
реакции mA+nB
![]() gC
имеет вид:
gC
имеет вид:
1)
![]() 2)
2)
![]() 3)
3) ![]() 4)
4) ![]()
При
увеличении концентрации SO2
в 4 раза скорость реакции 2SO2
+ O2
![]() 2SO3
увеличится в:
2SO3
увеличится в:
32 раза 3) 8 раз
16 раза 4) 4 раза
При
повышении давления в 3 раза скорость
реакции 2NO
+ O2
![]() 2NO2
возрастет
в:
2NO2
возрастет
в:
27 раз 3) 8 раз
9 раз 4) 6 раз
С
повышением температуры (to![]() )
химическое равновесие CO
+ H2O
)
химическое равновесие CO
+ H2O
![]() CO2
+ H2
(-
CO2
+ H2
(- ![]() H)
сместиться:
H)
сместиться:
вправо
![]()
влево
![]()
Если
повысить давление, то химическое
равновесие H2
+ Cl2![]() 2HCl
сместиться:
2HCl
сместиться:
вправо
![]()
влево
![]()
равновесие не сместится
Оптимальные условия синтеза оксида серы (VI)
2SO2
+ O2
![]() 2SO3
(-
2SO3
(-![]() Hx.p.):
Hx.p.):
P![]() ,
to
,
to![]() 3)
P
3)
P![]() ,
to
,
to![]()
P![]() ,
to
,
to![]() 4)
P
4)
P![]() ,
to
,
to![]()
Математическое
выражение Кр системы nA
+ mB
![]() gC
+ pD
имеет вид:
gC
+ pD
имеет вид:
1)
![]() ; 3)
; 3)
![]() ;
г
г
;
г
г
2)
![]() ; 4)
; 4)
![]() .
.
Равновесие
химической реакции 4HCl
+ O2
![]() 2Cl2
+ 2H2O
(-
2Cl2
+ 2H2O
(-![]() H)
смещается в сторону продуктов при
г
г
г г
H)
смещается в сторону продуктов при
г
г
г г
повышении температуры
повышении давления
наличие катализатора
понижении давления
Реакции,
протекающие с выделением тепла называются
экзотермические,
![]() Н
х.р.
имеет знак минус
Н
х.р.
имеет знак минус
Химическая реакция не возможна, если Δ Gх.р. больше 0
![]()
![]() Gх.р.
при н.у. рассчитывают по формуле ΔGх.р.
= Σ ΔGпрод
- ΣΔGисх
,
а при произвольных условиях:
Gх.р.
при н.у. рассчитывают по формуле ΔGх.р.
= Σ ΔGпрод
- ΣΔGисх
,
а при произвольных условиях:
Если
![]() G
х.р. = 0, то в системе наступает равновесие
G
х.р. = 0, то в системе наступает равновесие
Изменение энтропии системы рассчитывают по формуле:
1)
![]() Н
х.р
=
Н
х.р
= ![]() ;
;
2)
![]() ;
;
3)
![]() ;
;
4)
![]() .
.
Если
![]() G
х.р. <
0, то реакция идет
самопроизвольно
G
х.р. <
0, то реакция идет
самопроизвольно
