
- •Кафедра теоретических основ материаловедения
- •Гринева с.И., Сычев м.М., Лукашова т.В.,
- •Коробко в.Н., Мякин с.В.
- •Коррозия и методы защиты
- •Содержание
- •Введение
- •1 Краткие сведения о коррозионных процессах
- •1.1 Классификация коррозионных разрушений
- •1.2 Методы оценки коррозионной стойкости
- •1.3 Методы коррозионных испытаний
- •2 Факторы, влияющие на развитие коррозии материалов
- •2.1 Внутренние факторы коррозии
- •2.1.1 Термодинамическая устойчивость металла
- •2.1.2 Положение металла в периодической системе элементов
- •2.1.3 Химический состав и структура сплавов
- •2.1.4 Шероховатость поверхности и внутренние напряжения в деталях
- •2.2 Внешние факторы коррозии
- •2.2.1 Влияние рН на скорость коррозии
- •2.2.2 Влияние кислорода на скорость коррозии
- •2.2.3 Влияние температуры на скорость коррозии
- •2.2.4 Влияние давления на скорость коррозии
- •2.2.5 Влияние скорости движения электролита на скорость коррозии
- •2.2.6 Влияние состава и концентрации нейтральных солей на скорость коррозии
- •3 Химическая коррозия металлов
- •3.1 Газовая коррозия
- •3.1.1 Образование оксидных соединений на поверхности металла
- •3.1.2 Условия образования, защитных оксидных пленок
- •3.1.3 Скорость роста пленки на металлах
- •3.1.4 Газовая коррозия стали и чугуна
- •3.1.5 Катастрофическая газовая коррозия
- •3.1.6 Водородная коррозия. Водородный износ
- •3. 1.7 Карбонильная коррозия
- •3.1.8 Коррозия, вызываемая сернистыми соединениями
- •3.1.9 Коррозия, вызываемая хлором
- •3.1.10 Защита от газовой коррозии
- •3.2 Коррозия металлов в неэлектролитах
- •4. Электрохимическая коррозия
- •4.1 Особенности строения электролитов
- •4.2 Образование двойного электрического слоя
- •4.3 Электродные потенциалы
- •4.4 Механизм электрохимической коррозии
- •4.5 Поляризация электродов
- •4.6 Деполяризация электродов
- •4.7 Коррозионная диаграмма Эванса
- •4.8 Факторы, ограничивающие электрохимическую коррозию
- •5. Пассивность металлов
- •5.1 Теория пассивности металлов
- •5.2 Кинетика анодных процессов при пассивации металлов
- •6 Атмосферная коррозия металлов
- •6.1 Факторы, вызывающие атмосферную коррозию
- •6.2 Виды и механизм атмосферной коррозии
- •6.3 Скорость атмосферной коррозии
- •7. Подземная коррозия
- •7.1 Почвенная коррозия
- •7.2 Коррозия, вызванная действием блуждающих токов
- •8. Локальная коррозия
- •8.1 Точечная (питтинговая) коррозия
- •8.2 Щелевая коррозия
- •8.3 Межкристаллитная коррозия
- •8.4 Ножевая коррозия
- •9 Методы защиты от коррозии
- •9.1 Защита металлов от коррозии обработкой коррозионной среды
- •9.1.1 Удаление агрессивных компонентов из коррозионной среды
- •9.1.2 Защита металлов от коррозии ингибиторами
- •9.1.3 Механизм защитного действия ингибиторов
- •9.1.4 Влияние некоторых факторов на эффективность действия
- •9.2 Защитные покрытия
- •9.2.1 Металлические покрытия
- •9.2.2 Защитные покрытия на органической основе
- •9.2.3 Защитные покрытия на неорганической основе
- •9.3 Электрохимическая защита
- •9.3.1 Катодная зашита
- •9.3.2 Анодная защита
- •9.3.3 Защита от коррозии, вызываемой блуждающими
- •9.4 Защита от коррозии на стадии проектирования
- •9.4.1 Выбор материалов
- •9.4.2 Рациональные геометрические формы конструкций
- •Литература
- •Коррозия и методы защиты
9.1.4 Влияние некоторых факторов на эффективность действия
ингибиторов
К наиболее важным факторам, влияющим на эффективность действия ингибиторов, относятся: температура среды, концентрация ингибитора, кислотность среды, взаимное влияние ингибиторов.
Температура среды. Для большинства ингибиторов с увеличением температуры агрессивной среды наблюдается вначале возрастание ингибиторного эффекта γ, а затем, по достижении определенной температуры, снижение его, как показано на рисунке 30. Температурный
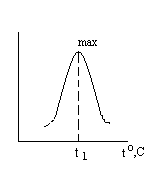 Рисунок
30 — Зависимость ингибиторного эффекта
от
Рисунок
30 — Зависимость ингибиторного эффекта
от
температуры
максимум ингибиторного эффекта γmax для многих ингибиторов лежит в пределах 60—80 °С. Принято подразделять ингибиторы на высокотемпературные и низкотемпературные. Те ингибиторы, которые имеют максимум ингибиторного эффекта при температуре выше 60 — 80 °С, называются высокотемпературными. Максимум ингибиторного эффекта обнаружен для некоторых ингибиторов в нейтральных средах. Учет этого фактора имеет большое значение при определении оптимальных температурных режимов.
Концентрация ингибиторов. Максимальное ингибирование будет достигаться при введении в коррозионную среду ингбитора в количестве, достаточном, чтобы покрыть поверхность металла мономолекулярным слоем.
Для большинства органических ингибиторов характерно увеличение защитного действия по мере роста их концентрации до какого-то предельного значения, при дальнейшем же увеличении концентрации эффективность действия ингбиторов не меняется.
Совсем другая зависимость обнаруживается для неорганических анодных ингибиторов. При малых концентрациях анодных ингибиторов наблюдается рост скорости коррозии, и только при достижении определенной концентрации наступает резкое уменьшение скорости вследствие пассивации, металла. Для каждой конкретной системы оптимальную концентрацию ингибитора необходимо определять опытным путем.
Кислотность среды. Подавляющее число ингибиторов действует эффективно только при определенном значении рН. Так, для неорганических ингибиторов (карбонатов, фосфатов) реакция среды должна быть близкой к нейтральной.
Хроматы также эффективны только в нейтральных средах. В

1 — аддитивность; 2 — синергизм; 3 — антагонизм
Рисунок 31 — Возможные варианты действия двух смешанных
ингибитров
кислых средах хроматы восстанавливаются на поверхности металла по реакции
СгО42 - + 8Н+ + Зе → Сг3++4Н2О,
ускоряя катодную реакцию и коррозию металлов. В кислых средах эффективное действие проявляют многие органические соединения, так называемые ингибиторы травления.
Взаимное влияние ингибиторов. На рисунке 31 показаны возможные варианты взаимного действия смесей двух ингибиторов А и Б. Смеси ингибиторов, имеющие одинаковые или близкие физико-химические свойства, обладают, как правило, аддитивностью. Аддитивность на практике встречается редко. Смеси ингибиторов, имеющих различные химические свойства, могут проявлять антагонизм или синергизм. Антагонизм — ослабление эффективности действия ингибиторов в смеси. Такие сочетания ингибиторов недопустимы. Синергизм — увеличение эффективности действия ингибиторов в смеси, которое ведет к достижению большего защитного эффекта, чем при раздельном применении ингибиторов. Можно достигнуть того же защитного эффекта при меньшей суммарной концентрации ингибиторов в смеси по сравнению с концентрацией отдельных ингибиторов. При синергизме можно дорогой ингибитор заменить смесью дешевых ингибиторов, достигнув при этом равноценного эффекта.
Синергизм обнаруживается в смесях неорганических соединений, органических соединений, а также в смесях органических соединений с неорганическими. Эффект синергизма имеет важное практическое значение, используя его можно значительно увеличить эффективность применения промышленных ингибиторов. Синергизм, обнаруживаемый у смесей ингибиторов, пока не находит достаточно убедительного объяснения, поэтому для конкретной системы опытным путем подбираются наиболее эффективные смеси ингибиторов.
