
- •Государственное бюджетное образовательное учреждение
- •С о д е р ж а н и е
- •Задание №1
- •Литература:
- •Задание №2
- •Литература:
- •Задание №3
- •Литература:
- •Задание №4
- •Литература:
- •Задание №5
- •Литература:
- •Задание №6
- •Литература:
- •Задание №7
- •Вариант билета.
- •Литература:
- •Задание №8
- •Литература:
- •Задание № 9
- •Литература:
- •Задание №10
- •Литература:
- •Задание №11
- •Литература:
- •Задание №12
- •Литература:
- •Задание №13
- •Литература:
Задание № 9
УГЛЕВОДЫ. СТРОЕНИЕ И СВОЙСТВА МОНОСАХАРИДОВ
I. Подготовить ответы на следующие вопросы:
Углеводы. Классификация.
Моносахариды. Классификация по функциям и числу атомов углерода в цепи. Представители классов.
Энантиомерия, диастереомерия моносахаридов, эпимеры.
Образование циклических форм моносахаридов по Хеуорсу.
,-аномеры, таутомеры. Явление мутаротации.
Реакционная способность моносахаридов (свойства альдегидов, спиртов, полуацеталей и специфические свойства).
Производные моносахаридов (аминосахары, сахарные кислоты), их биологическая роль.
II. Подготовиться к лабораторной работе «Химические свойства моносахаридов».
III. Подготовиться к контрольной работе по теме «Моносахариды. Строение и химические свойства».
IV. Выполнить письменно упражнения:
Написать проекционные формулы таутомерной смеси для Д-глюкозы и Д- фруктозы. Назвать таутомеры.
Написать формулы , Д – галактопиранозы;,Д – дезоксирибофуранозы; 2-амино-2-дезокси-Д-глюкопиранозы.
Написать реакции:
а) окисления Д-рибозы;
б) восстановления Д-галактозы;
в) образование метил-,Д-галактопиранозида.
V. Разобрать устно обучающие задачи в учебнике: Тюкавкина Н.А. «Руководство к лабораторным занятиям по биоорганической химии», М., 1985, с.201-213, задачи №1,2,3,4.
Литература:
Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 377-406.
Материалы лекций.
Задание №10
СЛОЖНЫЕ УГЛЕВОДЫ
I. Подготовить ответы на следующие вопросы:
Состав и строение дисахаридов (мальтоза, лактоза, сахароза). Их биологическая роль.
Химические свойства дисахаридов, особенности сахарозы.
Состав и строение гомополисахаридов: крахмал, гликоген, клетчатка. Вторичная структура крахмала и клетчатки.
Гидролиз крахмала.
Биологическая роль гомополисахаридов.
Состав и строение гетерополисахаридов (гиалуроновая кислота). Гликопротеины. Их биологическая роль.
II. Подготовиться к лабораторной работе «Химические свойства сложных углеводов».
III. Подготовиться к контрольной работе по теме «Строение и химические свойства сложных углеводов».
IV. Выполнить письменно упражнения:
Написать уравнения реакций гидролиза сахарозы и лактозы.
Написать уравнение реакции окисления мальтозы гидроксидом меди (II) при нагревании.
Написать уравнение реакции образования сахарата меди (II).
Литература:
Тюкавкина Н.А., Бауков Ю.И. Биоорганическая химия. – М.: Медицина, 1991. – С. 407 - 430.
Руководство к лабораторно-практическим занятиям по биоорганической химии /Н.Н. Артемьева, В.Л. Белобородов, С.К. Еремин, и др.; / Под ред. Н.А. Тюкавкиной. – М.: Медицина, 1985.- С. 201-213, задачи №1,2,3,4.
Методическая разработка кафедры по теме «Дисахариды».
Материалы лекций.
Задание №11
АМИНОКИСЛОТЫ. БЕЛКИ.
I. Подготовить ответы на следующие вопросы:
Классификация и строение аминокислот.
Физико-химические характеристики боковой цепи аминокислот.
Кислотно-основные свойства аминокислот.
Химические свойства аминокислот. Реакции декарбоксилирования, переаминирования, окислительного дезаминирования, образования пептидов.
Пептиды. Пространственное строение пептидной группы. Белки. Уровни структурной организации белковой молекулы.
Биологическая роль аминокислот и белков.
II. Подготовиться к лабораторной работе «Химические реакции, лежащие в основе качественного определения белков и аминокислот».
III. Разобрать обучающую задачу:
Определить область значений рН, в которой находится изоэлектрическая точка (и.э.т.) трипептида сер-асп-ала.
Молекулярная формула пептида:
OO
IIII
H2N – CH – C – N – CH – C – N – CH – COOH
I I I I I
CH2 H CH2 H CH3
II
OHCOOH
сериласпарагилаланин
N-конец С-конец
В водном растворе ионное состояние пептида отвечает формуле:
O O
II II
H3N – CH – C – N – CH – C – N – CH – COO
I I I I I
CH2 H CH2 H CH3
II
OHCOO
Общий заряд пептида отрицательный. Это пептид кислотного характера. Его и.э.т. лежит в слабокислой среде.
Ответ: pJ<7
Какой заряд имеет пептид цис-гис-вал в растворе с рН 4,5?
Ионное состояние пептида цис-гис-вал отвечает формуле:
O O
II II
H3N – CH – C – N – CH – C – N – CH – COO
I I I I I

CH2 H CH2 H CH – CH3

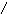
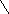
I HN I
S CH3


N
I
H
В кислой среде при рН 4,5 диссоциация групп кислотного характера подавлена. При этом формируется катион пептида:
OO
IIII
H3N–CH–C–N–CH–C–N–CH–COOH
I I I I I

CH2 H CH2 H CH – CH3

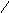
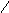
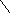
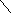
I HN I
SH СH3


N
I
H
Ответ: общий заряд положительный.
IV. Подготовиться к контрольной работе по теме: «Строение и химические свойства аминокислот».
V. Выполнить письменно упражнения:
Написать уравнение реакции переаминирования щавелевоуксусной и глутаминовой кислот.
Написать уравнение реакции декарбоксилирования лизина.
Составить схему реакции окислительного дезаминирования аспарагиновой кислоты.
Написать уравнение реакции образования трипептида глу-иле-фен и определить область значений рН, в которой находится и.э.т. данного пептида.
