
- •Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
- •Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
- •Рецензент:
- •А) изготовление простого фильтра;
- •Лабораторная работа № 18 Тема: методы очистки и выделения органических соединений. Перекристаллизация
- •18.1 Теоретическая часть
- •18.2 Экспериментальная часть
- •Лабораторная работа № 19 Тема: методы очистки и выделения органических соединений. Сублимация
- •19.1 Теоретическая часть
- •19.2. Экспериментальная часть
- •Лабораторная работа № 20 Тема: методы очистки и выделения органических соединений. Перегонка
- •20.1 Теоретическая часть
- •20.2. Экспериментальная часть
- •20.3. Отчет о работах №18-20
- •20.4. Контрольные вопросы
- •Лабораторная работа № 21 Тема: качественный элементный анализ органических соединений
- •21.1 Теоретическая часть
- •21.2 Экспериментальная часть
- •21.2.1 Обнаружение углерода пробой на обугливание (тяга !).
- •21.2.2 Обнаружение углерода и водорода окислением вещества оксидом меди (II).
- •21.2.3 Проба Бейльштейна на галогены.
- •21.2.4 Обнаружение галогенов действием натрия на спиртовой раствор органического вещества.
- •21.3 Отчет о работе
- •22.1.2 Химические свойства
- •22.2 Экспериментальная часть
- •22.2.3 Бромирование предельных углеводородов
- •22.3. Отчет о работе
- •22.4. Контрольные вопросы
- •22.5. Индивидуальное задание
- •23.1.2 Химические свойства
- •5. Окисление перманганатом калия в нейтральной или слабощелочной среде приводит к образованию гликолей.
- •Реакция часто применяется для определения положения двойной связи в молекуле, так как по образующимся карбонильным соединениям можно представить себе и строение исходного алкена.
- •23.2 Экспериментальная часть
- •23.2.1 Получение этилена и его горение
- •23.2.2 Присоединение к этилену брома
- •23.2.3 Отношение этилена к окислителям
- •23.2.4 Бромирование непредельных углеводородов
- •23.3 Отчет о работе
- •23.4. Контрольные вопросы
- •Лабораторная работа № 24 Тема: алкины
- •24.1 Теоретическая часть
- •24.1.1 Методы получения
- •24.1.2 Химические свойства
- •А. Реакции присоединения
- •5. Присоединение спиртов. В присутствии едкого кали под давлением ацетилен присоединяет спирты с образованием алкилвиниловых эфиров:
- •24.2 Экспериментальная часть
- •24.3 Отчет о работе
- •24.4. Контрольные вопросы
- •24.5. Индивидуальное задание
- •1. Получение бензола из ацетилена:
- •3. Из ароматических соединений:
- •4. Гомологи бензола получают из галогенпроизводных реакцией Вюрца-Фиттига:
- •25.1.2 Химические свойства
- •25.2 Экспериментальная часть
- •25.2.1 Окисление ароматических углеводородов
- •25.2.2 Бромирование ароматических углеводородов
- •25. 2.3. Алкилирование бензола.
- •25.3 Отчет о работе
- •25.4. Контрольные вопросы
- •Лабораторная работа №26 Тема: спирты и фенолы
- •26.1Теоретическая часть
- •26.1.1 Методы получения спиртов
- •26.1.2 Химические свойства спиртов
- •1. Взаимодействие с щелочными металлами:
- •26.1.3 Методы получения фенолов
- •26.1.4 Химические свойства
- •26.2 Экспериментальная часть
- •26.2.1 Обнаружение воды в спирте и обезвоживание спирта
- •26.2.2 Свойства изоамилового спирта
- •26.2.3 Отношение спиртов к индикаторам
- •26.2.4 Окисление этилового спирта окисью меди
- •26.2.5 Растворение фенола в воде
- •26.2.6 Получение фенолята натрия
- •26.2.7 Получение трибромфенола
- •26.3. Отчет о работе
- •26.4. Контрольные вопросы
- •Лабораторная работа №27 Тема: альдегиды и кетоны
- •27.1 Теоретическая часть
- •27.1.1 Методы получения
- •3. В технике альдегиды получают прямым присоединением со и н2 к олефинам:
- •27.1.2 Химические свойства альдегидов и кетонов
- •4. Присоединение спиртов:
- •6. Взаимодействие с аммиаком:
- •7. Образование оксимов с гидроксиламином:
- •27.2 Экспериментальная часть
- •27.2.1 Открытие альдегидов с фуксинсернистой кислотой (Реакция Шиффа)
- •27.2.2 Цветная реакция на ацетон с нитропруссидом натрия (Проба Легаля)
- •27.2.3 Окисление формальдегида аммиачным раствором оксида серебра (реакция Толленса)
- •27.2.4 Окисление формальдегида гидроксидом меди (II) в щелочной среде
- •27.3. Отчет о работе
- •27.4. Контрольные вопросы
- •27.5. Индивидуальное задание лабораторная работа №28 Тема: карбоновые кислоты
- •28.1 Теоретическая часть
- •28.1.3 Химические свойства
- •28.2 Экспериментальная часть
- •28.2.1 Растворимость карбоновых кислот в воде и органических растворителях
- •28.2.2 Получение и свойства муравьиной кислоты
- •28.2.3 Получение и свойства уксусной кислоты
- •28.2.4.Реакции олеиновой и сорбиновой кислот с бромной водой
- •28.2.5.Окисление олеиновой кислоты перманганатом калия
- •28.3. Отчет о работе
- •28.4. Контрольные вопросы
- •28.5. Индивидуальное задание
- •29.2 Экспериментальная часть
- •29.2.1. Гидролиз мыла
- •29.2.2. Выделение высших жирных кислот из мыла
- •29.2.3. Образование нерастворимых солей высших жирных кислот
- •29.2.4. Взаимодействие растительного масла с водным раствором перманганата калия (реакция Вагнера)
- •29.2.5. Омыление жира спиртовым раствором гидроксида натрия
- •29.2.6. Определение кислотного числа, числа омыления и эфирного числа (выполняется в порядке нирс)
- •29.3.Отчет о работе
- •29.4.Вопросы для контроля знаний
- •29.5. Индивидуальное задание
- •30.1.2. Свойства и реакционная способность
- •30.1.3.Применение
- •30.3. Экспериментальная часть
- •30.4. Контрольные вопросы
- •30.5. Индивидуальное задание лабораторная работа №31 Тема:качественные реакции на функциональные группы
- •31.1. Теоретическая часть
- •Простые эфиры – легколетучие жидкости (низшие) с характерным запахом. Качественной реакцией на простые эфиры является реакция с иодистоводородной кислотой:
- •31.2.Экспериментальная часть
- •31.2.1. Содержание задания
- •31.2.2.Ход анализа органических соединений
- •1. Предварительные испытания
- •31.2.3.Проведение некоторых качественныхреакций
- •31.3.Типовые экспериментальные задачи
- •Лабораторная работа №32 Тема:идентификация полимерных материалов
- •32.1.Теоретическая часть
- •32.2.Экспериментальная часть
- •31.3.Отчет о работе
- •Содержание
- •Лукашов Сергей Викторович
21.3 Отчет о работе
Таблица 2. – Результаты анализа органических веществ
|
№п/п |
Анализируемое вещество |
Открываемый элемент |
Метод |
Выводы |
|
|
|
|
|
|
21.4.Индивидуальное задание.
ЛАБОРАТОРНАЯ РАБОТА № 22
Тема: АЛКАНЫ
Цель работы: изучение методов получения и химических свойств алканов.
Задания: 1)освоить теоретический материал
2) провести опыты, представленные в экспериментальной части
3) оформить отчет о работе
4) выполнить индивидуальные задания
22.1 Теоретическая часть
22.1.1 Методы получения
Главным природным источником предельных углеводородов является нефть, а для первых членов гомологического ряда – природный газ. Однако, выделение индивидуальных соединений из нефти или продуктов ее крекинга –весьма трудоемкая, а часто и невыполнимая задача, поэтому приходится прибегать к синтетическим методам получения.
1. Алканы образуются при действии металлического натрия на моногало-генпроизводные – реакция Вюрца:
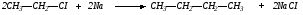
Если взяты разные галогенпроизводные, то образуется смесь трех различных алканов, так как вероятность встречи в реакционном комплексе одинаковых или разных молекул равна, а реакционная способность их близка:
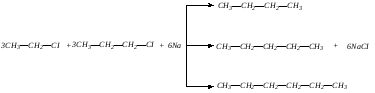
2. Алканы могут быть получены при восстановлении алкенов или алкинов водородом в присутствии катализаторов.
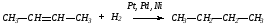
3. Самые разнообразные производные алканов могут быть восстановлены при высокой температуре йодоводородной кислотой:
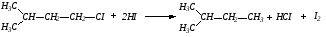
4. Алканы могут быть получены при сплавлении солей карбоновых кислот со щелочью. Образующийся при этом алкан содержит на один атом углерода меньше, чем исходная карбоновая кислота:
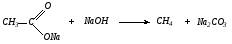
22.1.2 Химические свойства
Предельные
углеводороды при обычных условиях
обладают большой химической инертностью.
Это объясняется тем, что все
 -связи
углерод — углерод и углерод — водород
в них весьма прочны (энергии этих связей
порядка 350-400 кДж/моль). К реакциям
присоединения они вообще не способны
вследствие насыщенности всех связей
атомов углерода.C
большинством химических реагентов
алканы или вовсе не реагируют, или
реагируют чрезвычайно медленно. Так,
концентрированная серная кислота,
обугливающая многие органические
соединения, на предельные углеводороды
не действует при комнатной температуре.
Сильные окислители (например,
марганцeвокислый калий) при комнатной
температуре тоже не действуют на алканы.
-связи
углерод — углерод и углерод — водород
в них весьма прочны (энергии этих связей
порядка 350-400 кДж/моль). К реакциям
присоединения они вообще не способны
вследствие насыщенности всех связей
атомов углерода.C
большинством химических реагентов
алканы или вовсе не реагируют, или
реагируют чрезвычайно медленно. Так,
концентрированная серная кислота,
обугливающая многие органические
соединения, на предельные углеводороды
не действует при комнатной температуре.
Сильные окислители (например,
марганцeвокислый калий) при комнатной
температуре тоже не действуют на алканы.
1. Радикальное галогенирование. На свету галогены (энергичнее всего хлор, с йодом реакция не идет) последовательно замещают атомы водорода в предельных углеводородах:
CH4
+ Cl2
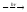 CH3Cl
+ HCl
CH3Cl
+ HCl
CH3Cl
+ Cl2
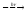 CH2Cl2
+ HCl
CH2Cl2
+ HCl
CH2Cl2
+ Cl2
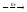 CHCl3
+ HCl
CHCl3
+ HCl
CHCl3
+ Cl2
 CCl4
+
HCl
CCl4
+
HCl

2. Нитрование. Азотная кислота при обычной температуре почти не действует на предельные углеводороды; при нагревании же действует главным образом как окислитель. При нагревании (около1400С) и под давлением азотная кислота действует как нитрующий агент, т. е. один из атомов водорода предельного углеводорода замещается на остаток кислоты –NO2 (нитрогруппа):
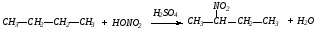
Эта реакция тоже радикального типа и подчиняется тем же закономерностям, что и реакция галогенирования, т. е. легче всего замещается водород у третичного атома, затем у вторичного и труднее всего у первичного атома углерода.
3. Окисление. Окислители, даже такие, как хромовая смесь и марганцевокислый калий, при обычных температурах не действуют на предельные углеводороды.
При температуре выше 300оС предельные углеводороды воспламеняются и сгорают с образованием СО2 и Н2О:
С5Н12
+ 8О2
 5СО2 + 6Н2О
5СО2 + 6Н2О
При очень высоких температурах в промышленности реализован процесс взаимодействия метана с водой:
СН4
+ Н2О
 СО + 3Н2О
СО + 3Н2О
4. Сульфохлорирование. Эта реакция имеет большое значение в производстве моющих средств. Тяжелые фракции синтетических углеводородов С12–С18 в условиях ультрафиолетового облучения подвергаются совместному действию Cl2 и SO2. Образующиеся сульфонилхлориды при омылении щелочами дают соли сульфокислот:
а)
Сl2
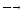 2Cl•;
2Cl•;
б)
CH3(CH2)10CH3
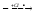 CH3(CH2)10CH2•
+ HCI
CH3(CH2)10CH2•
+ HCI
в)CH3(CH2)10CH2•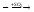 CH3(CH2)10CH2-SO2
CH3(CH2)10CH2-SO2
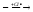
CH3(CH2)10CH2-SO2Сl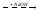 CH3(CH2)10CH2-SO3Na
+ HCI
CH3(CH2)10CH2-SO3Na
+ HCI
натриевая соль додекансульфо-кислоты (моющее средство)
Реакция сульфохлорирования, как и реакция радикального галогенирования, является цепной реакцией.
