- •Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
- •Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
- •Рецензент:
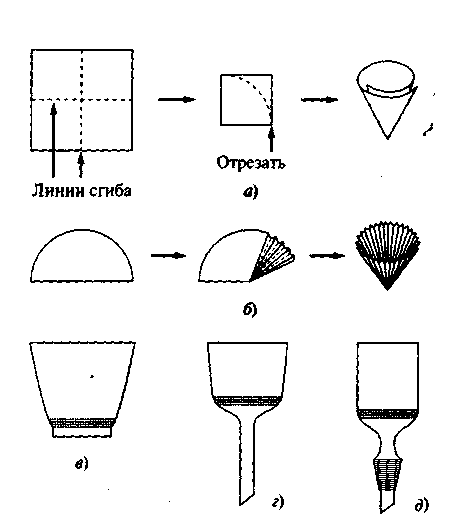
- •А) изготовление простого фильтра;
- •Лабораторная работа № 18 Тема: методы очистки и выделения органических соединений. Перекристаллизация
- •18.1 Теоретическая часть
- •18.2 Экспериментальная часть
- •Лабораторная работа № 19 Тема: методы очистки и выделения органических соединений. Сублимация
- •19.1 Теоретическая часть
- •19.2. Экспериментальная часть
- •Лабораторная работа № 20 Тема: методы очистки и выделения органических соединений. Перегонка
- •20.1 Теоретическая часть
- •20.2. Экспериментальная часть
- •20.3. Отчет о работах №18-20
- •20.4. Контрольные вопросы
- •Лабораторная работа № 21 Тема: качественный элементный анализ органических соединений
- •21.1 Теоретическая часть
- •21.2 Экспериментальная часть
- •21.2.1 Обнаружение углерода пробой на обугливание (тяга !).
- •21.2.2 Обнаружение углерода и водорода окислением вещества оксидом меди (II).
- •21.2.3 Проба Бейльштейна на галогены.
- •21.2.4 Обнаружение галогенов действием натрия на спиртовой раствор органического вещества.
- •21.3 Отчет о работе
- •22.1.2 Химические свойства
- •22.2 Экспериментальная часть
- •22.2.3 Бромирование предельных углеводородов
- •22.3. Отчет о работе
- •22.4. Контрольные вопросы
- •22.5. Индивидуальное задание
- •23.1.2 Химические свойства
- •5. Окисление перманганатом калия в нейтральной или слабощелочной среде приводит к образованию гликолей.
- •Реакция часто применяется для определения положения двойной связи в молекуле, так как по образующимся карбонильным соединениям можно представить себе и строение исходного алкена.
- •23.2 Экспериментальная часть
- •23.2.1 Получение этилена и его горение
- •23.2.2 Присоединение к этилену брома
- •23.2.3 Отношение этилена к окислителям
- •23.2.4 Бромирование непредельных углеводородов
- •23.3 Отчет о работе
- •23.4. Контрольные вопросы
- •Лабораторная работа № 24 Тема: алкины
- •24.1 Теоретическая часть
- •24.1.1 Методы получения
- •24.1.2 Химические свойства
- •А. Реакции присоединения
- •5. Присоединение спиртов. В присутствии едкого кали под давлением ацетилен присоединяет спирты с образованием алкилвиниловых эфиров:
- •24.2 Экспериментальная часть
- •24.3 Отчет о работе
- •24.4. Контрольные вопросы
- •24.5. Индивидуальное задание
- •1. Получение бензола из ацетилена:
- •3. Из ароматических соединений:
- •4. Гомологи бензола получают из галогенпроизводных реакцией Вюрца-Фиттига:
- •25.1.2 Химические свойства
- •25.2 Экспериментальная часть
- •25.2.1 Окисление ароматических углеводородов
- •25.2.2 Бромирование ароматических углеводородов
- •25. 2.3. Алкилирование бензола.
- •25.3 Отчет о работе
- •25.4. Контрольные вопросы
- •Лабораторная работа №26 Тема: спирты и фенолы
- •26.1Теоретическая часть
- •26.1.1 Методы получения спиртов
- •26.1.2 Химические свойства спиртов
- •1. Взаимодействие с щелочными металлами:
- •26.1.3 Методы получения фенолов
- •26.1.4 Химические свойства
- •26.2 Экспериментальная часть
- •26.2.1 Обнаружение воды в спирте и обезвоживание спирта
- •26.2.2 Свойства изоамилового спирта
- •26.2.3 Отношение спиртов к индикаторам
- •26.2.4 Окисление этилового спирта окисью меди
- •26.2.5 Растворение фенола в воде
- •26.2.6 Получение фенолята натрия
- •26.2.7 Получение трибромфенола
- •26.3. Отчет о работе
- •26.4. Контрольные вопросы
- •Лабораторная работа №27 Тема: альдегиды и кетоны
- •27.1 Теоретическая часть
- •27.1.1 Методы получения
- •3. В технике альдегиды получают прямым присоединением со и н2 к олефинам:
- •27.1.2 Химические свойства альдегидов и кетонов
- •4. Присоединение спиртов:
- •6. Взаимодействие с аммиаком:
- •7. Образование оксимов с гидроксиламином:
- •27.2 Экспериментальная часть
- •27.2.1 Открытие альдегидов с фуксинсернистой кислотой (Реакция Шиффа)
- •27.2.2 Цветная реакция на ацетон с нитропруссидом натрия (Проба Легаля)
- •27.2.3 Окисление формальдегида аммиачным раствором оксида серебра (реакция Толленса)
- •27.2.4 Окисление формальдегида гидроксидом меди (II) в щелочной среде
- •27.3. Отчет о работе
- •27.4. Контрольные вопросы
- •27.5. Индивидуальное задание лабораторная работа №28 Тема: карбоновые кислоты
- •28.1 Теоретическая часть
- •28.1.3 Химические свойства
- •28.2 Экспериментальная часть
- •28.2.1 Растворимость карбоновых кислот в воде и органических растворителях
- •28.2.2 Получение и свойства муравьиной кислоты
- •28.2.3 Получение и свойства уксусной кислоты
- •28.2.4.Реакции олеиновой и сорбиновой кислот с бромной водой
- •28.2.5.Окисление олеиновой кислоты перманганатом калия
- •28.3. Отчет о работе
- •28.4. Контрольные вопросы
- •28.5. Индивидуальное задание
- •29.2 Экспериментальная часть
- •29.2.1. Гидролиз мыла
- •29.2.2. Выделение высших жирных кислот из мыла
- •29.2.3. Образование нерастворимых солей высших жирных кислот
- •29.2.4. Взаимодействие растительного масла с водным раствором перманганата калия (реакция Вагнера)
- •29.2.5. Омыление жира спиртовым раствором гидроксида натрия
- •29.2.6. Определение кислотного числа, числа омыления и эфирного числа (выполняется в порядке нирс)
- •29.3.Отчет о работе
- •29.4.Вопросы для контроля знаний
- •29.5. Индивидуальное задание
- •30.1.2. Свойства и реакционная способность
- •30.1.3.Применение
- •30.3. Экспериментальная часть
- •30.4. Контрольные вопросы
- •30.5. Индивидуальное задание лабораторная работа №31 Тема:качественные реакции на функциональные группы
- •31.1. Теоретическая часть
- •Простые эфиры – легколетучие жидкости (низшие) с характерным запахом. Качественной реакцией на простые эфиры является реакция с иодистоводородной кислотой:
- •31.2.Экспериментальная часть
- •31.2.1. Содержание задания
- •31.2.2.Ход анализа органических соединений
- •1. Предварительные испытания
- •31.2.3.Проведение некоторых качественныхреакций
- •31.3.Типовые экспериментальные задачи
- •Лабораторная работа №32 Тема:идентификация полимерных материалов
- •32.1.Теоретическая часть
- •32.2.Экспериментальная часть
- •31.3.Отчет о работе
- •Содержание
- •Лукашов Сергей Викторович
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«Брянская государственная инженерно-технологическая академия»
Х И М И Я
Методические указания по выполнению лабораторных работ
(№18 - №32) и организации подготовки к их защите
для студентов направления подготовки бакалавров 280700 – «Техносферная безопасность»
БРЯНСК 2013
Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования
«Брянская государственная инженерно-технологическая академия»
УТВЕРЖДЕНО
Научно-методическим советом БГИТА
Протокол № ____ от_________2013г
Х И М И Я
Методические указания по выполнению лабораторных работ
(№18 - №32) и организации подготовки к их защите
для студентов направления подготовки бакалавров 280700 – «Техносферная безопасность»
БРЯНСК 2013
УДК: 542.2.9
Химия: Методические указания по выполнению лабораторных работ (№18 - №32) и организации подготовки к их защите для студентов направления подготовки бакалавров 280700 – «Техносферная безопасность»/ Брянск. гос. инженер.-технол. акад. сост. С.В. Лукашов, Л.А. Сильченко – Брянск БГИТА, 2013. – 115 с.
Настоящие методические указания наряду с методикой проведения опытов и обработки их результатов содержат методический материал, призванный помочь студенту в самоподготовке к защите тем лабораторных работ. Он включает теоретические пояснения к каждой работе, примеры решения типовых задач, перечень понятий и законов, которые должен знать студент, а также умений и навыков, которыми он должен обладать. В конце каждой темы приводятся задания для самоконтроля.
Рецензент:
кандидат хим. наук, доц. каф. БЖДиХ БГТУ Казаков О.Г.
Рекомендованы редакционно-издательской и методической комиссиями инженерно-экологического факультета БГИТА
Протокол № _____ от «____»___________ 2013 г.
ВВЕДЕНИЕ
Органическая химия – наука, изучающая углеводороды и их производные, в состав которых могут входить многие элементы периодической системы.
Органическая химия занимает особое положение, что обусловлено как многообразием органических соединений, наличием специфических свойств, отличающих их от соединений других элементов, так и тем, что органическая химия изучает высокоорганизованную материю и тесно связана с биологией (органические соединения являются основой жизнедеятельности животных и растительных организмов).
Органические соединения, с одной стороны, обеспечивают комфортность человеческого существования, а с другой стороны, представляют угрозу для жизни человека и окружающей среды (при химически и экологически неграмотном применении достижений органической химии).
Знания о закономерностях органической химии, свойствах и реакциях органических веществ приобретаются в ходе экспериментов. Проводя опыты, исследователь имеет возможность наблюдать то или иное явление, сопоставлять факты и делать выводы. Поэтому лабораторный практикум по органической химии – необходимый элемент изучения этой дисциплины.
Цель настоящего лабораторного практикума - ознакомить студентов с характерными свойствами и реакциями основных классов органических соединений, а также с индивидуальными особенностями их главнейших представителей.
При выполнении представленных ниже лабораторных работ студенты знакомятся с основными методами очистки и выделения органических соединений, их способами получения и химическими свойствами. Многие опыты выполняются студентами индивидуально: каждый получает задание и оформляет отчет по своим результатам, что развивает у студентов самостоятельность в решении поставленных задач.
Для более эффективного использования времени аудиторных занятий студент должен заранее ознакомиться с темой предстоящей работы, записать в лабораторный журнал название, цель, краткий конспект теоретической части, сжато описать методику проведения эксперимента.
После выполнения лабораторной работы студенты защищают ее. Для этого они должны: предъявить отчет о выполнении работы, который оформляется в лабораторном журнале; уметь изложить ход проведения лабораторных опытов, объяснить результаты эксперимента; по просьбе преподавателя составить соответствующие уравнения реакций, произвести расчеты, не выходящие за рамки типовых задач.
Правила работы в лаборатории органической химии
Выполнению лабораторных работ по органической химии предшествует самостоятельная домашняя подготовка студентов: работа с учебниками, учебными пособиями, лекционными записями.
На первом занятии студенты ознакомятся с правилами техники безопасности, пожарной безопасности и мерами оказания первой помощи при несчастных случаях. Следует ознакомиться с имеющимися в лаборатории средствами пожаротушения и знать их местонахождение.
Перед началом работы в лаборатории каждый студент проходит инструктаж по технике безопасности, после чего оформляется соответствующая запись в специальном журнале с обязательной распиской студента и преподавателя, проведшего инструктаж.
Работать в лаборатории студенты должны в халатах. При выполнении опытов в лаборатории студенты обязаны соблюдать следующие основные правила работы:
- при выполнении каждого опыта вначале необходимо внимательно ознакомиться с описанием опыта, а затем приступать к его выполнению;
-обращать особое внимание на те пункты, в которых указано “Осторожно!”;
- при использовании реактивов общего пользования поддерживать на полках порядок в расположении склянок с растворами и веществами; не перемещать их на другое место, ставить на полку так, чтобы надпись на склянке была хорошо видна всем работающим на этом месте. Склянки с летучими веществами тотчас после пользования следует быстро закрывать пробками;
- при выполнении опыта необходимо брать то количество реактива, которое указано в описании. Если количество реактива взято больше, чем необходимо для проведения опыта, лишнее количество выливать или пересыпать из пробирки в общие склянки не разрешается, во избежание порчи реактивов и растворов;
- при выполнении опытов с нагреванием необходимо пользоваться держателем пробирок. При нагревании отверстие пробирки должно быть направлено в боковую или внутреннюю сторону вытяжного шкафа;
- при нагревании пробирки с реакционной смесью ее следует держать в наклонном положении во избежание попадания брызг в лицо и глаза, непрерывно вращать и следить, чтобы с наружной стороны пробирка была сухой, в противном случае она лопнет;
- при работе с газоотводной трубкой необходимо помнить, что убирать горелку из-под пробирки с реакционной смесью можно только после того, как нижний конец газоотводной трубки удален из жидкости;
- использование собранного прибора без предварительной проверки его исправности не допускается;
- оставлять действующий прибор (или установку) без присмотра не разрешается;
- при работе с водяными холодильниками необходимо постоянно контролировать непрерывность тока воды;
- при перегонке веществ с температурой кипения выше 150оС необходимо применять холодильники с воздушным охлаждением;
- при перегонке жидкостей следует использовать специальные круглодонные колбы (колбы Вюрца, Кляйзена, двух- или трехгорлые колбы);
- плоскодонные колбы нельзя применять для работы в вакууме, а также для работы при температуре выше 100оС. Для отсасывания в вакууме применяют толстостенные колбы Бунзена;
-перенося сосуды с горячей жидкостью, нужно держать их двумя руками: одной за дно, другой – за горловину, используя при этом полотенце;
- при закрывании толстостенного сосуда пробкой следует держать его за верхнюю часть горла как можно ближе к пробке. Нагретый сосуд нельзя закрывать притертой пробкой, пока он не остынет;
- при переливании жидкостей необходимо пользоваться воронкой;
- особую осторожность следует проявлять при работе с газами, дающими взрывчатые смеси с воздухом (метан, этилен, ацетилен);
работу с летучими ядовитыми и сильно пахнущими веществами производить только в вытяжном шкафу;
- при пользовании концентрированными кислотами и щелочами исключить возможность попадания их на руки, лицо, одежду;
- запрещается пробовать химические вещества на вкус, всасывать ртом любые жидкости в пипетки. При исследовании запаха вещества следует осторожно направлять к себе его пары легким движением руки;
- все работы с концентрированными кислотами и щелочами проводить в вытяжном шкафу;
- работу с металлическим натрием обязательно проводить вдали от воды или брызгающих водопроводных кранов. Категорически запрещается выбрасывать остатки натрия в раковину. Их уничтожают, растворяя в спирте. Загоревшийся натрий следует гасить сухим хлоридом натрия;
- нагревать ЛВЖ следует на масляных, песчаных, водяных банях в колбах с обратными холодильниками (но не в открытой посуде). Работы проводить вдали от открытого огня. Диэтиловый эфир нагревают только с помощью горячей воды, предварительно нагретой вдали от рабочего места;
- некоторые органические вещества (эфиры, тетрагидрофуран, диоксан) при хранении на воздухе образуют пероксиды, поэтому перегонять их досуха нельзя. Проверить наличие пероксидов можно с помощью раствора иодида калия, подкисленного разбавленной соляной кислотой (окрашивание эфирного слоя в бурый цвет свидетельствует о наличии пероксидов);
- при воспламенении горючих веществ немедленно принимать меры к тушению огня (накрыть асбестовой сеткой, чашкой или засыпать песком). В случае большого очага пожара пользоваться огнетушителем;
- в конце работы убрать свое рабочее место и привести в полный порядок лабораторную посуду общего пользования. Качество уборки рабочих мест проверяет дежурный по группе, который уходит из лаборатории последним.
Правила безопасности при возникновении пожара
Следует тотчас же выключить вентиляцию, газ и все нагревательные приборы, удалить с участка загорания все горючие вещества.
При загорании электрических проводов немедленно выключить ток и тушить горящие провода песком или сухими огнетушителями, известив одновременно дежурного электрика.
Для тушения ЛВЖ используют противопожарные одеяла, песок, порошковые составы, пенные и углекислотные огнетушители.
При загорании одежды на человеке нужно немедленно закутать его в огнестойкую накидку, одеяло. Пострадавший не должен метаться и бегать.
Пожары, вызванные возгоранием щелочных металлов нельзя тушить ни водой, ни углекислотными огнетушителями. Применяется сухой песок.
Первая помощь при несчастных случаях
При ранении стеклом необходимо убедиться, что в ранке не осталось стекла, если в ранку попал кусочек стекла, надо прежде всего удалить его пинцетом. Затем (при небольшом ранении) протереть ранку ваткой, смоченной спиртом, смазать йодом и наложить повязку. Если кровотечение сразу не прекращается, к ране надо приложить кусочек ваты, смоченной 10%-ным раствором хлорида железа.
При сильном кровотечении, связанным с ранением более крупных кровеносных сосудов, надо временно перетянуть руку эластичным жгутом. Как только кровотечение остановится, жгут надо немедленно снять.
При термических ожогах, чтобы предупредить образование пузырей, нужно сразу же смочить обожженные места 5%-ным раствором танина в 40%-ном этиловом спирте. Лучше наложить небольшой компресс из ваты или марли, смоченной этим раствором.
При ожогах кислотами следует немедленно и тщательно промыть обожженный участок водой, а затем 2%-ным раствором питьевой соды.
При ожогах щелочами следует немедленно и тщательно промыть обожженный участок водой, а затем 2%-ным раствором борной кислоты.
При ожогах бромом следует смачивать пораженное место 1%-ным раствором карбоната натрия (пока не исчезнет бурая окраска от брома), а затем наложить компресс из ваты или марли, смоченной 5%-ным раствором мочевины. Бром можно также смыть спиртом и смазать пораженное место мазью от ожогов.
При ожогах фенолом следует промыть пораженный участок водой и наложить компресс из ваты или марли, смоченной глицерином.
При загрязнении помещения ртутью из разбитого термометра необходимо провести демеркуризацию, т.е механическую очистку от шариков ртути и химическую обработку кашицей хлорида железа (III), мыльным раствором и чистой водой.
При острых отравлениях чрезвычайно важно оказать неотложную помощь, используя следующие основные принципы:
- вывести (или вынести) пострадавшего из зоны отравления на свежий воздух, удалить остатки яда с кожи и одежды, слизистых оболочек, снять одежду;
- восстановить нарушенные функции организма (искусственное дыхание, массаж сердца);
- попытаться вывести яд из организма (промывание желудка, рвотные средства, адсорбенты);
- применить соответствующее противоядие и медикаменты.
МЕТОДЫ ВЫДЕЛЕНИЯ, ОЧИСТКИ И ИДЕНТИФИКАЦИИ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Для установления строения органического соединения т.е. его идентификации его необходимо получить в чистом виде. Выделение и очистка органических соединений осуществляются различными методами, наиболее употребимыми среди которых являются кристаллизация (перекристаллизация), возгонка сублимация, фильтрование, центрифугирование, различные виды перегонки, экстракция, хроматографические методы.
Перекристаллизация и дробная кристаллизация применяются для очистки твердых веществ. Кристаллизация включает растворение смеси при высокой температуре в растворителе или смеси растворителей. При охлаждении выкристаллизовывается тот компонент (или компоненты) смеси, который наименее растворим в используемом растворителе или смеси растворителей при низкой температуре.
Возгонка( сублимация )используется в случае твердых веществ, которые не плавятся, а переходят непосредственно в пар, а при охлаждении кристаллизуются.
Перегонка применяется для очистки жидкостей и заключается в постепенном переходе жидкой смеси веществ в газовую фазу с последующей конденсацией паров. Перегонку можно проводить при нормальном или пониженном давлении (вакуум-перегонка). При выделении или очистке нерастворимых или труднорастворимых в воде соединений прибегают к перегонке с водяным паром. С помощью перегонки можно отделять друг от друга компоненты смеси, достаточно различающиеся по температурам кипения. Если при перегонке нет фракций, говорят о простой перегонке. Если же наблюдаются отдельные фракции, перегоняющиеся в определенных температурных интервалах, перегонка называется дробной (фракционной).
Экстракцию проводят, действуя растворителем на размельченный твердый материал. Растворившийся компонент выделяют с помощью выпаривания. Экстракцию жидких веществ осуществляют, используя растворитель, не смешивающийся с экстрагируемой жидкостью.
Хроматографические методы включают, прежде всего, адсорбционную колоночную хроматографию, впервые используемую Цветом в 1903г. для разделения растительных красителей.
При хроматографировании имеются так называемые стационарная фаза (растворитель или адсорбент) и подвижная фаза (растворитель, элюент или газ-носитель), между которыми происходит распределение исследуемой смеси, вследствие различной растворимости или адсорбционной способности. По физическим принципам хроматографические методы делятся на распределительные (разделение смеси между двумя растворителями), адсорбционные (разделение между растворителем и адсорбентом), вытеснительные (вытеснение вещества, захваченного адсорбентом, другим веществом). На химическом принципе основана афинная хроматография, используемая для выделения сложных биохимических соединений. На практике часто используют совместно разные методы.
По используемой методике различают колоночную, хроматографию на бумаге, тонкослойную, газовую, жидкостную, ионообменную на молекулярных ситах или на гелях (гель-фильтрация).
При этом в процессе очистки веществ часто используют сопутствующие лабораторные операции или процедуры как измельчение и перемешивание, нагревание и охлаждение, фильтрование и центрифугирование, высушивание, концентрирование и разбавление растворов.
Измельчение осуществляют путем дробления, размалывания или растирания. Небольшие количества вещества измельчают в ступках, причем фарфоровые и агатовые ступки предназначены только для растирания, а металлические и для раздробления. Для измельчения больших количеств веществ используются шаровые мельницы.
Перемешивание осуществляют с помощью мешалок различных форм, как стеклянных, так и проволочных. В лабораторной практике используются также магнитные мешалки.
Нагревание осуществляют с помощью различных нагревательных приборов.
Бани с соответствующими теплоносителями используются для равномерного нагрева в определенном интервале температур: водяная – для нагрева не выше 100оС. Масляная, заполняемая более высококипящим, чем вода, теплоносителем, позволяет осуществлять нагрев в интервале температур 100-300оС, песчаная баня – еще более сильный нагрев.
Термостаты предназначены для поддержания строго определенной температуры. Бывают воздушные и жидкостные.
Охлаждение используется для снижения скорости реакции, инициирования кристаллизации, а также в других случаях. Простейший способ охлаждения состоит в помещении сосуда с охлаждаемым веществом в баню с холодной водой или льдом. Для достижения температур ниже 0оС используют охлаждающие смеси, состоящие из льда и неорганических солей. Глубокое охлаждение (от -70оС до -80оС) достигается с помощью твердого диоксида углерода (сухого льда). Для получения очень низкой температуры (до -180оС) охлаждение проводят сжиженными газами (жидким воздухом или азотом). В последних двух случаях используют сосуды Дьюара (сосуды с двойными стенками, из внутреннего пространства которых откачан воздух, аналогами их являются внутренние сосуды бытовых термосов).
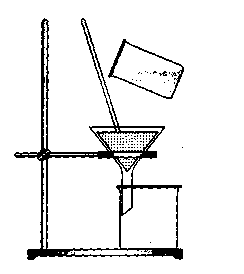
Фильтрование позволяет отделить суспендированный в жидкости осадок путем пропускания жидкости с осадком через фильтрующий материал.
Фильтрующие материалы: фильтровальная бумага, стеклянные тигли с пористым стеклянным дном или стеклянные воронки с впаянными в них пористыми пластинками.
Виды фильтрования: простое, фильтрование в вакууме, фильтрование с помощью ампул и баллончиков (при работе с микроколичествами веществ), горячее фильтрование (рис. 1-4)