
Polnyj_kurs_lekcij
.pdf
biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
211 |
|
|
|
УТИЛИЗАЦИЯ ЭТАНОЛА
Метаболизм поступающего этанола в организме происходит в печени двумя путями. Первый путь заключается в окислении спирта по алкогольдегидрогеназному пути до уксусной кислоты, которая в виде ацетил-S-КоА поступает в ЦТК. Через этот путь проходит от 70% до 90% всего этанола.
Оставшаяся часть окисляется в эндоплазматическом ретикулуме (микросомах) алкогольоксидазой. При регулярном поступлении этанола доля микросомального окисления возрастает, количество молекул алкогольоксидазы увеличивается.
Так как избыток "алкогольного" ацетил-S-КоА ингибирует пируватдегидрогеназу и при утилизации этанола образуется большое количество НАДН, то в цитозоле гепатоцитов активируется реакция превращения пирувата в лактат. Это приводит к гипогликемии, поскольку пировиноградная кислота является субстратом глюконеогенеза. Свободное проникновение молочной кислоты в кровь обуславливает лактатацидемию.
Если запасы гликогена в печени изначально невелики (голодание, недоедание, астеническое телосложение) или израсходованы (после физической работы), то при приеме алкоголя натощак гипогликемия наступает быстрее и может быть причиной потери сознания. К этому стоит добавить сильный диуретический эффект этанола, ведущий к быстрому обезвоживанию организма и снижению кровоснабжения головного мозга со всеми вытекающими последствиями.
СПИРТОВОЕ БРОЖЕНИЕ
Образование этилового спирта из глюкозы происходит в анаэробных условиях в дрожжах и некоторых видах плесневых грибков. Суммарное уравнение реакции:
C6H12О6 → 2 CО2 + 2 С2Н5ОН + 2 АТФ
До стадии образования пирувата реакции спиртового брожения совпадают с реакциями гликолиза. Отличия заключаются только в дальнейшем превращении пировиноградной кислоты.
Цель этих превращений у указанных организмов – удалить пируват из клетки и окислить НАДН, который образовался в 6-й реакции.
Строение и обмен углеводов |
212 |
|
|
|
|
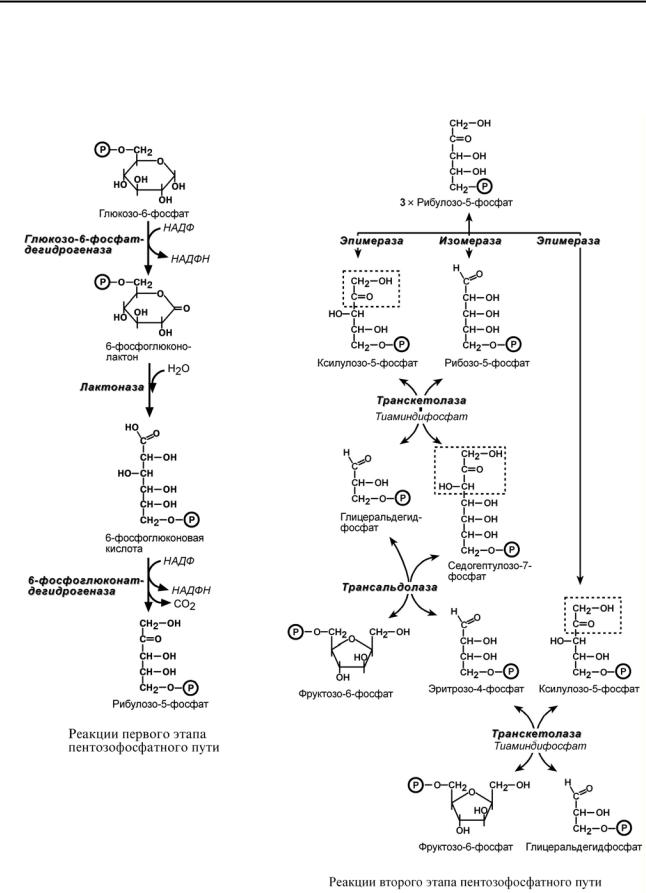
ПЕНТОЗОФОСФАТНЫЙ ПУТЬ ОКИСЛЕНИЯ ГЛЮКОЗЫ
Наиболее активно реакции пентозофосфатного пути (ПФП) идут в цитозоле клеток печени, жировой ткани, эритроцитах, коре надпочечников, молочной железе при лактации, в гораздо меньшей степени в скелетных мышцах. Этот путь окисления глюкозы не связан с образованием энергии, а обеспечивает анаболизм клеток. В связи с этим у новорожденных и детей первых лет жизни его активность довольно высока.

biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
213 |
|
|
|
Пентозофосфатный путь включает два этапа – окислительный и неокислительный.
На первом, окислительном, этапе глюкозо-6-фосфат в трех реакциях превращается в рибулозо-5-фосфат, реакции сопровождаются восстановлением двух молекул НАДФ до НАДФН.
На этом этапе происходит регуляция процесса: инсулин повышает активность глюко-
зо-6-фосфат-дегидрогеназы и фосфоглюконат-дегидрогеназы.
Второй этап – этап структурных перестроек, благодаря которым пентозы способны возвращаться в фонд гексоз. В этих реакциях рибулозо-5-фосфат изомеризуется до рибозо- 5-фосфата и ксилулозо-5-фосфата. Далее под влиянием ферментов транскетолазы и трансальдолазы происходят структурные перестройки с образованием других моносахаридов. При реализации всех реакций второго этапа пентозы превращаются во фруктозо-6-фосфат и глицеральдегидфосфат. Из глицеральдегид-3-фосфата при необходимости могут образоваться гексозы.
Значение пентозофосфатного пути
Значение первого этапа пентозофосфатного пути заключается в синтезе НАДФН и ри- бозо-5-фосфата.
Образованный НАДФН используется:
o для синтеза жирных кислот,
o холестерола и других стероидов,
o для синтеза глутаминовой кислоты из α-кетоглутаровой кислоты (реакция восстановительного аминирования),
o для синтеза дезоксирибонуклеотидов,
o для систем защиты клетки от свободно-радикального окисления (антиоксидантная защита).
Рибозо-5-фосфат абсолютно не-
обходим для синтеза пуриновых и пиримидиновых нуклеотидов и нуклеиновых кислот.
При определенных условиях клетка может подключать второй неокислительный этап. Благодаря этому рибозо-5-фосфат
не будет накапливаться и его углероды перейдут в состав фруктозо-6-фосфата (например, в эритроците) и уйдут в гликолиз. Либо глицеральдегид-3-фосфат восстановится до глицерол- 3-фосфата и будет использован для синтеза триацилглицеролов.
Нарушения пентозофосфатного пути
Генетическая недостаточность глюкозо-6-фосфат-дегидрогеназы отмечается примерно с частотой 1:60, то есть на Земле имеется около 100 млн. человек с этим заболеванием, которое, к счастью, не всегда проявляется. Следствием ферментного дефекта является снижение синтеза НАДФН в клетке. Особенно существенно это влияет на эритроциты, в которых окислительный этап пентозофосфатного цикла является единственным источником НАДФН. Из разнообразных функций НАДФН в данном случае имеет значение одна – участие в работе антиоксидантной системы,
При употреблении некоторых лекарственных препаратов (сульфаниламиды (стрептоцид, сульфацил-Na, норсульфазол), парацетамол, аспирин, примахин, метиленовый синий) в клетках активируются процессы свободнорадикального окисления. Здоровая клетка, и эритроцит в том числе, довольно легко справляются с дополнительной нагрузкой. При недоста-

Строение и обмен углеводов |
214 |
|
|
точности глюкозо-6-фосфат-дегидрогеназы активность антиоксидантных систем ослабевает и перекись водорода накапливается в эритроците, усиливается повреждение его мембран и гемолиз до 20% всех эритроцитов.
РЕГУЛЯЦИЯ КОНЦЕНТРАЦИИ ГЛЮКОЗЫ В КРОВИ
Нервная регуляция концентрации глюкозы в крови выражается в положительном влиянии n.vagus на секрецию инсулина и тормозящем влиянии на этот процесс симпатической иннервации. Кроме этого, выделение адреналина в кровь подвержено симпатическим влияниям.
Основными факторами гормональной регуляции являются глюкагон, адреналин,
глюкокортикоиды, соматотропный гормон с одной стороны, и инсулин с другой. Инсу-
лин является единственным гормоном организма, действие которого нацелено на снижение уровня глюкозы крови. При его влиянии глюкозу поглощают мышцы и жировая ткань. Все остальные гормоны увеличивают гликемию, влияя на печень.
Снижение глюкозы крови |
Повышение глюкозы крови |
Инсулин |
Адреналин |
Повышение ГлюТ 4-зависимого транспорта |
Активация гликогенолиза в печени |
глюкозы в клетки |
Глюкагон |
Усиление синтеза гликогена |
Активация гликогенолиза в печени |
Активация ПФП |
Стимуляция глюконеогенеза |
Активация гликолиза и ЦТК |
Глюкокортикоиды |
|
Усиление глюконеогенеза |
|
Уменьшение проницаемости мембран для |
|
глюкозы |
Снижение концентрации глюкозы крови инсулином достигается следующими путями:
o |
переход глюкозы в клетки – активация белков-транспортеров ГлюТ 4 на цитоплаз- |
|
матической мембране, |
o |
вовлечение глюкозы в гликолиз – повышение синтеза глюкокиназы – фермента, |
|
получившего название "ловушка для глюкозы", стимуляция синтеза других ключевых |
|
ферментов гликолиза – фосфофруктокиназы, пируваткиназы, |
oувеличение синтеза гликогена – активация гликогенсинтазы и стимуляция ее синтеза, что облегчает превращение излишков глюкозы в гликоген,
oактивация пентозофосфатного пути – индукция синтеза глюкозо-6-фосфат-
дегидрогеназы и 6-фосфоглюконатдегидрогеназы,
o усиление липогенеза – вовлечение глюкозы в синтез триацилглицеролов (см "Липиды", "Синтез триацилглицеролов").
Многие ткани совершенно нечувствительны к действию инсулина, их называют инсулиннезависимыми. К ним относятся нервная ткань, стекловидное тело, хрусталик, сетчатка, клубочковые клетки почек, эндотелиоциты, семенники и эритроциты.
Глюкагон повышает содержание глюкозы крови:
o увеличивая мобилизацию гликогена через активацию гликогенфосфорилазы,
oстимулируя глюконеогенез – повышение работы ферментов пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы.
Адреналин вызывает гипергликемию:
o активируя мобилизацию гликогена – стимуляция гликогенфосфорилазы,
Глюкокортикоиды повышают глюкозу крови o за счет подавления перехода глюкозы в клетку,
oстимулируя глюконеогенез – увеличивают синтез ферментов пируваткарбоксилазы, фосфоенолпируват-карбоксикиназы, фруктозо-1,6-дифосфатазы.

biokhimija.ru Тимин О.А. Лекции по биологической химии 215
ГИПЕРГЛИКЕМИЧЕСКИЕ СОСТОЯНИЯ
Гипергликемическим является состояние, при котором концентрация глюкозы в крови более 6 ммоль/л.
По происхождению выделяют две группы таких состояний: 1. Физиологические
o алиментарные – связаны с приемом пищи и продолжаются в норме не более 2 часов после еды.
o нейрогенные – нервное напряжение, стимулирующее секрецию адреналина и мобилизацию гликогена в печени,
o гипергликемия беременных – связана с относительной недостаточностью инсулина при увеличении массы тела и потребностью плода в глюкозе.
2. Патологические
oпри заболеваниях гипофиза, коры и мозгового слоя надпочечников, щитовидной железы, поджелудочной железы, при органических поражениях ЦНС.
САХАРНЫЙ ДИАБЕТ
Сахарный диабет (СД) – полиэтиологическое заболевание, связанное: o со снижением количества β-клеток островков Лангерганса,
o с нарушениями на уровне синтеза инсулина,
o с мутациями, приводящими к молекулярному дефекту гормона,
o со снижением числа рецепторов к инсулину и их аффинности в клетках-мишенях, o с нарушениями внутриклеточной передачи гормонального сигнала.
Выделяют два основных типа сахарного диабета:
1.Инсулинзависимый сахарный диабет (ИЗСД, диабет I типа) – диабет детей и подростков (ювенильный), его доля составляет около 20% от всех случаев СД.
2.Инсулиннезависимый сахарный диабет (ИНЗСД, диабет II типа) – диабет взрослых, его доля – около 80%.
Причины
Развитие ИЗСД обусловлено недостаточным синтезом инсулина в β-клетках островков Лангерганса поджелудочной железы. Среди причин этого в настоящее время на первый план выдвигаются аутоиммунные поражения и инфицирование β-тропными вирусами (вирусы Коксаки, Эпштейна-Бар, эпидемического паротита).

Строение и обмен углеводов |
216 |
|
|
Для ИНЗСД ведущей причи-
ной является инсулинорезистент-
ность из-за снижения чувствительности клеток-мишеней к гормону в результате функциональных или структурных нарушений инсулиновых рецепторов, а также из-за вероятных нарушений механизмов передачи и реализации сигнала.
Например, эти нарушения возникают при увеличении диаметра жировых клеток, из-за повышенной вязкости мембран и сниженной подвижности рецепторов и, соответственно, возрастания времени до "встречи" гормона с рецептором.
Сравнительная характеристика типов сахарного диабета
|
Инсулинзависимый |
Инсулиннезависимый |
|
|
сахарный диабет |
сахарный диабет |
|
Возраст |
Дети, подростки |
Средний, пожилой |
|
Начало |
Острое (несколько дней) |
Постепенное (годы) |
|
Внешний вид (до лечения) |
Худощавое |
У 80% ожирение |
|
Снижение массы тела (до лечения) |
Обычно есть |
Не характерно |
|
Концентрация инсулина в крови |
Снижена в 2-10 раз |
В норме или повышена |
|
Концентрация С-пептида |
Резко снижена |
В норме или повышена |
|
или отсутствует |
|||
|
|
||
Семейный анамнез |
Отягощен редко |
Часто отягощен |
|
Зависимость от инсулина |
Полная |
Только у 20% |
|
Склонность к кетоацидозу |
Есть |
Нет |
|
|
|
|
Осложнения сахарного диабета
Быстрые последствия
Быстрые последствия, как правило, характерны для ИЗСД.
1.Высокая гипергликемия – так как практически отсутствует влияние эндогенного инсулина и превалирует влияние глюкагона, адреналина, кортизола, гормона роста.
2.Глюкозурия – в результате превышения почечного порога для глюкозы, т.е. концентрации глюкозы в крови при которой она появляется в моче (около 10,0 ммоль/л). В норме в моче уровень глюкозы 0,8 ммоль/л и до 2,78 ммоль/сут, в других единицах около 0,5 г/сут, при СД количество теряемой глюкозы составляет до 100 г/сут и более.
3.Преобладание катаболизма белков над анаболизмом ведет к накоплению продуктов азотистого обмена, в первую очередь мочевины и ее повышенному выведению. Углеродный скелет аминокислот уходит в глюконеогенез.

biokhimija.ru |
Тимин О.А. Лекции по биологической химии |
217 |
|
|
|
4.Глюкоза и мочевина осмотически удерживают воду в просвете почечного канальца и возникает полиурия. Объем мочи возрастает в 2-3 раза. Активируется центр жажды и начи-
нается полидипсия.
5.Повышенный распад ТАГ в жировой ткани и печени обуславливает аномально высокое окисление жирных кислот и накопление их недоокисленных продуктов – кетоновых тел. Это приводит к кетонемии, кетонурии и кетоацидозу. При сахарном диабете концентрация
кетоновых тел возрастает в 100-200 раз и достигает 350 мг% (норма 2 мг% или
0,1-0,6 ммоль/л).
6.При полиурии с мочой теряются ионы натрия и калия, и ионы бикарбоната, что усугубляет ацидоз.
7.В результате п.п.4,5,6 возникает дегидратация (в тяжелых случаях до 5 л) организма, которая заключается в падении объема крови, приводит к обезвоживанию клеток и их сморщиванию (дряблая кожа, запавшие глаза, мягкие глазные яблоки, сухость слизистых),

Строение и обмен углеводов |
218 |
|
|
уменьшению артериального давления. Ацидоз вызывает одышку (дыхание Kussmaul, быстрое и глубокое) и дополнительную дегидратацию.
8. Дегидратация неминуемо приводит к недостаточности кровообращения в тканях – активируется анаэробный гликолиз, накапливается лактат и в дополнение к кетоацидозу воз-
никает лактоацидоз.
10.Закисление среды вызывает изменение взаимодействия инсулина с рецепторами, клетки становятся нечувствительными к инсулину – инсулинорезистентность.
11.Ацидоз крови уменьшает концентрацию 2,3-дифосфоглицерата в эритроцитах. Это, повышая сродство гемоглобина к кислороду, создает тканевую гипоксию и усугубляет лактоацидоз.
Отдаленные последствия
Характерны для обоих типов СД.
Гипергликемия резко повышает потребление глюкозы инсулиннезависимыми тканями (в частности, клетки артериальных стенок, эндотелий, клетки Шванна, эритроциты, хрусталик и сетчатка глаза, семенники и гломерулярные клетки почек), в них вынужденно активируются особые пути метаболизма глюкозы. Интенсивность последних определяется только доступностью глюкозы:
1. Превращение глюкозы в сорбитол.
Сорбитол плохо проникает через клеточные мембраны, его накопление в цитозоле приводит к осмотическому набуханию клеток и нарушению их функций. Например, возникновение катаракты хрусталика, развитие нейропатий (нарушение осязания) из-за нарушений в клетках Шванна.
2. Неферментативное гликозилирование различных белков, изменение их свойств и активация их синтеза за счет избытка энергии:
oувеличивается синтез гликопротеинов
базальной мембраны почечных клу-
бочков, что приводит к окклюзии ка-
пилляров и нарушению фильтрации,
oувеличивается синтез гликопротеинов в стекловидном теле и сетчатке гла-
за, что вызывает отек сетчатки и кровоизлияния,
oгликозилированные белки хрусталика объединяются в крупные агрегаты, рассеивающие свет, что вызывает помутнение хрусталика и катаракту,
oгликозилирование гемоглобина в эритроцитах, образование гликозилированного гемоглобина HbA1C,
o гликозилирование белков свертывающей системы, что увеличивает вязкость крови,
oгликозилирование белков ЛПНП уменьшает их связывание с рецепторами и повышает концентрацию ХС в крови, что вызывает макроангиопатии и развитие атеросклероза сосудов мозга, сердца, почек, конечностей.
oгликозилирование белков ЛПВП, что усиливает их сродство к рецепторам и быструю элиминацию из кровотока.
Из-за трех последних нарушений возникают макроангиопатии, развивается атеросклероз сосудов мозга, сердца, почек, конечностей. Это характерно в основном для ИНЗСД.

СТРОЕНИЕ И ОБМЕН ЛИПИДОВ
КЛАССИФИКАЦИЯ ЛИПИДОВ
Классификация липидов сложна, так как в класс липидов входят вещества весьма разнообразные по своему строению. Их объединяет только одно свойство – гидрофобность. По отношению к гидролизу в щелочной среде все липиды подразделяют на две большие группы: омыляемые и неомыляемые. Среди неомыляемых определена большая группа стероидов, в состав которой входят холестерол и его производные: стероидные гормоны, стероидные витамины, желчные кислоты. Среди омыляемых липидов существуют простые липиды, т.е. состоящие только из спирта и жирных кислот (воска, триацилглицеролы, эфиры холестерола), и сложные липиды, включающие, кроме спирта и жирных кислот, вещества иного строения (фосфолипиды, гликолипиды, сфинголипиды).
ФУНКЦИИ ЛИПИДОВ
Функции липидов существенно зависят от их вида:
1.Резервно-энергетическая функция – триацилглицеролы подкожного жира являются основным энергетическим резервом организма при голодании. В адипоцитах жиры могут составлять 65-85% веса. Для поперечно-полосатой мускулатуры, печени и почек они являются основным источником энергии.
2.Структурная функция – мембраны клеток состоят из фосфолипидов, обязательным компонентом являются гликолипиды и холестерол. Основным компонентом сурфактанта легких является фосфатидилхолин.
3.Сигнальная функция – гликолипиды выполняют рецепторные функции и задачи взаимодействия с другими клетками. Фосфатидилинозитол непосредственно принимает участие в передаче гормональных сигналов в клетку. Производные жирных кислот – эйкозаноиды – являются "местными гормонами", обеспечивая регуляцию функций клеток.
Т.к. активность мембранных ферментов зависит от состояния и текучести мембран, то
жирнокислотный состав и наличие определенных видов фосфолипидов, количество холестерола влияет на активность мембранных липидзависимых ферментов (например, аденилатциклаза, Nа+,К+-АТФаза, цитохромоксидаза).
4.Защитная функция – подкожный жир является хорошим термоизолирующим средством, наряду с брыжеечным жиром он обеспечивает механическую защиту внутренних органов. Фосфолипиды играют определенную роль в активации свертывающей системы крови.

Строение и обмен липидов |
220 |
|
|
