
- •Гидролиз солей
- •1 Материалы, реактивы, оборудование:
- •2 Основные теоретические положения
- •3 Методика эксперимента и порядок выполнения работы
- •2.3 Влияние температуры на степень гидролиза соли
- •Опыт 3. Смещение равновесия гидролиза
- •Физико-химические свойства белков
- •2 Общие положения
- •2.1 Определение изоэлектрической точки белков
- •2.2 Высаливание белков сульфатом аммония
- •2.3 Денатурация белков при нагревании
- •2.4 Разделение и очистка белков методом диализа
- •Определение показателей качества жиров
- •1 Материалы, реактивы и оборудование
- •2 Общие положения
- •2.1 Определение кислотного числа
- •2.2 Определение йодного числа жиров
- •2.3 Определение перекисного числа
2.2 Определение йодного числа жиров
Йодное число выражается количеством граммов йода, необходимого для насыщения ненасыщенных жирных кислот, содержащихся в 100 г жира.
Йодное число является одним из наиболее важных показателей для масел (жиров). Одно позволяет судить о степени насыщенности масла (жира), о склонности его к высыханию, прогорканию и другим изменениям, происходящим при хранении и переработке пищевых и технических масел. Чем больше содержится в жире ненасыщенных жирных кислот, тем выше йодное число. Уменьшение йодного числа в процессе хранения масла является показателем его порчи.
Растительные жиры (масла), имеющие в основном жидкую консистенцию, содержат, главным образом, непредельные кислоты.
Жиры животного происхождения – в большинстве своем твердые, так как в их состав входят преимущественно триглицериды предельных жирных кислот.
Принцип метода основан на свойстве ненасыщенных жирных кислот присоединять галогены по месту двойных связей.
Взаимодействие ненасыщенных жирных кислот с йодом протекает по уравнению
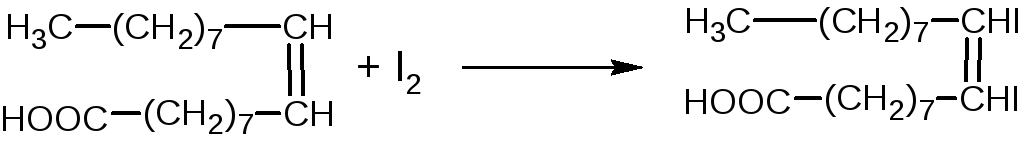
I2 + 2Na2S2O3 = 2NaI + Na2S4O6
Непрореагировавший йод оттитровывают 0,1 н. раствором тиосульфата натрия.
Техника определения: сухую коническую колбу со шлифом емкостью 250 см3 взвешивают на аналитических весах, помещают туда около 0,5 г масла и снова взвешивают колбу. По разности масс определяют величину навески масла. В колбу добавляют 25 см3 этилового спирта для растворения навески. Если масло плохо растворяется, колбу нагревают на водяной бане. Во вторую колбу приливают 25 см3 спирта без жира «слепой опыт». В обе колбы (опыт и контроль) прибавляют по 12,5 см3 0,2 н. спиртового раствора йода, добавляют по 100 см3 дистиллированной воды и закрывают пробкой. Через 5 минут содержимое колб оттитровывают 0,1 н. раствором тиосульфата сначала до появления слабо-желтого окрашивания, а потом, прибавив 1 см3 раствора крахмала, титруют до исчезновения синего окрашивания.
Обработка результатов:
При расчетах учитывают, что 1 см3 0,1 н. тиосульфата натрия соответствует 1 см3 0,1 н. раствора йода. Йодное число (ИЧ) вычисляют по формуле
![]() ,
,
где Vк – количество 0,1 н. раствора тиосульфата, пошедшее на титрование контрольного опыта, см3;
Vо – количество 0,1 н. раствора тиосульфата, пошедшее на титрование опытного образца, см3;
k – поправочный коэффициент к титру приблизительно 0,1 н. раствора тиосульфата;
0,0127 – титр раствора тиосульфата по йоду;
m – навеска масла, г.
2.3 Определение перекисного числа
Указанное число показывает суммарное количество перекисей, образовавшихся при окислении как ненасыщенных, так и насыщенных жирных кислот. Образование гидроперекисей в случае насыщенных жирных кислот происходит с меньшей скоростью в сравнении с ненасыщенными. Однако и в этом случае образуется свободный перекисный радикал:

При взаимодействии с другими жирными кислотами свободный перекисный радикал стабилизируется, «отрывая» от них атом водорода:

Образовавшийся новый радикал взаимодействует с кислородом по прежней схеме:

Свободный перекисный радикал может превратиться в альдегиды путем его изомеризации с образованием нестойкой диалкилперекиси:

Образующиеся гидроперекиси могут также активно превращаться в кетоны:

Доказано также, что гидроперекиси могут взаимодействовать с двойными связями ненасыщенных жирных кислот с образованием эпоксидов:

Именно набор всех вышеуказанных соединений с различной молекулярной массой и обуславливает наличие в хранящемся молочном жире таких пороков вкуса как «салистый», «олеистый», «рыбный», «грибной» и т.д.
Сильнейшими активаторами окисления являются ионы металла.
Принцип метода: количественное определение перекисей в масле основано на реакции выделения йода перекисями из йодата калия в кислой среде (пример циклической перекиси):

Выделившийся йод оттитровывают раствором тиосульфата.
Техника определения: в конической колбе или склянке с притертой пробкой емкостью 200 см3 отвешивают на аналитических весах около 2-3 г масла. Навеску растворяют в 20 см3 смеси ледяной уксусной кислоты и хлороформа (2:1), прибавляют 5 см3 насыщенного раствора йодистого калия, сосуд закрывают пробкой и ставят в темное место на 10 минут, после чего добавляют 50 см3 дистиллированной воды и оттитровывают выделившийся йод 0,002 н. раствором тиосульфата (индикатор-крахмал). Одновременно проводят также контрольное определение (без масла).
Обработка результатов:
Перекисное число (ПЧ) (количество граммов йода, выделенного перекисями, содержащимися в масле) рассчитывают по формуле
![]() ,
,
где Vк – количество 0,002 н. раствора тиосульфата, израсходованное при титровании контрольного образца, см3;
V0 – количество 0,002 н. раствора тиосульфата, израсходованное при титровании опытного образца, см3;
k – поправочный коэффициент раствора тиосульфата;
0,0002538 – титр 0,002 н. раствора тиосульфата по йоду (1 см3 раствора соответствует 0,0002538 г йода);
m – навеска масла, г.
Таблица 1 – Показатели качества жира
|
Наименование жира |
Кислотное число |
Йодное число |
Перекисное число |
Стандартные показатели | ||
|
Кислотное число |
Йодное число |
Перекисное число | ||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ОБЩИЕ ВЫВОДЫ:
СПИСОК ИСПОЛЬЗУЕМОЙ ЛИТЕРАТУРЫ
1 Химия и биохимия липидов: Методические указания к выполнению лабораторных работ для студентов специальностей 1-49 01 01, 1-49 01 92, 1-91 01 01 /Могилевский государственный университет продовольствия; сост. А.Я. Гузиков, О.Н.Макасеева,Л.М.Ткаченко.–Могилев,2007.–41с.).
