
- •Гидролиз солей
- •1 Материалы, реактивы, оборудование:
- •2 Основные теоретические положения
- •3 Методика эксперимента и порядок выполнения работы
- •2.3 Влияние температуры на степень гидролиза соли
- •Опыт 3. Смещение равновесия гидролиза
- •Физико-химические свойства белков
- •2 Общие положения
- •2.1 Определение изоэлектрической точки белков
- •2.2 Высаливание белков сульфатом аммония
- •2.3 Денатурация белков при нагревании
- •2.4 Разделение и очистка белков методом диализа
- •Определение показателей качества жиров
- •1 Материалы, реактивы и оборудование
- •2 Общие положения
- •2.1 Определение кислотного числа
- •2.2 Определение йодного числа жиров
- •2.3 Определение перекисного числа
2.4 Разделение и очистка белков методом диализа
Диализом называется процесс разделения высокомолекулярных и низкомолекулярных веществ с помощью полупронецаемых мембран. Белковые молекулы, обладая большой молекулярной массой, не способны проникать через полупронецаемые перегородки (искусственные и естественные мембраны). При этом низкомолекулярные частицы (органические и неорганические) легко проходят через поры полупроницаемых мембран.
Диализ широко используется для очистки белков от низкомолекулярных примесей (соли, сахара и других), которые легко проходят через поры полупроницаемых мембран. Прибор, в котором проводят диализ, называется диализатором. Целлофановый или коллодиевый мешочек, опущенный в сосуд с водой, представляет простейший диализатор (рис.1). Белок, помещенный в мешочек, остается в нем, а низкомолекулярные вещества диффундируют через мембрану в воду.
Методом диализа можно разделить альбумины и глобулины. При переходе солей из белкового раствора в окружающую среду глобулины будут выпадать в осадок, т.к. они не растворимы в водной среде, а альбумины будут оставаться в растворе. Простейшим диализатором может служить целлофановый мешочек, опущенный в стакан с водой. Солевой раствор белка помещают в мешочек, при этом молекулы низкомолекулярных веществ (ионы соли) диффундируют через стенку мешочка, а крупные молекулы белка остаются внутри мешочка.
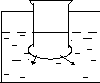
Белок +
(NН4)2SО4
2 NН4+ SО42-
Н2О
Рисунок 1Схема диализатора
Ход работы. 10–15 мл раствора яичного белка, содержащего альбумины, глобулины и сульфат аммония, помещают в целлофановый мешочек и погружают в стакан с дистиллированной водой так, чтобы уровень жидкости в мешочке совпадал с уровнем воды. Для ускорения диализа необходимо менять воду в сосуде. Через 1 час анализируют воду из стакана: в одной пробирке проводят биуретовую реакцию и убеждаются, что белки через мембрану не проходят; в другой пробирке проводят реакцию на ион SO42-, добавлением нескольких капель 10%-ного раствора ВаСI2для установления проникновения соли через стенку целлофанового мешочка. Через 2–3 часа отмечают появление осадка глобулинов внутри мешочка, который отфильтровывают. В фильтрате остаются белки альбуминовой фракции.
Глобулиновую природу белков осадка доказывают растворением его в растворах солей (10%-ный раствор хлористого аммония, хлористого натрия и др.) При разбавлении раствора водой вновь выпадает осадок.
Альбуминовую природу белков фильтрата подтверждают разбавлением водой с отсутствием осадка или полным насыщением сернокислым аммонием (выпадает осадок).
НАБЛЮДЕНИЯ И ВЫВОДЫ
СПИСОК ИСПОЛЬЗУЕМОЙ ЛИТЕРАТУРЫ
1 Белки. Методические указания к лабораторному практикуму по дисциплине «Биохимия» для студентов специальностей 49 01 01 «Технология хранения и переработки растительного сырья», 49 01 02 «Технология хранения и переработки животного сырья», 91 0101 «Производство продуктов и организация общественного питания». /Могилевский государственный университет продовольствия; сост.: О,Н. Макасеева, О.В. Дудинская, Л.М.Ткаченко.–Могилев.МГУП:2003.–37с.
Министерство образования Республики Беларусь
Учреждение образования
«Могилевский государственный университет продовольствия»
Кафедра химической технологии высокомолекулярных соединений
