- •Вопросы к экзамену по дисциплине «Аналитическая химия.
- •2. Методы аналитической химии. Классификации методов определения. На основании предложенной классификации представьте методы определения железа, каковы их преимущества и недостатки.
- •4. Абсолютные и относительные методы анализа. Процесс градуировки. Стандартные образцы.
- •5. Виды погрешностей и ошибок. Систематические ошибки, их классификация. Устранение систематических ошибок. Рассмотрите на конкретном примере:
- •1) Кислотно-основного титриметрического определения уксусной кислоты в уксусной эссенции;
- •2) Гравиметрического определения хроматов в электролите для хромирования.
- •13. Загрязнение осадков. Явление соосаждения, его роль и причины. Адсорбция. Окклюзия. Правила Панета-Фаянса-Гана. Изоморфное соосаждение. Правило Хлопина. На конкретных примерах.
- •14. Методы отгонки. Вещества, определяемые методом отгонки. Прямые и косвенные методы отгонки. Поглотители для прямого метода отгонки. Методы определения карбонатов в карбонатных породах.
- •23. Титрование в неводных средах. Его необходимость, преимущества и недостатки. Кривая титрования смеси хлороводородной и бензойной кислот в этиловом спирте.
- •31.Броматометрия: стандартные вещества и индикаторы. Броматометрическое определение сурьмы, фенола. КТхлороводородного раствора хлорида сурьмы (III).
- •32 Йодометричопред меди (II). Окислительно-восстановительная способность пары i2/2i-. Kривая титрования йода Na2s203. Факторы, влияющие на ход кт. Способы установления ктт в йодометрии.
- •33. Йодометрическое определение нитрит-ионов, глюкозы, сульфитов. Основные реакции метода йодометрии. Приготовление и стандартизация рабочих растворов.
- •3.Атомно-абсорбционный метод.
- •38. Сравните гравиметрические и титриметрические методы определения меди. Принципы методов, их преимущества и недостатки, возможности усовершенствования.
- •39. Сравните гравиметрические и титриметрические методы определения кальция. Принципы методов, их преимущества и недостатки, возможности усовершенствования.
- •40. Сравните гравиметрические и титриметрические методы определения алюминия. Принципы методов, их преимущества и недостатки, возможности усовершенствования.
2. Методы аналитической химии. Классификации методов определения. На основании предложенной классификации представьте методы определения железа, каковы их преимущества и недостатки.
Методы аналитической химии разделяют в соответствии с операциями, использованными в хим. анализе
А) методы отбора проб
б) методы разложения проб
в) методы разделения компонентов
г) методы обнаружения
д) метод определения
Практически все методы определения основаны на зависимости между составом вещества и его экстенсивными свойствами.
Экстенсивные свойства:
Масса осадка
ОВ емкость
Объем титранта
Сила тока
Интенсивность спектральной линии
Радиоактивность
Интенсивность окраски
Электропроводимость
При проведении количественного химического анализа сначала измеряют экстенсивные свойства, т.е. получают аналитический сигнал, далее по нему находят содержание определяемого компонента.
Метод анализа- достоверный универсальный теоретически обоснованный способ определения состава безотносительно к определенному компоненту и анализируемому объекту.
Когда говорят о методе анализа , то имеют в виду:
Принцип, положенный в основу анализа
Количественное выражение связи между составом и экстенсивными свойствами
Отработанные приёмы техники осуществления
Устройство для практической реализации
Способы обработки результатов
Классификация методов анализа
1)По характеру измеряемого свойства или по способу регистрации соответствующего сигнала: химические, физические, биологические.
2)в зависимости от способа использования реакции
X+R=P(опр. В-ва, реагент, продукт)
1)измеряют количество образовавшегося продукта (гравиметрия, фотометрия)
2)измеряют количество реагента израсходанного на реакцию с определяемым веществом (титриметрия)
3)фиксируются изменения происходящие с определяемым веществом
3. По типу химической реакции
А) основанные на кислотно-основных реакциях
Б) основанные на реакциях комплексообразования
В) основанные на окислительно-восстановительных реакциях
3. Метод анализа. Выбор метода анализа. Этапы анализа. Рассмотрите на примере дихроматометрического способа определения железа в рудах. Преимущества данного способа определения. Редокс-индикаторы, применяемые в дихроматометрии.
Метод анализа- достоверный универсальный теоретически обоснованный способ определения состава безотносительно к определенному компоненту и анализируемому объекту.
Критерии выбора метода:
1)концентрация вещества в растворе
2) количество пробы
3)количество образцов
4)качественный состав образца
Если концентрация велика- используют химические методы анализа; мала- физические
Чем меньше количество пробы, тем чаще используют физический анализ
Если анализ единичный, то используют химические методы, т.к. физические методы, в частности приборы, необходимо длительно калибровать. А так же необходимы стандартные образцы, по которым проводится калибровка. А вот для серийных анализов, физические методы удобнее.
5)содержание компонентов в образце
- основной: ω=5-100% (химические методы)
-побочный: ω=0,01-5% (химические и физико-химические методы)
-следовый: ω<0,01% (физико-химические, физические и биологические методы)
6)метрологические характеристики:
Правильность-качество химического
анализа, отображающее близость к нулю
систематической погрешности
Воспроизводимость- характеризует степень близости друг к другу единичный определений (рассеяние единичных результатов относительно среднего значения
Точность- собирательная характеристика метода или методики , включающая их правильность и воспроизводимость .
Чувствительность- величина, определяемая минимальным количеством вещества, которое можно обнаружить данным методом
7)быстрота
8)стоимость
Этапы анализа:
1. отбор пробы
Главный критерий- представительность- химический состав пробы должен отражать состав всего анализируемого объекта
Отдельные порции анализируемого объекта берутся в разных точках- первичная проба
Из первичной пробы путем сокращения получают лабораторную пробу 1-25 кг, которую делят на три части
-для предварительный анализов
-для анализа
-для возможных арбитражных анализов
2. Перевод пробы в требуемое агрегатное состояние
Перевод в раствор:
Вода
Минеральные кислоты: HCl,H2SO4,H3PO4,HNO3,H3BO3
Плавни : Na2CO3, NaOH, Na2O2, NH4Cl, K2S2O7, CaO, Na2B4O7
Переведение образца в раствор не должно сопровождаться потерей определяемого элемента, а так же загрязнением пробы.
3. Отделение мешающих компонентов или их маскирование, концентрирование
4. Перевод определяемого компонента в аналитическую активную форму
5. Проведение, измерение величины аналитического сигнала.
Определение содержания железа в рудах
Этапы определения :
1)подготовка пробы руды для титрования
2) титрование анализируемого раствора железа (II) раствором K2Cr2O7
3)расчет граммового и процентного содержания железа в руде
В основе определения железа (II) лежит реакция: 6Fe2++Cr2O72-+14H+→6Fe3++2Cr3++7H2O
В процессе титрования повышается концентрация ионов Fe3+ , следовательно , возрастает потенциал системы
Fe3+/Fe2+, что приводит к преждевременному изменению окраски индикатора. Поэтому в титруемый раствор добавляютH3PO4, которая связываетFe3+ в бесцветный комплекс и понижает потенциал системы.
Ход анализа:
Подготовка пробы руды для титрования.Точную навеску анализируемого материала (0,7-1г) помещают в жаростойкий стакан ёмкостью 300 мл, прибавляют 40 млHCl(1:4), закрывают часовым стеклом и растворяют при нагревании на песочной бане или на электроплитке с асбестом. Затем добавляют 2-5 мл азотной кислоты и продолжают нагревание. Растворение считается законченным, когда на дне стакана остается серовато-белый осадок, состоящий в основном из кремниевой кислоты. Выпаривают раствор досуха, остаток обрабатывают 10 мл концентрированнойHClи снова выпаривают раствор. Операцию выпаривания с концентрированнойHСlповторяют 2 раза, затем добавляют 4 мл концентрированнойHClи разбавляют горячей водой примерно до 50 мл. Раствор отфильтровывают через фильтр с белой лентой в мерную колбу ёмкостью 200 или 250 мл. Хорошо промывают фильтр горячей 0,05 моль/лHCl, охлаждают, разбавляют водой до метки и перемешивают.
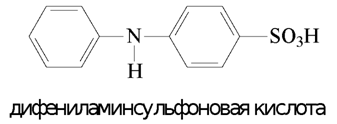
Титрование анализируемого раствора железа (II) раствором K2Cr2O7 .Аликвотную часть раствора 10,0 мл пипеткой переносят в коническую колбу, добавляют 5 мл концентрированнойHCl. Закрывают колбу маленькой воронкой, вносят в колбу 3-4 гранулы металлического цинка, нагревают на песчаной бане или электроплитке с асбестом до обесцвечивания раствора и растворения цинка. Охлаждают содержимое колбы под струёй воды, добавляют 3-4 мл серной кислоты, снова охлаждают , вводя 5 мл фосфорной кислоты, 15-20 мл воды, 2-4 капли раствора дифениламина и медленно титруют раствором дихромата калия до появления синей окраски раствора.
Расчет граммового и процентного содержания железа в руде. Титрование повторяют несколько раз. Из трех сходящихся результатов ( отличных не более чем на 0,1 мл) вычисляют среднее знаение объёма титранта. Расчет граммового содержании железа ведут по формуле:
mFe,г=C( K2Cr2O7)·
K2Cr2O7)· (K2Cr2O7)·K(K2Cr2O7)·Mэкв(Fe)
·P·10-3
(K2Cr2O7)·K(K2Cr2O7)·Mэкв(Fe)
·P·10-3
Расчет процентного содержании железа в руде ведут по формуле:
ωFe=
Преимущества дихроматометрии
K2Cr2O7легко получить химически чистым. Стандартный раствор готовят по точной навеске
Растворы K2Cr2O7устойчивы. Титр не изменяется в течении долгого времени независимо от температуры, действияO2илиCO2 ,воздуха и т.д.
Титрование дихроматом калия можно проводить в солянокислой среде, тогда как титрование перманганатом калия в присутствии HClневозможно из-за окисления хлорид-ионов
K2Cr2O7 труднее, чем перманганат калия восстанавливается органическими веществами, попадающими в дистиллированную или деионизированную воду
В отличие от более слабых окислителей , например йода, дихромат-ионы окисляют многие органические соединения
В ряде случаев титрование дихроматом можно проводить на холоде
Кроме титрования восстановителей K2Cr2O7 широко применяется для определения окислителей путем предварительного восстановления их солями железа(II) и последующего титрования избыткаFe2+ стандартным раствором дихромата калия
Редокс-индикаторы, применяемые в дихроматометрии.