
- •Государственное бюджетное образовательное учреждение высшего профессионального
- •Введение
- •Изучение студентами лечебного факультета модуля «Гигиена лечебно-профилактических организаций» формирует следующие компетенции:
- •План изучения темы.
- •I.Проверка исходного уровня знаний.
- •II. Ознакомление с основными понятиями и положениями темы.
- •Задача № 1
- •2. Что предусматривается при архитектурно – планировочном решении и оборудовании современных больниц?
- •3. Какие гигиенические требования предъявляются к планировке в эксплуатации лечебных учреждений?
- •4. Какие условия являются оптимальными при выборе участка для больницы?
- •7. В каких случаях децентрализованная система застройки считается наиболее рациональной?
- •План изучения темы:
- •I. Проверка исходного уровня знаний.
- •II.Ознакомление с основными положениями темы.
- •IV.Подведение итогов занятии.
- •V.Задание на следующее занятие. Основные положения темы:
- •1. Укажите структурные основные подразделения современной больницы:
- •План изучения темы.
- •I.Проверка исходного уровня знаний.
- •II. Ознакомление с основными понятиями и положениями темы.
- •9. В каком из перечисленных случаев размещение операционного блока больницы отвечает гигиеническим требованиям?
- •План изучения темы:
- •I. Проверка исходного уровня знаний.
- •II.Ознакомление с основными положениями темы.
- •Организация работы комиссии по профилактике внутрибольничных инфекций
- •Задача № 1
- •План изучения темы:
- •I. Проверка исходного уровня знаний.
- •II.Ознакомление с основными положениями темы.
- •IV.Подведение итогов занятии.
- •V.Задание на следующее занятие. Основные понятия и положения темы:
- •Требования к правилам личной гигиены пациентов
- •Требования к условиям труда медицинского персонала
- •IV. Санитарно - противоэпидемический режим в отделении.
- •План изучения темы:
Организация работы комиссии по профилактике внутрибольничных инфекций
Клинически выраженные заболевания микробного происхождения, которые поражают пациентов в результате поступления в больницу или обращения за медицинской помощью, а так же заболевания сотрудников вследствие работы в данной организации подлежат учету и регистрации как внутрибольничные инфекции. Это регламентировано СанПиН 2.1.3.2630-10 «Санитарно-эпидемиологические требования к организациям, осуществляющим медицинскую деятельность».
В медицинских организациях хирургического профиля структура внутрибольничных инфекций на 75% представлена хирургической раневой инфекцией, возникающей в послеоперационном периоде или результате реанимационных мероприятий. Руководитель как частной, так и государственной медицинской организации несет ответственность за профилактику внутрибольничных инфекций, вызываемых патогенными возбудителями, то есть возбудителями обычных инфекционных заболеваний в результате их заноса в стационар, и хирургических гнойно-септических инфекций вызываемых условно патогенными бактериями, которые и составляют основную массу, а именно три четверти всех ВБИ.
Внутрибольничные послеоперационные осложнения.
В СанПиН 2.1.3.2630-10 впервые даны четкие критерии определения послеоперационных ГСИ по временному показателю, и по степени тяжести клинических проявлений. Внутрибольничные послеоперационные осложнения – это заболевания, возникшие в течение 30 дней после операции. По степени клинической тяжести процесса выделяются три категории. 1) Поверхностная инфекция разреза: -гнойное отделяемое и/или выделение микроорганизмов; -боль, припухлость, краснота, местное повышение температуры (минимум два признака);
2) Глубокая инфекция, при которой в процесс вовлекаются глубокие мягкие ткани (фасциальный или мышечный слой): -гнойное отделяемое из глубины разреза и/или выделение микроорганизмов; -лихорадка выше 37.5°C повторная операция (абсцесс или иные причины, требующие ревизии послеоперационной раны);
3) Инфекция полости или органа, при которой в процесс вовлекается любая часть организма помимо области разреза и имеется один из перечисленных признаков:-гнойное отделяемое из дренажа; -выделение микроорганизмов из органа или полости; -лихорадочное состояние; -выявление инфекции полости или органа (перитонит, остеомиелит, медиастинит и т.д.) при повторной операции.
Основные возбудители ГСИ – условно патогенные микроорганизмы, причем для каждого хирургического отделения характерна своя собственная микрофлора. Внутрибольничные штаммы микроорганизмов, циркулирующие в хирургических и реанимационных отделениях, обладают повышенной устойчивостью к неблагоприятным факторам внутрибольничной среды.
Назовем источники формирования микробного пейзажа в отделении:
микрофлора, привносимая пациентами, чаще всего с гнойно-септическими инфекциями, пролеченными в отделении;
микрофлора, носителями которой являются сотрудники отделения;
резервуар инфекций;
внутрибольничная среда.
Успешная профилактика ГСИ зависит от слаженной и скоординированной работы всех подразделений стационара (лечебно-диагностического, лабораторного, инженерного). Как организовать такую работу и кому ее можно поручить? В санитарных правилах вы найдете ответы на эти вопросы.
Организация противоэпидемических и профилактических мероприятий по профилактике ВБИ. Организацию противоэпидемических и профилактических мероприятий по профилактике внутрибольничных инфекций осуществляет врач-эпидемиолог (заместитель руководителя медицинской организации по эпидемиологической работе) и/или помощник врача-эпидемиолога (в зависимости от мощности и вида учреждения). Если таких специалистов нет, организация противоэпидемических и профилактических мероприятий возлагается на одного из заместителей руководителя лечебной организации. Для обеспечения этой работы в штате медицинской организации должны быть предусмотрены специалисты соответствующего санитарно-гигиенического и эпидемиологического профиля. Успех работы госпитального эпидемиолога по организации профилактики ВБИ зависит от его квалификации, административного ресурса, которым он должен обладать, и от поддержки руководителя – без нее успех в данном случае невозможен.
Для контроля внутрибольничных инфекций в лечебной организации создают комиссию, по профилактике ВБИ, полномочия которой распространяются на все подразделения и службы. В своей деятельности комиссия руководствуется положением, разработанным и утвержденным для каждой конкретной медицинской организации.
Состав комиссии по профилактике ВБИ. В состав комиссии по профилактике ВБИ входят председатель – заместитель руководителя лечебной организации по эпидемиологической работе (при его отсутствии – один из заместителей руководителя лечебной организации по лечебной работе), эпидемиолог и/или помощник эпидемиолога, главная медицинская сестра, которая представляет среднее звено медицинского персонала, хирург (заведующий одним из хирургических отделений или заведующий операционным блоком), анестезиолог-реаниматолог (заведующий реанимационным отделением), бактериолог (заведующий лабораторией), заведующий аптекой, инфекционист, патологоанатом, другие специалисты (на усмотрение председателя комиссии. Заседания комиссии проводятся не реже одного раза в квартал.
Основные задачи комиссии по профилактике ВБИ.
-Анализ эпидемиологической ситуации в организации.
-Информирование персонала о наличии случаев ГСИ, факторах, способствующих их возникновении. (нарушения противоэпидемического режима), микробном пейзаже отделений, антибиотикоустойчивости выделенных штаммов.
-Принятие решений по результатам эпидемиологического анализа.
-Обеспечение взаимодействия всех служб стационара (отделений).
-Взаимодействие с органами, уполномоченными осуществлять государственный санитарно-эпидемиологический надзор.
Микробиологический мониторинг.
Проблемы возникновения и распространения хирургической раневой инфекции осложняются современными особенностями микроорганизмов, которые с конца прошлого века эволюционировали. В настоящее время неуклонно растет удельный вес метицилин/ванкомицин резистентного стафилококка. В 2010 году стали известны грамотрицательные бактерии, содержащие ген ферментаметаллобеталактамазы, который разрушает все беталактамные антибиотики – пенициллины, цефалоспорины карбопенемы и монобактамы, а также некоторые другие. Этот ген получил название NDM-1.
На этом неблагоприятном эпидемическом фоне отмечается устойчивая тенденция к снижению динамики охвата микробиологическими обследованиями пациентов с ГСИ с 83% в 2000 году до 53% в 2010-м. чтобы исправить данную ситуацию, в СанПиН 2.1.3.2630-10 сделан упор на клинический микробиологический мониторинг, без которого успехи в современной хирургии невозможны.
Для своевременного и адекватного лечения в послеоперационном периоде у пациентов берут материал на бактериологический посев во время операций по поводу гнойных процессов (брать материал следует непосредственно из патологического очага до начала санации раны и антибактериальной терапии), а также при повторных вмешательствах по поводу послеоперационных осложнений любого генеза (ревизия операционных ран или полостей).
Цель микробиологического мониторинга – предотвратить селекцию и распространение антибиотикоустойчивых штаммов.
Назовем показания к взятию материала на микробиологические исследования:
Повторная ревизия операционной раны;
Подозрение на послеоперационное осложнение любого генеза:
-гнойно-септическое;
-кровотечение (так как возможен лизис сосудов в результате гнойного поражения);
-несостоятельность швов;
-порез кишечника в послеоперационном периоде;
-вмешательство по поводу гнойных процессов.
Комиссия по профилактике ВБИ призвана неустанно следить за динамикой эпидемического процесса возникновения ГСИ. Для этого микробиологическая служба представляют лечащему врачу и эпидемиологу информацию, подлежащую дальнейшему анализу:
Число клинических образцов, направленных на исследование из каждого отделения;
Число выделенных и идентифицированных до видов микроорганизмов (отдельно по каждому отделению);
Число выделенных микробных ассоциаций;
Чувствительность выделенных микроорганизмов к антибиотикам и другим антимикробным средствам (отдельно по каждому отделению).
Для проведения целенаправленных лечебных, профилактических и противоэпидемических мероприятий особое внимание необходимо обращать на микроорганизмы, имеющие множественную лекарственную устойчивость.
Многочисленные исследования, проведенные в разных странах мира, свидетельствуют о том, что даже при идеальном соблюдении принципов асептики полностью избежать контаминации хирургических ран во время операции не удается. Для стандартизации риска возникновения послеоперационной раневой инфекции в зависимости от степени микробной обсемененности операционной раны выделено 4 типа операций. Определение этих типов дано в СанПиН 2.1.3.2630-10.
К чистым относят операции, при которых нет контакта с просветом полого органа, обладающего собственной микрофлорой, и не нарушается асептика.
Условно чистые операции предусматривают вскрытие полого органа обладающего собственной микрофлорой, чаще всего желудочно-кишечного тракта или просвета дыхательных путей.
Под загрязненными подразумевают операции, при которых неминуема значительная обсемененность операционных ран.
Грязные операции – это группа оперативных вмешательств по поводу гнойных процессов.
Числовые значения рисков развития ГСИ обозначены в зависимости от типа оперативных вмешательств, а именно:
Риск при чистых операциях – 1 – 5%;
Риск при условно чистых вмешательствах - 3 – 11%;
Риск при загрязненных операциях – 10 – 17%;
Риск при грязных вмешательствах – более 25-27%.
Алгоритм работы комиссии по профилактике ВБИ. Самое большое эпидемиологическое значение имеет рост числа осложнений после чистых и условно чистых операций, что может свидетельствовать о нарушениях противоэпидемического режима, приведших к этим осложнениям. Комиссия по профилактике ВБИ обсуждает данные вопросы и устанавливает их причины, после чего незамедлительно принимаются меры.
Ежемесячные сведения о ведущей микрофлоре в каждом отделении при конкретной патологии ориентируют врачей на проведения адекватной антибиотикопрофилактики и рациональной терапии у пациентов до получения антибиотикограммы. Информация микробиологического мониторинга может использоваться при планировании закупок наиболее эффективных антибактериальных препаратов для стационара и его отделений.
Своевременная микробиологическая диагностика помогает избежать тяжелых ГСИ и летальных исходов от них. Для успешной профилактики ГСИ и выполнения требований СанПиН 2.1.3.2630-10 сотрудники микробиологической службы стационара должны обучить персонал методике взятия материала в соответствии с МУ 4.2.2039-05 «Техника сбора и транспортирования биоматериалов в микробиологические лаборатории» и с госпитальным эпидемиологом и клиническим фармакологом информировать хирургов о результатах микробиологического мониторинга пациентов и окружающей среды, циркуляции госпитальных штаммов, а также атибиотикоустойчивости наиболее часто встречающейся микрофлоры.
Клинический фармаколог не реже одного раза в квартал проводит анализ результатов микробиологического мониторинга и рекомендует своевременную смену лекарственных средств, используемых для атибиотикотерапии. На рюду с этим он доводит данную информацию до сведению оперирующих хирургов.
Госпитальный эпидемиолог в оперативном режиме по компьютеру отслеживает истории болезней пациентов, длительно находящихся на лечении, в послеоперационном периоде, чтобы выявить признаки, не исключающие ГСИ, и своевременно проконтролировать назначение микробиологического исследования. Также с заведующими хирургического отделения он проводит проспективное наблюдение с целью определения истинного уровня заболеваемости ГСИ по хирургическим отделениям (по видам плановых операций) и дальнейшего проведения мероприятий по его снижению.
Кроме того, госпитальный эпидемиолог контролирует забор материала на микробиологическое исследование от пациентов во время ревизии операционной раны, а также при условно чистых, загрязненных и грязных ранах. Не реже одного раза в квартал он проводит заседания комиссии по профилактике ВБИ с ведением протокола.
Работа комиссии по профилактике ВБИ детализирована в СанПиН 2.1.3.2630-10. Важна неформальная ее работа в связи с актуальностью внутрибольничных инфекций, широтой их распространения и развитием новой, не редко тяжелой патологии, угрожающей жизни пациентов.
Микробная загрязненность воздуха имеет большое значение, так как через воздух могут передаваться многие инфекционные заболевания. Микроорганизмы находятся в воздухе в виде бактериального аэрозоля (дисперсионная среда –воздух, дисперсная фаза –капельки жидкости или твердые частицы, содержащие микроорганизмы). Различают 3 фазы микробного аэрозоля: крупноядерную жидкую фазу с диаметром капель более 0.1 мм, мелкоядерную жидкую фазу с диаметром капель менее 0.1 мм и фазу бактериальной пыли. Способность микробов сохраняться в той или иной фазе аэрозоля определяется устойчивостью их к высушиванию. Например, в крупноядерной фазе выживают даже малостойкие микроорганизмы (вирусы гриппа, кори и др.)в мелкоядерной фазе – палочки дифтерии, стрептококки, менингококки и др., в фазе бактериальной пыли – микобактерии туберкулеза, споры бактерий, грибы.
Оценку чистоты воздуха помещений производят на основании определения общего количества микроорганизмов, содержащихся в 1 м кубическом воздуха, и наличия санитарно-показательных микроорганизмов (гемолитических стрептококков и стафилококков) – обычных обитателей дыхательных путей человека. Особенно важен контроль за микробным загрязнением воздуха в хирургических и педиатрических отделениях больниц, в родильных домах, где возникновение госпитальных инфекций наиболее опасно. Здесь главное внимание должно уделяться определению патогенных стафилококков и других патогенных бактерий – возбудителей послеоперационных и послеродовых инфекций и заболеваний новорожденных. В качестве показательных микроорганизмов для оценки воздушной среды используют определение патогенных (коагулазоположительных) гемолитических стафилококков.
При систематическом контроле обнаружение небольшого количества патогенных стафилококков в отделениях, где отсутствует госпитальная инфекция, является закономерным и не может рассматриваться как выходящее за рамки допустимого. Показателем санитарного неблагополучия является большое, особенно нарастающее, обсеменение лечебных учреждений этими микроорганизмами. При оценке результатов необходимо установить, какое место среди обнаруживаемых патогенных стафилококков занимают виды, устойчивые к антибиотикам, и не преобладает ли среди высеваемых культур какой-либо один или немногие фаготипы. нарастание количества патогенных стафилококков при одновременном сужении круга и повышении удельного веса полирезистентных к антибиотикам форм следует рассматривать как грозный предвестник возможного появления госпитальных инфекций.
Плановые исследования воздуха на общую бактериальную обсемененность и наличие золотистых стафилококков проводятся 1 раз в месяц в помещениях лечебно-профилактических учреждений, таких, как операционные, асептические, реанимационные палаты хирургических отделений, родильные залы и детские палаты акушерских стационаров; по показаниям на наличие грамотрицательных микроорганизмов – в асептических отделениях.
По эпидпоказаниям спектр определяемых в воздухе микроорганизмов может быть расширен.
В таблице представлены допустимые уровни бактериальной обсемененности воздуха. В зависимости от принципа улавливания микроорганизмов выделяют следующие методы бактериологического исследования воздуха: 1) Седиментационный; 2) фильтрационный; 3) основанный на принципе ударного действия воздушной струи.
Наиболее простым является седиментационный метод, который позволяет уловить самопроизвольно оседающую фракцию микробного аэрозоля. Посев производят на открытые на больший или меньший срок горизонтально поставленные чашки Петри с плотной питательной средой. После инкубации подсчитывают количество выросших колоний. Этот метод рекомендуется использовать в настоящее время только для получения сравнительных данных о чистоте воздуха помещений в различное время суток, для оценки эффективности санитарно-гигиенических мероприятий (вентиляция, влажная уборка) и т.д.
Фильтрационный метод посева воздуха заключается в просасывании определенного объема воздуха через жидкую питательную среду. Для посева микроорганизмов используют бактериоуловитель Речменского и прибор ПОВ-1, действие которых основано на сорбции микробов в жидкой питательной среде, распыляющейся в струе исследуемого воздуха.
Одним из наиболее совершенных приборов, в котором используется принцип ударного действия воздушной среды, является прибор Кротова, представляющий собой цилиндрический корпус, в основании которого установлен электромотор с центробежным вентилятором, а в верхней части размещен вращающийся диск. На этот диск устанавливается чашка Петри с питательной средой. Корпус прибора герметически закрывается крышкой с радиально расположенной клиновидной щелью. При работе прибора аспирируемый вентилятором воздух поступает через клиновидную щель и струя его ударяется об агар, в результате чего к нему прилипают частицы микробного аэрозоля. Вращение диска с чашкой Петри и клиновидная форма щели гарантируют равномерное распределение микробов по поверхности агара. Для пересчета величины бактериального загрязнения на 1 м3 воздуха регистрируют скорость просасывания воздуха. Зная время отбора пробы, определяют общее количество аспирированного воздуха.
аналог прибора Кротова, «Тайфун Р-40»

прибор Кротова
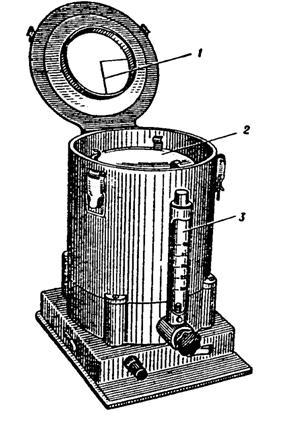
клиновидная щель; 2) вращающийся диск; 3) реометр.
Задание № 1. Провести бактериологический посев воздуха с помощью прибора Кротова.
Методика бактериологического исследования воздуха с помощью прибора Кротова.
Подключить прибор к сети.
Установить на диск открытую чашку Петри с плотной питательной средой. При определении общей бактериальной обсемененности для посева используют 2% мясо-пептонный агар, при определении стафилакокков – желточный агар Чистовича, стрептококков – сахарно-кровяной агар с генциановым синим (среда Гаро)
Закрыть прибор с чашкой и включить электромотор.
С помощью регулятора установить нужную скорость всасывания воздуха (около 25 л в 1 мин).
Прососав необходимое количество воздуха (для определения общего количества колоний при среднем загрязнении воздуха пропускают около 50 л; при отборе проб для выделения стрептококков и стафилококков на элективных питательных средах объем аспирированного воздуха увеличивается дл 250л и более), прибор отключают. Чашку Петри инкубируют в термостате при 37оС в течении 48 ч.
Количество выросших колоний пересчитывают на 1 м3.
Уровень бактериальной загрязненности воздуха – общее микробное число (ОМЧ) рассчитывается по формуле: С * 1000
ОМЧ = ---------------
V
где С – число выросших колоний, V – объём воздуха, взятого для исследования в литрах.
Задание № 2. Решить ситуационные задачи, дать заключение о бактериальной загрязненности воздуха и способах предупреждения внутрибольничной инфекции.
