
- •3. Химическое производство, его структура, назначение основных и вспомогательных подсистем.
- •5 6 7
- •4. Качественные и количественные показатели оценки эффективности химического производства: технологические, экономические, социальные, эксплуатационные.
- •5,6. Классификация сырья. Обогащение твердого сырья: основные методы, применяемые в промышленности. Методы концентрирования жидкого и газообразного сырья..
- •7. Комплексное использование сырьевых ресурсов. Вторичные сырьевые ресурсы.
- •10. Воздух, его применение в химической промышленности.
- •15. Термодинамические расчеты химико-технологических процессов.
15. Термодинамические расчеты химико-технологических процессов.
Термодинамическими называются характеристики процессов, связанные с передачей энергии в форме теплоты и работы при осуществлении последних и учетом состояний равновесности в ХТП. Их подразделяют на энергетические и статические характеристики ХТП соответственно.
По энергетическим характеристикам процессы делятся на экзотермические и эндотермические. Экзотермические процессы – процессы, идущие с выделением энергии, эндотермические процессы – процессы, идущие с поглощением энергии. Экзотермические процессы сопровождаются повышением температуры, а эндотермические – с понижением температуры. Если и экзотермические, и эндотермические эффекты очень малы по абсолютной величине независимо от знака то такие процессы называют атермическими процессами, как например следующая
[Ca(OH)2]+{Na2CO3}=[CaCO3]+2{NaOH} – атермическая реакция.
Энергетической характеристикой химического процесса является энтальпия (тепловой эффект):
ΔrH0298<0 – экзотермический процесс
ΔrH0298>0 – эндотермический процесс
ΔrH0298≈0 – атермический процесс.
Тепловые эффекты процесса влияют на энергозатраты производства.
11. Хим. пр-ть – крупнейший потребитель топлива и электроэнергии.
Тепловая энергия исп. для нагрева, плавления, сушки, выпаривания. Тепл. проц. б. высоко-, средне-, низкотемпературные и криогенные. Эту энергию получают за счет сжигания различных видов топлива . Теплоносителем в данном случае являются топочные газы.
Электрич. энергия - для проведения электрохим. (электролиз растворов и расплавов) и электротермич. (плавление, нагревание) проц. Эта энергия служит для освещения и используется для получ. мех. энергии.
Механич. энергия- для физ. операций: дробления, измельчения, смешения, центрифугирования.
Энергетические ресурсы б. топливные и нетопливные, возобновляемые и невозобновляемые, первичные и вторичные.
Первичные: Топливные б.тверд. (угли, торф, дрова, жидкие (нефть, бензин, керосин) газообразные (прир., попутный газ ).Возобновляемые ресурсы- солн. энергия, энергия ветра.Невозобновляемые - те ресурсы, кот. по мере их добычи необратимо уменьшаются.
Вторичными энергетическими ресурсами(ВЭР) наз. энергетический потенциал продукции, отходов, побочных и промежуточных продуктов, образующихся в агрегатах, кот. не применяются в самом технологическом агрегате, но могут частично или полностью использ. для энергоснабжения других агрегатов. По виду энергии они б.:
горючие (топливные) ВЭР– химическая энергия отходов.
тепловые ВЭР– физическая теплота отходящих газов агрегатов, основной, побочной, промежуточной продукции и отходов производства.
ВЭР избыточного давления(силовое)– потенциальная энергия газов и жидкостей, выходящих из агрегатов, находящихся при изб. давлении.
Направления использования вторичных энергетических ресурсов: топливное(горючие комп-ты в качестве топлива);тепловое(использование теплоты, получаемой в качестве вторичных энергетических ресурсов);силовое;комбинированное(использование теплоты, электрической или механической энергии, одновременно вырабатываемых за счет вторичных энергетических ресурсов).
Ценность источников энергии определяется количеством энергии, кот. м. б. получена при сжигании 1 кг топлива. Ист. энергии являются входящие потоки, несущие энергию топлива Qтопл, электроэнергиюQэл, тепло сырьяQсыри вспомогательных материаловQмат, экзотермические реакцииQэкз. Их суммарное кол-во – потребление, или затраты энергииQзатр. Из системы энергия выводится с потоками целевых продуктовQпрод. цели побочных продуктовQпрод. поб, с энергетическими потокамиQэн, затрачивается на проведение эндотермич.реакцийQэнди теряется естественным путемQпот. Энерг.эф-ость ХТС хар-ют КПД
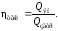
Полное использ. энерг. ресурсов направлено на минимизацию затрат на энергетические и тепловые ресурсы
Qтопл Qпрод. цел
Qэл Qпрод. поб
Qсыр ХТС Qэн
Qмат Qэнд
Qэкз Qпот
. Целью ХТП явл. получ. продукта при мин. экономических затратах. Поэтому надо выбир. оптимальн.режимы и конструции.Исп. реакроры – ап. для хим. превращ.
Требования , кот. д. обеспечить:
высокую производительность единицы реакционного объема;
значительную селективность для сложного процесса;
низкие энергетические затраты;
простоту обслуживания, малую стоимость изготовления и выполнение требований техники безопасности;
надежность регулирования и устойчивость технологического режима;
низкую стоимость продукции.
Важнейших показат. реактора - его интенсивность, кот. хар. количеством целевого продукта, получаемого в единицу времени при заданных условиях с единицы объема (площади) реактора. Интенсивность тем выше, чем меньше времени затрачивается на получение продукта. Поэтому главной задачей при изучении процессов, протекающих в реакторах любого типа, является установление зависимости времени пребывания реагентов в реакторе от различных факторов:
τ = f [х,C,v],
характеристическое ур
по гидродинамической обстановке.
Реакторы смешения – это емкостные ап. с перемешиванием мех. мешалкой или циркуляционным насосом. Реакторы вытеснения – трубчатые ап., имеющие вид удлиненного канала. Есть два типа ап. – реактор идеального смешения и вытеснения.Для идеального смешения хар-но полное выравнивание всех пар-ов по объему реактора.Идеальное вытеснение - любое количество реагентов и продуктов через реактор перемещается как твердый поршень, и по длине реактора
по условиям теплообмена. реакции сопровождаются тепловыми эффектами, поэтому изменяется температура и возник. разность температур между реактором и окружающей средой - движущ. сила теплообмена.
При отсутствии теплообмена с окр. ср. реактор является адиабатическим- теплота идёт на нагрев или охлаждение смеси.
Изотермический, если за счет теплообмена с окружающей средой в нем обеспечивается постоянство температуры.
Автотермические , в кот. поддержание температуры процесса осущ. за счет теплоты хим процесса без исп. внешних источников энергии.
по фазовому составу реакционной смеси. Для проведения гомогенных проц применяют реакторы для газофазных и жидкофазных реакций, для гетерогенных проц – газожидкостные, реакторы для проц в сист. газ – ТВ., ж – тв. ,реакторы для гетерогенно-кат. проц.
по способу организации процесса. периодические, непрерывно действующие и полунепрерывные
В реакторе периодического действия - отдельные стадии протекают последовательно и характеризуются различной продолжительностью. Все реагенты вводят в аппарат до начала реакции, а смесь продуктов отводят после окончания процесса. Параметры изменяются во времени.
В реакторе непрерывного действия все стадии процесса хим превращения вещества осущ. параллельно, одновременно
Реактор полунепрерывного действия - один из реагентов поступает в него непрерывно, а другой – периодически.
по характеру изменения параметров процесса во времени. –стац и нестац режим. Стац – протек. х.р. в люб. т. ,хар-ся одинак. знач конц.,Темпер. в люб. момент вр.Пар-ры на выходе не зав от вр. Нестац – происх. измен. пар-ов во вр.
по конструктивным характеристикам. емкостные; колонные реакторы; реакторы типа теплообменника; реакторы типа реакционной печи
21. В гетеро- проц. компоненты нах. в разн фазах, и процессы связаны с переносом в-ва через поверхность фаз. Конструкция и устройство реакторов д. обеспеч. наилучшие условия для массопередачи, создавать большую поверхность соприкос. фаз.
Реакторы для проведения реакций Г – Т или Ж – Т. Исходя из этого, целесообразно разделить реакторы для гетерогенных процессов в системе Г – Т (Ж – Т) на две группы:
– реакторы, где условия, близки к режиму вытеснения;
– реакторы, где условия близки к режиму смешения.
Для реакторов, работающих в режиме вытеснения, характерно, что состав фаз меняется по мере прохождения через реактор, процессы в таких реакторах, являются неизотермическими. Недостатки описанных реакторов – плох. перемешивание фаз, либо полное его отсутствие, практически полное отсутствие обновления поверхности контакта фаз. Поэтому такие реакторы невыгодно применять там, где необходимо интенсивное перемешивание. В этом случае используют реакторы, относящиеся ко второй группе, где твердый материал находится в режиме смешения.Исп.ап., где перемешивание ТВ. матер. происходит в потоке газа - печи для обжига колчедана и ап. с псевдоожиженным (кипящим) слоем твердого материала Псевдоожиженный слой твердых частиц образуется при пропускании газа снизу вверх через слой твердого материала .Но скорость потока такова, что частицы не покидают пределов слоя и кажет. что материал кипит. Продукты реакции непрерывно выводятся из реактора.
Для проведения процессов в системе Ж – Т часто применяются кубовые или емкостные реакторы с механическими мешалками, а также с пневматическим перемешиванием. Исп. разн. типы мешалок. Для проведения процессов растворения, выщелачивания исп. горизонтальные шнековые реакторы, в которых перемешивание реакционной массы и ее транспортировка осуществляются непрерывным движением шнека.
Реакторы для проведения реакций в системах газ – жидкость (Г – Ж) Реакторы для проведения процессов в системе Г – Ж конструируются по принципу абсорбционных аппаратов, имеют большой объем, но относительно просты и легки в эксплуатации. Чаще это реакторы непрерывного действия, реакторы полупериодические,Взаимодействие газа с жидкостью осуществляют тремя способами: прямо- или противоточным движением сплошных потоков газа и жидкости; барботажем газа в жидкость; разбрызгиванием жидкости в газе
В трубчатом реакторе (рис. 27, а) жидкость стекает по стенкам трубок, одновременно контактируя со встречным потоком газа. Потоки хорошо разделены. Тепловой режим поддерживается регулироваием температуры трубок. Такие реакторы используют в производствах, где нужно точно выдерживать необходимый режим и быстро его регулировать

Рис. 27. Реакторы для процессов, протекающих в системе газ - жидкость:
а, б – трубчатые реакторы; в – насадочная колонна;
г, д – барботажные реакторы; е – распылительная колонна;
ж, з – тарельчатые колонны
Аппараты типа колонн с насадкой, барботажные колонны, либо аппараты оросительного типа. Общий вид насадочных реакторов показан на рис. 27, 3
17.Кинетическими расчетами называются расчеты скоростей. Скорость процесса определяет его интенсивность. Интенсификация процессов состоит в увеличении скорости процесса. Уравнения для определения скорости процессов называются кинетическими.
Для гомофазных процессов при Т=constскорости процессов м. б. представлены как функции концентраций или парциальных давлений всех компонентов реакционной смеси согласно выражению:
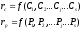
Простой
необратимый процесс А1→А2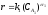
Простой
необратимый процесс A1+A2→A3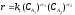 ,
,
Если
реакция обратима: А1↔А2,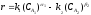
Если
протекает обратимая реакция A+B↔L+D,
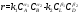 .
.
С – концентрации реактантов, k1 и k2 – константы скорости; α1, α2, β1, β2 - степени при концентрациях – частные порядки реакций относительно реагентов.
Суммарный порядок реакции не должен превышать трех.
Константа скорости показывает вероятность взаимодействия молекул Константа зависит от температуры. Эта зависимость носит название уравнения Аррениуса:
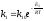
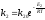
Е1, Е2 – энергия активации прямой и обратной реакции. Энергия активации – высота преодолеваемого барьера, который нужно преодалеть для совершения акта химического взаимодействия.
Чем больше величина энергии активации, тем сильнее зависит константа скорости от температуры. При низких температурах реакция более чувствительна к изменению температуры и подчиняется правилу Вант-Гоффа: при изменении температуры на 100, скорость реакции увеличивается в 2 – 3 раза. Гомофазные реакции очень чувствительны к температуре.
