

Luciana Dobjanschi
generală ajungând pe calea sangvină în toate celulele diferitelor organe şi ţesuturi.
În celule, glucidele pot suferi diferite transformări, care pot fi anabolice (în cadrul cărora au loc sinteze de glucide din alţi compuşi glucidici şi neglucidici) şi catabolice (în cadrul cărora moleculele glucidice sunt degradate cu eliberare de energie).
Catabolismul glucidic
Glucidele care servesc cel mai frecvent substrate al transformărilor catabolice la animale, plante şi microorganisme este glucoza
Schema metabolizării glucozei




 4
4 





G 1 |
|
G-6-P |
5 |
oze (3-7c) + NADPH + H+ |
|
2 |
3 |
6 |
|
|
|
|
|
|
|
|
|
piruvat |
|
|
G-1-P |
9 |
glicogen |
|
|
|
|||
CO2 2a |
|
2c |
|
8 |
|
|
|
|
|
7 |
|
acetil-CoA |
|
lactat + |
energie |
|
acid glucuronic |
2CO2 |
CAT |
reactii de conjugare vitamina C |
|
||
|
|
|
|
2b |
|
lant respirator |
H2O + energie |
|
|
|
|
1 - fosforilarea glucozei, 2 – glicoliza, 2a – decarboxilarea oxidativă a piruvatului, 2b – ciclul Krebs şi lanţul respirator, 2c, 3, 4 – gluconeogeneza, 5 – calea pentozofosfatului, 6 – calea de interconversie în cei doi esteri ai glucozei, 7 – gliconeogeneza, 9 – glicogenoliza.
13

Biochimie farmaceutică
Ficatul utilizează glucoza astfel:
-o parte o utilizează pentru necesităţi proprii;
-o parte o depozitează sub formă de glicogen;
-cea mai mare parte este repusă în circulaţie pentru a servi altor ţesuturi.
Glucoza şi fructoza sunt transformate în ficat în glucoză, care reprezintă forma principală de utilizare de către organismul animal.
În ficat:
25% din glucoză se transformă pe calea 2;
2% din glucoză se transformă pe calea 5;
18% din glucoză se transformă pe calea 8;
55% din glucoză este repusă în circulaţie graţie căii nr. 4, catalizată de către glucozo-6-fosfatază. Această cale este prezentă în rinichi, intestin, lipseşte din muşchi, creier, ţesut adipos.
Eritrocitele folosesc
90% din glucoză pe calea 2;
10% din glucoză pe calea 5.
Creierul
Nu face depozit de glicogen;
Când nu primeşte glucoză pe cale sangvină rămâne fără substrat glucidic, astfel că în caz de hipoglicemie, se ajunge uşor la lipotimie.
Calea nr. 1
-cale obligatorie pentru intrarea glucozei în transformări metabolice.
|
Mg+2 |
|
G + ATP |
|
G-6-P + ADP |
|
||
|
glucokinaza |
|
|
hexokinaza |
|
-procesul de fosforilare este endergo-dependent ireversibil;
-procesul are loc cu scăderea entalpiei libere;
-enzime: glucokinaza (enzimă specifică)
hexokinaza (enzimă nespecifică). Ambele enzime au rol cheie în metabolismul glucozei.
13

Luciana Dobjanschi
X.1. Glicoliza
Calea nr. 2 – ciclul Embden – Meyerhof – Parnas (glicoliza)
-procesul de degradare a glucozei până la piruvat sau lactat;
-procesul are loc cu producere de energie;
-se desfăşoară în faza solubilă a celulei (citoplasmă), deoarece acolo se găseşte întregul set de enzime necesare desfăşurării procesului.
Etapele glicolizei
I degradarea glucozei până la trioze (proces consumator de energie); II descompunerea glicerinaldehid-3-fosfatului până la piruvat (proces în care se produce energie)
I.
|
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
CH2OP |
|
|
|
glucozo-6-fosfat CH2OP |
|
CH2OH |
||||||||||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
glucokinaza |
|
|
|
|
|
|
|
|
|
|
izomeraza |
|
|
O |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
HO |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
ATP |
|
|
ADP |
HO |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2-O-P |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C=O |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
fosfofructo |
|
|
CH2OP |
|
|
|
|
|
CH2OH |
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
kinaza |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
fosfotriozo |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
CH=O |
|
|
izomeraza |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HC |
|
-OH |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
II. |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OP |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
fosfogliceroil |
|
COOH |
|
|
|||||||||
|
|
CH=O |
|
|
|
glicerinaldehid-3-fosfat |
|
|
C - O |
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
kinaza |
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
dehidrogenaza |
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
H-C-OH |
|
|
|
|
|
|
|
|
|
|
ADP |
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OP |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CH2OP |
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
CH OP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
2 |
|
NAD+ |
|
|
|
|
NADH + H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ATP |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
13
Biochimie farmaceutică
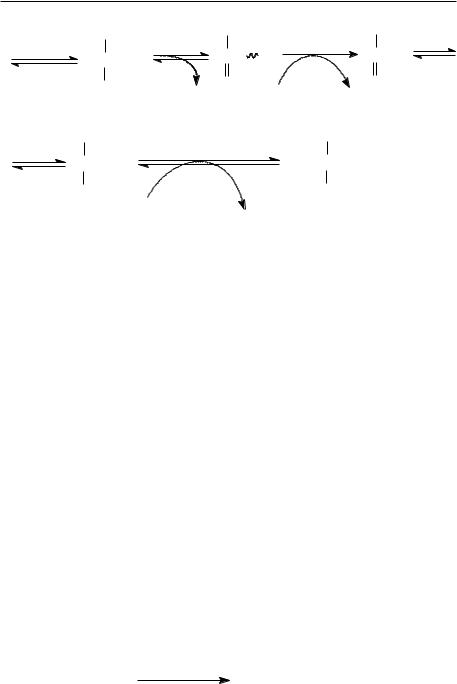
fosfoglicerat |
COOH |
enolaza |
COOH |
piruvat kinaza |
COOH |
|
mutaza |
H-C-OP |
C-O P |
C-OH |
|||
|
|
|
|
|||
|
CH2OH |
H2O |
CH2 |
ADP |
ATP |
CH2 |
|
|
|
|
|||
COOH |
|
COOH |
C = O |
lactat dehidrogenaza |
H - C - OH |
|
||
CH3 NADH + H+ |
CH3 |
|
|
NAD+ |
|
Importanţa glicolizei
-glicoliza este o etapă obligatorie în procesul de degradare a glucozei, ca substrat energetic până la dioxid de carbon şi apă;
-este cea mai importantă cale sub aspect cantitativ de degradare a glucozei;
Bilanţul energetic al glicolizei
I |
- consum |
2 ATP |
(reacţiile 1 |
şi 3) |
||
II |
- câştig |
4 ATP |
(reacţiile 7 |
şi 10) |
||
|
Glicoliza este: |
|
|
2 ATP |
|
|
|
|
|
|
|||
-un proces metabolic cu bilanţ exergonic;
-o importantă sursă de energie atât pentru ţesuturile ce
lucrează anaerob, cât şi pentru cele ce lucrează aerob.
Fermentaţia alcoolică
Unele microorganisme (drojdia de bere) au capacitatea de a transforma glucoza în etanol cu eliberare de dioxid de carbon. Procesul se numeşte fermentaţie alcoolică, şi are un mers asemănător cu glicoliza până la formare de acid piruvic. De aici, fermentaţia alcoolică îşi are mersul său caracteristic.
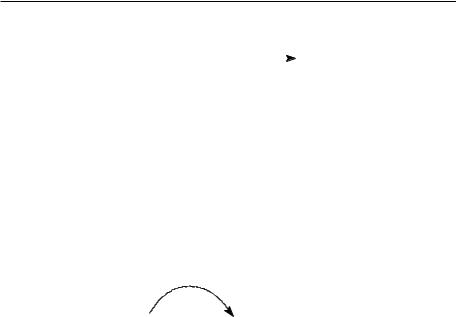
Astfel, într-o primă etapă, acidul piruvic este decarboxilat, sub acţiunea piruvat decarboxilazei.
piruvat
H3C - CO - COOH decarboxilaza H3C - CH=O + CO2
(TPP, Mg+2)
Acetaldehida rezultată este redusă la alcool etilic, sub acţiunea alcool dehidogenazei, care necesită prezenţa coenzimei NADH.
13
Luciana Dobjanschi
|
alcool |
|
+ dehidrogenaza |
+ |
|
H3C - CH=O + NADH + H |
|
H3C - CH2 - OH + NAD |
|
||
Ecuaţia globală este:
glucoza + 2 Pa + 2 ADP  2 CH3-CH2OH + 2 CO2 + 2 ATP + 2 H2O
2 CH3-CH2OH + 2 CO2 + 2 ATP + 2 H2O
Procesul prezintă importanţă industrială deosebită, deoarece stă la baza fabricării băuturilor alcoolice de fermentaţie.
În fermentaţia acetică, acetaldehida sub acţiunea alcool dehidrogenazei, care are ca şi coenzimă NAD+, se transformă în acid acetic.
H3C - CH=O + H2O  H3C - COOH
H3C - COOH
NAD+ |
NADH + H+ |
13

Biochimie farmaceutică
X.2. Calea pentozofosfatică
O altă cale de degradare a glucozei în celulele organismului uman este reprezentată de calea pentozofosfat sau şuntul pentozofosfat. Această cale se realizează în porţiunea solubilă a citoplasmei extramitocondriale din celulele animale. În procesul de degradare a glucozei pe această cale se pot distinge două etape:
1.oxidativă (obţinerea de pentoze din hexoze);
2.calea ce permite interconversia dintre diferite glucide.
1.Etapa oxidativă
CH2OP |
|
CH2OP |
|
|
|
O |
|
O |
|
|
|
|
|
|
HO OH |
OH |
NADH+H+ |
HO OH |
O |
|
OH NAD+ |
OH |
|
|
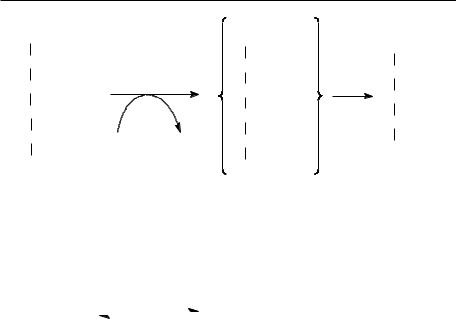
În această reacţie glucozo-6-fosfatul se oxidează sub acţiunea glucozo-6-fosfat dehidrogenazei (GDPH) formând 6- fosfogluconolactonă. GPDH are drept coenzimă NADP+ care funcţionează ca şi acceptor de electroni şi hidrogen. În continuare 6- fosfogluconolactona, hidrolizează spontan sau sub influenţa unei lactonaze formează acid 6-fosfogluconic.
|
|
|
|
|
|
|
|
|
COOH |
||
|
|
CH2OP |
|
|
H2O |
|
|
||||
|
|
|
|
H-C-OH |
|||||||
|
|
|
|
O |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
O |
|
HO-C-H |
||||
|
|
|
|
|
|
|
|
||||
|
|
OH |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
||||||
|
|
|
|
|
H-C-OH |
||||||
|
|
|
|
|
|
|
|
|
|||
HO |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
||
|
|
|
|
OH |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||
CH2-O-PO3H2
În etapa următoare, catalizată de 6-fosfogluconat dehidrogenază (PGDH) are loc concomitent o oxidare şi o decarboxilare. Enzimele utilizează NADP ca şi coenzimă.
13
|
Luciana Dobjanschi |
|
|
|
COOH |
COOH |
|
CH2-OH |
|
H-C-OH |
H-C-OH |
|
||
|
C=O |
|||
HO-C-H |
|
|
||
O=C |
|
H-C-OH |
||
H-C-OH |
|
- CO2 |
||
H-C-OH |
H-C-OH |
|||
|
||||
H-C-OH |
|
|
||
NADP+ NADPH+H+ H-C-OH |
|
CH2-O-PO3H2 |
||
CH2-O-PO3H2 |
CH2-O-PO3H2 |
|
|
Sub acţiunea unei izomeraze, ribulozo-5-fosfatul se izomerază la nitrozo-5-fosfat.
CH2-OH |
|
CH=O |
||||
|
|
C=O |
ribulozo-5-fosfat |
|
|
|
|
H-C-OH |
|||||
|
|
|
|
izomeraza |
|
|
H-C-OH |
|
H-C-OH |
||||
|
||||||
|
||||||
|
|
|
|
|
||
H-C-OH |
|
H-C-OH |
||||
|
|
|
|
|||
CH2-O-PO3H2 |
CH2-O-PO3H2 |
|||||
În unele cazuri procesul se poate opri aici, din oxidarea glucozo-6-fosfatului rezultă dioxid de carbon, NADH+H+ ce intră în reacţiile de biosinteză, care au loc în citoplasma extramitocondrială şi D-ribozo-5-fosfat, care este un precursor în sinteza nucleotidelor.
Ecuaţia globală este:
G-6-P + 2 NADP+ 
 Ribozo-5-fosfat + CO2 + 2 NADPH + H+
Ribozo-5-fosfat + CO2 + 2 NADPH + H+
În alte cazuri, insă, pentozele rezultate pot fi din nou convertite în hexoze, în cadrul unei secvenţe de reacţii de sine stătătoare.
În etapa anterioară din glucozo-6-fosfat a rezultat ribulozo-5- fosfat, care sub acţiunea unei izomeraze se transformă în ribozo-5- fosfat, iar sub acţiunea unei epimeraze se transformă în xilulozo-5- fosfat.
14

Biochimie farmaceutică
CH2-OH C=O
|
|
|
|
|
|
|
|
|
|
|
|
|
|
t |
|
|
|
|
|
|
|
|
|
|
|
|
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
f |
||
|
|
|
|
|
|
|
|
|
|
|
s |
|
||
|
|
|
|
|
|
|
|
|
|
o |
|
|
||
|
|
|
|
|
|
|
|
|
f |
|
|
|
||
|
|
|
|
|
|
|
|
- |
|
|
|
|
||
|
|
|
|
|
|
|
5 |
|
|
|
|
|
||
|
|
|
|
|
|
- |
|
|
a |
|
||||
|
|
|
|
|
o |
|
|
|
|
|||||
|
|
|
|
z |
|
|
|
z |
|
|
||||
|
|
|
o |
|
|
|
a |
|
|
|
||||
|
|
l |
|
|
|
r |
|
|
|
|
||||
|
u |
|
|
|
e |
|
|
|
|
|
||||
b |
|
|
m |
|
|
|
|
|
|
|||||
i |
|
|
|
|
|
|
|
|
|
|||||
r |
|
|
|
o |
|
|
|
|
|
|
|
|
||
|
|
|
z |
|
|
|
|
|
|
|
|
|
||
|
|
i |
|
|
|
|
|
|
|
|
|
|
||
CH=O
H-C-OH
H-C-OH
H-C-OH
CH2-O-PO3H2 ribozo-5-fosfat
H-C-OH
H-C-OH
CH2-O-PO3H2 ribulozo-5-fosfat
r |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
i |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
b |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
u |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
l |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
|
||
e |
|
|
z |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
o |
|
|
|
|
|
|
|
|
|
||
p |
|
|
|
- |
|
|
|
|
|
|
|
|||
|
i |
|
|
|
5 |
f |
|
|
|
|
||||
|
|
m |
|
|
|
|
|
|
|
|
|
|||
|
|
|
e |
|
|
|
- |
|
|
|
|
|||
|
|
|
|
|
|
|
|
o |
|
|
|
|||
|
|
|
|
r |
|
|
|
|
|
s |
|
|
||
|
|
|
|
a |
|
|
|
|
|
f |
|
|
||
|
|
|
|
|
z |
|
|
|
a |
CH2-OH |
||||
|
|
|
|
|
|
|
a |
|
|
|
t |
|||
|
|
|
|
|
|
|
|
|
|
|
||||
C=O
HO-C-H
H-C-OH
CH2-O-PO3H2 xilulozo-5-fosf
Aceste transformări sunt reversibile, iar echilibrul se stabileşte în următoarele rapoarte cantitative. 35% ribulozo-5-fosfat, 25% ribozo-5-fosfat şi 40% xilulozo-5-fosfat.
În etapa următoare, sub acţiunea transcetolazei are loc transferul unei grupări glicolaldehidice de la xilulozo-5-fosfat la ribozo-5-fosfat. Reacţia necesită prezenţa TPP ca şi coenzimă şi ioni de magneziu, iar produsul care rezultă este o heptoză, seduheptulozo- 7-fosfat şi o trioză.
|
|
|
|
|
|
|
|
|
CH2-OH |
|
|
|
|||
|
CH=O |
CH2-OH |
|
|
|
|
|
C=O |
|
|
|
||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|
C=O |
|
|
transcetolaza |
HO-C-H |
|
CH=O |
|||||||
|
|
|
+ H-C-OH |
|
|
|
|
|
|
|
|
|
|||
H-C-OH |
|
|
|
H-C-OH |
+ |
H-C-OH |
|||||||||
|
|
|
|||||||||||||
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
H-C-OH |
|
|
|
H-C-OH |
|
CH2-O-PO3H2 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
glicerinaldehid-3-fosf |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
CH2-O-PO3H2 |
CH -O-PO H |
|
|
|
|
|
|
||||||||
ribozo-5-fosfat |
2 |
3 2 |
|
|
H-C-OH |
|
|
|
|||||||
ribulozo-5-fosfat |
|
|
|
|
|
|
|
|
|||||||
|
CH2-O-PO3H2 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||
seduheptulozo-5-fosfat
14

Luciana Dobjanschi
În continuare în prezenţa unei transaldolaze, are loc transferul unei grupări de dihidroxiacetonă la seduheptulozo-7-fosfat la glicerinaldehid-3-fosfat. Din reacţie rezultă o primă moleculă de hexoză şi anume fructozo-6-fosfatul, precum şi o moleculă de eritrozo-4-fosfat. Fructozo-6-fosfatul este un produs ce face legătura cu secvenţa glicolitică.
|
CH2-OH |
|
|
|
CH2-OH |
|
CH=O |
|||||
|
|
|
|
|
|
|
|
C=O |
|
|||
|
|
C=O |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|
HO-C-H |
CH=O |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|||||||
transaldolaza |
HO-C-H |
+ |
|
|
||||||||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
H-C-OH |
||
H-C-OH + |
H-C-OH |
|
|
|
|
|
|
|
||||
|
H-C-OH |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
CH2-O-PO3H2 |
|
H-C-OH |
CH2-O-PO3H2 |
|
H-C-OH |
|
eritrozo-4-fosfat |
|||||||
|
|
glicerinaldehid-3-fosfat |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||
H-C-OH |
|
|
|
|
|
|
|
|
||||
|
|
|
CH2-O-PO3H2 |
|
|
|||||||
|
|
|
|
|
|
|
|
|||||
CH2-O-PO3H2 |
|
fructozo-6-fosfat |
|
|
||||||||
seduheptulozo-7-fosfat |
|
|
|
|
|
|
|
|
||||
Produşii rezultaţi sunt tot intermediari ai secvenţei glicolitice. Enzimele cheie ale acestei căi sunt glucozo-6-fosfat dehidrogenaza şi 6-fosfogluconat dehidrogenaze.
Importanţa metabolică a ciclului pentozofosfat
Metabolizarea glucozei pe calea pentozofosfat nu constituie propriu-zis o formă de degradare sau de oxidare a glucozei. Calea pentozofosfat nu este cuplată cu lanţul respirator, ci în cadrul ei, nu se formează ATP, ci se consumă pentru activarea glucozei la glucozo-6- fosfat.
Importanţa sa metabolică o constituie faptul că diverşi produşi ai secvenţei metabolice sau intermediarii căii pentozofosfat sunt implicaţi în procese de biosinteză a unor compuşi de importanţă biologică majoră. NADPH + H+ este un furnizor de hidrogen şi de electroni în procesele de sinteză a acizilor graşi, a compuşilor steroidici. Diferitele tetroze, pentoze, hexoze şi heptoze rezultate sunt implicate în biosinteza monozaharidelor şi a acizilor nucleici.
Transformarea glucozei pe calea pentozofosfat constituie un mecanism tipic amfibolic de metabolizare. Diferitele etape ale acestei secvenţe metabolice au loc în faza solubilă a citoplasmei şi toate enzimele care participă la aceste reacţii au fost izolate în stare pură. Ciclul pentozofosfat este avantajos pentru economia celulară şi prin
14

Biochimie farmaceutică
faptul că necesită echipament enzimatic relativ redus, de unde şi denumirea de „şunt pentozofosfat”.
Patologia căii pentozofosfat
Glucozo-6-fosfat dehidrogenaza este o enzimă ce prezintă proprietatea de polimorfism genetic. Aceasta înseamnă că există numeroase variante genetice ale acestei enzime, ca urmare a unor mutaţii genetice.
Această enzimă este un exemplu tipic de enzimopatie farmacogenetică, deoarece se manifestă condiţionat de administrarea unor medicamente şi numai la indivizi cu variaţii genetice ale enzimei.
Exemple de medicamente ce pot provoca apariţia de enzimopatii sunt antimalaricele (chimina), sulfamidele, nitrofurantoina, vitamina K, aspirina. Posesorii de o astfel de enzimopatie nu prezintă suferinţe până când nu ingeră un astfel de medicament, când se produce hemoliză, anemie hemolitică şi methemoglobinurie.
Aceste medicamente cresc potenţialul oxidativ al celulei şi enzima nu mai face faţă.
14

Luciana Dobjanschi
X.3. Degradarea glucozei pe calea acizilor uronici
Pe lângă celelalte căi de degradare a glucozei în organismele animale şi la plantele superioare s-a observat şi o altă cale, care implică oxidarea glucozei la acid glucuronic.
Această cale este importantă din punct de vedere metabolic deoarece:
1.Furnizează acid glucuronic, care este utilizat în procesele de detoxificare hepatică prin conjugarea sa cu fenoli, bilirubină, cu diverşi hormoni, cu unele medicamente sau produşii lor de oxidare. Această conjugare are ca şi consecinţă scăderea toxicităţii acestor compuşi şi mărirea solubilităţii lor, ceea ce facilitează excreţia renală.
2.acidul glucuronic prezintă şi o importanţă structurală, deoarece intră în structura mucopolizaharidelor.
3.Atât în plantele superioare cât ţi în organismele animale (cu excepţia omului, a primatelor şi a cobailor), acidul glucuronic constituie o etapă intermediară în biosinteza acidului ascorbic din glucoză.
Formarea acidului glucuronic în organismele umane parcurge mai multe etape.
1.Glucozo-1-fosfatul rezultat din glicogen prin foforoliză sau din izomerizarea glucozo-6-fosfatului şi se activează prin cuplare cu UTP, cu formare de UDP-glucoză.
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||
|
|
CH2OH |
|
|
|
|
N |
|||||||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
O |
+ P |
P P - O - H2C O |
|
|
|
|
|
|
|
|
UDP-glucozo-pirofosforilaza |
|||||
|
|
|
|
|||||||||||||||||
HO |
|
OH |
OPO3H2 |
|
|
|
|
|
|
|
|
pp |
||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|||||||
14

Biochimie farmaceutică
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
||
|
|
CH2OH |
|
|
|
|
|
N |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
O |
|
|
|
|
|
O |
|
|
N |
|||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||
HO |
|
OH |
|
|
OH |
OH |
OH |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
O - P - O - P - O - P - O - H2C O |
||||||||||||||
|
|
|
||||||||||||||||
|
|
|
|
|
OH O |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|||||
UDP-glucoza
În etapa următoare UDP-glucoza se oxidează în prezenţă de UDP-glucozo dehidrogenază cu formare de acid UDP-glucuronic.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
O |
|
N |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
OH |
|
|
|
OH |
|
OH |
|
OH |
|
|
||||||||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
UDP-glucozopirofosfataza |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
O - P - O - P - O - P - O - H2C |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
OH O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
PP |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
OH |
OH OH |
|
|
|
|
|
|
|
|
N |
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
HO |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
O - P - O - P - O - P - O - H2C O |
||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
OH O O O
OH OH
acid UDP-glucuronic
Acidul UDP-glucuronic poate elibera şi UTP prin hidroliză sau poate intra direct în reacţii de conjugare.
14

Luciana Dobjanschi
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
||||
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|
H N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
OH |
OH |
|
OH |
|
|
|
O |
N |
|
UDP-glucozo- |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dehidrogenaza |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
HO |
|
|
|
|
|
|
|
O - P - O - P - O - P - O - H2C O |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
O |
O |
|
O |
|
|
|
|
|
|
|
|
|
|
2 NAD+ |
2NADH + 2H+ |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
||||
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
O |
|
|
OH |
|
|
OH |
OH |
|
|
O |
|
|
N |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
HO |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
O - P - O - P - O - P - O - H2C |
|
|
|
O |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
acid UDP-glucuronic |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
Acidul UDP-glucuronic poate elibera acidul glucuronic şi UTP prin hidroliză sau poate intra direct în reacţii de glucuronoconjugare.
reactii de  conjugare
conjugare
acid UDP glucuronic  vitamina C
vitamina C
 alicozaminoglican (gliciproteine)
alicozaminoglican (gliciproteine)
Transformarea acidului UDP-glucuronic pe calea 7a, reprezintă o cale de detoxifiere a organismului. Această cale se desfăşoară în ţesutul hepatic şi renal, vizând, în primul rând,
14

Biochimie farmaceutică
compuşii toxici de origine exogenă sau produşi rezultaţi în urma metabolismului normal. În urma acestui proces se formează glicuronide, compuşi solubili şi uşor de eliminat, prin care se neutralizează efectul toxic al unor metaboliţi ( de exemplu, compuşi fenolici, carboxilici, aminici etc.)
R-OH 


 UDP-glucuronic
UDP-glucuronic
 glucuronat transfera
glucuronat transfera
UDP
 R-O-glucunoril
R-O-glucunoril
La om, la maimuţe şi la cobai, acidul glucuronic rezultat prin hidroliza acidului UDP-glicuronic se oxidează la acid gulonic, cu formare finală de xiluloză şi dioxid de carbon (7c).
|
|
|
|
|
|
|
|
H H OHH |
|
|
|
|
|
|
H2 |
||||||
acid UDP-glucuronic |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
HOOC - C - C - C - C - CH=O |
|
|
|
|
||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
UDP |
|
HO |
OH H OH |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
acid glucuronic |
|
|
|
|
|
|
|
|
|||||
H H OHH |
|
CO2 |
|
|
OHH |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
HOOC - C - C - C - C - CH OH |
|
|
|
|
|
HOH2C - C - C - C - CH2OH |
|||||||||||||||
|
|
|
|
|
|||||||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
OH H OH |
|
H2 |
O |
H OH |
|
|
||||||||||||||
|
acid gulonic |
|
|
|
L-xiluloza |
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
L-xiluloza trece în D-xiluloză, care intră intră în calea pentozofosfat. Prezenţa xilulozei în cantitate mică în urina omului sănătos şi în cantităţi mari la bolnavii suferinzi de pentozurie carenţială, dovedeşte posibilitatea acestei căi de degradare a acidului glucuronic.
La plantele superioare şi la majoritatea animalelor, acidul glucuronic trece în acid ascorbic (7b).
14

Luciana Dobjanschi
|
|
|
CH=O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H - C - OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
HO - C - H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
O |
|
|
|
|
|
|
|
C - CH=O |
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H - C - OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
H - C - OH |
|
|
H2O |
|
OH OH |
|
|
|
|
|
|
|
|
|
|
H2 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
glucuronolactona |
|
|
|
|||||||||||||
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
O |
H |
|
|
|
|
|
|
|
|
|
|
O |
|
H |
||||||||||||||
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
C - CH2OH |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
C - CH2OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||||||
|
|
|
OH |
|
OH |
|
|
H2 |
|
|
OH |
|
OH |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
gulonolactona |
|
|
|
|
|
|
|
|
acid ascorbic |
|
|
|
||||||||||||||||||
Deficienţa genetică, care nu permite sinteza acidului ascorbic la om, primate şi cobai, constă în absenţa enzimei L-gulonolacton oxidază, care catalizează etapa finală abiosintezei de acid ascorbic.
14

Biochimie farmaceutică
X.4. Gluconeogeneza
Procesele de catabolizare a glucidelor în celule se desfăşăară concomitent cu cele de biosinteză. Astfel, deşi majoritatea proceselor metabolice sunt procese reversibile, calea de biosinteză a unei molecule nu reprezintă o simplă inversare a căii de degradare. În cadrul fiecărui proces metabolic trebuie să existe cel puţin o verigă prin care anabolismul să se diferenţieze de catabolism. Aceste verigi constituie, în general, tocmai punctele de control al căii metabolice respective.
Căile anabolice prezintă o anumită independenţă în raport cu cele catabolice, ele desfăşurându-se adesea în compartimente celulare diferite.
Cuplarea proceselor catabolice cu cele anabolice este realizată frecvent prin intermediul ATP-ului, transportor al energiei eliberate în cursul catabolismului şi totodată furnizor al energiei necesare în procesele de biosinteză.
În cadrul anabolismului glucidic, formarea glucozo-6- fosfatului constituie etapa nodală. Glucozo-6-fosfatul se poate forma pe mai multe căi:
1.prin fotosinteză (procesul se întâlneşte în organismele autotrofe);
2.prin conversia acidului lactic, respectiv a acidului piruvic în glucoză;
3.prin gluconeogeneză din intermediari ai ciclului acizilor tricarboxilici;
4.prin gluconeogeneză din aminoacizi;
5.prin interconversia altor hexoze în glucozo-6-fosfat. Gluconeogeneza este procesul de resinteză a glucozei din
material neglucidic. Este procesul ce contribuie la satisfacerea necesarului de glucoză a ţesuturilor între mese sau atunci cţnd aportul alimentar de glucoză este insuficient. Procesul poate avea loc plecând de la lactat sau piruvat prin inversarea etapelor glicolizei cu intercalarea anumitor etape unidirecţionale, care sunt soluţionate prin alte secvenţe de reacţii, cu participarea altor enzime. Acestea se numesc căi de ocolire şi sunt:
1.formarea fosfoenol piruvatului din piruvat;
2.transformarea fructozo-1,6-difosfatului în fructozo-6-fosfat;
3.transformarea glucozo-6-fosfatului în glucoză
Formarea fosfoenolpiruvatului. Trecerea fosfoenol
piruvatului în piruvat sub acţiunea piruvatkinazei este un proces care decurge cu o scădere apreciabilă a energiei libere, ceea ce face ca
14

Luciana Dobjanschi
reversibilitatea acestei reacţii să fie extrem de redusă. Din această cauză, fosforilarea piruvatului la fosfoenol piruvat, care pe cale directă ar fi puternic endergonică, decurge pe o cale deviată, care implică participarea atât a unor enzime din citoplasmă cât şi din mitocondrii. Astfel într-o primă etapă piruvatul este carboxilat în mitocondrii cu formare de oxalilacetat. Reacţia necesită participarea ATP-ului, ca donor de energie şi prezenţa acetil CoA, ca modulator de reacţie.
CH3 |
|
COOH |
|
|||
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
CH2 |
+ ADP + Pa |
||
C = O + CO2 + ATP |
|
|
|
|
||
|
|
|
|
|||
|
C = O |
|||||
|
COOH |
|
|
|||
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
Acidul oxalilacetic rezultat este apoi redus la malat, tot în mitocondrii, sub acţiunea NADH.
COOH |
|
|
COOH |
|
|||
|
|
|
|
|
|
|
|
|
CH |
|
|
CH2 |
|
||
|
2 |
+ NADH + H+ |
|
|
|
|
+ NAD+ |
C = O |
|
|
CHOH |
|
|||
|
COOH |
|
|
|
|
COOH |
|
|
|
|
|
|
|||
Acidul malic difuzează din mitocondrie în citoplasmă unde este reoxidat la acid oxalil acetic, sub acşiunea malat dehidrogenazei.
COOH |
|
|
COOH |
|
||||
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|||||
CH |
|
|
|
|
||||
|
|
2 |
+ NAD+ |
|
|
|
|
+ NADH + H+ |
|
|
CHOH |
|
|
C = O |
|
||
|
|
COOH |
|
|
|
|
COOH |
|
|
|
|
|
|||||
|
|
|
|
|
|
|||
Acidul oxalilacetic sub acşiunea fosfoenolpiruvat dehidrogenazei şli cu participarea GTP ca donor de energie se decarboxilează şi se fosforilează concomitent formând fosfoenol piruvat.
15

Biochimie farmaceutică
COOH |
|
|
|
CH2 |
|||||||
|
|
|
|
|
Mg+2 |
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
CH2 |
|
|
|
|
|
|
|||
|
|
+ GTP |
|
C - O PO3H2 + GDP + CO2 |
|||||||
|
|
|
|||||||||
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
C = O |
|
|
|
|
|
|
|
|
|||
|
|
|
|
COOH |
|||||||
|
|
|
COOH |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Ecuaţia globală a procesului este: |
|||||||
CH |
|
|
|
|
|
CH2 |
|||||
3 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|||
C = O |
+ ATP + GTP |
|
|
|
C - O PO3H2 + GDP + ADP + Pa |
||||||
|
|
|
|||||||||
|
|
|
|||||||||
|
COOH |
|
|
|
|
|
|
|
COOH |
||
|
|
|
|
|
|
|
|||||
Deci, pentru fosforilarea enolpiruvatului la fosfoenolpiruvat a fost necesară energia unei molecule de ATP şi una de GTP. În continuare fosfoenolpiruvatul format, se transformă prin inversarea reacţiilor glicolitice până la stadiul de fructizo-1,6-difosfat.
Hidroliza fructozo-1,6-difosafatului este a doua reacţie din cursul biosintezei glucozei care are un mecanism propriu şi nu constă dintr-o inversare a reacţiei din cadrul glicolizei.
Fructozo-1,6-difosfat + H2O |
fructozofosfataza |
Fructozo-6-fosfat + Pa |
|
În etapa următoare fructozo-6-fosfatul sub acţiunea izomerazei este transformată în glucozo-6-fosfat.
Fructozo-6-fosfat 
 Glucozo-6-fosfat
Glucozo-6-fosfat
Glucozo-6-fosfatul este un compus cheie în cadrul metabolismului glucidic, deoarece el constituie compusul iniţial pentru multiple transformări anabolice şi catabolice ale glucozei. În vederea biosintezei glucozei libere, glucozo-6-fosfatul hidrolizează în baza unui mecanism propriu şi nu prin inversarea procesului de formare.
Hidroliza glucozo-6-fosfatului. În secvenţa glicolitică, glucozo-6-fosfatul se formează prin fosforilarea directă a glucozei de către ATP şi în prezenţa hexokinazei. Reacţia inversă este endergonică şi puţin probabilă.
Formarea glucozei libere se realizează prin hidroliza glucozo- 6-fosfatului sub acţiunea glucozo-6-fosfatazei
15

Luciana Dobjanschi
Glucozo-6-fosfat + H2O glucozo-6-fosfataza |
Glucoza + P |
Această enzimă este repartizată selectiv în RE din ficat şi rinichi. Este o enzimă cu funcţii multiple poate cataliza şi hidroliza pirofosfatului sau biosinteza glucozo-6-fosfatului din glucoză şi pirofosfat.
În acest caz glucozo-6-fosfatul nu se găseşte în muşchi şi creier, care nu au capacitatea de a forma glucoza liberă.
Organismul poate să producă glucide şi din alţi precursori (intermediari ai ciclului acizilor tricarboxilici, amino acizi etc).
În procesul de gluconeogeneză există patru enzime ce constituie puncte de control a acestei căi: piruvat carboxilaza, fosfoenolpiruvat carboxilaza, fructozodifosfataza şi glucozo-6 fosfataza, de fapt sunt enzimele care catalizează etapele de ocolire din procesul de gluconeogeneză.
Gluconeogeneza este un proces endergonic ce se desfăşoară în ficat, rinichi şi mai puţin în alte ţesuturi. Dacă în proces se pleacă de la lactat şi piruvat se consumă şase molecule de ATP pentru o moleculî de glucoză.
15

Biochimie farmaceutică
X.5. Metabolismul glicogenului
Glicogenul reprezintă forma majoră de stocare (uşor disponibilă) a excesului de glucoză în organismul animal. La acestă formă se face apel în faza catabolică a metabolismului.
Glicogenul este un polimer ramificat alcătuit din α-D- glucoză, legate majoritar prin prin legături α 1-4 glicozidice şi cu o frecvenă de cca 10 unităţi legături α 1-6 glicozidice, care for crea punste de ramificare.
CH2OH |
|
|
|
CH2OH |
|
|
|
CH2OH |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
OH |
|
O |
|
OH |
|
O |
|
OH |
|
O |
|
|
CH2 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
OH |
|
|
|
|
|
OH |
|
|
|
|
|
OH |
|
|
|
|
OH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||
Glicogenul este localizat în ficat (cca 60%) şi în muşchi (≤
1%). Cantitatea de glicogen depozitată în ficat este mai mică decât cea din muşchi, deoarece masa musculară este mai mare decât masa ficatului. Glicogenul va fi folosit în scopuri diferite în funcţie de locul de depozitare.
Gliconeogeneza şi glicogenoliza, ca şi alte căi metabolice decurg decur distinct şi se conformează principiului general al dualităţii reglării, ceea ce asigură funcţionarea lor nesincronă.
Glicogenoliza – reprezintă procesul de degradare a glicogenului, care presupune desfacerea legăturilor α 1-4 şi α 1-6-
glicozidice din structura acestuia. Procesul se desfăşoară sub acţiunea conjugată a două enzime specifice.
Prima etapă (limitantă de viteză) este o fosforoliză adică transferul unui rest glucozil, de la capătul nereducător al polizaharidei pe o moleculă de acid fosforic (fosforoliză). În urma transferului rezultă glucozo-1-fosfat şi glicogen cu o unitate de glucoză mai puţin.
glicogen (n+1) + P |
fosforilaza |
glucozo-1-fosfat + glicogen ( |
|
Fosforilaza sau 1-4 glucozil-fosfo-glicozil transferaza este o enzimă specifică care acţionează asupra legăturii glicozidice 1-4.
15

Luciana Dobjanschi
Acţiunea acestei enzime încetează la o distanţă de patru unităţi de glucoză faţă de punctul de ramificare. Aici intră în acţiune enzima de deramificare, care îndeplineşte două roluri: desprinde un rest de trei unităţi de glucoză (rest trizaharidic) pe care-l va transfera pe lanţul învecinat.
enzima de |
enzima de |
deramificare |
deramificare |
Enzima de deramificare funcţionează ca o transferază. În apropierea punctului de ramificare mai existp o singură unitate de glucoză. Aceeaşi enzimă de deramificare, dar cu activitate 1-6 glicozidică va desface şi acest ultim rest de glucoză.
Glucozo-1-fosfatul rezultat în urma procesului de fosaforoliză se va transforma în glucozo-6-fosfat, care în ficat, sub acţiunea glucozo-6-fosfatazei trece în glucoză, care trece în sânge şi va servi ca sursă de energie prin trecere prin secvenţa glicolitică.
În muşchi nu există glucozo-6-fosfatază, astfel că glucozo-6- fosfatul va trece direct în glicogenoliză (glicogenul muscular nu poate funcţiona direct ca sursă de glucoză sanguină).Totuşi, metabolismul ţesutului muscular poate contribui la glucoză sanguină indirect, prin aceea că lactatul produs în muşchi poate fi convertit la glucoză în ficat. Aceată secvenţă de reacţii prin care poartă numele de ciclul lui
Cori.
Deci, degradarea glicogenului la glucoză implică 4 reacţii catalizate de 4 enzime:
-fosforilaza, care hidrolizează legăturile α-1,4
-enzima de deramificare, care îndepărtează ramificaţiile cu legături α-1,6
-fosfoglucomutaza, care converteşte G 1P în G 6P
-glucozo-6 fosfataza, care converteşte G 6P în glucoză.
Gliconeogeneza reprezintă etapa de formare a glicogenului din resturi de glucoză şi glicogen cu unităţi mai puţine de glucoză (primer).
În procesul de formare a glicogenului din glucoză, mai întâi glucoza este transformată în glucozo-6 fosfat, din care apoi se formează
15

Biochimie farmaceutică
glucozo-1 fosfat. Glucozo-1 fosfatul reacţionează cu UTP pentru a forma UDP-glucoza. UDP-glucoza reacţionează cu o moleculă iniţială de glicogen preexistentă din metabolismul glicogenului, denumită iniţiator (primer) pe care vor fi transferate una câte una unităţi de glucoză de pe forma activată a aceasteia.
La început se formează legăturile 1-4-α-glicozidice sub acţiunea glicogen sintetazei (rol reglator). Se porneşte de la o moleculă iniţială de glicogen preexistentă din metabolismul glicogenului, denumită iniţiator (primer), pe care vor fi transferate una câte una unităţi de glucoză de pe forma activă a acestuia.
|
|
|
UDP |
|
||
glicogen (n) + UDP-glucoza |
|
|
|
|
glicogen (n+1 |
|
|
|
|
|
|||
(primer) |
GS |
|||||
|
||||||
Reacţia decurge în acest fel până se leagă cel puţin 11 resturi de glucoză. După această fază intervine enzima de ramificare, care creiază legături 1-6 glicozidice. Această enzimă desprinde un rest de şase unităţi de glucoză şi îl transferă pe un lanţ învecinat cu apariţia unui punct de ramificare. Acţiunea combinată a moleculei primer de glicogen, a glicogensintetazei şi a enzimei de ramificare duce la formarea moleculei de glicogen.
enzima de ramificare
Deci, secvenţa de reacţii din biosinteza glicogenului cuprinde următoarele etape:
-legarea a aproximativ 8 resturi de glucoză la molecula primer de glicogen
-creşterea catenei α-1,4 sub acţiunea glicogen-sintetazei
-formarea legăturilor α-1,6 de către enzima de ramificare
-creşterea ulterioară a catenelor α-1,4 de cătreglicogensintetaza
-repetarea etapelor 3 şi 4.
15
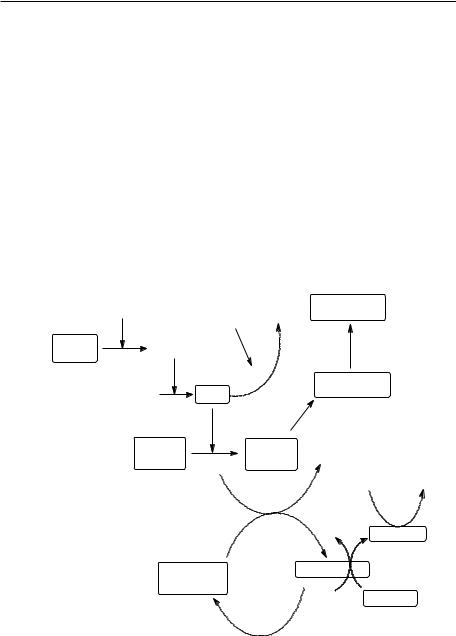
Luciana Dobjanschi
Reglarea şi controlul metabolismului glicogenului
Reglarea glicogenolizei
-afectează în mod special fosforilaza, această enzimă este supusă unui control metabolic variat şi complex realizat atât prin modificări de covalenţă cât şi allosterice.
-Sistemul fosforilază este alcătuit din mai multe enzime:
-fosforilaza b (formă inactivă)
-fosforilaza a (forma activă)
-alte două fosforilaze
-bosforilaz-b-kinaza (transformă forma inactivă b în forma activă a)
-fosforilaz-b-fosfataza (catalizează reacţia
inversă)
|
epinefrina |
insulina |
AMP |
|
|
|
|
adenilat |
adenilat-ciclaza |
|
|
ciclaza |
|
||
|
|
|
|
|
|
E |
|
|
|
D |
|
|
|
P |
|
|
ATP |
AMPc |
|
glicogensintetaza fosforilata
glicogensintetaza defosforilata
proteinkinaza |
|
proteinkinaza |
ADP |
|
AMPcinactiva |
ATP |
AMPc |
glucozo-1-fosfat |
|
|
a |
|
glicogen (n) + glicogen (n-1) |
|
|
|
|
|
|
|
|
|
ADP |
fosforilaza a |
fosforilazkinaza b |
|
fosforilazkinaza a fosforilazfosfataza |
||
defosforilata |
|
ATP |
fosforilaza b |
|
|
|
|
||
fosforilazfosfataz kinaza
La apariţia unui stimul intră în acţiune epinefrina care acţionează pe Rβ şi determină activitatea adenilat ciclazei, care
transformă AT în AMPc. Este vorba de o activare în cascadă a glicogenului care duce la o amplificare a semnalului iniţial.
15

Biochimie farmaceutică
adrenalina
DAG (diacilgliceride) |
I3P3(inozitol-3-fosfat) |
|||||||
CH2OOC-R1 |
|
OH OH |
||||||
PO |
|
|
|
|
||||
|
|
|
|
|
|
|||
|
|
|
|
|||||
CHOOC - R2 |
||||||||
|
|
HO |
|
|||||
|
|
|
|
|
||||
CH2OH |
||||||||
|
|
|
|
|
OP |
|||
|
|
|
|
|||||
|
|
|
|
|
|
|
||
|
|
|
OH |
|
|
|||
Cele două căi metabolice, glicogenoliza şi gşiconeogeneza sunt distincte, dar în reglare intervin aceleaşi mecanisme: creşterea c- AMP afectează şi procesul glicogenezei, acţionând asupra glicogensintetazei, favorizând fosforilarea acesteia de către proteinkinază.
Reglarea acestor procese se realizază nu numai ca AMPc, ci şi în urma interacţiunii hormonului (andrenalină) cu Rα1-adrenergici şi
prin intermediul altor mesageri secunzi (I 3P)
Inozitol-3-fosfatul acţionează prin scoaterea calciului din RE, creşterea tranzitorie a concentraţiei intracelulare a ionului de calciu, care poate acţiona fie independent, sau cuplat cu sisteme de formare a acestuia sub acţiunea altor mesageri. Acţiunea poate să fie o acţiune rapidă, de scurtă durată (10-7s) – mai ales când se produce un influx de ioni de calciu din exterior, sau poate fi o acţiune de mai lungă durată, în cazul în care acţiunea sa este cuplată cu a altor mesageri secunzi (ex. inozitol-3-fosfat).
Ionul de calciu acţionează cuplat cu calmodulina, proteină cu mare flexibilitate conformaţională, cu patru domenii similare de legare a ionului de calciu. Atât ionul de calciu cât şi calmodulina, separat, sunt inactivi. Prin legare de ion de calciu, calmodulina trece într-o conformaţie compactă activă, capabilă să scţioneze asupra altor proteine, determinând la acestea o tranziţie cu implicaţii în activitatea acestora. Uneori calmodulina constituie o parte integrantă a unei enzime fosforilazkinază.
Prin creşterea concentraţiei ionilor de calciu intracelular, calmodulina fixează calciu şi duce la transformări conformaţionale favorizând activitatea fosforilazkinazei.
15

Luciana Dobjanschi
Inhibarea glicogenolizei
AMPc  5'AMP
5'AMP
Insulina este un hormon ce activează PDE, favorizând trecerea AMPc la 5’-AMP, deci inactivează glicogenoliza.
Tulburări metabolice. Datorită unei deficienţe ereditare a sistemului enzimatic implicat în cele două căi ale glicogenului duc la depuneri masive de glicogen în ficat sau muşchi sau depunere anormală de glicogen cu o evoluţie blândă sau dramatică (mortale uneori). Maladia se numeşte glicogenoză.
Există câteva defecte genetice ce duc la stări în care se acumulează glicogenul. Acestea au consecinţe severe asupra sănătăţii ţesuturilor, în special a ficatului. Ele sunt cunscute sub denumirea de boli de stocare a glicogenului.Una din cele mai comune boli se datoreşte deficienţei glucozo-6-fosfatazei şi este cunoscută ca tipul 1 de boală de stocare a glicogenului sau boala Von Gierke. În acest caz se observă nivel scăzut al glicemiei în timpul repausului alimentar şi ficat mărit cu un nivel ridicat al glicogenului.
15

Biochimie farmaceutică
X.6. Glicoproteine şi proteoglicani.
Conjugaţii glucidelor
Sunt complecşi formaţi prin asociere de glucide cu proteine şi/sau lipide, de exemplu, glicoproteinele, proteoglicanii, lipoproteinele etc.
Glicoproteinele şi proteoglicanii sunt compuşi care se formează prin ataşarea covalentă de lanţuri oligo sau polizaharidice la schelete polipeptidice. Distincţia se face în raport cu componenta glucidică.
Glicoproteinele sunt formate din lanţuri de oligozaharide, de obicei ramificate, unite în proporţie variabilă cu lanţuri proteice.
Structura unităţii glucidice
Unităţile glucidice pot fi reprezentate de:
-unităţi glucidice: galactoză, glucoză, manoză
-oze N-acetilate (doi aminoacizi): N-acetilactozamina, N- acetilglucozamina
-acid sialic (NANA – ac. N-acetilneuraminic)
-fucoza
|
|
CH2OH |
|
|
|
|
|
|
|
CH2OH |
|
|
|
|||||||||||
HO |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
HO |
|
|
|
|
|
|
OH |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
NH-CO-CH3 |
|
|
|
|
|
|
NH-CO-CH3 |
|
|
|
|||||||||
|
N-acetilgalactozamina |
|
|
|
|
N-acetilglucozamin |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
COOH |
|
|
|
|
|
OH |
|
|
C-OH |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
HOOC |
|
|
|
|
|
CH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
H N-C-H |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|||||||||||||
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
HO-C-H |
|
|
|
HO O |
|
|
|
|
|
H2N-C-H |
||||||||||||
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|
|
|
|
||||
|
|
|
H-C-OH |
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C-H |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H-C-OH |
|
|
|
|
|
|
|
|
H-C-OH |
H-C-OH |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH |
|
|
|
|
|
CH2OH |
H-C-OH |
||||||||||||||
CH2OH
acid sialic (NANA) = acilarea ac. Neuraminic
15

|
|
Luciana Dobjanschi |
||
CHO |
CHO |
|||
|
|
|
|
|
HO-C-H |
HO-C-H |
|||
|
|
|
|
|
H-C-OH |
H-C-OH |
|||
|
|
|
|
|
H-C-OH |
H-C-OH |
|||
|
|
|
|
|
HO-C-H |
HO-C-H |
|||
|
|
|
|
|
CH2OH |
CH3 |
|||
L-galactoza |
fucoza |
|||
Lanţurile zaharidice se leagă de lanţurile proteice prin legătură O- sau N-glicozidică. De exemplu, în colagen (glicoproteină) se leagă de hidroxilul lizinei.
|
|
|
|
CH2OH |
|
|
|
|
||||
|
HO |
|
|
|
O |
|
|
|
|
|||
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
OH |
O |
|
|
|
||||
|
|
|
|
|
|
|
|
|
CH2-NH2 |
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
||
|
|
O |
|
|
|
O |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
(CH2)2 |
||||
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
CH-CO- |
|||||
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
||
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
Biosinteza
Componentele se sintetizează separat, după care se cuplează formând glicoproteina.
Sinteza oligozaharidei
În sinteza oligozaharidei îl are un compus lipofil cu structură poliizoprenică, poliizoprenol = dolichol.
H3C - C = CH - CH2 - [CH2 - C = CH - CH2 -]n- CH2 - CH - CH2 - CH2OH
|
|
CH3 |
|
|
CH |
CH |
|||
3 |
|
3 |
||
dolidol |
|
|
|
|
16

Biochimie farmaceutică
Etapele sintezei
1.Asamblarea lanţului oligozaharidic şi transferul său pe scheletul peptidic.
2.Prelucrarea glicoproteinei formate în prima etapă.
1.
Dol |
kinaza |
Dol-P |
UDP-glu |
|
ATP ADP
Dol-P-P-Glu UMP
UDP-N-acetil-gal
 UDP
UDP
Dol-P-P-glu-N-Ac-gal
GDP-manoza
 GDP
GDP
Dol-P-P-glu-N-Ac-gal-man
Dol-P-P-oligozaharida
lant polipeptidi
oligozaharid transferaza
Dol-P-P



glicoproteina primara
Dol-P
P
16

Luciana Dobjanschi
2. În etapa a doua are loc prelucrarea enzimatică a glicoproteinelor primare prin eliminarea şi adăugarea de unităţi glucidice sub acţiunea unor glicozidaze şi a unei glicozil transferază, ce adaugă alte subunităţi cu formare de glicoproteine de anumite tipuri.
Rolul glicoproteinelor este divers şi multiplu.
-rol structural: - colagen
-peretele celular;
-rol de transport – glicoproteinele ce transportă ioni metalici, lipide, vitamine etc.
-rol lubrifiant şi protecţie – mucina
-rol enzimatic – factori de coagulare
-unii hormoni sunt glicoproteine
-rol în imunitate
-rol în reacţii de recunoaştere (rol receptor) ex. recunoaşterea unei bacterii sau a unui virus.
Proteoglicani.
Proteoglicanii sunt compuşi formaţi dintr-un lanţ polizaharidic legat de un lanţ polipeptidic. În structura lor ponderea mare o are componenta glucidică (95%) polizaharide şi 5% proteică. Proteoglicanii sunt specifici celulelor animale şi formează matricea ţesutului conjunctiv. Partea glucidică este reprezentată de glicozaminoglicani (mucopolizaharide) – polimeri liniari de natură heteropolizaharidică.
În structura lor intră:
-hexoze aminate
-acizi uronici
1. Acid hialuronic
Acidul hialuronic este un polimer linear cu masă moleculară foarte mare, fiind format din acid glucuronic şi N-acetilglucozamină, legate alternativ prin legături β-1,3-glucuronidice şi β-1,4- glucozamidinice. SE întâlneşte în ţesutul conjunctiv, piele, corpul vitros, cartilagii, lichid sinovial. Legăturile glicozidice ale acidului hialuronic pot fi hidrolizate de către hialuronidaza bacteriană, ceea ce duce laalterarea capacităţii de filtru selectiv al substanţei fundamentale şi la expunerea ţesuturilor la invazia bacteriană.
16

|
|
|
|
|
|
|
|
|
Biochimie farmaceutică |
|||||||
|
|
|
|
COOH |
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
OH |
|
|
O |
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
OH CH3CONH |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH2OH
2.Condroitin-sulfaţii sunt glicozaminoglicanii majori din proteoglicanii cartilagiilor, arterelor, corneei, fiind alcătuiţi din acid glucuronic şi N-acetilgalactozamină legate β-1,3-glucuronidic şi β- 1,4-galactomidinic. Numărul mare de sarcini negative din molecula condroitinsulfaţilor îi consacră un rol de răşini schimbătoare de cationi, având un rol important în reglarea homeostaziei matriceicartilajului şi în mineralizarea matricei osoase.
3.Dermatansulfatul este un constituient fundamental al
ţesutului conjunctiv dermic. Se întâlneşte în tendoane, valvele cardiace, peretele vascular.
4. Heparina
Heparina este un glicozaminoglican ce are o serie de particularităţi funcţionale. Heparina este sintetizată în mastocite şi în toate ţesuturile ce le conţin. Acţiunea anticoagulantă a heparinei s-ar explica prin abilitatea acesteia de a accentua acţiunea de inhibare a trombinei, manifestată prin antitrombina III. Legarea de heparinei la antitrombina III induce în molecula acesteia o tranziţie allosterică ce favorizează legarea sa la trombină. Heparina joacă un rol important şi în procesul de clarificare a plasmei prin acţiunea de eliberare în circulaţie a lipoproteinlipazei din pereţii capilarelor.
|
|
|
|
|
|
|
|
|
CH2OSO3H |
COOH |
CH2OSO3H |
|||||||||||||||||||
|
|
|
|
O |
|
|
O |
|
|
O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
COOH |
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
O |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
O |
|
OH |
|
|
|
O |
|
|
|
|
|
O |
|
|
|
|
OH |
|
|
|
O |
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
OSO3H |
|
|
|
|
NHSO3H |
|
|
|
|
OSO3H |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
NHOCCH3 |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
16

Luciana Dobjanschi
Patologia metabolismului glucidic
Desfăşurarea normală a metabolismului glucidic este controlată atât la nivel molecular prin intermediul enzimelor reglatoare, cât şi la nivel superior, de factorii de reglare cum sunt: hormonii, sistemul nervos.
Starea de echilibru a metabolismului glucidic este indicată de glicemie, care reprezintă concentraţia glucozei din sânge. În condiţii fiziologie, la 12 ore de la ultima ingestie alimentară glicemia este cuprinsă între 80 şi 120 mg%. Tulburprile metabolismului glucidic, mecanism deosebit de complex, se poate manifesta prin hiperglicemii, iar în formă mai avansată prin glicozurie (apariţia glucozei în urină) este diabetul zaharat, care constă într-o alterare complexă a întregului metabolism intermediar, îndeosebi a celui glucidic în corelare cu cel lipidic. Diabetul zaharat implică şi tulburări endocrine grave, mai ales a secreţiei insulinei din pancreas.
O altă categorie de tulburări ale metabolismului normal al glucidelor o constituie sindroamele hipoglicemice, care au la bază modificări patologice ale activităţii principalilor factori de reglare şi control care intervin în metabolismul glucidic, respectiv hormonii pancreatici, insulina şi glucagonul.
În patologia metabolismului glucidic sunt întâlnite şi boli de depozitare ale glicogenului, numite glicogenoze. Acestea sunt boli congenitale şi familiale rare şi sunt caracterizate prin depunerea în diverse ţesuturi ţi organe a unor cantităţi neobişnuite de glicogen.
X.7. Metabolismul altor hexoze
Metabolismul galactozei
Galactoza este o componentă a catenei oligoglucidice care intră în constituţia unor glicolipide, glicoproteine şi proteoglicani.Deasemenea intră în compiziţia lactozei, care este diglucida din lapte. Galactoza este un important substrat energetic.
16

Biochimie farmaceutică
Schema metabolizării galactozei
NADH + H+ |
NAD+ |
|
|
|
dulcitol |
|
galactoza |
hexokinaza |
galactozo-6-fosfat |
aldoreductaza |
|
|||
|
|
|
|
|
ATP ADP
ATP


galactokinaza (1)
ADP
galactozo-1-fosfat UDP-glucoza
UDP-galactoza |
glucozo-1-fosfat |
glicogen |
|
glucozo-6-fosfat |
|
glucoza |
|
glicoliza |
|
|
Prima etapă în metabolismul galactozei o constituie formarea galactozo-1 fosfatului, sub acţiunea unei kinaze, numită galactokinaza.
|
|
CH2 |
|
|
|
|
CH |
||||||||||
HO |
|
|
O |
|
ATP ADP HO |
|
|
|
2 |
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
O |
|
|
|
|||||||
|
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
||
|
|
|
|
galactokinaza |
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
OH |
|
|
|
|
O |
|
P |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||
galactoza |
|
|
galactozo_ 1 fosfat |
||||||||||||||
16

Luciana Dobjanschi
În continuare Gal-1 fosfatul reacţionează cu UDP-glu şi formează UDP-gal şi glucozo-1 fosfat.
|
CH |
|
|
|
|
CHOH |
|
|
|
|
|
CH2OH |
|
|
|
|
CH2OH |
||||||||||||||||||
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
HO |
|
2OH |
|
|
|
|
|
|
O |
|
|
|
uridil _ |
|
HO |
|
O |
|
|
|
|
|
|
O |
|
|
|
||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
OH |
|
|
+ |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
OH |
|
|
+ |
|
|
OH |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
transferaza |
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
UDP |
|
|
|
|
|
O |
|
UDP |
HO |
|
|
|
O |
|
P |
|||||
|
|
|
|
O |
|
P |
HO |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
OH |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Gal1P |
|
|
UDP_glu |
|
|
UDP_gal |
|
|
G1P |
||||||||||||||||||||||||||
|
|
UDP_gal |
epimeraza |
UDP_ glu |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Aceste reacţii au loc în ficat, motiv pentru care viteza de metaboliare a galactozei reflectă capacitatea de funcţionare a ficatului. Acest lucru se foloseşte în practică prin testul de încărcare cu galactoză.
La nivelul glandei mamare UDP-galactoza reacţionează cu glucoza sub acţiunea enzimei lactozo-sintetaza şi formează lactoza.
CH |
|
|
|
|
CH2OH |
|
|
CH |
|
CH2OH |
|
||||||||||||||||
HO |
2OH |
|
|
|
|
|
O |
|
|
|
HO |
2OH |
|
|
O |
|
|
|
|||||||||
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
OH |
|
|
+ |
|
|
OH |
|
|
lactozo_sintetaza |
OH |
|
|
|
|
OH |
|
|
|
+ UDP |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
O |
|
UDP |
HO |
|
|
|
OH |
|
|
|
|
|
|
|
O |
|
|
|
OH |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
OH |
|
|
|
OH |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Dismetaboliile galactozei
Acestea apar ca urmare a deficienţei enzimelor care intervin în metabolismul galactoze. Prin deficienţa galactokinazei, prima enzima de transformare a galactozei apare galactozemia. Aceasta duce la acumularea galactozei în sânge. Acumularea galactozei în cristalin duce la transformarea acesteia în prezenţa aldo-reductazei în galactil, care este responsabil de apariţia cataractei.
Prin absenţa celei de-a doua enzime (uridil-trabsferaza), se acumulează
16

Biochimie farmaceutică
Gal-1P, care este un produs toxic pentru organism. La copii lipsa acestei enzime este destul de severă, deoarece UDP-gal nu se mai formează. Sugarul prezintă tulburări de creştere, iar în lipsa unui tratament pot apărea afecţiuni hepatice, boli mintale, cataracta şi leziuni ale tubilor renali. Galactozemia se trataează prin excluderea galactozei din alimentaţie.
Metabolismul fructozei
Fructoza, în urma metabolizării ei oferă intermediari metabolici cu importanţă metabolică majoră, în special ai glicolizei. Pentru a putea fi metabolizată fructoza trebuie să fie în prealabil fosforilată. Fosforilarea poate avea loc cu ajutorul unei hexokinaze (F6Pcalea minoră) sau a unei fructokinaze F1Pcalea majoră). Fructokinaza este o enzimă cu afinitae mare pentru fructoză, nu este dependentă de insulină şi este influenţată de natura dietei, astfel că fructoza este un zahăr care poate fi folosit de către diabetici. Fructozo-1 fosfatul poate fi scindat de o aldolază (fructoaldolaza) la DOAP şi gliceraldehidă (nefosforilată). Gliceraldehida poate să fie la rândul ei fosforilată la gliceraldehid-3 fosfat în prezenţă de gliceraldehidkinază sau să fie redusă la glicerol, în prezenţa unei reductaze ce necesită NADH + H +.
Glicerolul rezultat poate să fie fosforilat la glicerol-fosfat de o glicerol-kinază. Glicerol-fosfatul la rândul său poate să fie oxidat printr-o reacţie de dehidrogenare cu ajutorul unei gliceroldehidrogenaze cu formare de DOAP. Deci, fructoza se poate integra în glicoliză pe mai multe căi: calea minoră, prin DOAP, prin glicerolkinază şi calea ocolită.
16

|
|
|
|
Luciana Dobjanschi |
|
|
||||||
|
|
|
+ |
|
+ |
|
|
|
|
|
|
|
|
NADH+ |
|
|
|
|
|
|
|
|
|
||
|
G |
|
H NAD |
|
|
|
|
|
|
|
||
|
AR |
Sorbitol |
|
|
|
|
|
|
||||
G6P |
|
|
NAD+ |
|
|
|
|
|
|
|||
|
|
Sor_DH |
|
|
|
|
|
|
||||
|
ADP |
|
|
NADH +H+ |
|
|
|
|
|
|||
|
|
ATP |
|
|
|
|
|
|
|
|
|
|
F6P |
|
|
F |
|
|
|
|
|
|
|
|
|
HK |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
ATP |
|
|
|
|
|
|
|||
|
|
|
FK |
|
|
|
|
|
|
|||
|
|
|
|
ADP |
|
|
|
|
|
|
||
F1,6DP |
|
|
F1P |
|
|
|
|
|
|
|
|
|
|
|
|
|
FA |
|
|
|
|
|
|
|
|
|
DOAP |
|
|
|
GA |
+ |
+ |
|
|
|
||
Ga3P |
|
|
|
|
|
|
NADH |
H |
|
|
|
|
|
|
|
|
|
ADH NAD+ |
|
|
|
|
|
||
|
TK |
|
|
|
|
|
GK |
|
|
|||
|
|
ATP |
glicerol |
glicerol_3 fosfat |
||||||||
|
|
|
|
|
||||||||
piruvat |
|
|
ADP |
|
|
|
|
|
ATP |
|
ADP |
NAD+ |
|
|
|
|
|
|
|
|
NADH+H+ |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
DOAP |
AR- aldozo-reductaza
HKhexokinaza
FK – fructokinaza
FA – fructoaldolaza
TK – tiokinaza
GK – glicerolkinaza
Fructoza se administrează diabeticilor sub formă de perfuzii. Fructoza se transformă în mare parte în glucoză, astfel că în
circulaţia posthepatică ajunge o cantitate destul de mică de fructoză, deoarece se metabolizează în glucoză. Apariţia α-glicerofosfatului ca metabolit al fructozei, leagă metabolismul glucidic de metabolismul lipidic. Calea de formare a fructozei din glucoză prin intermediul sorbitolului se numeşte calea poliol.
16

Biochimie farmaceutică
Glu |
AR |
|
Sor_DH_aza |
||
Sor |
|
|
F |
||
|
|
|
|||
NADH+H+ NAD+ NAD+
NADH+H+
Aspecte de patologie
Deficienţa fructokinazei duce la apariţia enzimopatiei numită fructozurie esenţială (nu se fosforilează fructoza, aceasta se acumulează în sânge, apoi trece în urină).
Deficienţa de fructozoaldolază duce la acumularea de Fructozo-1P, ceea ce provoacă intoleranţă ereditară la fructoză 8boală Gravă). Sugarul prezintă tzlbiurări digestive cu formare de emeză, hepatomegalie, icter, uneori moarte. Tratamentul constă în excluderea fructozei din alimentaţie pentru toată viaţa.
Administrarea de fructoză în perfuzii, în cantităţi mari, precum şi a excesului alimentar de zaharoză, duce la încărcarea sângelui cu fructoză, care stimulează sinteza de grăsimi şi implicit reşte lipemia.
Patologia metabolismului glucidic
Desfăşurarea normală a metabolismului glucidic este controlată atât la nivel molecular prin intermediul enzimelor reglatoare, cât şi la nivel superior de factorii de reglare cum sunt: hormonii, sistemul nervos.
Starea de echilibru a metabolismului glucidic este indicată de glicemie, care reprezintă concentraţia de glucoză din sânge. În condiţii fiziologice, la 12 ore de la ultima ingestie alimentară, glicemia este cuprinsă între 80-120mg%. Tulburările metabolismului glucidic se pot manifesta prin hiperglicemii sau hipoglicemii. Cea mai gravă maladie care se manifestă prin hiperglicemie, iar în forma cea mai avansată prin glucozurie este diabetul zaharat, care constă într-o alterare complexă a întregului metabolism intermediar, îndeosebi a celui glucidic în corelare cu cel lipidic. Diabetul zaharat implică însă şi tzlburări endocrine grave, mai ales ale secreţiei hormonului insulină din pancreas.
O altă categorie de tulburări ale metabolismului normal al glucidelor o constituie sindroamele hipoglicemice, care au la bază tot
16

Luciana Dobjanschi
modificări patologice ale activităţii principalilor factori de reglare şi control care intervin în metabolismul glucidic, respectiv hormonii pancreatici: insulina şi glucagonul.
În patologia metabolismului glucidic sunt întâlnite şi boli de depozitare a glicogenului, numite glicogenoze. Acestea sunt boli congenitale şi familiale rare şi sunt caracterizate prin depunerea în diverse ţesuturi şi organe a unor cantităţi neobişnuite de glicogen, cu structură normală şi anormală.
XI. Metabolismul lipidic
Lipidele sunt biomolecule organice, insolubile în apă ce se pot extrage din celule şi ţesuturi cu solvenţi organici nepolari. Lipidele au câteva funcţii biologice importante, servind drept:
-componente structurale ale membranelor
17

Biochimie farmaceutică
-forme de depozitare şi de transport al combustibililor
-înveliş protector al multor organe
-drept componente ale suprafeţei celulare implicate în
recunoaşterea celulară, în specificitatea de specie şi imunitatea tisulară.
Unele substanţe din clasa lipidelor, cum sunt unele vitamine şi hormoni au o importantă activitate biologică.
Clasificarea lipidelor
Din punct de vedere structural lipidele se împart în:
-I. Lipide simple : – esteri ai acizilor graşi cu glicerina (triacilgliceroli)
-esteri ai acizilor graşi cu alcooli superiori monocarboxilici (ceruri)
-II. Lipide complexe: - glicerofosfolipide: esteri ai
glicerinei cu acizi graşi, compuşi azotaţi şi un rest de acid fosforic
- sfingolipide: conţin un alcool (sfingozina), acizi graşi, compuşi azotaţi şi un rest de acid fosforic
Exemple: - fosfolipide
-glicolipide
-sulfatide
-aminolipide
-lipoproteine
-III. Derivaţi ai lipidelor sunt compuşi rezutaţi prin hidroliza lipidelor simple şi complexe.
Exemple: - acizii graşi: - saturaţi - nesaturaţi
-glicerina
-steroizi
-aldehide grase
-corpi cetonici
Din punct de vedere funcţional lipidele se împart în :
-I. Lipide de rezervă. Acestea sunt localizate în ţesutul adipos şi sunt constituite în special din trigliceride de provenienţă exogenă (alimentară)
-II. Lipidele citoplasmatice sunt lipide complexe care alcătuiesc elementul constant care variază numai în funcţie de natura ţesutului.
17

Luciana Dobjanschi
XI.1. Structura şi proprietăţile acizilor graşi saturaţi
Acizii graşi sunt elemente constitutive ale diferitelor clase de lipide. În stare liberă acizii graşi se întâlnesc în cantităţi mici în celule şi ţesuturi. Acizii graşi conţin un lanţ de hidrocarbură saturată sau nesaturată şi o grupare carboxilică terminală. Acizii graşi din lipidele plantelor şi animalelor superioare cuprind un număr par de atomi de
17

Biochimie farmaceutică
C, în majoritate lanţuri formate din 14-22 atomi de carbon. Acizii graşi saturaţi pot exista într-un număr infinit de conformaţii datorită faptului că legatura simplă permite rptaţia liberă a atomilor de carbon. Forma cea mai probabilă este cea extinsă, cu un conţinut minim de energie. Acizii graşi nesaturaţi prezintă conformaţia cis. În cazul acizilor polinesaturaţi dublele legături nu sunt niciodată conjugate.
Acizii graşi sunt insolubili în apă, dar solubili în solvenţi nepolari, de asemenea ei se solubilizează în NaOH şi KOH cu formare de săruri numite săpunuri. Acizii graşi saturaţi sau nesaturaţi nu absorb lumina nici în vizibil nici în UV. Prin încalzire cu KOH acizii graşi polinesaturaţi pot fi izomerizaţi în acizi graşi cu duble legături conjugate, formă sub care absorb lumina UV între 230-260 nm. Acizii graşi nesaturaţi dau reacţii de adiţie la legătura dublă. Adiţia de halogeni (iod) are utilitate practică în determinarea numărului de duble legături din acizii graşi liberi sau din acizii graşi care alcătuiesc lipidele.
Exemple de acizi graşi saturaţi:
H3C |
|
|
( CH ) |
|
|
|
COOH |
acid butiric |
||
|
|
|
|
|
||||||
|
2 |
2 |
|
|
|
|
||||
H3C |
|
( CH2)4 |
|
COOH |
acid capronic |
|||||
|
|
|||||||||
H3C |
|
(CH2)6 |
|
|
|
COOH |
acid caprilic |
|||
|
|
|
|
|||||||
H3C |
|
(CH2)8 |
|
|
|
COOH |
acid caprinic |
|||||
|
|
|
|
|||||||||
H3C |
|
(CH2)10 |
|
|
COOH |
acid lauric |
||||||
|
|
|
||||||||||
H3C |
|
(CH2)12 |
COOH |
acid miristic |
||||||||
|
||||||||||||
H3C |
|
|
|
(CH ) |
|
|
|
|
COOH |
acid palmitic |
||
|
|
|
|
|
|
|
||||||
|
|
2 14 |
|
|
|
|
|
|||||
H3C |
|
(CH2)16 |
|
|
|
COOH |
acid stearic |
|||||
|
|
|
||||||||||
H3C |
|
(CH2)18 |
|
|
|
COOH |
acid arahidic |
|||||
|
|
|
||||||||||
H3C |
|
(CH2)22 |
|
|
|
COOH |
acid lignoceric |
|||||
|
|
|
|
|||||||||
Acizii graşi nesaturaţi se clasifică în:
-acizi monoenoici
H3C (CH2)5 CH CH (CH2)7 H3C (CH2)7 CH CH (CH2)7
-Acizi polienoici
COOH acid palmitoleic COOH acid oleic
17

Luciana Dobjanschi
H3C |
|
|
|
(CH2)4 |
|
|
|
CH |
|
|
|
CH |
|
|
|
|
CH2 |
|
|
|
CH |
|
|
|
|
CH |
|
|
|
(CH2)7 |
|
|
COOH acid linoleic |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
H3C |
|
|
|
CH2 |
|
|
CH |
|
|
CH |
|
CH2 |
|
|
CH |
|
|
CH |
|
|
|
|
CH2 |
|
|
CH |
|
CH |
|
|
(CH2)7 |
|
COOH acid linolenic |
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
H3C |
|
|
(CH2)4 |
|
CH |
|
CH |
|
CH2 |
|
CH |
|
|
CH |
|
|
CH2 |
|
|
|
CH |
|
|
CH |
|
CH2 |
|
|
CH |
|
|
CH |
|
|
(CH2)3 |
|
COOH acid arahidonic |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
Acizii linoleic, linolenic şi arahidonic sun acizi graşi esenţiali.
17

Biochimie farmaceutică
XI.2. Metabolismul acizilor graşi saturaţi
Catabolismul acizilor graşi
Acizii graşi se degradează prin cedarea succesivă a unor fragmente de 2 atomi de C, în urma unui proces de oxidare ce ar avea loc la nivelul carbonului din poziţia β în raport cu gruparea carboxil.
Catabolismul acizilor graşi presupune activarea şi transportul acizilor graşi saturaţi în mitocondrie unde are loc oxidarea propri-zisă (β-oxidarea).
Activarea acizilor graşi se face cu consum de ATP şi participarea CoA cu formare de tioesteri, ce nu penetrează membrana internă. Pentru traversarea barierei are loc o transesterificare de pe CoA pe o moleculă carrier numită carnitină.
(CH3)3N+ CH2 CH CH2 COOH carnitina OH
Activarea şi transportul acizilor graşi saturaţi
Pentru activarea şi transportul acizilor graşi saturaţi sunt necesare anumite enzime: tiokinaze (acil CoA -sintetaze) şi acil CoAtransferaze.
Aceste enzime se găsesc în membrana mitocondrială externă, intramitocondrial precum şi în microzomi.
Activarea acizilor graşi se realizează în membrana mitocondrială externă, după care are loc transferul acidului gras activat cu ajutorul canitinei în mitocondrie, unde pune în libertate carnitina şi acidul gras intră în procesul de β-oxidare propriu-zis.
R COOH +ATP +CoASH tiokinaza R |
CO SCoA |
carnitina |
carnitina |
R CO SCoA |
AMP +PP |
aciltransferaza |
|
aciltransferaza |
|
|
CoA |
acilcarnitina |
acilcarnitina |
β− oxidarea |
|
CoASH |
membrana
membrana mitocondriala externa mitocondriala mitocondrie interna
17

Luciana Dobjanschi
Oxidarea propriu-zisă (β- oxidarea)
Procesul de β-oxidare sau ciclul lui Lynen se desfăşoară în mitocondrie. Etapele procesului de β-oxidare sunt următoarele:
-dehidrogenarea de tip α- β
-aditia stereospecifică a moleculei de apă
-dehidrogenare
-clivare α- β (tioliză)
|
|
R |
|
CH2 |
|
|
CH2 |
|
CO SCoA |
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NAD+ |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
acil_CoA_dehidrogenaza |
|
|
|
|
LR |
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NADH+H+ |
|
|
3 ATP |
|
|
||||||||||
|
|
R |
|
|
|
CH |
|
|
|
CH |
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
SCoA |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
R |
|
|
|
|
|
CH |
|
|
|
CH2 |
|
|
|
|
CO |
|
SCoA |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
FAD |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
dehidrogenaza |
|
|
|
|
FADH2 |
|
LR |
|
2ATP |
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
R |
|
|
|
C |
|
CH2 |
|
|
|
|
CO |
SCoA |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
CoASH |
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
tiolaza |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H C |
|
|
CO |
|
SCoA |
|
|
|
TCA +LR |
|
12 ATP |
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
R |
|
CO |
|
SCoA |
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Degradarea acizilor graş prin β-oxidare are loc pe o cale alcătuită di 2 reacţii de dehidrogenare, întrerupte de o hidratare şi o scindare prin tioliză, când se pierd 2 atomi de C sub formă de acetilCoA. Restul obţinut, mai scurt cu e atomi de C repetă calea până este integral degradat la acetilCoA.
Acidul gras se oxidează total până la CO2, apă şi energie.
17

Biochimie farmaceutică
Exemplu:
Pentru oxidarea acidului palmitic care este format din 16 atomi de C, acesta trece de 7 ori prin procesul de β-oxidare propriuzisă, rezultând la final 7 molecule de acetil-CoA.
Bilanţul energetic pentru oxidarea aciduli palmitic este următorul:
Din cele 8 Ac-CoA ----- 8 x 12 ATP = 96 ATP
În fiecare tur de β-oxidare se formează 5 ATP---- 7 x 5ATP = 35 ATP
În procesul de acticare se consumă 1 ATP
Total: 130 ATP / moleculă de acid palmitic oxidat.
Pe lângă procesul de β-oxidare se mai cunosc şi alte procese de oxidare a acizilor graşi cum ar fi: α-oxidarea şi Ω- oxidarea.
Catabolismul acizilor graşi cu număr impar de atomi de carbon
Oxidarea acizilor graşi cu număr impar de atomi de carbon se realizează după acelaşi model ca şi β-oxidarea şi presupune aceleaşi etape: activarea, transportul în mitocondrie, integrarea în β-oxidare. În final se ajunge la un rest cu 5 atomi de carbon. Acesta se scindează la acetil –CoA şi propionil-CoA. Propionil-CoA se transformă în succinil-CoA, care intră în TCA.
|
|
CH3 |
CO2 |
|
COOH |
|
|
CH2 |
|
|
|
COOH |
|||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
H3C |
|
CH |
|
|
|
|
|
|
|
|
|
TCA |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
propionil |
|
CO SCoA |
mutaza |
CH2 |
|
|
CO SCoA |
|||||||
|
CO SCoA |
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
carboxilaza |
|
|
|
|
|
|
|
|
|
|
|
|
||
XI.3. Biosinteza acizilor graşi
Biosinteza acizilor graşi saturaţi se realizează din acetil-CoA (precursorul principal). Procesul are loc în toate organismele, dar este predominant în ficatul, şesutul adipos şi glandele mamare ale animalelor superioare. Procesul debiosinteză diferă de cel al oxidării acizilor graşi. Biosinteza acizilor graşi are loc în citosol, iar oxidarea lor are loc în mitocondrii. Deasemenea, prezenţa citratului este necesară pentru obţinerea unor viteze maxime de sinteză, dar nu este cerută pentru oxidarea lor. O altă deosebire o constituie faptul că CO2 este esenţial pentru sinteza acizilor graşi în extractele celulare, deşi nu este încoporat în acizii nou sintetizaţi. Aceste observaţii au dus la
17

Luciana Dobjanschi
concluzia că sinteza acizilor graşi se realizează au un grup de enzime total diferit de cel folosit la oxidarea acizilor graşi.
Reacţia de sinteză a acizilor graşi este catalizată de un sistem multienzimatic complex din citosol, numit complexul sintetazei acizilor graşi.
Biosinteza acidului palmitic
Precursorul esenţial al acizilor graşi este acetil-CoA. Totuşi, din cele 8 unităţi acetil necesare pentru biosinteza acidului palmitic, numai una este furnizată de acetil-CoA. Restul sunt furnizate sub formă de malonil-CoA, formată din actil-CoA şi HCO3- într-o reacţie de carboxilare. Restul acetil şi cele 7 resturi malonil sunt supuse unor trepte succesive de condensare care eliberează 7 CO2 formând acidul palmitic.
Ac_CoA + |
+14 |
+ |
+ |
|
|
|
+ |
|
CO |
|
+ CoA + |
NADP+ + H O |
|
|
H3C (CH2)14 |
7 |
2 |
||||||||||
7 malonil_CoA |
NADPH |
H |
|
|
8 |
14 |
6 2 |
||||||
Singura moleculă de Ac-CoA necesară procesului serveşte ca iniţiator, cei doi atomi de C ai acestei grupări acetil devenind atomii de C terminali ai acidului format. Creşterea lanţului acidului gras începe la gruparea carboxil a acetil-CoA şi continuă prin adiţia succesivă a resturilor acetil la capătul carboxil al lanţului care creşte. Fiecare rest acetil este obţinut dintr-un rest de acid malonic, care pătrunde în sistem sub formă de malonil-CoA. Al 3-lea atom de C al acidului malonic este eliminat sub formă de CO2.
Intermediarii acil al procesului de alungire a lanţului sunt tioesteri, dar nu ai CoA, ca în cazul oxidării acizilo graşi, ci ai unui conjugat proteic, numit proteină acil-transportoare (PTA). Această proteină poate forma un complex cu cele 6 enzime implicate pentru sinteza completă a acidului palmitic. În majoritatea celulelor eucariotelor, toate proteinele complexului sintetazei acizilor graşi sunt asociate într-un grup multienzimatic.
Sursa de atomi de carbon
Principala sursă de carbon este acetil-CoA, formată în mitocondrii prin decarboxilarea oxidativă a piruvatului, prin degradarea oxidativă a unor aminoacizi sau prin oxidarea acizilor graşi cu lanţuri lungi. Acetil-CoA nu poate trece ca atare din mitocondrie în citosol. Citratul format în mitocondrii din acetil-CoA şi oxalil-acetat, poate să treacă prin membrana mitocondrială în citoplasmă pe calea sistemului de transport tricarboxilat. În citosol
17

Biochimie farmaceutică
acetil-CoA este regenerată din citrat sub acţiunea ATP-citrat liazei, care catalizează reacţia:
Citrat + ATP + CoA = acetil-CoA + ADP + Pa + oxalil-acetat
Formarea de malonil-CoA
Malonil-CoA se formează din acetil-CoA şi bicarbonat în citosol, prin acţiunea acetil-CoA carboxilazei.
|
|
|
|
- COOH |
||
H3C |
|
CO |
SCoA |
+HCO3- +ATP acetil CoA |
+ADP + Pa |
|
|
||||||
|
|
|
|
carboxilaza |
CH2 |
|
|
|
|
|
|
CO |
SCoA |
Atomul de C al bicarbonatului devine carbonul carboxilic distal sau liber al malonil-CoA. Acetil-CoA carboxilaza este o enzimă ce conţine biotină ca grupare prostetică. Biotina legată covalent este transportor intermediar al unei molecule de CO2, într-un ciclu de reacţii în două trepte.
HCO3- H+ ATP |
biotin_enzima |
malonil_CoA |
ADP Pa |
carboxi_biotin_enzima |
acetil_CoA |
|
|
Reacţia catalizată de acetil-CoA carboxilaza (enzimă allosterică) este etapa reglatoare care limitează viteza în cadrul biosintezei acizilor graşi.
Citratul este modulatorul pozitiv al acestei reacţii deplasând echilibrul între monomerul inactiv şi polimerul activ, în favoarea celui din urmă.
Reacţia acetil-CoA carboxilazei este de fapt mai complexă decât a fost descrisă anterior. Unitatea monomerică a enzimei conţine 4 subunităţi diferite. Una dintre aceste subunităţi, biotin-carboxilaza (BC), catalizează prima treaptă a reacţiei totale şi anume carboxilarea resturilor de biotină legată de a doua subunitate, care se numeşte proteina transportoare biotin-carboxil (PTBC).
17

Luciana Dobjanschi
sububitatea BC
Biotin_PTBC HCO3- H+ ATP
HCO3- H+ ATP  carboxi_biotin_PTBC ADP Pa
carboxi_biotin_PTBC ADP Pa
carboxibiotin_PTBC |
|
|
subunitatea CT |
COOH |
|||
|
|
|
|
|
|||
|
|
|
|
|
|||
H3C |
|
CO SCoA carboxil |
biotin_PTBC |
||||
|
|
|
CH2 |
||||
|
|
|
transferaza |
|
|||
|
|
|
|
CO SCoA |
|||
|
|
|
|
|
|
|
|
Resturile de biotină ale proteinei transportoare de carboxil servesc ca pârghii în transportul ionului bicarbonat de pe subunitatea biotin-carboxilzei la acetil-CoA, care este legată la situsul activ al subunităţii carboxil-transferazei. Trecerea de la forma monomerică inactivă a acetil-CoA carboxilazei la forma polimerică activă a enzimei are loc când citratul este legat de cea de-a patra subunitate a fiecărui monomer.
Reacţiile sistemului sintetazei
După formarea malonil-CoA, urmează sinteza acizilor graşi într-o secvenţă de 6 trepte succesive, catalizate de 6 enzime ale complexului sintetazei acizilor graşi. Cea de-a şaptea proteină din sistem, nu are activitate enzimatică, ea este proteină transportoare de acil, de care este atşat covalent lanţul de formare a acidului gras.
Complexul acid gras-sintetazei este un dimer; fiecare monomer conţine 2 grupări – SH, una aparţine 4-fosfopantoteinei din ACP (Acyl-Carrier-Protein), a doua unei cisteine din β- cetoacilsintetazei. Cei 2 monomeri sunt astfel aranjaţi îcât în apropierea ACP-SH dintr-un monomer se găseşte o grupare Cis-SH din cetoacilsintetaza.
Biosinteza acidului gras începe prin legarea unei molecule de acetil-CoA de gruaprea Cis-SH, catalizată de acetil-transacilaza. Malonil-CoA se combină cu gruparea –SH a 4-fosfopantoteinei legată de ACP din celălat monomer în prezenţa malonil-transacilazei. În continuare acetilul atacă gruparea metilen din malonil, reacţie catalizată de β-cetoacil-sintetaza cu eliberarea de Co2 şi formarea de β-cetoacil enzima. Gruparea SH a cisteinei rămâne liberă. Prin reacţia de decarboxilare se eliberează energie necesară condensării şi desfăşurării secvenţei de reacţii. Gruparea cetoacil legată de enzimă este redusă, deshidratată, redusă din nou pentru a forma acil enzima saturată. Reacţiile sunt analoage celor din β-oxidare, cu deosebirea că β-hidroxiacidul este izomerul D(-), iar donorul este NADPH. În continuarea a nouă grupare malonil atacă gruparea SH a fosfopantoteinei deplasând restul acil saturat la gruparea SH liberă a cisteine. Secvenţa de reacţii se repetă de 7 ori, de fiecare dată fiind încorporat un rest malonil, până la formarea acidului palmitic.
18

Biochimie farmaceutică
Reacţiile procesului de biosinteză sunt următoarele:
(1) |
|
|
Cis_SH |
|
H3C |
|
COSCoA |
|
|
|
|
|
|
|
acetiltransacilaza |
(1) |
|
|
Cis |
|
S |
|
CO |
|
|
CH3 |
|
|
|
|
betacetoacil |
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(2) |
|
|
|
Pan_SH |
|
HOOC |
|
|
|
CH2 |
|
|
COSCoAmaloniltransacilaza(2) |
|
|
|
Pan |
|
|
S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
sintetaza |
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
CH2 |
|
|
|
COOH |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2CoASH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
(1) |
|
|
|
Cis_SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
β- cetoacilreductaza |
(1) |
|
|
Cis_SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2) |
|
|
|
|
Pan_S |
|
|
CO |
|
|
CH2 |
|
CH |
|
|
CH3 |
||||||||||||||||||
|
CO2 |
(2) |
|
|
|
|
Pan_S |
|
|
CO |
|
|
CH2 |
|
|
|
|
CO |
|
|
CH3 |
NADPH H+ |
|
|
|
NADP+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1) |
|
|
Cis_SH |
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
hidrataza |
(1) |
|
|
|
Cis_SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
enoilreductaza |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(2) |
|
|
|
Pan_S |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
|
CH2 |
|
|
CH2 |
|
|
|
CH3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
(2) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
H2O |
|
|
|
|
|
|
Pan_S |
|
|
|
CO |
|
|
C |
|
|
C |
|
CH3 |
NADPH H+ |
|
|
|
NADP+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
maloniltransferaza |
(1) |
|
|
Cis_S |
|
|
|
CO |
|
|
CH2 |
|
|
|
CH2 |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
(2) |
|
|
|
|
|
Pan_S |
|
|
CO |
|
CH2 |
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
malonil- CoA |
|
|
CoASH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
(1) |
|
|
|
|
Cis_SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
tioesteraza (1) |
|
|
Cis_SH |
|
H3C |
|
|
|
|
|
|
(CH2)14 |
COOH |
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Pan_SH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
(2) |
|
|
|
|
Pan_S |
|
|
|
CO |
|
|
|
|
|
(CH2)14 |
|
|
|
CH3 |
|
|
|
|
|
|
|
(2) |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
Ecuaţia globală de obţinere a acidului palmitic este:
8H C |
|
CO |
|
SCoA |
|
+ |
|
|
H C |
|
|
|
COOH |
CoASH |
14NADP |
+ 7ADP 7Pa |
|
|
|
|
|
|
(CH ) |
||||||||||
|
|
|
|
|
|
|||||||||||
3 |
|
|
|
|
14 NADPH 14 H |
|
7ATP H2O |
|
|
|
8 |
|
||||
|
|
|
|
|
|
3 |
2 14 |
|
|
|
|
|||||
Acidul palmitic format pentru a putea fi încorporat într-o cale metabolică este activat în prezenţa de tikinază şi ATP la palmitilCoA.
Moleculele de NADPH necesare reacţiilor de reducere se formează prin oxidarea glucozo-6-fosfatului pe calea fosfogluconatului.
Etapele ce conduc la biosinteza acizilor graşi diferp de cele implicate în oxidarea acizilor graşi astfel:
-localizarea intracelulară
-tipul de transportor de grupări acil
-forma sub care sunt adăugate sau îndepărtate unităţile cu 2 atomi de carbon
-specificitatea faţă de NADP+ a reacţiei β-cetoacil β- hidroxiacilului
-configuraţia stereoizomerică a intermediarului β- hidroxiacil
-sistemul acceptor-donor de e- ai etapei crotonil-butiril
18

Luciana Dobjanschi
-răspunsul la citrat şi HCO3-.
XI.4. Metabolismul lipidelor simple
18

Biochimie farmaceutică
Biosinteza acilglicerolilor
Acilglicerolii sunt sintetizaţi de organismul animalelor şi plantelor superioare. Sinteza are loc în majoritatea ţesuturilor, dar importanţă practică prezintă ficatul şi ţesutul adipos. Precursorii pentru sinteză sunt glicerol-3-fosfatul şi acizii graşi activaţi sub formă de acil-CoA. Glicerina este activată prin fosforilare la glicerol- 3-fosfat în prezenţă de glicerolkinază şi ATP. Enzima este prezentă în ficat, rinichi, mucoasa intestinală, glanda mamară în lactaţie şi este absentă în muşchi şi ţesutul adipos. În ţesuturile în care enzima este absentă sursa de glicerină o formează dihidroxiacetonfosfatul, intermediar din glicoliză. Transformarea dihidroxiacetonfosfatului în glicerin-3-fosfat se face în prezenţă de NADH şi glicerin-3-fosfat dehidrogenaza.
CH2 |
|
|
|
OH |
CH2 |
|
|
OH glicerin- 3- fosfat |
CH2 |
|
|
OH |
||||||||||||
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
glicerolkinaza |
|
|
|
|
|
|
|
dehidrogenaza |
|
|
|
|
|
|
|
|
glicoliz |
CH |
|
|
|
OH |
CH |
|
OH |
|
C |
|
O |
|
|
|||||||||||
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
OH ATP ADP |
|
|
|
|
|
OP NAD+ NADH H+ |
|
|
|
|
|
|
|
|
|
|||
CH2 |
|
|
OP |
|||||||||||||||||||||
CH2 |
|
|
CH2 |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||
Acizii graşi sunt activaţi prin transformarea lor în derivaţi de CoA în prezenţă de ATP şi CoASH,reacţie catalizată de tiokinază. Astfel în prezenţă de acil-CoA, glicerin-3-fosfat şi transferaze specifice se formează ca intermediar 1,2-diacilglicerolfosfatul (acidul fosfatidic).
Reacţia are loc în 2 trepte. Se observă că acidul fosfatidic este intermediar atât în sinteza acilglicerolilor cât şi a fosfolipidelor. Pentru a fi convertit în triacilglicerină acidul fosfatidic este hidrolizat în prezenţa unei fosfataze.
În mucoasa intestinală există a cale alternativă care pleacă de la 2-monoacilglicerină. Aceasta în prezenţa unui acil-CoA şi a monoacilglicerinaciltransferazei este convertit la 1,2-diacilglicerină. Triacilglicerina se formează cu participarea diacilglicerintransferazei şi a unei molecule de acil-CoA.
18

Luciana Dobjanschi
|
|
|
CH2 |
|
|
OH |
glicerol- 3- fosfat |
|||||||
|
|
|
|
|||||||||||
HO |
|
C |
|
H |
|
|
|
|
acil- |
transferaza |
||||
|
|
|
|
R1 |
|
|
COSCoA CoA |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
CH2 |
|
|
|
OP |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|||||
HO |
|
|
CH2 |
|
|
O |
|
CO |
|
R1 |
||||||
|
|
|
|
|
|
|||||||||||
|
C |
|
H |
|
|
|
|
|
||||||||
R2 |
|
COSCoA CoA |
||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||
CH2 |
|
OP |
|
|||||||||||||
|
|
|
|
|
||||||||||||
|
||||||||||||||||
acid lizofosfatidic |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
O |
|
CO |
|
R1 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
CH2 |
|
O CO |
|
R1 fosfohidrolaza |
R2 |
|
CO |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
R2 |
|
CO |
|
|
|
|
|
|
|
|
O |
|
C |
|
H |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
O |
|
C |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
P |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
CH2 |
|
|
OP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
OH |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
diacilgliceril |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
O |
|
CO |
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
aciltransferaza |
|
|
R2 |
|
|
|
|
CO |
|
|
O |
|
C |
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
R3 |
|
COSCoA CoA |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
|
R3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
În ţesuturile în care este absentă glicerina se porneşte de la dihidroxiacetonfosfatul rezultat din glicoliză.
|
CH2 |
|
|
|
OH |
|
|
CH2 |
|
|
|
OH |
||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
C |
|
|
O |
|
|
|
|
HO |
|
|
|
|
|
|
|
TAG |
||||
|
|
|
|
|
|
|
|
C |
|
H |
|
|||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
CH2 |
|
|
|
|
OP NADH |
|
H+ NAD+ |
|
|
|
|
|
|
|
OP |
|||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
CH2 |
|
|||||||||||||||
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||
R1 |
|
SCoA |
CH2 |
|
|
OCO |
|
R1 |
|
|
|
|
CH2 |
|
|
OCO |
|
R1 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
CoA |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
C |
|
|
|
O |
|
|
|
|
|
|
HO |
|
C |
|
|
|
H |
|
TAG |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
NADH |
|
H+ |
|
|||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
OP |
|
NAD+ |
|
CH2 |
|
|
OP |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
Catabolismul triacilglicerolilor
Primul pas în degradarea triacilglicerolilor îl constituie hidroliza legăturii ester (lipoliza) în prezenţa unor nzime numite lipaze. Se cunosc triglicerolipaze deosebite prin localizare şi funcţie.
Exemplu:
-lipaza pancreatică este localizată în sucul pancreatic şi ajută la digestia triacilglicerolilor din alimentaţie
-lipaza hormon sensibilă este localizată în adipocite şi serveşte la mobilizarea lipidelor
-lipoproteinlipaza este localizată în capilare şi ajută la utilizarea triacilglicerolilor în lipoproteine
18

Biochimie farmaceutică
-lipaza hepatică este localizată în ficat şi are rol în catabolismul lipoproteinelor.
În ţesutul adipos hidroliza triacilglicerolilor are semnificaţie cantitativă şi reprezintă procesul de mobilizare a lipidelor cu eliberarea acizilor graşi liberi în plasmă. Aceştia sunt captaţi de ţesuturi şi utilizaţi în scop energetic sau pentru sinteza lipidelor proprii. Ţesutrul adipos conţine mai multe lipaze. Hormonii au rol lipolitic (catecolaminele), acţionează prin intermediul c-AMP printrun mecanism analog cu cel responsabil de stimularea glicogenolizei.
Lipoliza este un proces hidrolitic care se desfăşoară în trepte.
|
CH2 |
|
OCO |
|
R1 |
|
|
CH2 |
|
|
|
OH |
|
|
lipaza |
|
|
CH2 |
|
|
|
OH |
|
lipaza |
|
|
CH2 |
|
|
|
OH |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
OCO |
|
|
|
R2 lipaza |
|
|
|
|
OCO |
|
|
R2 |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
OH |
||||||||||||||||||
CH |
|
|
CH |
|
|
CH |
|
|
|
|
|
|
CH |
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
CH2 |
|
|
|
|
OCO |
|
|
|
|
R3 |
R1COOH |
|
CH2 |
|
|
|
OCO |
|
|
R3 |
R2COOH |
|
CH2 |
|
|
|
OCO |
|
R3 |
R3COOH |
|
CH2 |
|
|
|
|
OH |
|||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
TAG |
|
|
|
|
|
|
|
DAG |
|
|
|
|
|
MAG |
|
|
|
|
Glicerol |
|||||||||||||||||||||||||||||
Etapa limitantă de viteză este reacţia de îndepărtare a primului rest de acid gras dinTAG, catalizată de lipaza adipolitică sau lipaza hormon-dependentă.
18

Luciana Dobjanschi
XI.5. Metabolismul lipidelor complexe
Biosinteza glicerofosfolipidelor
Acidul fosfatidic este precursor comun pentru două căi separate în biosinteza glicerofosfolipidelor:
1.O cale în care acidul fosfatidic se activează cu CTP şi formează CDP-diacilglicerina, care apoi reacţionează cu componenta polară (mioinozitol, serina, fosfatidilglicerina) formând glicerofosfolipidele respective.
2.O a doua cale în care acidul fosfatidic sub acţiunea fosfohidrolazei pierde fosfatul şi trece în 1,2-diacilglicerol, care reacţionează apoi cu formele activate ale bazelor cu formare de cefaline şi lecitină
În ambele căi citidin-trifosfatul are rol de activator.
1.Biosinteza glicerofosfolipidelor plecând de la acid fosfatidic
Această cale este specifică bacteriilor, dar este utilizată şi de ţesuturile animal în special pentru biosinteza cardio-lipinei şi a fosfatidilinozitolului. Activarea acidului fosfatidic cu citin-trifosfat (CTP) are loc sub acţiunea fosfatidil-citidil-transferazei.
|
|
|
|
CH2 |
|
|
OCO |
|
R1 |
fosfatidilcitidil |
|
|
CH2 |
|
|
|
OCO |
|
R1 |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
R2 |
|
COO |
|
|
CH |
|
|
|
|
transferazei |
R2 |
|
COO |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
CTP |
|
|
|
|
|
|
|
O |
|
|
|
O |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
OPO3H2 |
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
citidil |
||||
|
|
|
|
|
P |
|
|
O |
|
P |
|
O |
|
|||||||||||||||||||||||||
|
|
|
|
CH2 |
|
|
PP |
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
OH |
|||||||||
CDPdiacilglicerina
În bacterii CDP-diacilglicerina reacţionează cu gruparea OH a serinei şi formează fosfatidilserina.
18

Biochimie farmaceutică
|
|
|
|
|
CH2 |
|
|
|
OCO |
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
HO |
|
CH2 |
|
CH |
|
COOH |
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
R2 |
|
COO |
|
|
CH |
|
|
|
|
|
O |
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
CMP |
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
CH2 |
|
|
|
P |
|
|
|
|
O |
|
|
P |
|
|
O |
|
citidil |
|
|
|
NH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
CH2 |
|
|
|
|
OCO |
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
R2 |
|
COO |
|
|
CH |
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
P |
|
|
O |
|
|
CH2 |
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
OH NH2
fosfatidilserina
Fosfatidilserina printr-o reacţie de decarboxilare trece în fosfatidiletanolaminei (cefalina), care mai departe în urma unui proces de metilare formează fosfatidilcolina (lecitina).
|
|
|
|
|
CH2 |
|
|
OCO |
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
PALPO |
|
|
|
CH2 |
|
|
|
OCO |
|
|
R1 |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
R2 |
|
COO |
|
|
CH |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
|
COO |
|
|
CH |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
COOHCO2 |
|
|
|
|
|
|
CH2 |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
P |
|
O |
|
CH2 |
|
|
|
|
|
|
|
|
P |
|
|
O |
|
CH2 |
|
CH2 |
|
NH2 |
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
fosfatidilserina |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
cefalina |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
OCO |
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
COO |
|
|
CH |
|
|
|
|
|
|
|
O |
|
N+(CH3)3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
3SAM |
3SAH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
O |
|
CH2 |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
lecitina |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
CDP-diacilglicerolul reacţionează cu inozitolul în prezenţa CDP-diacilglicerol-inozitol-transferazei formând fosfatidilinozitolul.
18

Luciana Dobjanschi
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OHOH |
|
||||||
|
|
|
|
|
CH2 |
|
|
OCO |
|
|
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
HO |
|
||||||||||||||||||||||
R2COO |
|
|
|
CH |
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
CH2 |
|
|
|
O |
|
|
|
P |
|
|
|
O |
|
|
P |
|
|
|
citidil |
|
|
|
|
|
|
|
|
CMP |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
inozitol |
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
OCO |
|
|
R1 |
OHOH |
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
R2COO |
|
|
|
|
|
|
CH |
|
O |
|
|
O |
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
P |
|
|
O |
|
|
HO |
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
fosfatidilinozitolul |
|
OH |
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
Prin fosforilarea grupărilor OH din inozitol în prezenţă de ATP şi o unei kinaze rezultă formele fosforilate: fosfatidilinozitol-4- fosfat şi fosfatidilinozitol-4,5-bifosfat. Ultimul este considerat mesager de ordinul II care sub acţiunea unor efectori (hormoni neurotransmiţători) determină răspunsuri specifice la nivel celular.
Cardiolipina se găseşte în mitocondrii, cloroplaste şi bacterii. Se sintetizează de la CDP-diacilglicerol care reacţionează cu glicerin- 3-fosfat şi formează fosfatidilglicerolfosfat. Acesta sub acţiunea unei fosfataze pierde fosfatul formând fosfatidilglicerina care este precursorul cardiolipinei. Fosfatidilglicerolul reacţionează cu o noă moleculă de CDP-diacilglicerol şi formează difosfatidilglicerolul.
18

Biochimie farmaceutică
|
|
|
|
|
|
|
|
CH2 |
|
OCO |
|
R1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
R2COO |
|
|
CH |
|
|
|
|
|
|
|
|
|
O |
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
CH |
|
|
OH O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CMP |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
CH2 |
|
|
|
|
P |
|
|
O |
|
|
P |
|
|
citidil |
|
|
|
|
CH2 |
|
|
|
|
|
O |
|
|
|
P |
|
|
|
|
OH |
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
R1 |
|
|
|
|
|
COO |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
OH fosfatidilglicerolfosfataza |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
COO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
CH |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
H2O |
H3PO4 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
O |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
fosfatidilglicerolfosfat |
|
|
|
CDP_diacilglicerol |
|
|
CMP |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
R1 |
|
|
|
|
COO |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
COO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
O |
|
|
|
CH2 |
|
|
|
|
CH |
|
|
|
|
|
CH2 |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
fosfatidilglicerol |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
R1 |
|
|
|
COO |
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
OCO |
|
|
R1 |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
R2 |
|
|
|
|
|
|
|
|
COO |
|
|
CH |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
CH |
|
|
OCO |
|
|
R2 |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
|
O |
|
|
|
CH2 |
|
|
|
|
|
|
|
CH |
|
|
|
|
CH2 |
|
|
|
O |
|
P |
|
O |
|
CH2 |
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
cardiolipina |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
2. Biosinteza glicerolfosfolipidelor plecând de la 1,2-diacilglicerol
Pe această cale se sintetizează lecitina şi cefalina în ţesuturile animale. În acest caz acidul fosfatidic pierde radicalul fosfat şi se transformă în 1,2-diacilglicerină care este acceptorul de fosforil-bază. Rolul CTP este de a activa bazele azotate.
18

Luciana Dobjanschi
Biosinteza fosfatidilcolinei şi foafatidiletanolaminei
În prima etapă bazele (etanolamina şi colina) se fosforilează în prezenţă de ATP şi a unei kinaze specifice, apoi reacţionează cu CTP formând CDP-colina, respectiv CDP-etanolamina. În ultima etapă baza fosforilată este transferată pe diacilglicerol cu formarea fosfolipidei şi eliberarea CMP.
|
|
|
|
|
|
|
colinkinaza |
|
|
O |
|
|
|
|
||||||
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
N+(CH3)3 |
||
HO |
|
CH2 |
|
CH2 |
|
N+(CH3)3 |
|
P |
|
O |
|
CH2 |
|
CH2 |
|
|||||
|
|
|
ATP |
ADP |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
OH |
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
fosfocolin_citidil_ |
|
|
|
O |
|||
transferaza |
|
|
|
|
|
|
|
CDP |
|
O |
|
P |
|
||
CTP PP |
|
|
|
||||
|
|||||||
|
|
|
|
|
|
|
|
|
OH |
||||||
O
O P O CH2 CH2 N+(CH3)3 OH
fosfocolin_diacil_ |
|
|
|
|
CH2 |
|
|
OCO |
|
|
R1 |
||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
transferaza |
R2 |
|
COO |
|
|
CH |
|
|
|
O |
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
CMP |
|
|
|
|
|
|
|
|
|
|
|
+ |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
1,2- diacilglicerol |
|
|
|
|
CH2 |
|
|
|
O |
|
P |
|
|
O |
|
CH2 |
|
CH2 |
|
N (CH3)3 |
|||||
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
Această cale de sinteză a lecitinei se mai numeşte şi cale de recuperare, deoarece lecitina provenită din alimente în urma catabolismului eliberează colina, care poate fi reciclată în acest sens.
În ţesuturile animale lecitina se formează şi prin metilarea succesivă a fosfatidiletanolaminei sub acţiunea unui donor de metil (SAM), care trece în SAH. Metilarea are loc în ficat având ca substrat unic fosfatidiletanolamina (cefalin) şi depinde de disponnibilitatea faţă de SAM.
19

Biochimie farmaceutică
NH2 |
|
|
3 |
N |
+ |
|
||
N |
|
|
N |
O CH2 S+ CH3 |
|
|
|
|
|
|
(CH2)2 |
OHOH CH NH2
SAM COOH
NH2
N
3 |
+ |
 N
N N
N
O CH2 S
(CH2)2
OHOH CH NH2
SAH COOH
|
|
CH2 |
|
|
OCOR1 |
|||||||||||||
|
||||||||||||||||||
|
|
CH |
|
|
|
OCORO 2 |
||||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
CH2 |
|
CH2 |
|
NH2 |
CH2 |
|
|
||||||||||||||||
|
|
|
|
|
P |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
||||||||||||||
|
|
|
|
|
OH |
|||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||
|
CH2 |
|
|
OCOR1 |
|||||||||||||
|
|
||||||||||||||||
|
CH |
|
|
|
OCOR |
||||||||||||
|
|
||||||||||||||||
|
|
|
|
|
|
|
O 2 |
||||||||||
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
O |
|
CH2 |
|
CH2 |
|
N+(CH3)3 |
CH2 |
|
|
|
O |
|
P |
|
|
|
|
|||||||
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
OH |
||||||||||||||
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
lecitina |
|||||||||
Biosinteza fosfatidilserinei
În ţesuturile animale sinteza fosfatidilserinei constă în înlocuirea enzimatică a etanolaminei din cefalină cu serina. Reacţia este reversibilă întrucât fosfatidilserina se poate decarboxila şi reface fosfatidiletanolamina. Fosfatidiletanolamina în continuare se metilează şi formează lecitina.
Toate aceste transformări au drept scop formarea de lecitină pentru sistemul nervos şi creier, care necesită cantităţi sporite de lecitină.
Catabolismul glicerofosfolipidelor
Degradarea glicerofosfolipidelor este un proces complex catalizat de enzime numite fosfolipaze. Locul de acţiune a fosfolipazelor asupra diferitelor legături din molecula substratului.
Exemplu:
19

Luciana Dobjanschi
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
A1 |
|
|
|
|
|||||||||
R2 |
|
OC |
|
|
|
O |
|
|
CH2 |
|
|
O |
|
|
|
|
|
|
|
CO |
|
|
R1 |
|||||
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O D |
|
|
||||||||||
CH |
|
|
|
|
|
|
||||||||||||||||||||||
|
A |
|
|
|
|
|
O |
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
P |
|
|
O |
|
baza |
||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
OH |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Fosfolipaza A1 scindează legătura ester din poziţia 1 a fosfolipidei eliberând acidul gras. Fosfolipaza A2 acţionează asupra legăturii ester din poziţia 2 eliberând acidul gras nesaturat. Prin îndepărtarea unui acid gras din glicerofosfolipide rezultă lizoglicerofosfolipide, care sunt intermediari în metabolismul glicerofosfolipidelor. În general se găsesc în concentraţii mici în celule şi ţesuturi, în concentraţii mari sunt toxice şi au acţiune distructivă asupra membranelor datorită proprietăţii lor tensioactive.
Asupra lizofosfolipidelor acţionează fosfolipaza B sau lizofosfolipaza care îndepărtează acidul gras rămas şi formează glicerol-fosforil-baza.
Fosfolipaza C atacă legătura ester din poziţia 3 eliberând 1,2- diacilglicerolul şi baza fosforilată.
Fosfolipza D hidrolizează baza şi eliberează acid fosfatidic. În urma acestei reacţii este posibil schimbul de baze prin transfer între fosfolipide.
Scindarea difritelor părţi componente ale fosfolipidelor se face cu viteze diferite, astfel că degradarea parţială poate fi urmată de resinteză. De xemplu, catabolismul lecitinei poate avea loc pe mai multe căi: o cale importantă constă în hidroliza de către fosfolipaza A2 a acidului gras din poziţia 2 cu formare de lizolecitină, care fie că este reciclată, fie că suferă catabolism în continuare până la glicerolfosfat şi colină. Lizolecitina se poate forma şi pe o cale alternativă care implică lecitin-colesterol-aciltransferaza (LCAT).
lecitina + colesterolLCAT lizolecitina + colesterol esterifi
lizolecitina + colesterol esterifi
Enzima se găseşte în plasmă şi probabil în ficat şi transferă acidul gras din poziţia 2 a lecitinei pe colesterol, formând colesterol esterificat la nivelul lipoproteinelor plasmatice.
19

Biochimie farmaceutică
Fosfolipaza A2 care scindează acidul gras nesaturat din poziţia 2 furnizează astfel acizi graşi nesaturaţi pentru sinteza prostaglandinelor, tromboxanilor şi leucotrienelor. În pancreatita acută fosfolipaza A2 trece în sânge unde transformă lecitinele în lizolecitine a căror proprietăţi hemolizante stau la baza anemiilor din pancreatite.
Fosfolipaza B care scindează acizii graşi din poziţia 1 sau 2 a lizofosfolipidelor are rol şi în resinteza fosfatidilcolinei, conform următoarei reacţii:
lizofosfatidilcolina + acilCoA |
fosfatidilcolina + CoAS |
Toxinele bacteriene conţin fosfolipaza C care degradează lecitinele la digliceride şi fosfocolină.
19

Luciana Dobjanschi
XI.6. Metabolimul sfingolipidelor
Sfingolipidele sunt lipide complexe care se găsesc în cantităţi mari în creier şi ţesut nervos. Toate au ca unitate structurală ceramida (formată dintr-un aminoalcool, sfingozina, şi un acid gras) precum şi o componentă polară. În funcţie de componenta polară se clasifică în:
-sfingomieline care conţin ca grupare polară fosforilcolina sau fosforiletanolamina
-glicosfingolipide care au ca grupare polară una sau mai multe oze.
Exemplu:
Prin acilarea grupării amino din sfingozină cu un acid gras cu catena lungă rezultă N-acilsfingozina sau ceramida.
H3C |
|
(CH2)12 |
|
|
CH |
|
CH |
|
|
|
|
CH |
|
|
|
|
CH |
|
|
|
CH2OH |
+ R |
|
|
|
COSCoA |
|
||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
OH |
|
NH2 |
|||||||||||||||||||||||||||
|
|
sfingozina |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
H3C |
|
|
(CH ) |
|
|
CH |
|
|
CH |
|
CH |
|
CH |
|
|
CH OH + CoASH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
2 12 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|||||||||
|
|
|
|
|
|
ceramida |
|
|
|
|
|
|
OH NH |
|
CO |
|
|
R |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
Alte exemple de sfingolipide:
Sfingomielina, cerebrizidele, sulfatidele şi gangliozidele.
Degradarea sfingolipidelor
Sfingolipidele sunt degradate de către sfingomielinază, o enzimă care îndepărtează restul de fosforilcolină. Cerebrozidele şi gangliozidele sunt hidrolizate de către hidroxilaze, care îndepărtează câte un rest de oză de la capetele nereducătoiare ale lanţului glucidic.
Arilsulfatazele îndepărtează resturile sulfat din molecule. Toate acestea sunt enzime lizozomale a căror deficit determină boli lizozomale. Aceste boli se caracterizează prin acumularea în ţesuturile substratului de lipde a căror enzime de degradare sunt deficitare şi se numesc sfingolipidoze.
19

Biochimie farmaceutică
XI.7. Metabolismul colesterolului
Colesterolul este un sterol major în organism şi se găseşte în cantitate mare în ficat, piele, creier, sistem nervos, corticosuprarenală, aortă. Colesterolul intră în structura memebranelor celulare şi a lipoproteinelor plasmatice şi este punct de plecare pentru biosinteza acizilor biliari, a hormonilor steroizi şi a vitaminei D3.
Colesterolul din organism este de origine exogenă şi endogenă. Colesterolul exogen provine din alimentaţie (0,3g/zi), (gălbenuş de ou, carne, ficat, creier, unt=, iar colesterolul endogen provine prin biosinteză.
Schema metabolizării colesterolului
formarea membranelor |
hormoni steroizi |
alimente  colesterol
colesterol  colesterol sintetiza
colesterol sintetiza
vitamina D3 |
esteri ai colesterolului |
acizi biliari |
(lipoproteine plasmatic |
Din colesterolul sintetizat 50% se transformă în acizi biliari, care sunt excretaţi în bilă. O parte se transformă la nivelul pielii în vitamina D3, la nivelul corticosuprarenalei în hormoni steroizi şi intră în structura membranelor. Excesul se excretă ca atare, mai întâi în bilă, apoi în intestin unde sub acţiunea florei bacteriene se tranformă în coprostanol şi colestanol, care se elimină prin fecale.
Biosinteza colesterolului
Toate ţesuturile ce conţin celule nucleate au capacitatea de a sintetiza colesterol, dar cele mai active sunt ficatul, pielea şi aorta. Biosinteza colesterolului este un proces complex, care constă dintr-un număr mare de reacţii ce se transformă în faza solubilă a citoplasmei şi în microzomi.
Procesul de biosinteză a colesterolului se desfăşoară în etape, şi anume:
1.transformarea acetil-CoA în acid mevalonic
2.transformarea acidului mevalonic în scualen
3.transformarea scualenului în colesterol.
19

Luciana Dobjanschi
În biosinteza colesterolului singura sursă de atomi de carbon este acetil-CoA. Reacţiile se desfăşoară în faza solubilă a citoplasmei şi reacţiile sunt catalizate de enzime, care în marea lor majoritate sunt ataşate de RE şi necesită prezenţa unor cofactori şi coenzime: NADH, ATP, CoA.
Etapele biosintezei colesterolului
1. Formarea acidului mevalonic din acetil-CoA
Acidul mevalonic se formează prin condensarea a 3 molecule de acetil-CoA. În prima etapă se condensează numai 2 molecule de acetil-CoA în prezenţa β–cetotiolazei, formând acetoacetil-CoA. În continuare are loc condensarea acetoacetil-CoA cu a treia moleculă de acetil-CoA în prezenţa β–hidroxi,β-metil- glutaril-CoA-sintetazei (HMG-CoA-sintetaza) şi formează HMGCoA. Mai departe gruparea carboxilică legată de CoA este redusă la grupare hidroxilică, cu eliminare de CoA. Reacţia are loc în prezenţa unui sistem multienzimatic catalizat de HMG-CoA-reductaza, care necesită NADPH + H+, ca donor de hidrogen. Reacţia catalizată de HMG-CoA-reductaza este etapă limitantă de viteză sau etapă reglatoare în procesul de biosinteză a colesterolului. Când colesterolul se acumulează în cantitate prea mare în celulă înhibă sinteza de HMG-CoA-reductaza.
|
2H3C |
|
|
CO |
|
|
SCoA tiolaza H3C |
|
|
|
CO |
|
CH2 |
|
|
CO |
|
|
SCoA + CoASH |
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
H C |
|
CO |
|
|
CH |
|
|
|
|
|
|
|
CO |
|
|
|
|
|
|
SCoA |
+ |
|
H C |
|
CO |
|
|
SCoA |
HMG_CoA sintetaza |
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
3 |
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
HOOC |
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
CH2 |
|
|
COSCoA |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HMG_CoA reductaza |
||||||||||||||
|
HOOC |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
C |
|
|
|
|
CH |
|
|
|
|
|
COSCoA |
|
|
|
|
|
|
|
|
|
|
+ |
|
+ |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
+ |
|
|
NADPH |
|
|
H |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
2 |
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
HOOC |
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
OH + 2NADP+ + CoASH |
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
CH2 |
|
CH2 |
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
19

Biochimie farmaceutică
2. Transformarea acidului mevalonic în scualen
Acidul mevalonic se fosforilează în 3 etape. În prima etapă în prezenţă de ATP şi mevalonatkinază are loc formarea de acid 5-fosfomevalonic. În a 2-a etapă sub acţiunea fosfomevalonatkinazei, acidul mevalonic trece în acid 5-pirofosfomevalonic. Cea de-a treia fosforilare are loc în poziţia 3 şi rezultă acid 3-fosfo-5- pirofosfomevalonic. Acesta este un compus instabil care se decarboxilează şi pierde o grupare fosfat şi rezultă izopentenilpirofosfat.. 3-izopentenilpirofosfatul se izomerizează la
3,3-dimetilalilpirofosfat |
|
sub |
|
acţiunea |
|
izopentenilpirofosfatizomerazei. |
Dimetilalilpirofosfatul |
se |
|||
condensează |
cu |
izopentenilpirofosfatul |
sub |
acţiunea |
|
geranilpirofosfatsintetazei şi formează geranilpirofosfatul(10atomi de C). În continuare geranilpirofosfatul se condensează cu o nouă moleculă de izopentenilpirofosfat şi rezultă farnezilpirofosfat (15 atomi de C). Prin condensarea reductivă a 2 molecule de farnezilpirofosfat la capetele pirofosfatice rezultă scualen (30 atomi de C).
OH
HOOC CH2 C CH2 CH3
fosfomevalonat kinaza
HOOC CH2
ATP ADP
|
|
|
|
|
|
mevalonatkinaza |
|
|
|
|
|
|
|
|
||||||||||
CH2 |
|
OH |
|
|
|
|
|
|
|
HOOC |
|
|
CH2 |
|
||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
ATP |
ADP |
|
|
|
|
|
|
|
|
|||||||||
OH |
|
|
|
O |
|
O |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
C |
|
CH2 |
|
CH2 |
|
O |
|
P |
|
O |
|
P |
|
OH |
||||||||||
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
CH3 |
|
|
|
OH |
|
OH |
||||||||||||||||||
OH
C CH2 CH2 OPO3H2 CH3
CH3
pirofosfomevalonat kinaza (Mg+)
ATP ADP
|
|
|
|
|
|
|
|
|
|
|
OPO3H2 |
|
|
|
|
|
|
|
O |
|
O |
|
pirofosfomevalonat |
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
HOOC |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
decarboxilaza |
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
C |
|
|
CH2 |
|
|
|
CH2 |
|
|
|
O |
|
|
P |
|
|
O |
|
P |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
+ H PO |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
2 |
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
3 4 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
O |
||||||||||||||||||||
H2C |
|
C |
|
CH2 |
|
CH2 |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
P |
|
O |
|
P |
|
OH |
|
|
|
|
|
|
H3C |
|
C |
|
CH |
|
CH2 |
|
O |
|
P |
|
O |
|
P |
|
OH |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
||||||||||||||||||||||||||||||||||||||
19

Luciana Dobjanschi
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
O |
|
|
|
|
geranilpirofosfat |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
sintetaza |
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
C |
CH2 |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
CH2 |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
P |
|
O |
|
|
P |
|
OH |
+ |
|
|
|
|
|
|
|
P |
|
|
O |
|
|
P |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||
H3C |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2C |
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
OH |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
PP |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C CH2 |
CH2 |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
O |
|
|
|
|
H2C |
|
|
|
|
|
P |
|
O |
|
|
P |
|
OH |
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
C |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
CH2 |
|
O |
|
P |
|
O |
|
P |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
H3C |
|
CH |
|
|
|
|
|
|
CH2 CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
PP |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
geranilpirofosfat |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
farnezilpirofosfat |
|
CH3 |
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
sintetaza |
|
|
|
C |
|
CH2 |
C |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
CH2 O |
|
|
P |
|
|
O |
|
|
|
P |
|
|
|
OH |
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
CH |
|
|
|
|
CH2 |
CH |
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
farnezilpirofosfat |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
2 |
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
C |
CH2 |
C |
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
C |
|
|
|
|
CH2 O |
|
|
|
P |
|
|
O |
|
|
P |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||
|
H3C |
|
|
CH |
|
CH2 CH |
|
|
|
|
CH2 |
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
CH3 |
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
CH |
|
|
|
CH |
|
|
|
CH3 |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
CH CH2 |
|
|
|
|
|
|
CH C CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
C |
CH CH2 CH2 |
C CH CH2 CH2 |
|
CH2 |
CH2 |
C |
2 |
CH2 |
C |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
H3C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
CH3 |
||||||||||||||||||||||
scualen
3. Transformarea scualenului în colesterol
Scualenul în urma ciclizării formează primul sterol, lanosterolul. Înainte de închiderea ciclului, scualenul se hidroxilează în poziţia 3 sub acţiunea unei monooxigenaza formând 2,3-epoxidul scualenului.
19

Biochimie farmaceutică
|
O2 |
|
O |
scualen |
2,3_epoxidulscualenului |
HO
 lanosterolul
lanosterolul
Lanosterolul conţine 3 grupări metil în plus faţă de colesterol. Grupările metil sunt oxidate de către un sistem hidroxilazic microzomal ce necesită O2 şi NADPH şi sunt îndepărtate sub formă de CO2. Compusul rezultat este zimosterolul (C27 ), care diferă de colesterol prin poziţia legăturii duble din nucleul B şi printr-o legătură dublă la catena laterală.
Prin dehidrogenare şi deplasarea dublei legături, zimosterolul trece în 7-dehidrodesmosterol, care este precursorul desmosterolului şi a 7-dehidrocolesterolului, care sunt precursorii colesterolului.
HO |
HO |
HO |
|
|
|
lanosterol |
zimosterol |
7_dehidrodesmosterol |
|
19

Luciana Dobjanschi
HO |
7_dehidrodesmosterol |
|
NADPH +H+ |
||
NADPH +H+ |
||
NADP+ |
NADP+ |
HO7_dehidrocolesterol |
HO |
desmosterol |
|
||
|
+ + |
|
NADPH +H+ |
|
NADPH H |
NADP+ |
|
NADP+ |
HO

 colesterol
colesterol
Reacţiile de transformare ale scualenului în colesterol sunt catalizate de enzime microzomale şi necesită în plus prezenţa a două proteine din faza solubilă a citoplasmei, numite proteine transportoare de scualen, respectiv de steroli. Rolul lor este de a forma complcşi solubili cu sterolii facilitând astfel reacţiile din mediul apos din celulă.
Dacă am face bilanţul biosintezei colesterolului am constata că este un proces consumator de energie şi echivalenţi reducători. Astfel pentru sinteza unui mol de colesterol se consumă 18 moli de acetil-CoA, 16 moli NADPH şi 36 legături macroergice de ATP.
Colesterolul eliberat este utilizat de către celulă, în general, pentru sinteze de membrane, iar în celulele specializate este utilizat şi în alte scopuri: sinteza de acizi biliari în ficat, hormoni steroizi în corticosuprarenală, hormoni sexuali în gonade.
20

Biochimie farmaceutică
Cantitatea de colesterol eliberată de LDL determină viteza metabolismului colesterolului, reglarea la nivel celular, astfel, excesul de colesterol acumulat în celulă acţionează prin 3 mecanisme importante:
1.Înhibă sinteza de novo, adică reduce capacitatea celulei de a sintetiza colesterol, prin înhibarea sintezei enzimei HMGCoA reductaza, în lipsa căruia celula va utiliza numai colesterol extracelular introdus prin receptori.
2.Colesterolul extras din LDL facilitează stocarea lui în celulă prin activarea enzimei acil-colesterol-aciltransferazei(ACAT), care esterifică colesterolul în exces în vederea depunerii lui sub formă de picături în citoplasmă.
3.Acumularea colesterolului înhibă prin mecanism feed-back sinteza de noi receptori pentru LDL. Înhibarea are loc la nivelul biosintezei proteinelor în etapa transcrierii.
Absorbţia şi transportul colesterolului
Colesterolul exogen provine din alimente de natură animală în care se găseşte liber şi esterificat. Raţia zilnică a unui adult conţine 0,6-1,2g colesterol, din care se absoarb 0,3-0,4g/zi. Când concentraţia lui din hrană este mai mică, absorbţia este mai eficientă şi invers. Când se urmăreşte scăderea absorbţiei colesterolului la persoane la persoane cu hipercolesterolemie, se impun restricţii severe, adică o scădere a colesterolului din dietă până la 0,1-0,3g/zi. Spre deosebire de colesterol, sterolii vegetali nu se absorb, ei sunt total excretaţi de lumenul intestinal.
In lumenul intestinal colesterolul din hrană este încorporat în agragate micelare mixte formate din acizi biliari, fosfolipid şi colesterol. Colesterolul esterificat la nivelul micelelor este hidrolizat de către colesterol-esteraza pancreatică, deoarec numai colesterolul liber este absorbit de către celulele mucoasei intestinale. O parte din colesterolul este reexcretat în intestinul subţire şi eliminat prin fecale. Cea mai mare parte din colesterolul absorbit împreună cu cel sintetizat în intestin, se esterifică în celulele mucoasei intestinale sub acţiunea ACAT (acil-colesterol-aciltransferazei), enzimă ce transferă un acid gras activat pe colesterol.
Colesterolul liber şi esterificat este integrat în chilomicroni, lipoproteine mari, încărcate cu trigliceride. Chilomicronii ajung în sânge şi la nivel extrahepatic (ţesut adipos şi muscular) descarcă trigliceridele cu ajutorul lipoprotein-lipazei din endoteliul capilar.
20

Luciana Dobjanschi
Chilomicronii reziduali ce conţin esteri ai colesterolului şi colesterol sunt captaţi de către ficat unde esterii sunt hidrolizaţi.
Ficatul sintetizează probeta-lipoproteinele sau VLDL, care conţin trigliceride şi colesterol esterificat. Când VLDL traversează vasele capilare ale ţesutului adipos şi muscular cedează trigliceridele, iar particulele rămase, de talie mică, ce conţin esteri ai colesterolului sunt aşa-numitele lipoproteine cu densitate intermediară (IDL).
IDL dispar rapid din circulaţie, în aproximativ 2-6 ore de la formarea VLDL, în urma interacţiunii lor cu ficatul. Acesta extrage colesterolul din Idl şi-l utilizează pentru sinteza de VLDL şi acizi biliari. Lipoproteinele Idl care nu sunt utilizate de către ficat rămân în circulaţie şi după un timp apoi se disociază şi devin beta-lipoproteine.
IDL reprezintă fracţiunea care conţine cea mai mare proprţie de colesterol. Transportul colesterolului de la ţesuturile extrahepatice la ficat se face de către α–lipoproteine (HDL), care se sintetizează în ficat şi intestin. La nivelul HDL are loc esterificarea colesterolului din plasmă printr-o reacţie de transesterificare între acidul gras din poziţia 2 a lecitinei şi colesterol. Reacţia este catalizată de LCAT. Esterii colesterolului de pe HDL sunt transferaţi pe LDL, apo pe IDL pentru a fi reciclaţi. HDL sunt apoi catabolizate de către ficat şi intestin. HDL şi LCAT au rolul de a purifica ţesuturile extrahepatice de colesterol.
În final, tot colesterolul este destinat excreţiei în ficat, apoi excretat în bilă, fie ca atare, fie ca acizi biliari.
Concentraţia normală de colesterol plasmatic la adult este în medie de 200mg%. Există variaţii în funcţie de vârstă, sex (mai crescută la bărbaţi decât la femei până la menopauză), în funcţie de alimentaţie şi variază de la un individ la altul.
Aproximativ 65% din colesterolul plasmatic se găseşte sub formă esterificată. Determinările de colesterol se fac άjeun, adică la 12-14 ore de la ultima masă, când în mod normal în plasmă nu există chilomicroni şi există puţine probeta-lipoproteine (VLDL). În aceste condiţii colesterolul este conţinut în cea mai mare parte în fracţiunea LDL şi HDL.
Creşterea colesterolului plasmatic sau hipercolesterolemia apare în diferite boli cum sunt: hipercolesterolemia familială şi aterosclerpoza.
Hipercolesterolemia familială este o boală genetică ce se caracterizează prin creşterea beta-lipoproteinelor şi a colesterolului în plasmă.
Ateroscleroza este o boală ce se caracterizează prin depunerea de colesterol esterificat pe pereţii arterelor sub formă de plăci numite
20

Biochimie farmaceutică
ateroame. Acest fapt duce la îngustarea lumenului capilarelor şi în cele din urmă la apariţia infarctului.
Catabolismul colestrolului
Degradarea nucleului steranic în compuşi simpli nu are loc în organism, el se elimină sub formă de derivaţi ai steranului, inactivi biologic. Astfel, în funcţie de ţesut, colesterolul suferă următoarele transformări:
|
intestin |
steroli neutri |
coprostanol |
|
colestanol |
||
|
ficat |
acizi biliari |
|
colesterol |
|
piele  7- dehidrocolesterol(provitaminaD3)
7- dehidrocolesterol(provitaminaD3)
corticosuprarenale hormoni steroizi
hormoni steroizi
Sterolii neutri
O parte din colesterolul exogen se excretă ca atare prin intestin, fără să fie absorbit. O altă parte se transformă în intestinul gros sub acţiunea florei bacteriene în steroli neutri: coprostanol şi colestanol, care se elimină prin fecale.
Acizii biliari
Formarea acizilor biliari primari are loc în ficat, prin introducerea grupelor hidroxil în molecula colesterolului şi scindarea catenei laterale. În urma acestei transformări (hidroxilare nşi scindarea catenei laterale) rezultă acizii biliari sub formă activată cu CoA şi anume: colil-CoA şi chenodezoxicolil-CoA. Urmează apoi conjugarea cu glicocolul şi taurina cu formarea de acizi biliari primari:
-glicocolic, glicochenodezoxicolic
-taurocolic, taurochenodezoxicolic
Acizii biliari sunt excretaţi în bilă unde datorită mediului alcalin vor forma săruri biliare de Na şi K.
20

Luciana Dobjanschi
OH 
COOH |
COOH |
HO |
OH |
HO |
OH |
acid colic |
|
acid chenodezoxicolic |
|
Din bilă acizii biliari sunt deversaţi în intestin. La nivelul intestinului o parte din acizii biliari primari sunt transformaţi sub acţiunea florei bacteriene în acizi biliari secundari. Aceste transformări constau din conjugarea prin hidroliza glicocolului şi a taurinei şi îndepărtarea grupării OH din poziţia 7. Astfel acidul colic trece în acid dezoxicolic, iar acidul chenodezoxicolic trece în acid litocolic.
|
OH |
COOH |
|
COOH |
|
HO |
7 |
7 |
|
HO |
|
acid dezoxicolic |
acid litocolic |
|
În condiţii normale un om sintetizează 200-500mg acizi acizi biliari pe zi. Rata sintezei este reglată de cantitatea de acizi biliari care se reîntorc din intestin în ficat, pentru a se înlocui pierderile de acizi biliari eliminaţi prin intestin. În acest fel, rezervorul de acizi biliari rămâne constant.
Acizii biliari primari şi secundari din intestin sunt reabsorbiţi în proprţie de 99% şi se reîntorc prin circulaţia portală la ficat. De la ficat sunt reexcretaţi în bilă, apoi în intestin, efectuând aşa-numitul ciclu enterohepatic. În condiţii normale zilnic parcurg acest ciclu 3- 5g acizi biliari din care numai 1% sunt excretaţi prin fecale.
Funcţiile acizilor biliari sunt următoarele:
-Datorită proprietăţilor tensioactive, acizii biliari au rol în emulsionarea grăsimilor la nivelul intestinului, favorizând
20

Biochimie farmaceutică
digestia şi absorbţia lor, precum şi a vitaminelor liposolubile: A, D, E şi K.
-Acizii biliari activează lipaza pancreatică şi colesterolesteraza pancreatică. Deasemenea împreună cu lecitinele contribuie la solubilizarea colesterolului sub formă de micele din bilă.
-Acizii biliari au acţiune coleretică, de stimulare a secreţiei biliare şi acţiune colagogă, de contracţie a vezicii biliare.
Biotransformareacolesterolului în vitamina D3
Colesterolul la nivelul pielii se transformă în 7- dehidrocolesterol sau provitamina D3, care sub acţiunea radiaţiilor UV formează vitamina D3. Vitamina D3 sau colecalciferolul face parte din grupul vitaminelor D, substanţe liposolubile care au acţiune antirahitică la copil şi previn osteomalacia la adult.
Vitamina D se formează prin iradiere cu lumina UV a sterolilor nesaturaţi din plante şi animale. Astfel, din ergosterol rezultă ergocalciferolul sau vitamina D2, iar din 7-dehidrocolesterol rezultă colecalciferol sau vitamina D3.
|
UV |
HO |
HO |
ergosterol |
vitamina D2 |
|
UV |
|
HO |
HO |
|
vitamina D3 |
||
7_dehidrocolesterol |
20

Luciana Dobjanschi
Omul are 2 surse de vitamine: una exogenă din alimente şi una endogenă din fotoliza 7-dehidrocolesterolului din piele.
Vitaminele D2 sau D3 din alimente se absorb la nivelul intestinului sub formă de micele, apoi este transformată în sânge de o globulină specifică şi ajunge la ficat. În ficat vitamina D3 este hidroxilată în poziţia 25 de către o hidroxilază specifică, rezultând calciferol, care este metabolitul principal din circulaţie.
20

Biochimie farmaceutică
XI.8. Acizii graşi esenţiali (AGE)
Importanţa acizilor graşi esenţiali în alimentaţie afost subliniată de la începutul secolului prin experienţe pe animale. Carenţa se manifestă prin tulburări de creştere, reproducere, dermatite, rezistenţa scăzută la stres şi unele deficienţe în transportul lipidelor.
Acizii graşi esenţiali îndeplinesc în organismun rol multiplu, încă incomlet ărecizat. Pe lângă faptul că sunt surse de eicosanoide, ei se găsesc în lipidele structurilor celulare, sunt implicaţi în menţinerea integrităţii membranei mitocondriale. De asemenea ei se găsesc în cantitate mare în organele de reproducere şi intră în structura fosfolipidelor.
Eicosanoidele reprezintă un grup de compuşi ce derivă din acizii graşi eicosanoidici şi cuprind prostanoidele şi leucotrienele (LT). Prostanoidele cuprind la rândul lor: prostagladinele (PG), tromboxanii(TX) şi prostaciclinele (PC).
Biosinteza prostaglandinelor
Prostaglandinele au fost descoperite prima dată în plasma seminală, de unde şi numele, iar ulterior au fost găsite în toate ţesuturile. Prostagalndinele sunt compuşi foarte aczivi biologic, în concentraţie de numai 1 μg/l produc contracţia musculaturii netede.
Din punct de vedere structural, derivă din acizi graşi cu 20 de atomi de carbon, care pot avea în moleculă 3,4 sau 5 duble legături. Din aceşti precursori derivă prostaglandinele primare (seria E, PGE), care prezintă la carbonul C9 o grupare cetonică, iar la carbonul C11 o grupare hidroxilică sau seria F, când au în ambele poziţii C şi C grupări hidroxilice. Prostaglandinele secundare derivă prin modificări enzimatice din prostaglandinele din seria E.
Exemple de prostaglandine naturale:
O |
|
HO |
COOH |
|
COOH |
|
|
|
|
|
|
HO |
|
HO |
OH |
OH |
|
|
|
PGE1 |
|
|
PGF1 |
20

Luciana Dobjanschi
O |
|
HO |
|
COOH |
|
|
COOH |
|
|
|
|
HO |
|
HO |
OH |
|
OH |
PGE2 |
|
PGF2 |
O |
HO |
COOH |
|
||
|
COOH |
|
|
|
|
HO |
HO |
OH |
OH |
|
|
PGE3 |
|
PGF3 |
Cel mai frecvent precursor al prostaglandinelor este acidul arahidinic, care este foarte răspândit în ţesuturi. Acesta sub acţiunea unei ciclooxigenaze se transformă într-un endoperoxid ciclic (PGG2) care este precursorul imediat al prostaglandinelor, tromboxanilor şi al prostaciclinelor.
COOH |
COOH |
|
acid eicosatrienoic |
acid arahidonic |
|
PGE1, PGF1 |
PGE2, PGF2 |
|
COOH |
|
acid eicosapentaenoic |
|
PGE3, PGF3 |
20

Biochimie farmaceutică
Obţinerea prostaglandinelor din acidul arahidonic se face pe calea ciclooxigenazei. Sub influenţa acestei enzime acidul arahidonic se transformă într-un endoperoxid ciclic (PGG2).
fosfolipaza
fosfolipide A2 membranare 
COOH
acid arahidonic
O2  ciclooxigenza
ciclooxigenza
O |
COOH |
|
|
O |
endoperoxid ciclic |
|
OOH PGG2
prostagladinsintetaza
O



 COOH
COOH
HO
OH
PGE2
HO


 COOH
COOH
HO
OH
PGF2
Cicloxigenaza poate să fie înhibată de aspirină şi indometacin, care sunt antiinflamatori nesteroidieni. Blocând ciclooxigenaza,
20

Luciana Dobjanschi
antiinflamatoarele nesteroidiene opresc biosinteza prostaglandinelor, dobândind astfel eficienţa terapeutică în tratamentul proceselor inflamatorii. Acidul arahidonic necesar sintezei prostaglandinelor este rezultat din fosfolipidele membranare sub acţiunea fosfolipazei A2, care poate să fie înhibată de corticosteroizi cu efect antiinflamator.
Tot din acid arahidonic se pot sintetiza şi alte eicosanoide cum ar fi: prostaciclinele, tromboxanii şi leucotrienele.
Schema biosintezei eicosanoizilor
fosfolipide |
|
activata de adrenalina, |
|
|
angiotensina II |
||
lizofosfolipide |
fosfolipaza A2 |
|
|
|
|
inhibata de AINS |
|
|
|
|
|
acid arahidonic |
inhibata de indometacin, |
||
|
|
|
|
|
|
|
aspirina (AINS) |
c.lipooxigenazei |
c.ciclooxigenazei |
|
|
|
|
|
|
LT4 |
|
PG2, PGI2, TX2 |
|
Acţiunea biologică a prostaglandinelor este extrem de complexă. Uneori diferitele prostaglandine au efecte opuse şi din interacţiunea lor rezultă echilibrele biologice ale anumitor funcţiuni ale organismului.
Prostaglandinele acţionează atât asupra adenilatciclazei cât şi asupra guanilatciclazei, influenţând biosinteza AMPc şi GMPc. Prin intermediul acestor mesageri secunzi influenţuază secreţia unor glande endocrine cum sunt: tiroida, suprarenalele, ovarul, paratiroidele. Alţi hormoni cum sunt: bradikinina, acetilcolina, histamina stimulează şi ei sinteza de prostaglandine. Deasemenea o excitare sau o lezare a membranelor celulare declanşează biosinteza de prostaglandine prin eliberarea de acizi graşi nesaturaţi din fosfolipide.
Principalele efecte ale prostaglandinelor sunt: efectul lipolitic, efectul asupra apei şi electroliţilor, de unde decurge intervenţia
21

Biochimie farmaceutică
prostaglandinelor şi asupra metabolismului Ca, stimulând activitatea osteoclastelor şi producând hipercalcemie.
Prostaglandinele influenţează contracţia musculaturii netede, îndeosebi a uterului gravid, precum şi a aparatului respirator şi a tractului gastro-intestinal.
Efectele metabolice multiple ale prostaglandinelor deschid căi variate de utilizare a lor în terapeutică. Astfel sunt utilizate în tratamentul astmului bronşic, a ulcerelor, a bolilor cardiovasculare. Sunt utilizate pentru declanşarea travaliului în sarcinile ajunse la termen. Deasemenea sunt implicate în procesele inflamatorii şi unele medicamente antiinflamatoare nesteroidiene, cum este de exemplu aspirina care îşi datoreză acţiunea farmacodinamică capacităţii lor de a inhiba sinteza prostaglandinelor.
Procesul de degradare a prostaglandinelor se realizează rapid prin oxidare la carbonul 15 şi prin β–oxidarea acidului gras, începând de la capătul ce conţine gruparea carboxilică, -COOH.
21

Luciana Dobjanschi
XI.9. Metabolismul corpilor cetonici
Corpii cetonici sunt produşi în cantităţi mari în ficat, de unde trec prin difuziune în sânge. În anumite condiţii metabolice ficatul produce cantităţi mari de acid acetilacetic şi acid β–hidroxibutiric. Acidul acetilacetic suferă o decarboxilare spontană şi trece în acetonă. Aceşti 3 compuşi sunt cunoscuţi sub denumirea de corpi cetonici.
CH3 |
|
CH3 |
|
|
|
|
CH3 |
|||||||||
|
|
|
|
|
CH |
|
OH |
|||||||||
C |
|
O |
|
C |
|
O |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
+ |
|
CH2 |
||||||||
CH3 |
CO2 |
|
|
2 |
NADH +H+NAD |
|
COOH |
|||||||||
|
|
|||||||||||||||
acetona |
|
|
|
COOH |
|
|||||||||||
|
|
|||||||||||||||
|
acid acetilacetic |
acid betahidroxibutiric |
||||||||||||||
Acidul acetilacetic şi hidroxibutiric sunt în echilibru, acesta fiind controlat de raportul NAD+/NADH din mitocondrie. În sânge raportul acid betahidroxibutiric/acid acetilacetic este cuprins între 1:1 şi 1:10.
Concentraţia normală de corpi cetonici din sânge este de sub 1mg%, iar eliminarea lor prin urină este de sub 1mg/24 de ore. Cantităţi peste valorile normale în sânge (cetonemia) şi eliminarea lor în urină (cetonuria) reprezintă o stare cunoscută sub numele de cetoză. Condiţia de cetoză este asociată cu deplasarea hidraţilor de carbon utilizabili, cuplată cu mobilizarea acizilor graşi liberi. Deoarece acidul acetilacetic are caracter acid pronunţat, excreţia prin urină poate duce la la cetoacidoză, care poate să fie fatală într-un diabet netratat.
În vivo, ficatul pare să fie singurul organ care produce cantitîţi semnificative de corpi cetonici, iar ţesuturile extrahepatice le utilizează ca substrate respiratorii. Fluxul de corpi cetonici de la ficat spre ţesuturile extrahepatice se datoreşte unui mecanism enzimatic de producere în ficat, cuplat cu o activitate scăzută a enzimelor responsabile în utilizarea lor; în schimb în ţesuturile extrahepatice situaţia se inversează. Enzimele responsabile de formarea corpilor cetonici sunt localizate în mitocondrie.
Substratul cetogenezei este acidul acetilacetic, care rezultă din fragmentul C4 terminal rezultat prin oxidarea acizilor graşi în ficat,
21

Biochimie farmaceutică
fie prin reversarea reacţiei catalizată de tiolază. Dezactivarea acetoacetil-CoA la acetoacetat se poate realiza pe două căi.
Prima cale este deacilarea acetoacetil-CoA în prezenţa acetoacetil-CoA deacilazei, conform reacţiei:
H3C |
|
CO |
|
CH2 |
|
CO SCoA |
|
H3C |
|
CO |
|
CH2 |
|
COOH |
|
|
|
|
|
|
|||||||||
|
|
|
|
CoASH
A doua cale este aceea prin care are loc condensarea unei molecule de acetoacetil-CoA cu o moleculă de acetil-CoA cu formare de β–hidroxi-β-metilglutarilCoA, catalizată de HMG-CoA sintetaza. Acesta este scindat în prezenţa β–hidroxi-β-metilglutaril-CoA liazei mitocondriale cu formare de acetoacetat.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HMG_CoA |
|
|
OH |
||||||||
|
H3C |
|
CO |
|
CH2 |
|
CO SCoA +H3C |
|
CO SCoAsintetaza |
|
H3C |
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
C |
|
CH2 |
|
CO SCoA |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
HMG_CoA |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
COOH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
liaza |
H3C |
|
CO |
|
CH2 |
|
COOH + H3C |
|
CO SCoA |
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
Ambele enzime sunt localizate în mitocondriile hepatice, locul de formarea a corpilor cetonici. Acetoacetatul format poate fi transformat în beta-hidroxibutirat în prezenţa beta-hidroxibutirat- dehidrogenazei.
Ficatul dispune de echipamentul enzimatic necesar sintezei corpilor cetonici, dar nu dispune de cel necesar în reactivarea lor pentru a putea fi metabolizaţi. Acest proces are loc în ţesuturile extrahepatice şi se poate realiza pe două căi.
Una din căi presupune reacţia acetoacetatuluicu succinil-CoA în prezenţa succinil-CoA-acetoacetat-CoA transferazei.
CH |
COOH |
CH3 |
|
COOH |
||||||||
|
3 |
transferaza C |
|
O |
+ |
|
CH2 |
|||||
|
|
|
|
|
|
|
|
|||||
C |
|
O |
+ |
CH2 |
||||||||
|
|
|||||||||||
|
|
|||||||||||
|
|
|||||||||||
|
|
|
|
|
|
CH2 |
||||||
|
|
|
|
|
||||||||
CH |
CH |
CH |
|
|||||||||
|
2 |
|
|
|
||||||||
|
2 |
|
2 |
|
|
|
|
SCoA |
|
COOH |
||
|
COOH |
|
CO SCoA |
|
CO |
|
||||||
Cea de-a doua cale activează acetoacetatul în prezenţă de ATP şi CoA şi acetoacetatkinază.
21

Luciana Dobjanschi
CH |
|
|
|
|
|
|
CH3 |
||||||
|
|
3 |
|
|
|
|
|
|
|
|
|||
C |
|
|
O |
|
|
tiokinaza |
|
C |
|
O |
|||
|
|
|
|
||||||||||
|
|
|
|
|
|
||||||||
|
|
|
|
|
|||||||||
|
|
|
|
|
+ |
ATP |
+ CoASH |
|
|
|
|
|
|
|
CH2 |
||||||||||||
CH |
|
|
|||||||||||
|
|||||||||||||
|
|
2 |
|
|
AMP +PP |
|
|
|
|
||||
|
|
|
|
|
|
|
|||||||
|
|
COOH |
|
|
|
CO SCoA |
|||||||
În mod normal corpii cetonici sintetizaţi în ficat reprezintă substrate uşor metabolizabile pentru ţesuturile extrahepatice unde sunt scindaţi în acetil-CoA în prezenţa tiolazei şi oxidaţi prin ciclul citric. Oxidarea corpilor cetonici în ţesuturile extrahepatice se face proprţional cu concentraţia lor în sânge. Pânp la o concentraţie de 70mg% ei sunt oxidaţi, peste această valoare, capacitatea oxidativă a sistemului de degradare este depăşită, concentraţia va creşte şi vor fi eliminaţi prin urină.
21

Biochimie farmaceutică
XII. Metabolismul proteinelor
XII.1. Digestia şi absorbţia proteinelor
Majoritatea compuşilor cu azot ingeraţi de om sunt proteine. Deci, atunci când discutăm digestia proteinelor, implicit discutăm şi digestia compuşilor cu azot. Moleculele proteice intacte nu pot fi absorbite ca atare prin tractul gastro-intestinal la animalele adulte, decât în cazuri excepţionale şi foarte rare. Pentru a putea fi absorbite proteinele sunt hidrolizate la structuri cu molecule mai mici de aminoacizi sau peptide mici. Cu toate că proteinele au structuri complexe, ele sunt formate de un număr redus de aminoacizi (cca. 20) diferiţi, legaţi între ei prin legături peptidice. Legătura peptidică se rupe uşor conducând la un amestec de aminoacizi liberi. Teoretic, o singură enzimă specifică poate asigura scindarea legăturilor peptidice şi deci digestia proteinelor. În realitate situaţia este mai complexă, deoarece enzimele digestive prezintă a mare specificitate pentru localizarea respectivei polipeptide, localizarea punctului de hidroliză şi natura aminoacizilor, care intervin în legătura peptidică respectivă.
Cu toate că în alimentaţie există în mod obişnuit milioane de proteine, el pot fi digerate de un număr redus de enzime proteolitice, ce pot fi clasificate în 2 mari grupe: exopeptidaze şi endopeptidaze.
Exopeptidazele au rolul de a îndepărta un aminoacid de la capătul lanţului prin hidroliza unei legături peptidice cu obţinerea unui aminoacid şi a unei polipeptide cu un aminoacid mai puţin în moleculă. De exemplu: carboxipeptidaza, aminopeptidaza, dipeptidaza, tripeptidaza.
Endopeptidazele au rolul de a hidroliza în general legături peptidice din interiorul lanţului, dând naştere unor lanţuri polipeptidice mai mici. De exemplu: pepsina, tripsina, chimotripsina, elastina.
Proteinele pătrunse în tractul digestiv suferă acţiunea diferitelor enzime degradându-se până la stadiul de aminoacizi, care la rândul lor sunt apoi catabolizaţi pe căi diferite.
O enzimă deosebit de importantă pentru laboratorul clinic, din categoria N-aminoacidpetidazelor este LAP (leucinaminopeptidaza). Nivelul acestei enzime creşte mult şi specific în afecţiunile căilor biliare, dar rămâne nemodificatîn leziunile parenchimului hepatic. Deasemenea are valoare în diagnosticul diferenţial al icterului
21

Luciana Dobjanschi
mecanic faţă de cel hepatocelular şi cel hemolitic. În ultimele 2 forme de icter, nivelul rămâne cel normal.
Schema degradării proteinelor
Proteine alimentare
endopeptidaze: pepsina, tripsina, chimotripsina oligopetide
exopeptidaze: N- aminoacidpeptidaza, C- aminoacidpeptidaza
aminoacizi si oligopeptide
Ficat 

tesut enterohepatic - aminoacizii
 catabolizati
catabolizati
 utilizati in biosinteza proteinel catabolizati
utilizati in biosinteza proteinel catabolizati
 utilizati in biosinteza proteinelor
utilizati in biosinteza proteinelor
21

Biochimie farmaceutică
XII.2. Metabolismul intermediar al aminoacizilor
Aminoacizii sunt substanţele cele mai importante ale metabolismului azotului în organismele heterotrofe. Deasemenea ei pot servi ca sursă de energie în special prin intermediul oxidării scheletului hidrocarbonat. Metabolismul aminoacizilor se găseşte într-o stare dinamică, la fel ca şi cel al hidraţilor de carbon şi al lipidelor.
Metabolismul aminoacizilor include câteva probleme de interes medical. Acestea ar fi: sinteza şi degradarea proteinelor, conversia scheletului hidrocarbonat al aminoacizilor în intermediari amfibolici, sinteza ureei şi formarea unor compuşi fiziologici activi( adrenalina, noradrenalina, DOPA, dopamina, serotonina, acidul-γ-aminobutiric sau GABA, tirozina, creatina, creatinina, nucleul heminic, bazele purinice.
Catabolismul N-aminoacidic
Cei cca 20 de aminoacizi care intră în structura proteinelor prezintă pe de o parte mecanisme specifice de metabolizare, ier pe de altă parte mecanisme comune.
Căile comune de degradare se referă pe de o parte la soarta grupărilor funcţionale, aminice şi carboxilice, iar pe de altă parte la soarta catenelor ternare, care în aceste etape trec prin transformări comune. Principalele mecanisme generale de transformare ale aminoacizilor sunt:
-transaminarea
-decarboxilarea
-dezaminarea aminoacizilor
Transaminarea
În cel puţin 12 aminoacizi gruparea α-aminică este îndepărtată enzimatic prin transaminare. În aceste reacţii, gruparea α-aminică este transferată pe atomul de carbon α al unui α–cetoacid, care, de obicei este acidul α–cetoglutaric cu formarea α–cetoacidului analog aminoacidului iniţial şi a acidului L-glutamic.
21

Luciana Dobjanschi
HOOC |
|
|
CH2 |
|
|
CH |
|
|
|
COOH |
+ |
HOOC |
|
CH |
|
CH |
|
|
C |
|
COOH |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
HOOC |
|
|
CH |
|
C |
|
COOH + HOOC |
|
|
CH |
|
|
CH |
|
|
CH |
|
COOH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
2 |
2 |
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Enzimele care catalizează acest tip de reacţii se numesc aminotransferaze sau tranaminaze. Cele mai multe transaminaze folosesc ca acceptor de grupare aminică α-cetoglutaratul, fiind astfel specifice pentru substratul α-cetoglutarat-L-glutamat. Specificitatea pentru donorul de grupări aminice este mai puţin strictă, decât cea pentru acceptorul de grupări aminice. Totuşi, enzimele manifestă anumite preferinţe şi, astfel anumiţi aminoacizi sunt transaminaţi mai rapid decât alţii.
De exemplu: aspartat transaminaza catalizează reacţia dintre acid aspartic şi acid α-cetoglutaric cu formare de acid oxalilacetic şi acid L-glutamic.
Această enzimă are activitate mai mare atunci când donorul de grupări aminice este acidul L-aspartic, dar poate fi folosită şi pentru alţi aminoacizi ca şi donori.
Ţesuturile animale mai conţin pe lângă aspartat-transaminază şi alte transaminze, ce folosesc tot α-cetoglutaratul ca acceptor de grupări aminice ca : alanin-transaminaza, leucin-transaminaza, tirozin-transaminaza, ce catalizează următoarele reacţii:
H3C |
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
COOH + HOOC |
|
|
|
CH2 |
|
|
CH2 |
C |
|
|
|
COOH |
alanin_tr |
ansaminaza |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
C |
|
|
|
|
|
|
COOH + HOOC |
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
|
CH |
|
|
|
COOH |
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH le |
ucin_tr |
ansaminaza |
|||||||||||||||||||||
H3C |
|
|
CH |
|
CH2 |
|
|
|
CH |
|
|
|
|
|
COOH + HOOC |
|
CH2 |
|
|
|
CH2 |
|
|
C |
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
COOH |
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
|
CH |
|
|
|
|
CH2 |
|
|
|
C |
|
|
|
|
COOH + |
HOOC |
|
|
|
CH2 |
|
|
|
|
CH2 |
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
HO |
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
COOH tirozin_tranaminaza |
||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
+ HOOC |
|
CH2 |
CH2 |
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
CH |
|
|
COOH |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
C |
|
|
|
|
|
COOH + |
HOOC |
|
|
|
CH2 |
|
|
CH2 |
|
|
|||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
21

Biochimie farmaceutică
Reacţiile de transaminare sunt uşor reversibile, ele se pot desfăşura în ambele direcţii. Glutamatul, produsul final al majorităţii transaminărilor, cedează apoi gruparea aminică într-o serie de reacţii final, ce duc la formarea compuşilor azotaţi de excreţie.
Tranasaminazele se găsesc atât în mitocondriile, cât şi în citossolul celulelor eucariote. La mamifere, aspartat transaminaza din citosol catalizează reacţiile de transaminare a diferiţilor aminoacizi cu formarea glutamatului. Glutamatul format intră apoi în matricea mitocondrială, printr-un sistem specific de transport prin membrană. Aici, glutamatul este fie dezaminat direct, fie cedează gruparea aminică osalilacetatului, într-o reacţie catalizată de aspartat transaminaza mitocondrială, cu formarea aspartatului, donorul imediat de grupări aminice în sinteza ureei.
Transaminazele au drept coenzimă piridoxalfosfatul, care poate fixa aminoacidul formând o cetimină sau baza Schiff, cu următoarea structură:
H
RC COOH N
C O
HO

 CH2 O P O-
CH2 O P O-
O-
H3C N
Hidrogenul de la Cα este eliberat ca proton, ceea ce conduce la restructurarea moleculei, cu deplasarea dublei legături şi a centrului nucleofil la C unde se fixează protonul. Acest produs este tot o bază Schiff, care prin hidroliză eliberează un cetoacid şi piridoxalfosfatul, care reintră într-un nou ciclu de reacţii. Procesulare loc în felul următor:
21

Luciana Dobjanschi
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H+ |
|
R |
|
|
C |
|
COOH |
|
|
|
|
|
|
||||||||||||||
R |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
C |
|
COOH |
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
C |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
O |
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
|
|
|
|
O |
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
HO |
|
C |
|
|
|
|
|
O |
|
HO |
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
CH2 |
|
O |
|
P |
|
O- |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
CH2 |
|
O |
|
P |
|
O- |
|
|
|
|
|
|
|
|
CH2 |
|
O |
|
P |
|
O- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
- |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|||
H3C |
|
N |
|
|
|
|
|
O- |
|
H3C |
|
|
|
N |
|
|
|
|
|
|
O- |
H3C |
|
|
N |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
RC COOH N
|
|
|
|
|
O |
|
R |
|
|
C |
|
COOH |
|
|
|
|
|
|
||||||||||
HO |
|
CH2 |
|
|
H2O |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
CH2 |
|
O |
|
P |
|
O- |
|
|
O |
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
H3C |
N |
|
|
O- |
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
CH2 |
|
|
O |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
O |
|
P |
|
O- |
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C |
|
|
|
N |
|
|
O- |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
Piridoxal-fosfatul, legat foarte strâns, dar nu covalent de proteina enzimatică este transportorul de grupări aminice. În cursul ciclului său catalitic el suferă tranziţii reversibile între forma sa liberă de aldehidă (piridoxal-fosfatul) şi forma sa aminată (piridoaminfosfatul). Schema completă cu cei doi timpi ai procesului de transaminare este următoarea:
I.
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
E |
|
CH |
|
NH + R |
|
|
|
C |
|
COOH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
R CH |
COOH |
|
|
|
|
|
|
|
|
R CH |
|
COOH |
|
R1 C COOH |
|
|
2 |
2 |
1 |
|
|
|
|
|
|||||||||||||||||||
1 |
|
|
|
|
+ E C |
O |
1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O piridoxamin_ |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
NH2 |
|
|
|
|
|
|
|
H2O |
|
|
N |
|
|
|
|
|
N |
|
|
|
|
O |
||||||||||||||||||
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
piridoxal_fosfat_ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
_fosfat_enzima |
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
C |
|
|
H |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
enzima |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
EE
aldimina |
cetimina |
22
Biochimie farmaceutică
II.
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
R2 |
|
C |
|
COOH + E |
|
CH2 |
|
NH2 |
|
R2 |
|
C |
|
COOH |
|
R2 |
|
|
CH |
|
COOH |
|
R2 |
|
CH |
COOH + E |
|
CH |
|
O |
|||||
|
|
|
|
|
|
|
|
H2O |
|
NH2 |
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
piridoxal_fosfat_ |
||||||||||
|
|
O |
piridoxamin_fosfat_ H2O |
|
|
N |
|
|
|
N |
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
_enzima |
|||||||||||||||||
|
|
|
|
|
_enzima |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
E |
|
|
|
E |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
cetimina |
|
aldimina |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
Piridoxal-fosfatul format poate să reintre într-un nou ciclu de transformări. Reacţia de transaminare este un exemplu de dublă dislocare, cu cinetica ping-pong corepsunzătoare.
În enzima liberă, piridoxal-fosfatul se leagă de proteina enzimatică nu numai prin azotul din ciclu, ci şi prin formarea unei baze Schiff cu gruaparea ε-amino a unei lizine din proteină. Aminoacidul substrat dislocă gruparea lizil-ε-amino din legătura cu piridoxal-fosfatul, formând o aldimină substrat-piridoxal fosfat.
Acidul glutamic, drept colector universal de grupări aminice joacă un rol central în metabolismulaminoacizilor din două puncte de vedere. Acesta poate prelua direct sau indirect grupările aminice de la majoritatea aminoacizilor şi poate regenera, prin dezaminarea oxidativă acidul α-cetoglutaric, care devine apt să accepte grupările aminice.
Exemplu:
aminoacid |
alfa_cetoglutarat |
|
+ ++ NH |
|
NADH H |
3 |
|||
transaminaza |
glutamat dehidrogenaza |
|
||
cetoacid |
glutamat |
+ |
H O |
|
|
NAD + |
2 |
|
|
22

Luciana Dobjanschi
Dezaminarea oxidativă
Glutamatul format sub acţiunea transaminazelor poate fi rapid dezaminat oxidativ sub acţiunea glutamat dehidrogenazei, o piridinenzimă prezentă atât în citosol, cât şi în mitocondriile hepatocitului.
HOOC |
|
CH2 |
|
CH2 |
|
|
CH |
|
COOH+ NAD+(NADP+)+H2O |
|
HOOC |
|
CH2 |
|
CH2 |
|
C |
|
COOH+ NH4++ NADH(NADPH) |
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Grupările aminice colectate de la diferiţi aminoacizi de către glutamat sunt descărcate sub formă de ioni de NH4+ . În această reacţie are loc şi o dehidrogenare. Se presupune că dehidrogenarea glutamatului are loc în două etape: în prima etapă se formează α- iminoglutaratul, care în a 2-etapă este hidrolizat la cetoacid.
HOOC |
|
|
CH2 |
|
|
CH2 |
|
|
|
CH |
|
COOH+NAD+ |
|
|
HOOC |
|
|
CH2 |
|
|
CH2 |
|
|
C |
|
|
COOH+NADH+H+ |
||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
|
|
CH |
|
CH |
|
C |
|
COOH+NH3 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
HOOC |
|
CH2 |
CH2 |
|
C COOH+H2O |
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
2 |
|
2 |
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
||||||||||||
Enzima care catalizează această reacţie se numeşte L-glutamat dehidrogenaza. Aceasta poate folosi ca acceptor de electroni atât NAD+ cât şi NADP+, preferat fiind NAD+. NADH –ul format este oxidat în lanţul transportor de electroni. L-glutamat dehidrogenaza are un rol cheie în dezaminarea aminoacizilor. Este o enzimă allosterică, înhibată de ATP, GTP şi NADH şi stimulată de ADP, GDP.
Multe oerganisme conţin aminoacid oxidaze flavindependente, care şi ele catalizează dezaminarea oxidativă a aminoacizilor. L-aminoacid axidaza este specifică pentru dezaminarea L-aminoacizilor şi catalizează reacţia:
L- aminoacid + H2O+ E- FMN cetoacid +NH3 +E_FMNH2
cetoacid +NH3 +E_FMNH2
22

Biochimie farmaceutică
L-amionoacidoxidaza are ca grupare prostetică FMN strâns legată de proteina enzimatică. Se găseşte în reticulul endoplasmatic din ficat şi rinichi.
O altă flavoproteină ce catalizează dezaminarea oxidativă este D-aminoacid oxidaza, prezentă în ficat şi rinichi, care oxideazp D- aminoacizii la α-cetoacizii corespunzători.
|
|
E_FADH |
|
D- aminoacid + H O + E- FAD |
cetoacid + NH3 + |
2 |
|
2 |
|
|
|
Rolul D-aminoacidoxidazei este de a iniţia degradarea D- aminoacizii proveniţi din degradarea enzimatică a peptidoglicanilor din pereţii celulari ai bacteriilor intestinale, care conţin acid D- glutamic şi alţi D-aminoacizi.
Formel reduse al L- şi D-aminoacidoxidazelor pot reacţiona direct cu O2 formând H2O2 şi regenerând enzimele sub forma lor oxidată.
E_FMNH2+ O2  E_FMN +H2O2
E_FMN +H2O2
E_FADH2 +O2  E_FAD +H2O2
E_FAD +H2O2
Apa oxigenată formată este descompusă de catalază la apă şi oxigen molecular.
H2O2 H2O + 1/2O2
H2O + 1/2O2
În celulele eucariote, L-şi D-aminoacidoxidazele precum şi uratoxidaza sunt localizate în microcorpi. Tot în aceste organite se găseşte şi catalza. Din acest motiv organitele repective se mai numesc şi peroxizomi.
Decarboxilarea aminoacizilor
Un alt mecanism de degradare a aminoacizilor îl constituie decarboxilarea sub acţiunea aminoaciddecarboxilazelor, acăror coenzimă este piridoxal-fosfatul. În urma procesului de decarboxilare se formează aminele primare corespunzătoare, numite şi amine biogene.
22

Luciana Dobjanschi
|
|
|
|
|
|
aminoacid |
|
|
|
|
|
|
|
|
|
|
decarboxilaza |
|
|
|
|
R |
CH NH2 |
R |
|
CH |
|
NH |
||||
|
|
|
|
|
|
CO2 |
2 |
2 |
||
|
|
|
COOH |
|
|
|
|
|||
Pentru ca reacţia să aibă loc, şi în acest se formează o bază Sciff între aminoacid şi piridoxal-fosfat. Deplasările electronilor spre N piridinic labilizaează legătura dintre Cα şi gruparea carboxilică. Are loc eliberarea unei molecule de CO2 urmată de hidroliza bazei Schiff astfel rezultate. Din hidroliză rezultă piridoxalfosfatul şi se pune în libertate amina respectivă.
Mecanismul reacţiei este următorul:
R |
|
CH2 |
|
|
|
CH |
|
|
|
COOH + HO |
|
|
|
OH |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
P |
|
|
O |
|
|
CH2 |
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
|
CH2 |
C |
|
H |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
C |
N+ |
H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
P |
|
|
O |
|
|
CH2 |
|
|
|
|
|
|
|
|
|
O- |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
.. |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
CH3 |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
HO |
|
|
|
OH |
|
|
|
|
|
|
|
|
|
CH |
|
|
O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
P |
|
O |
|
|
CH2 |
|
|
|
|
|
|
|
|
OH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
N |
|
CH3 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
R |
CH2 |
CH C |
O |
O |
|
|
O- |
|||
|
OH |
H |
C |
N+ H |
CO2 |
|
CH |
|
|
|
|
||
|
HO P O CH2 |
|
O- |
|
||
|
O- |
|
|
|||
+N |
CH3 |
O |
|
+N |
CH3 |
|
|
|
|
||||
|
|
H |
|
|||
H |
|
|
|
|
|
|
RCH2 CH2
|
|
|
|
|
|
H |
|
|
N+ |
|
|
OH |
|
|
C |
H |
|||
HO |
|
|
|
|
|
|
|
|
|
|
P |
|
O |
|
CH2 |
|
|
O- |
|
|
|
|
|
|
|||||
ON  CH3
CH3
+R CH2 CH2 NH3+
22

Biochimie farmaceutică
Exemple de reacţii de decarboxilare:
N |
CH |
CH |
NH |
|
|
N |
CH |
CH |
NH |
|
|
2 |
|
2 |
|
|
2 |
2 |
2 |
||
|
N |
|
COOH |
CO2 |
N |
|
|
|||
|
|
|
|
|
|
|||||
|
H |
|
|
|
H |
|
|
|||
histidina |
|
|
|
|
|
histamina |
|
|
||
H2C CH COOH |
|
H2C |
CH2 |
NH2 |
|
|
||||
|
OH NH |
|
CO2 |
|
OH |
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
||
serina |
|
|
|
|
colamina |
|
|
|
||
|
CH2 |
CH |
COOH |
HO |
|
CH2 CH |
COOH |
HO |
CH2 CH2 |
NH2 |
|
O2 |
|
|
|||||||
|
N |
NH2 |
hidroxilaza |
N |
NH2 |
|
N |
|
|
|
|
|
|
CO2 |
|
|
|||||
|
H |
|
|
|
H |
|
H |
|
|
|
serotonina
Din decarboxilarea histidinei, triptofanului, 5- hidroxitriptofanului, tirozinei rezultă histamina, triptamina, serotonina şi tiramina cu rol de hormoni tisulari. Din decarboxilarea treoninei, cisteinei şi acidului aspartic rezultă propanolamina, cisteamina, β-alanina, care intră în structura cobalaminei şi CoA. Din decarboxilarea acidului glutamic se formează acidul γ-aminobutiric, important pentru metabolismul ţesutului nervos; iar din decarboxilarea aminoacizilor bazici ca: lizina, ornitina, arginina rezultă cadaverina, putresceina, care sunt produşi de putrefacţie.
XII.3. Metabolismul amoniacului
22

Luciana Dobjanschi
Formarea şi eliminarea amoniacului
În afara amoniacului care apare în ţesuturi ca rezultat al metabolismului aminoacizilor (dezaminarea oxidativă), o cantitate considerabilă se mai formează din proteinele alimentare sub acţiunea bacteriilor intestinale şi din ureea prezentă în lichidele secretate din tractul gastro-intestinal. Acest amoniac este absorbit din intestin în sângele portal venos, care conţine cantităţi mai mari de amoniac decât sângele sistemic. În condiţii normale, ficatul îndepărtează prompt amoniacul din sângele portal, astfel încât sângele ce părăseşte ficatul, este în mod virtual liber de amoniac. Acest lucru este esenţial deoarece cantităţi mici de amoniac sunt toxice pentru sistemul nervos (normal în sânge se găsesc 10-20μg NH3 /100ml).
Simptomele intoxicaţiei cu amoniac sunt rezultatul unei slăbiri ale funcţiilor creierului şi se manifestă prin greaţă şi vărsături, letargie, ataxie, convulsii, iar în cazuri mai grave comă prin hiperamoniemie (cc 100μg NH3 /100 ml) şi chiar moartea. Aceste simptome sunt asemănătoare comei hepatice, când nivelul amoniacului din ficat şi probabil din creier este foarte crescut. Intoxicaţia cu amoniac pare să fie un factor etiologic în coma hepatică. Simptome asemănătoare apar şi în hepatomegalie şi în general, când funcţiile hepatice sunt puternic alterate, deoarece ficatul este sediul transformării amoniacului în uree.
Mecanismul prin care amoniacul îşi exercită efectul asupra creierului nu se cunoaşte încă. SE presupune că se datoreşte descreşterii formării de ATP pe calea ciclului citric din cauza transformării unei cantităţi excesive de α-cetoglutarat în glutamat şi glutamină. Nivelul acestor metaboliţi, la fel ca şi a amoniacului este crescut în creier în decursul intoxicaţiei cu amoniac. Alterări ale proceselor de transmisie neurală datorită unor formări excesive de acid γ-aminobutiric (GABA) din glutamat pot fi, deasemenea implicate.
Conţinutul de amoniac din sângele din venele renale, mai mare decât în arterele renale, indică faptul că amoniacul este produs în rinichi şi apoi trece în sânge. Excreţia în urină a amoniacului produs în celulele tubilor renali constituie cel mai semnificativ aspect al metabolismului amoniacului renal. Producerea de amoniac este un mecanism important al tubilor renali, de reglare a balanţei acidobazice şi conservare de cationi, fiind foarte crescut în acidoza metabolică şi scăzut în alcaloză.
22

Biochimie farmaceutică
Amoniacul produs la nivelul rinichilor derivă din aminoacizii intracelulari şi în special din glutamină. Eliberarea de amoniac este catalizată de glutaminaza renală, conform reacţiei:
H2N |
|
C |
|
CH2 |
|
CH2 |
|
|
CH |
|
COOH |
glutaminaza |
HOOC |
|
CH2 |
|
CH2 |
|
|
CH |
|
COOH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
H2O NH3 |
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||||
|
O |
NH2 |
|
|
|
|
|
|
|
|
|||||||||||||||
glutamina |
|
|
|
|
|
|
|
acid glutamic |
|||||||||||||||||
Amoniacul poate fi excretat sub formă de săruri de amoniu. Marea majoritate este excretată sub formă de uree, care se formează în ciclul ureogenetic. Practic amoniacul format în ţesuturi, dar prezent în sângeleperiferic în urme, este îndepărtat rapid din circulaţie sub formă de glutamină şi uree.
Formarea de glutamină este catalizată de glutamin-sintetază, enzimă prezentă în cantităţi mari în ţesutul renal.
|
|
|
|
|
|
|
|
|
ATP |
ADP +Pa |
|
|
|
|
|
|
|
|
|
|
|
|
||
HOOC |
|
CH2 |
|
CH2 |
|
CH |
|
COOH |
|
|
|
H2N |
|
C |
|
CH2 |
|
CH2 |
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
NH3 |
H2O |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
NH2 |
|
O |
|
NH2 |
||||||||||||||
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
glutamin_sintataza |
|
|
|
|
|
|
|
|
|
|
|
|
|||
acid glutamic |
|
|
|
|
glutamina |
|
|
|
|
|||||||||||||||
La animale, plante şi microbi există o reacţie catalizată de L- asparaginază, analoagă celei catalizate de glutaminază la om. Asparaginaza şi glutaminaza sunt utilizate ca agenţi antitumorali, deoarece tumorile necesită cantităţi mari de acid aspartic şi acid glutamic.
În timp ce la nivelul creierului calea majoră de îndepărtare a amoniacului este formarea glutaminei, în ficat calea majoră o constituie transformarea în uree.
Un adult cu o activitate normală, moderată excretă zilnic 16,5g azot. Din acesta 95% se elimină prin rinichi, iar 5% este stocat şi apoi eliminat prin fecale. Ureea constituie 80-90% din azotul excretat.
Interconversia amoniacului şi a glutaminei, catalizată de glutaminsintetază şi glutaminază, poate fi prezentată schematic astfel:
22

Luciana Dobjanschi
acid glutamic +Mg_ATP Mg_ADP



 glutamin sintetaza
glutamin sintetaza
NH + |
H2N |
|
C |
|
CH2 |
|
CH2 |
|
CH |
|
COOH |
||
|
|
|
|
|
|||||||||
4 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
NH2 |
|||||||





 glutaminaza
glutaminaza
acid glutamic 



 H2O
H2O
XII.4. Ciclul ureogenetic
22

Biochimie farmaceutică
În cursul reacţiilor ce alcătuiesc un ciclu complet dintr-un mol de amoniac rezultă un mol de uree şi se consumă 3 moli de ATP. Reacţiile succesive sunt catalizate de 5 enzime.
Carbamoil sintetaza prezentă în mitocondriile hepatice ale organismelor ureotelice, inclusiv organismul uman, catlizează sinteza carbamoilfosfatului cu consum de 2 moli de ATP.
|
|
Mg+2 |
|
|
O |
|
|
|
|
|
|
|||
NH3 + CO2 |
+ 2AT P |
HO |
|
|
|
|
|
|
|
|
|
|
NH2 + 2ADP +Pa |
|
|
P |
|
O |
|
C |
|
||||||||
|
|
|
|
|
||||||||||
|
carbamoil |
|
|
|
|
|
|
|
|
|
|
|
||
|
sintetaza |
OH |
|
O |
|
|
||||||||
Ornitincarbamoilaza se găseşte în mitocondriile hepatice şi catalizează reacţia de sinteză a citrulinei, pentru care are o mare specificitate.
CH2 |
|
|
NH2 |
|
|
O |
|
|
|
|
|
|
|
|
CH2 |
|
|
NH |
|
C |
|
NH2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
||||
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
+ H3PO4 |
|||||||
|
|
|
|
+ |
HO |
|
P |
|
O |
|
C |
|
NH2 |
|
|
CH2 |
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
ornitin |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
carbamoilaza |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
CH |
|
|
NH2 |
|
OH |
|
|
O |
|
CH |
|
|
NH2 |
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|||||||||||
ornitina |
|
|
|
|
|
|
|
|
|
|
|
|
citrulina |
|
|
|||||||||||||
În continuare citrulina în prezenţă de arginino-succinat- sintetaza formează arginino-succinatul.
|
CH2 |
|
|
NH |
|
C |
|
NH2 |
COOH |
||||
|
|
|
|
|
|||||||||
|
CH2 |
|
|
|
|
|
|
|
H2N |
|
|
|
|
|
|
|
|
|
|
CH |
|||||||
|
|
|
|
|
O |
|
|
||||||
|
|
|
|
|
|||||||||
|
CH2 |
|
|
|
|
|
|
+ |
|
|
|
||
|
|
|
|
|
|
|
|
|
CH2 |
||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
CH |
|
|
NH2 |
|
|
|
COOH |
|||||
|
|
|
|
|
|
||||||||
|
COOH |
|
|
|
|||||||||
|
|
|
|
|
|
||||||||
citrulina |
|
acid aspartic |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
CH2 |
|
|
NH |
|
C |
|
N |
|
|
|
||
ATP AMP+PP |
|
|
|
|
|
|
CH |
|||||||||
|
|
|
|
|
||||||||||||
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||
|
CH2 |
|
|
|
NH2 |
|
|
CH2 |
||||||||
|
|
|
|
|
|
|
|
|
||||||||
|
H2O |
|
CH2 |
|
|
|
|
|
|
|
|
|
COOH |
|||
arginino_succinat |
CH |
|
NH2 |
|
|
|
||||||||||
|
|
|
|
|||||||||||||
sintetaza |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
COOH |
|
|
|
|||||||||||||
|
|
|
|
|
|
|||||||||||
argininosuccinat
Mai departe, argininosuccinaza, prezentă în ţesutul hepatic şi renal al mamiferelor catalizează reacţia de scindare a
22

Luciana Dobjanschi
argininosuccinatului în arginină şi acid fumaric, care intră în ciclul citric.
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
CH2 |
|
|
NH |
|
C |
|
NH |
|
HOOC |
|
|
CH |
|||||
|
CH2 |
|
|
NH |
|
C |
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
CH2 |
|
NH2 |
|
|
|
|
|
|
|
||||||||||||||||||||||
CH2 |
|
NH2 |
|
|
CH2 |
|
|
|
|
|
|
+ |
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
arginino |
|
HC COOH |
|||||||||||||||||||||||||||||||
|
CH2 |
|
|
|
|
|
|
|
|
COOH |
|
CH2 |
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
succinaza |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
CH |
|
NH2 |
|
|
|
|
|
|
CH |
|
|
NH2 |
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
COOH |
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
||||||||||||||||||
argininosuccinat |
|
|
|
|
|
arginina |
|
acid fumaric |
|||||||||||||||||||||||||
În continuare acidul fumaric intră în ciclul citric şi va suferi o transformare obişnuită, adică în prezenţă de fumarază trece în acid malic, care la rândul său sub acţiunea malatdehidrogenazei trece în oxalilacetat. Oxalilacetatul intră într-o reacţie de transaminare la care participă acidul glutamic şi transaminaza glutamicooxalacetică(GOT), formţnd acidul aspartic.
H |
|
|
C |
|
|
COOH |
|
COOH |
malat |
|
|
COOH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
fumaraza |
|
CH |
|
OH dehidrogenaza |
C |
|
O |
|||||||||
|
|
|
|
|
|
|
||||||||||||||
|
||||||||||||||||||||
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|||
HOOC |
|
|
|
|
|
|
|
|
|
H2O |
CH2 |
|
NAD+ |
NADH+H+ |
|
|||||
|
|
C |
|
|
|
H |
|
|
|
|||||||||||
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
COOH |
||||
acid fumaric |
|
acid malic |
|
|
|
acid oxalilacetic |
||||||||||||||
COOH |
|
COOH |
COOH |
|
|
|
COOH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
GOT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
NH2 |
|
|
CH |
|||||||||
C |
|
O |
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
||||||||||||
|
+ |
|
CH2 |
|
|
|
|
|
+ |
|
|
|
2 |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
CH2 |
|
|
CH2 |
|||||||||||
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
CH2 |
|
CH2 |
|
|
|
|||||||||||||
|
|
|
COOH |
|
C |
|
O |
||||||||||||
COOH |
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
CH |
|
NH2 |
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
COOH |
||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
Deasemenea arginina formată este scindată de arginază (enzimă prezentă în ficatul tuturor organismelor ureotelice) la ornitină şi uree. Arginaza se găseşte în cantităţi mici şi în rinichi, creier, glanda mamară, ţesut testicular şi piele. Emzima poate fi înhibată competitiv de ornitină şi lizină.
23

Biochimie farmaceutică
|
CH2 |
|
|
|
NH |
|
C |
|
NH |
|
|
|
CH2 |
|
|
NH2 |
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
NH2 |
arginaza |
|
|
|
|
|
H2N |
|
C |
|
NH2 |
||||||||||
|
|
|
|
|
CH2 |
|
|
|
+ |
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
CH2 |
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
NH2 |
|
|
|
|
H2O |
CH |
|
|
|
|
O |
|||||||||||
CH |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|||||||||
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
arginina |
|
|
|
|
|
|
|
|
|
ornitina |
|
uree |
|
|
|
|
||||||||||
Ornitina rezultată poate să reia un nou ciclu, iar ureea formată este excretată urinar.
Deci, ciclul ureogenetic este o cale metabolică foarte costisitoare pentru organism, deoarece pentru fiecare moleculă de uree ce se formează se consumă 3 legături macroergice.
Cantitatea de uree excretată de un adult normal prin urină este de 25-30g în 24 de ore. Această cantitate reprezintă 90% din substanţele azotate şi variază proporţional cu cantitatea de proteină ingerată.
În condiţii normale excreţia de amoniac reprezintă numai de 2,5-4,5% din totalul azotului urinar. Excreţia amoniacului reprezintă o funcţie importantă în menţinerea balanţei acido-bazice. Amoniacul se formează la nivelul rinichilor unde se combină cu ionii de hidrogen formând ioni de amoniu. Conţinutul său creşte în acidoză şi scade în alcaloză.
Ureogeneza este un proces semiciclic deoarece ornitina consumată în reacţia 2 este regăsită în ultima reacţie.
Boli metabolice legate de dereglări apărute în ciclul ureogenetic
Lipsa uneia dintre enzimele care intervin în ciclul ureogenetic determină apariţia unor afecţiuni, care toate sunt cauzate de intoxicaţia cu amoniac. Acesta nu se mai poate transforma în uree, produs netoxic care se elimină.
Deficitul de carbamoilfosfatsintetază este probabil ereditar şi cauzează hiperamoniemia de tip 1.
Deficitul de transcarbamoilază duce la apariţia enzimopatiilor congenitale. Boala se numeşte hiperamoniemie de tip II. În aceste cazuri în sânge, lichid cerebrospinal şi urină s-au găsit cantităţi mari de glutamină, iar în ţesuturi cantităţi mari de amoniac.
Lipsa activităţii argininosuccinat-sintetazei duce la citrilinemie, o boală foarte rară. În sângele şi în lichidul cerebrospinal
23

Luciana Dobjanschi
al pacienţilor se găsesc cantităţi mari de citrulină, iar în urină eliminarea este masivă (1-2g citrulină/24 de ore).
Absenţa argininosuccinazei duce la argininosuccinurie. Enzima este absentă în creier, ficat, rinichi, eritrocite şi fibroblastele din piele.
Absenţa arginazei conduce la hiperargininemie. Aceasta se caracterizează prin creşterea nivelului de arginină în sânge şi în lichid cerebrospinal. Arginaza cerebrospinală nu este întotdeauna absentă, uneori este mai scăzută.
XII.5. Utilizarea scheletului de atomi de carbon ai aminoacizilor
Aminoacizii sunt utilizaţialături de glucide şi lipide la acoperirea necesităţilor energetice ale organismelor animale. În condiţiile unei alimentaţii echilibrate şi în stare noemală, organismul uman îşi procură cel mult 10% din necesarul de energie prin degradarea aminoacizilor.
Pentru producerea de energie, scheletul de atomi de carbon al aminoacizilor este degradat oxidativ la CO2 şi H2O. S-a constatat că atomii de carbon din scheletul aminoacizilor se regăsesc nu numai în CO2 ci şi în strucrura glucozei şi lipidelor sintetizate endogen. Aminoacizii din care se sintetizează glucoză se numesc glucogeni, iar cei din care se sintetizează lipide se numesc cetogeni. Unii aminoacizi sunt atât glucogenici cât şi cetogenici.
Atât în vederea utilizării pentru producerea de energie cât şi pentru sinteza de lipide şi glucoză, aminoacizii sunt transformaţi pe căi mai simple sau mai complexe în intermediari ai ciclulu Krebs sau în compuşi aflaţi în strânsă legătură cu acest ciclu: oxalilacetat, α- cetoglutarat, succinil-CoA, fumarat, piruvat, acetil-CoA.
În cazul unora dintre aminoacizi există căi specifice de trecere apre 2 dintre compuşii menţionaţi: triptofanul la acetil-CoA şi acetoacetil-CoA, tirozina la fumarat şi acetoacetil-CoA.
23

Biochimie farmaceutică
Schema generală de metabolizare a scheletului de atomi de C ai aminoacizilor
Ala, Gly, Cys,
Ser, T hr Try, Leu, Lys,
Phe, Tyr
acid piruvic |
acetoacetilCoA |
|
|
|
|
|
|
Ile, Leu, Try |
acetilCoA |
|
|
Asp, Asn |
acid oxalilacetic |
acid citric |
|
|
|
||
|
|
acid izocitric |
|
acid malic |
acid alfacetoglutaric |
Gln, Glu, His, |
|
|
|
|
Pro, Arg |
Tyr, Phe |
acid fumaric |
succinilCoA |
Ile, Met,Thr,Val |
|
|||
acid succinnic
Defecte în metabolizarea aminoacizilor
În legătură cu metabolismul aminonoacizilor sunt descrise mai multe afecţiuni cauzate în principal de defecte la sinteza unor enzime cheie.
Exemplu:
Fenilcetonuria apare atunci când lipseşte fenilalaninhidroxilaza. Fenilalanina nu se mai poate transforma în tirozină şi astfel se transformă în acid acid fenil-piruvic acid fenil-lactic, toxici pentru creiercare se elimină parţial prin urină.
Alcaptonuria apare datorită absenţei homogentizatoxidazei. Aceasta duce la pigmentarea anormală a ţesutului conjunctiv, datorită unui pigment negru ce se formează la nivelul ţesutului conjunctiv.
Albinismul apare prin lipsa tirozinazei, enzimă ce iniţiază oxidarea tirozinei pentru formarea pigmenţilor melaninici. Astfel pielea şi părul sunt decolorate.
Histidinemia apare datorită lipsei enzimei histidin-amonio- liazei. Histidina se elimină parţial prin urină, parţial se transformă în acid imidazol-piruvic. Acestea duc la întârzierea dezvoltării generale şi a vorbirii.
23

Luciana Dobjanschi
Cistinuria apare datorită unei reabsorbţii tubulare defectuoase a cistinei, ceea ce determină eliminarea ei în cantităţi mari prin urină. Fiind puţin solubilă, cistina formează calculi.
23

Biochimie farmaceutică
XII.6. Biosinteza aminoacizilor
Dintre aminoacizii cunoscuţi numai un număr de 20 prezintă importanţă pentru biosinteza proteinelor. Unele forme de viată (plante, bacterii) sunt capabile să sintetizeze toţi cei 20 de aminoacizi din intermediari amfibolici. Altele, inclusiv mamiferele şi în special omul, pot sintetiza numai o parte din ei, care au fost numiţi aminoacizi neesenţiali. Cei ce nu pot fi sintetizaţi şi care trebuie suplimentaţi prin dietă sunt numiţi aminoacizi esenţiali.
Exemplu:
Aminoacizi esenţiali: arginina, histidina, izoleucina, leucina, lizina, metionina, fenilalanina, treonina, triptofan, valina.
Aminoacizi neesenţiali: alanina, asparagina, acid aspartic, cisteina, acid glutamic, glutamina, glicina, hidroxiprolina, prolina, serina, tirizina.
Sinteza de aminoacizi neesenţiali din intermediari amfibolici
Alanina se sintetizează din acid piruvic printr-o reacţie de transaminare.
H3C |
|
C |
|
COOH |
transaminaza |
|
|
|
|
|
|||||
|
|
|
|
|
H3C |
|
|
CH |
|
COOH |
|||||
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
Glu(Asp) |
|
|
|
|
|
|||||
|
O |
|
KG |
|
NH2 |
||||||||||
Acidul glutamic se formează din acid α-cetoglutaric printr-o reacţie catalizată de L-glutamat dehidrogenază.
COOH |
L_glutamat |
COOH |
||
C O |
CH NH2 |
|||
dehidrogenaza |
||||
(CH2)2 |
+ H O |
(CH2)2 |
||
|
NH4 |
2 |
COOH |
|
COOH |
NADPH +H+ |
NADP+ |
||
|
|
|
||
Acidul aspartic se sintetizează din acid oxalilacetic prin reacţia de transaminare.
23

Luciana Dobjanschi
COOH |
transaminaza |
|
COOH |
|||||||||
|
|
|
|
|
CH |
|
NH2 |
|||||
C |
|
O |
||||||||||
|
|
|
||||||||||
|
||||||||||||
|
|
|||||||||||
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
CH2 |
||
|
CH2 |
Glu KG |
|
|||||||||
|
COOH |
|
|
|
|
|
|
COOH |
||||
Glutamina se sintetizează printr-o reacţie catalizată de către glutaminsintetază, plecând de la acid L-glutamic. Reacţia necesită ATP ca şi donor de energie.
COOH |
glutaminsintetaza |
COOH |
|||||||||||
CH |
|
NH2 |
|
|
|
|
NH2 |
||||||
|
CH |
|
|||||||||||
|
|
|
|||||||||||
|
|||||||||||||
|
|
|
|
+ NH4+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Mg+2 |
(CH2)2 |
||||||||
(CH2)2 |
|||||||||||||
ATP |
ADP +P |
|
|
CONH2 |
|||||||||
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
||||
COOH |
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|||||
Asparagina se sintetizează printr-o reacţie similară plecând de la acid L- aspartic sub acţiunea aparaginsintetazei ATP trece, în acest caz la AMP şi PP.
COOH |
|
|
|
|
COOH |
|||||
|
|
|
||||||||
CH NH asparaginsintetaza |
|
|
|
|
||||||
CH |
|
NH2 |
||||||||
|
||||||||||
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
||||
|
CH2 |
|
|
|
||||||
|
|
|
|
CONH2 |
||||||
|
COOH |
|
|
|
||||||
|
|
|
|
|
|
|
|
|||
În cazul serinei, în ţesutul mamiferelor coexistă două căi de biosinteză. În ambele cazuri punctul de plecare în sinteză este acidul 3-fosfogliceric, intermediar din glicoliză.
23

Biochimie farmaceutică
|
CH2 |
|
OPO3H2 |
|
|
|
|
|
CH2 |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
OH |
|
|
|
|
CH2 |
|
|
OH |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
CH |
|
OH |
|
|
|
|
CH |
|
|
OH |
|
|
|
|
|
|
|
|
|
|
C |
|
O |
|
|
|
|
|
C |
|
|
O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
H2O |
P |
|
|
|
|
|
|
|
|
|
+ |
NADH |
+ |
+ |
|
|
|
|
|
|
|
|
|
|
AA KA |
|
COOH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
COOH |
|
|
|
COOH NAD |
|
H |
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
CH2 |
|
OPO3H2 |
|
|
|
|
|
CH2 |
|
|
OPO3H2 |
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
C |
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
KA |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
NAD+ NADH +H+ |
|
|
|
AA |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
COOH |
|
|
|
|
H2O |
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
Calea prin intermediul derivaţilor fosforilaţi necesită în prima etapă o dehidrogenază, apoi o transaminază şi o fosforilază. Calea prin intermediari nefosforilaţi, necesită o fosfatază şi o transaminază.
Sinteza glicinei în ţesutul mamiferelor poate să se facă pe mai multe căi. În citosolul hepatic se găseşte glicintransaminaza care transformă acidul glioxilic şi acizii glutamic şi aspartic în glicină.
La mamifere există două căi importante de sinteză a glicinei, una plecând de la colină şi alta de la serină.
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
colinoxidaza |
|
|
|
|
|
|
|
|
|
|
|
|
|
betainaldehid |
|
+ |
|
|
|
||||||||
|
(H3C)3N |
+ |
|
CH2 |
|
CH2OH |
(H3C)3N |
+ |
CH2 |
|
|
CHO |
dehidrogenaza |
|
(H3C)3N |
CH2 |
|
COOH |
|||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
colina |
|
2[H] |
betainaldehida |
|
|
|
|
|
NAD+ NADH +H+ |
betaina |
|||||||||||||||||||||||||||||||||
transmetilare |
|
|
dimetilglicinoxidaza H C |
|
|
NH |
|
CH |
|
COOH |
sarcozinoxidaza |
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
(H3C)2N CH2 COOH |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
3 |
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
|
|
CH3 |
dimetiglicina |
|
|
|
CH2O |
|
|
|
|
|
|
|
|
sarcozina |
CH2O |
||||||||||||||||||||||||||||
|
|
|
|
|
|
HOH2C |
|
|
|
CH |
|
|
COOH |
|
|
|
|
H2N |
|
CH2 |
|
COOH |
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
H4 folat |
Metilen H4 folat |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
În cea de a doua cale serina suferă o reacţie de hidroximetilare în prezenţa tetrahidrofolatului.
Sinteza de aminoacizi neesenţiali din alţi aminoacizi neesenţiali
La mamifere prolina se sintetizează pornind de la acid glutamic printr-o serie de reacţii reversibilecare sunt utilizate şi în catabolismul prolinei.
23

Luciana Dobjanschi
|
|
H2C |
|
|
|
CH2 |
|
|
|
|
|
|
|
|
H2C |
|
|
|
CH2 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HO |
|
C |
|
|
|
CH |
|
COOH |
|
|
|
|
|
|
|
CH |
CH |
|
COOH |
|||||||
|
|
|
|
|
NADH + H+ |
NAD+ |
|
|
||||||||||||||||||
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
O |
|
NH2 |
|
|
|
|
|
|
|
|
O |
NH2 |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
COOH |
|||
|
|
H2O |
|
|
|
|
N |
|
+ H+NAD+ |
|
N |
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
NADH |
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
||
Hidroxiprolina se sintetizează din prolină prin acţiunea prolin hidroxilazei. Reacţia necesită oxigen molecular, Fe+2 şi vitamina C.
|
|
HO |
|
N |
COOH |
N |
COOH |
|
|
||
H |
|
H |
|
Sinteza de aminoacizi neesenţiali care iau naştere din aminoacizi esenţiali
23

Biochimie farmaceutică
Cisteina se sintetizează din L-serină şi homocisteină, care provin ca intermediari în metabolizarea metioninei.
|
|
CH2 |
|
|
SH |
HO |
|
|
|
CH2 |
|
|
|
|
|
CH2 |
|
|
|
|
S |
|
|
|
CH2 |
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2 |
|
|
|
|
|
|
|
CH |
|
NH2 |
||||||||||||||||
CH2 |
+ |
|
|
|
|
CH |
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
COOH |
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
||||||||||||||
|
|
CH |
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
L_serina |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
COOH |
|
|
|
COOH |
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
L_homocisteina |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
cistationina |
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
HO |
|
CH2 |
|
CH2 |
|
|
CH |
|
COOH + |
HS |
|
CH2 |
|
|
|
CH |
|
|
|
COOH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
H2O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
L_homoserina |
|
|
|
L_cisteina |
|
|
|
|
|
||||||||||||||||||||||||
Tirozina se sintetizează din fenilalanină sub acţiunea fenilalanin hidroxilazei. Reacţia este ireversibilă şi necesită prezenşa de NADPH, oxigen molecular şi tetrahidrobiopterina.
|
|
|
|
|
fenilalaninhidroxilaza |
HO |
|
|
|
|
|
|
|
CH2 |
|
|
CH |
|
COOH |
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
CH2 |
|
CH |
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
I |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
NH2 |
H4 biopterina |
|
|
|
|
|
|
|
|
|
|
|
NH2 |
||||||
|
|
|
H2 biopterina |
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
II |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NADP+ |
NADPH +H+ |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Complexul fenilalanin hidroxilazei prezintă două activitaţi distincte:
1 – reducerea oxigenului molecular la apă şi a fenilalaninei la tirozină 2 – reducerea dihidrobiopterinei la tetrahidrobiopterină pe socoteala NADPH.
La fel ca şi prolina hidroxilizina este prezentă în fibra de colagen. Hidroxilizina este, însă, absentă din aproape toate proteinele mamiferelor, provine din lizina alimentară prin hidroxilare, dar numai după încorporarea lizinei în legătura peptidică, analog formării hidroxiprolinei din prolină. Enzima care catalizează această reacţie este lizinhidroxilaza.
XIII. Metabolismul nucleotidelor
23

Luciana Dobjanschi
Nucleotidele ocupă un loc central în procesele biochimice, deoarece ele sunt:
-precursori în biosinteza acizilor nucleici
-principalele rezervoare de legături macroergice
-componenţi ai mai multor coenzime
-efectori allosterici.
ARN din diferite celule şi clase este continuu hidrolizat la nucleotide şi resintetizat după necesităţi în toate celulele. Procesul este mai rapide în acele celulel sau organe în care eliminarea de secreţii bogate în proteine sau restructurarea diferitelor căi metabolice necesită o biosinteză proteică activă: glandele digestive exocrine şi ficat. Unele tipuri de celulle au o viaţă relativ scurtă (celulele epidermei mucoasei intestinale, celulele sanguine), în cazul lor fiind supus unui proces asemănător şi ADN, evident la nivelul întregului organism.
Transformările metabolice ale nucleotidelor libere formează o schemă unitară în care biosinteza este corelată cu biodegradarea la diferite nivele prin circuite de recuperare. În acest sens se pot face următoarele precizări generale, şi anume:
1.Nucleotidele sunt constant degradate până la nucleozide şi apoi la bazele azotate corespunzătoare şi ribozo-1-fosfat )sau dezoxiribozo-5-fosfat)
2.Nucleozidele, bazele azotate şi ribozofosfatul pot fi reutilizate în căi de recuperare pentru resinteză de nucleotide
3.O parte din bazele purinice sunt catabolizate până la acid uric care se elimină, iar cele pirimidinice până la intermediari metabolici din alte căi.
4.ribozofosfatul poate fi utilizat în calea pentozofosfatului
5.Nucleotidele pot fi sintetizate de novo pornind de la intermediari simpli anumiţi aminoacizi (glicocol, acid aspartic, glutamina), dioxid de carbon şi grupări C1 activate (legate de acizi tetrahidrofolici).
6.Reutilizarea bazelor şi biosinteza lor de novo sunt controlate prin disponibilitatea formei activate a ribozo-5-fosfatului cum ar fi 5-ribozo-α -D-ribozil pirofosfat (PRPP); enzima care-l formează PRPPsintetaza (sau ATP fosforil transferaza) este activată de fosfatul anorganic şi înhibată allosteric de nucleotide, asigurând concentraţia lor constantă.
24

Biochimie farmaceutică
Hidroliza acizilor nucleici
Lanţurile lungi a acizilor nucleici sunt hidrolizate de către nucleaze în fragmente scurte. Ele sunt, în general, de două tipuri:
I.Exonucleazele care desfac succesiv nucleotidele de la una din capete, fiind 5’ sau 3’specifice şi necesită un anumit mod de terminare (cu sau fără fosfat) a
capătului atacant.
II.Endonucleazele care desfac legăturile situate în interiorul lanţului formând astfel lanţuri oligonucleotidice. Sunt cunoscute numeroase enzime de acest tip cu localizări şi roluri diferite. Acţiunea lor poate specifică pentru un anumit de acid nucleic (ADN sau ARN) sau nespecifică hidrolizându-le pe amândouă. Specificitatea poate privi şi alte aspecte cum ar fi existenţa ADN ca moleculă dublu sau monolanţ, mai ales pentru unele exonucleaze, recunoaşterea unui anumit nucleotid dintre cele două
sunt unite prin legătura atacată (unele exndonucleaze) sau a unei secvenţe întregi de nucleotide din vecinătate (enzime de restricţie). Nucleazele intervin în digestia acizilor nucleici din alimente sau în prelucrarea şi distrugerea acizilor nucleici endogeni (cu numeroase aspecte).
Digestia acizilor nucleici are loc în duoden. Sub acţiunea endonucleazelor pancreatice (ribonucleaza şi dezoxiribonucleaza) se eliberează oligonucleotide din care diesterazele intestinului subţire eliberează 5’ şi 3’ nucleotide.
24

Luciana Dobjanschi
Lanturi polinucleotidice
 H2O ribonucleazadezoxiribonucleaza
H2O ribonucleazadezoxiribonucleaza
Oligonucleotide + Nucleotide

 H2O fosfodiesteraze
H2O fosfodiesteraze
5'_Nucleotide
H2O nucleotidaza
 P fosfomonoesteraze
P fosfomonoesteraze
Nucleozide
P |
|
|
|
|
nucleozidfosforilaze |
|
|||
R1_P |
|
R5_P |
|
Calea |
|
||||
|
|
|||
|
||||
|
|
|||
(dR1_P) |
(dR5_P) |
pentozofosfatulu |
||
Baze purinice
Baze pirimidinice
Catabolismul general al nucleotidelor la baze purinice şi pirimidinice
Nucleotidele sunt hidrolizate specific de către 5’-nucleozide şi fosfat. Există o mare varietate de asemenea enzime, unele secretate de mucoasa intestinală cu rol în digestie, altele în general răspâdite în organism cu localizare pe membrana periplasmatică, în lizozomi, microzomi sau citoplasmă, care intervin în metabolismul nucleotidelor endogene. Membrana perplasmatică este impermeabilă pentru nucleotide dar permite pătrunderea nucleozidelor. Ecto-5’- nucleotidaza fixată pe faţa externă a plasmei dă posibilitatea utilzării nucleotidelor, extracelulare (mai ales a AMP) hidrolizându-le vectorial la nucleozide (adenozină). În hematii există o 5’- nucleotidază specifică pentru nucleotidele pirimidinice.
Cea mai mare parte din adenozin-5’- monofosfat este catabolizat printr-o dezaminare la inozin-5’ - monofosfat.
Adenilat deaminaza are mai multe izoenzime, una din ele fiind abundentă în muşchi. Aşa cum se va vedea IMP este primul
24

Biochimie farmaceutică
nucleotid purinic format prin sinteza de novo şi prezintă un punct de încrucişare între căile catabolice şi cele anabolice.
Adenozina care rezultă din restul AMP-ului este, la rândul ei, dezaminată de către adenozin deaminază la inozină. O mare parte de adenozină provine în urma hidrolizei S-adenozilhomocisteinei (SAH), formată din S-adenozilmetionină în urma procesului de metilare. Un caz particular îl prezintă celulele musculare ale miocardului. Ele sunt lipsite de adenilatdeaminază iar AMP produs, în urma contracţiei, este fie hidrolizat la adenozină, care se eliberează în sânge, fie refosforilat până la ATP. Ajungând până la arterele coronare, adenozina cauzează vasodilatţia şi consecutiv creşterea debitului circulator. Deoarece producerea adenozinei creşte proprţional cu hipoxia, efectul ai primeşte semnificaţia unei autoreglări a fluxului sanguin în funcţie de necesităţile miocardului.
Desfacerea nucleozidelor poate decurge pe două tipuri de acţiuni enzimatice şi anume hidrolitică şi fosforolitică. Nucleotidazele, într-o reacţie ireversibilă, hidrolizează nuclozidele la baze purinice şi pirimidinice şi riboză (sau dezoxiriboză).
Nucleozida + |
nucleozidaza |
purinica |
|
Baza |
|
+ Riboza(dezoxiriboz |
|
H2O |
|
pirimidinica |
|
|
|
|
Astfel de enzime sunt răspândite în diferite ţesuturi fără a se cunoaşte numărul şi specificitatea lor exactă. Nucleozifosforilazele scindează cu ajutorul fosfatului anorganic şi eliberează din nucleozide bazele azotate şi ribozo-1-fosfat (sau dezoxiribozo+1+fosfat). Există nucleozid fosforilaze specifice pentru purine şi pentru pirimidine. Purinucleozid fosforilazele nu pot folosi ca substrat adenozina. Din acest motiv este necesar ca AMP şi adenozina să fie în prealabil dezaminate.
Acţiunea acestor fosforilaze este reversibilă, ele putând servi şi în biosinteză, deşi sensul fiziologic este catabolic.
purin_pirimidin |
purinica |
|
|
|
||
nucleozifosforilaza |
|
|
|
|||
Nucleozida + fosfat |
|
baza |
|
+R _P(dR _P) |
||
|
|
|||||
|
|
pirimidinica |
1 |
1 |
||
|
|
|
|
|
||
În digestie se absorb nucleozide, catabolizate în interiorul celulelor intestinale ca produşi finali. Din acest motiv majoritatea bazelor azotate din nucleotidele alimentare nu pot fi utilizate de către organismul uman.
24

Luciana Dobjanschi
Catabolismul bazelor purinice
Din catabolismul nucleotidelor purinice rezultă două baze azotate principale: hipoxantina (din inozină) şi guanina (din guanizină). Ele sunt oxidate mai departe până la acid uric, produs final de catabolism la om, primate, păsări şi unele reptile.
Guanina este dezaminată, în prealabil, până la xantină de către o xantioxidază sau o xantindehidrogenază.
În mod normal, în celule, se formează foarte puţină adenină liberă, provenind din fosforilarea 5’-metioninadenozinei. Adenina nu poate fi catabolizată direct organismul uman fiind lipsit de adenindeaminază, prezentă doar la bacterii şi nevertebrate, care s-o transforme în hipoxantină. Cea mai mare parte din adenină este utilizată în căile de recuperare. În cazul unor deficite enzimatice ereditare sau în aportul alimentar crescut, excesul de adenină este oxidat de către xantinoxidază la 8-hidroxixantină şi apoi la 2,8- dihidroxiadenină, substanţă puţin solubilă, care formează calculi renali.
|
OH |
|
|
|
|
|
OH |
|
|
|
|
N |
|
N |
fosfomonoesteraza |
|
N |
N |
purin_nucleozid |
||||
H N |
N |
N |
H2N |
N |
N |
||||||
fosforilaza |
|||||||||||
2 |
|
|
|
|
|
HO H2C O |
|
|
|
||
-2O3PO H2C O |
|
H2O |
P |
|
|
P |
R_1_P |
||||
|
OHOH |
|
|
|
|
OHOH |
|
|
|||
guanizin_5'_fosfat |
|
|
|
|
guanizina |
|
|
||||
|
OH |
|
|
O |
|
|
|
O |
|
|
|
|
|
|
|
|
|
HN |
|
N |
|||
N |
|
N |
|
HN |
N |
|
guanaza |
|
|||
|
|
|
|
|
|||||||
|
|
|
|
O |
N |
|
N |
||||
|
|
N |
|
N |
N |
|
|
||||
H2N |
N |
H2N |
|
|
H |
||||||
H |
|
H |
|
|
H |
|
|
||||
xantina
guanina
24

Biochimie farmaceutică
OH |
|
|
|
|
OH |
|
|
||
N |
N |
fosfomonoesteraza |
N |
N |
purin_nucleozid |
||||
N |
N |
N |
N |
||||||
|
|
|
fosforilaza |
||||||
-2O3PO H2C O |
|
H2O |
P |
|
HO H2C O |
P |
R_1_P |
||
OHOH |
|
|
|
OHOH |
|
|
|||
inozin_5'_fosfat |
|
O |
|
inozina |
O |
|
|||
OH |
|
|
|
|
|
|
|||
|
|
|
NAD+ |
NADH +H+ HN |
N |
||||
N |
N |
|
HN |
N |
|||||
|
|
|
H2O2 O |
N |
N |
||||
|
N |
|
N |
N |
H2O +O2 |
||||
N |
|
H |
|||||||
H |
|
|
H |
|
|
H |
|
||
hipoxantina |
xantina |
|
În organismul uman xantinoxidaza se găseşte mai ales în mucoasa intestinală şi în ficat, restul organelor prezentând doar urme de activitate. În consecinţă purinele din alimente formează direct acid uric, iar sursa majoră de acid uric endogen este ficatul. O parte din acidul uric este excretat în intestin prin bilă. În general acidul uric din organismul uman (în jur de 1,2g) provine din trei surse principale:
1.din nucleotidele alimentare
2.catabolismul purinelor endogene
3.transformarea directă a IMP sintetizat de novo
Concentraţia normală de acid uric în ser este ceva mai mare la
bărbaţi (6,9-7,5mg/dl) decâţ la femei (5,7-6,6 mg/dl). Hiperurinemii apar în guta primară şi secundară, hipouricemii în deficienţele de xantinoxidază ereditară sau în cadrul unei insuficienţe hepatice. Eliminarea urinară este ăntre 400 şi 800 mg/24 ore variind şi în funcţie de alimentaţie. Rinichiul uman elimină acidul uric într-un proces destul de complicat. La nivelul glomerulilor este filtrat, apoi reabsorbit în tubii contorţi distali. O serie de medicamente interferează cu aceste procese renale.
24

Luciana Dobjanschi
|
O |
|
H2O +O2 |
H2O2 |
|
O |
H |
|
|
|
|
|
|||
|
HN |
N |
|
HN |
N |
||
|
|
|
|
O |
|||
|
|
|
|
|
|
|
|
O |
N |
N |
|
|
O |
N |
N |
H |
NAD+ |
NADH +H+ |
|
H |
H |
||
|
H |
|
|
|
|||
|
xantina |
|
|
|
|
acid uric |
|
|
|
|
|
|
|
|
În afara semnificaţiei sale de produs final al catabolismului purinic, acidul uric serveşte pentru eliberarea amoniacului la păsări şi unele reptile, fiind puţin solubile acestea se elimină sub formă de pastă economisindu-se apă. Astfel de animale se numesc uricotelice şi nu posedă enzimele necesare formării de uree.
Mamiferele, cu excepţia primatelor, descompun în continuare acidul uric în prezenţă de uricază la alantoină pe care o elimină prin urină. La alte specii degradarea merge mai departe prin acţiunea alantoinazei la acid alantoic, sau continuă datorită alantoicazei până la uree şi acid glioxilic. Deci, flora intestinală descompune ureea cu ureează la dioxid de carbon şi amoniac, la unele nevertebrate.
|
O |
H |
|
|
|
H2N |
O |
|
|
|
|
|
|
|
|
uricaza |
|
|
|
NH |
|
|
|||
|
HN |
N |
|
|
|
|
|
alantoinaza |
||||
|
O |
|
O |
|
|
|
|
O |
||||
|
|
|
N |
N |
|
|
|
|||||
O |
N |
N |
|
O2 CO2 |
|
|
H2O |
|
||||
|
H |
H |
H2O |
|
H2O2 |
H |
H |
|
|
|
||
|
acid uric |
|
|
alantoina |
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
COOHNH |
|
H2N |
|
|
+ |
|
NH2 |
COOH |
|
|
|
|
|
2 |
alantoicaza |
|
|
|
|
+ |
CHO |
|
|
O |
|
|
O |
O |
|
|
|
|
|||
|
N |
N |
H2O |
NH2 |
|
H2N |
O |
acid glioxilic |
||||
|
|
|
|
|||||||||
|
|
H |
H |
|
ureea |
|
|
|||||
|
|
acid alantoic |
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
ureaza |
|
|
|
|
|
|
|
|
|
2 |
(CO |
2 |
+ NH ) |
|
|
|
|
|
|
|
|
|
|
2 |
3 |
|
|
||
24

Biochimie farmaceutică
La om se elimină prin urină în mod normal şi cantităţi mici de hipoxantină, xantină şi adenină. Bazele purinice minore, de exemplu, 7-metilguanina, nu pot fi catabolizate şi se elimină ca atare.
Biosinteza de novo a nucleotidelor purinice
Nucleotidele purinice pot fi sintetizate în citoplasmă printr-o succesiune de 10 reacţii enzimatice, heterociclul bazei fiind construit direct din robozo-5-fosfat.
Primul compus purinic format este un nucleotid, acidul inozinic (IMP), nu o purină liberă.
1. Prima etapă este catalizată de o aminotransferază care trece gruparea aminică a glutaminei pe PRPP (fosforibozopirofosfat) pentru a forma fosforibozil amina. Enzima are proprietăţi allosterice şi este etapa principală de reglare a biosintezei de novo.
O |
|
|
|
|
O |
|
O |
|
|
O |
|
|
|
|
|
|||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
P |
|
H C |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
2 O O |
|
P |
|
O |
|
P |
|
OH aminotransferaza HO |
P |
|
H2C |
|
|
NH2 |
|||||||||||
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
OH |
|
|
|
|
|
|
|
|
O |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
OH |
OH |
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Gln +H O |
Glu +PP |
|
|
|
|
|
|
|
|
||
|
|
|
|
OH |
|
OH |
2 |
|
|
|
OH |
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
OH |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
2. În a doua etapă prin hidroliza ATP se asigură energia necesară condensării glicocolului cu fosforibozilaminpentru a da fosforibozil-glicinamida, sub acţiunea unei sintetaze. Reacţia este reversibilă dar produsul reacţiei este îndepărtat în mod continuu deplasând echilibrul.
24

Luciana Dobjanschi
|
O |
|
|
|
|
|
|
|
|
|
|
|
HO |
O |
|
OC |
CH2 |
|
NH2 |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HO |
P |
|
H C |
O NH2 |
|
|
|
|
|
sintetaza |
P |
|
H2C |
O NH |
|||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
+HOOC |
|
CH2 |
|
NH2 |
ATP |
Mg+2 |
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ADP +P |
|
|
|
OH |
|
|
|
|
|
||||||
|
|
|
|
|
OH |
|
OH |
|
|
|
|
|
|
|
|
OH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
3. De pe N5, N10 –metenil-tetrahidrofolat, o transferază, trece, folosind o moleculă de apă, o grupă formil pe atomul de azot provenit din glicocol. În acest fel se completează atomii din ciclul pentatomic al purinei.
|
|
|
|
|
|
|
|
CH2 |
|
NH2 |
|
|
|
|
|
|
|
CH |
|
NH |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
O |
|
OC |
|
|
|
|
|
|
|
|
|
O |
|
|
OC |
|
2 |
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
O |
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
H2C |
|
|
|
|
NH |
|
transferaza |
HO |
P |
|
H C |
|
NH |
|
|
|
|
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
2 |
|
O |
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
N5N10_metilen THF |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
OH |
|
OH |
THF |
|
|
|
|
|
OH |
|
OH |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
4. Fosforibozil - N – formilglicina din etapa precedentă se transformă prin acţiunea unei sintetaze care schimbă CO a amidei cu NH provenit de la glutamină. Reacţia necesită hidroliza ATP. Produsul format este fosforibozil-N-formil glicinamidină.
|
CH2 |
NH |
|
|
|
O |
CH2 |
NH |
O |
OC |
CH O Gln |
Glu |
HO |
HN C |
CH O |
||
P |
H2C O NH |
|
||||||
HO P |
H2C O NH |
|
Mg+2 |
|
|
|||
|
|
|
|
|||||
OH |
|
|
H2O P |
|
|
OH |
|
|
|
|
ATP |
ADP |
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
OH OH |
|
|
|
OH OH |
|
|
|
|
|
|
|
5. Utilizând energia liberă eliberată prin hidroliza unui rest fosfat din ATP, o altă sintetază închide ciclul de cinci atomi şi
24

Biochimie farmaceutică
formează 5’-fosforibozil-5-aminoimidazol. Grupa =NH adăugată, în reacţia anterioară, apare acum ca un substituient amino al ciclului.
|
CH NH |
|
|
HC |
NH |
|
2 |
|
|
O H2N C CH |
|
O HN C CH O |
|
HO |
|||
HO P H2C |
O NH |
|
P H2C O |
N |
|
|
|
||||
OH |
|
Mg+2 |
ADP +P |
OH |
|
|
ATP |
|
|
|
|
OH OH |
|
|
OH OH |
||
6. În etapa următoare se adaugă un grup carboxil din dioxid de carbon. Carboxilaza este enzima care formează, astfel, 5’- fosforibozil-5-aminoimidazol-4-carboxilat nu are ca grupare prostetică biotina şi diferă ca mecanism de alte enzime care adaugă grupări carboxil.
|
O |
|
HC |
|
|
|
NH |
|
|
|
|
|
|
HOOC |
|
C |
|
NH |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
H2N |
C CH |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
carboxilaza |
|
|
H2N |
C CH |
||||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||
P |
|
H2C |
|
|
|
|
|
|
N |
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
O |
|
|
P |
|
H2C |
O |
N |
|||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
CO2 |
|
OH |
|
|
|
|
|||||||||||||||||||
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||
7. O sintetază condensează acidul aspartic cu produsul anterior de reacţie consumând o legătură macroergică din ATP. Condensarea are loc între grupa amino a acidului aspartic şi carboxilul imidazolului. Intermediarul 5-fosforibozil-4-(N- succincarboxamid)-5-aminoimidazol, care rezultă, serveşte pentru introducerea atomului N1 din inelul purinic.
24
Luciana Dobjanschi
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
HOOC |
CH2 |
COOH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH |
|
|
|
|
|
|
|
||||||||
|
|
|
HOOC |
C |
|
|
|
|
NH |
|
|
|
|
|
|
|
|
|
|
|
|
CO |
|
|
C |
|
NH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH |
|
|
|
|
|
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
O H N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O H N |
|
|
|
|
|
|||||||||||||||||
|
C CH |
|
|
|
ATP ADP |
+ |
P |
|
C CH |
||||||||||||||||||||||||||||||||
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Mn+2 |
|
|
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
P |
|
H2C |
|
|
|
|
|
N |
|
|
|
|
|
|
P |
|
|
H2C |
|
|
|
|
N |
||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
O |
|
|
|
COOH sintetaza |
|
|
|
|
O |
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
+ HOOC |
|
CH2 |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
OH |
|
|
|
|
OH |
|
|
|
|
||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
NH2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
OH |
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
||||||||||||||||||||||
8. Produsul reacţiei anterioare este scindat de către o liază la 5 –fosforibozil-4-carboxamid-aminoimidazol şi acid fumaric. Reacţiile 7 şi 8 se aseamănă sintezei argininei din citrulină din ciclul ureogenetic.
HOOC |
|
|
|
CH2 |
|
|
COOH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
CH |
|
|
|
|
|
|
|
|
|
|
|
H2N |
CO |
|
|
C |
|
|
NH |
|||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
HN |
|
CO |
|
|
C |
|
NH |
adenilatsuccinat liaza |
||||||||||||||||||||||||
|
|
|
|
|
|
|
|||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H2N |
C CH |
||||||||||||||
|
|
|
|
H2N |
C CH |
|
|
|
HO |
|
|||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||
HO |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
P |
|
|
H2C |
|
N |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
P |
|
|
H2C |
|
|
|
|
N |
|
acid fumaric |
||||||||||||||||||||||
|
|
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
||||||
|
|
|
|
|
|
|
|
OH OH |
|
|
|
|
|
|
|
|
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
9.În etapa următoare este transferată o grupă formil de pe N10formil tetrahidrofolat ducând la 5-fosforibozil-4-carboxamid-5- formamidoimidazol, care conţine toţi atomii ciclului purinic.
25

Biochimie farmaceutică
|
H2N |
CO |
|
C |
|
|
NH |
N10 _formil |
|
H2N |
CO |
|
|
C |
|
|
|
|
NH |
||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||||||
|
|
|
|||||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
||||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||
|
|
|
H2N |
C |
|
|
CH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||
HO |
|
|
|
|
THF |
THF |
|
OHC |
|
|
|
HN |
C |
|
|
|
|
CH |
|||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
||||||||||||||||||||||||||||||||||||
P |
|
|
H2C |
O |
|
N |
|
|
|
|
P |
|
O |
|
H2C |
|
|
|
|
|
|
N |
|||||||||||||||||
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||||||||||||||
|
|
|
|
|
|
|
formiltransferaza |
|
|
O |
|||||||||||||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|||||||||||||||||||||||||||||
|
|
OH |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
|
|
|
|
|
|
|
|
|
|
|
OH |
OH |
||||||||||||||||||
10. În fine, în ultima etapă prin eliminare de apă de către ciclohidrolază se închide şi inelul de şase atomi ducând la apariţia primului nucleotid purinic, acidul inozinic (IMP).
|
|
|
|
|
|
OH |
|
|
|
|
|
|
N |
N |
|
H2N |
CO |
C |
NH |
|
N |
||
|
|
||||||
OHC |
HN C |
CH |
|
N |
|||
P O |
H2C |
||||||
P O |
H2C |
N |
ciclohidrolaza |
O |
|||
|
|
O |
_CO2 |
|
|
||
|
|
|
|
|
|||
|
|
|
|
|
|
||
|
OH OH |
|
|
OH OH |
|||
|
|
|
|
|
|||
Se poate observa că pentru sinteza IMP se consumă şase legături macroergice, considerând şi formarea PRPP.
Aspecte de patologie din metabolismul nucleotidelor
Guta este una din cele mai răspândite boli de metabolism cu o frecvenţă de 0,3% din populaţia Europei. Sub acestă denumire sunt incluse un grup heterogen de boli caracterizate toate prin hiperuricemie, care duce la depunerea uratului de sodiu în sinoviala articulaţiilor, atacuri acute de artrite, formarea de depozite masive de urat şi apariţia urolitiazei.
25

Luciana Dobjanschi
Hiperuricemia poate apărea din numeroase cauze, unele determinate genetic, altele dobândite. Nu orice uricemie duce la apriţia gutei, În unele cazuri aceasta poate persista toată viaţa fără a provoca modificări patologice.
Guta poate să fie primară, ca boală ereditară de metabolism în sine, sau secundară dezvoltându-se ca o consecinţă a altor boli ereditare sau dobândite. Guta secundară poate să apară în deficienţă de glucozo-6-fosfatază sau în deficienţa totală a hipoxantin-guanin fosforibozil transferazei, precum şi în boli de distrugeri celulare masive: anemii hemolitice, leucemii, policitemii, etc. Tratamentul cu medicamente citotoxice în neoplazii poate declanşa apariţia secundară a gutei, ceea ce impune asocierea acestora cu inhibitori ai xantinoxidazei. O altă posibilitate a gutei secundare este în urma unei afecţiuni renale cu scăderea capacităţii de excreţie.
În majoritatea cazurilor de gută primar n se cunoaşte defectul enzimatic cauzal, putându-se evidenţia doar diferite situaţii generale. Astfel poate să fie vorba de:
1.o hiperproducţie endogenă crescută a acidului uric
2.o scădere a eliminării renale
3.o scădere a proteinei serice de vehiculare: α1 - α2 –globulina de legare a uratului.
Xantinuria ereditară este o boală relativ blîndă, acesea
asimptomatică ce se datorează deficitului de xantinoxidază. Bolnavii prezintă adesea hiperuricemie şi hiperuricozurie cu eliminări renale de xantină şi hipoxantină. Xantina fiind mai puţin solubilă decât acidul uric poate forma calculi renali.
25

Biochimie farmaceutică
XIV. Metabolismul hemoglobinei
Deoarece există o pierdere permanentă de hemoglobină prin catabolism şi prin îmbătrânirea hematiilor este nevoie de înlocuirea acesteia în mod permanent. Durata medie de viaţă a eritrocitelor umane este în jur de 120 de zile. Ele sunt apoi lizate şi hemoglobina conţinută în ele, este convertită în produşi de excreţie.
Biosinteza globinei se realizează din aportul corporal de aminoacizi într-o cantitate de 8 g pe zi. Aproximativ 14% din aminoacizii aprţinând proteinelor ingerate sunt utilizaţi pentru obţinerea globinei. Procesul de sinteză a globinei are loc în eritrocitele nucleate din măduva osoasă şi în reticulocite. Sinteza globinei are loc la nivelul ribozomilor într-un mod asemănător cu a altor proteine. Studii de electrnomicroscopie arată că sinteza hemoglobinei în reticulocite are loc pe structura multiribozomală care conţine cinci ribozomi. Aceşti ribozomi sunt înşiraţi pe un lanţ de ARNm.
Nucleul eritrocitelor nucleate din măduva osoasă umană nu sintetizează cantităţi semnificative de hemoglobină. Formarea globinei nu pare să implice factori genetici sau mecanism speciale. Cele două tipuri de lanţuri se formează independent sub controlul diferitelor gene şi de asemenea, cu viteze egale.
Biosinteza porfirinelor şi hemului constă din trei etape succesive:
1.biosinteza acidului δ –aminolevulinic din glicină şi succinilCoA
2. formarea porfibilinogenului din acid δ –aminolevulinic
3.conversia porbilinogenului într-un ciclu tetrahidropirolporfirinic şi apoi a hemului.
25

Luciana Dobjanschi
În etapa finală fierul este înserat în molecula protoporfirinei sub acţiunea ferochelazei formând hemul, produsul final de reacţie. Aproximativ 85% din hemul sintetizat pentru formarea hemoglobinei, cca 10% este utilizat pentru formarea mioglobinei şi 5% pentru formarea citocromilor sau alte proteine hemice.
Porfirinele care iau naştere în cantităţi mici sunt compuşi colaterali care ies din calea biosintezei hemului. Aceştia nu pot fi utilizaţi şi se elimină ca atare prin urină.
Formarea în cantitate mare a acestor porfirine reprezintă o perturbare în biosinteza hemului. Această perturbare reprezintă boli genetice, prin deficit enzimatic, cu sau fără manifestări clinice cunoscute sub numele de porfirii şi caracterizate printr-o eliminare crescută de porfirine prin urină, fotosensibilitate. Porfirinele constituie un grup heterogen de boli caracterizate prin excreţie crescută de porfirine şi precursori ai porfirinelor. Principalele tipuri de porfirii sunt:
-porfiria hepatică acută intermitentă
-porfiria eritropoetică congenitală
-coproporfiria ereditară
-protoprfiria
-porfiria cutanată tardivă
-porfiria toxică
-porfiria dobândită
-porfirii variate.
Catabolismul hemoglobinei
În condiţiifiziologice la un om adult se distrug 1-2 x 108 eritrocite pe zi. Astfel, un adult de 70 de kg prezintă un turnover de 6 g Hb/zi. Din eritrocitele îmbătrânite hemoglobina este eliberată prin fagocitoză în celulele reticuloendoteliale, în special în splină. Hemoglobina eliberată în sânge este captată de către o glicoproteină specifică numită heptaglobulină (Hp), care prezintă proprietăţi peroxidice.
Degradarea hemului are loc la nivelul microzomilor hepatici şi implică o oxidare unică a atomului de carbon α din puntea metilenică cu formare de monoxid de carbon. Reacţia este catalizată de către hemoxigenază, o enzimă microzomală, în prezenţă de oxigen molecular, citocrom c reductază şi NADH.
Inelul tetrapirolic al hemului se deschide şi atomul de fier este eliberat. Se formează, probabil caşi intermediar, verdohemină. Se ajunge
25

Biochimie farmaceutică
apoi la biliverdină care sub acţiunea biliverdin oxidazei şi NADPH, este transformată în bilirubină.
O parte din bilirubină se formează şi la nivelul altor ţesuturi din diferite hemoproteine şi este transportată la ficat şi legată de o albumină plasmatică. Bilirubina este insolubilă mîn mediu apos.
În ficat bilirubina este conjugată cu acid glucuronic formând acid bilirubin diglucuronic care este solubil în apă şi este rapid xcretat prin intermediul bilei în intestin. Bilirubin diglucuronidul este hidrolizat la nivelul intestinelor de către β-glucuronidază. Bilirubina este redusă de flora bacteriană trecând în D- sau L-urobilinogen incolor. O parte din el este reabsorbit şi excretat în urină sub forma unui compus de oxidare colorat în galben oraj, L-urobilină. Partea rămasă de urobilinogen este redus în intestin la L-stercobilinogen, care este xcretat în fecale sub forma unui produs de oxidare de culoare brună L-stercobilină.
25

Luciana Dobjanschi
XV. Bibliografie
1.Barrett A.J., Cantor C. R., Enzyme nomenclature, Academic Press, 1992
2.Bedeleanu D., Manta I., Biochimie medicală şi farmaceutică, Ed.Dacia Cluj-Napoca, 1985
3.Cristea-Popa E., Popescu A., Truţia E., Dinu V., Tratat de Biochimie Medicală, Ed. Medicală-Bucureşti, 1991.
4.Champe Pamela C., Harwey A. Richard, Biochemistry, J.B. Lippincott Company, 1994
5.Căpâlna S., Tănăsescu D., Truţia E., Biochimie medicală, Ed.Didactică şi Pedagogică Bucureşti, 1977
6.Felszeghy E., Abraham A., Biochimie, Ed. Didactică şi Pedagogică Bucureşti, 1972
7.Lehninger A.L. Biochimie, Ed.Tehnică Bucureşti, 1987
8.Gilău D., Antonescu A., Dobjanschi L., Gilău R.D., Gilău L.,
Compendiu de Biochimie medicală, Ed. Imprimeriei de Vest Oradea, 2002.
9.Gilău L. Proinov I., Biochimie, Ed. Universităţii din Oradea, 1999
10.Mureşan Mariana, Biochimie medicală, Ed. Universităţii din Oradea 2003
11.Mihele D., Biochimie clinică, Ed.Medicală Bucureşti, 2001.
12.Rosetti-Colţoiu Matilda, Mitrea Niculina, Biochimie, Ed. Didactică şi Pedagogică, Bucureşti, 1985
13.Thierry Grisar, Elements de biochimie humaine normale et pathologique, partium I, Les Editions de l’Univerite de Liege, 2004
14.Ţărmure Cornelia, Biochimie structurală şi metabolică vol.I, Ed.Dacia Cluj-Napoca, 1996
15.Vrana K.E., Biochemistry, Lippincott Williams Wilkins, Philadelphia,1999.
25
