
- •1.Горючая система. Осн. И доп. Компоненты.
- •2. Процессы, происходящие в гс.
- •3.Агрегатные состояния горючих веществ и окислителя.
- •4. Гетерогенная и гомогенная гс.
- •5. Диффузная и кинетическая гс.
- •6. Организованное и неорганизованное горение.
- •7. Классификация техногенных веществ, участвующих в горении.
- •8. Количественное представление о составе горючих веществ и окислителя.
- •9.Органическиё, сухой и горючий состав горючего вещества
- •10.Пересчет количества компонента от одного состава к другому.
- •11. Теплота сгорания. Высшая и низшая точка. Их соотношение
- •12. Определение теплоты сгорания вещества
- •13. Определение теплоты сгорания газовой смеси
- •14. Определение теплоты сгорания сложного вещества
- •15. Определение расхода окислителя
- •16. Определение состава продуктов горения
- •17. Тепловой баланс
- •18. Адиабатическая температура горения
- •19.Химическое равновесие в реакциях горения
- •20.Диссоциация продуктов горения
- •23.Цепная реакция
- •24.Цепная неразветвлённая реакция
- •25.Цепная разветвлённая реакция
- •26.Самовоспламенение. Термические условия
- •27.Нижний и верхний пределы самовоспламенения
- •28.Адиабатическое самовоспламенение
- •29.Температура самовоспламенения. Зависимость от условий
- •35.Экспериментальная скорость распространения пламени.
- •36. Определение нижнего концентрационного предела распространения пламени
- •37.Классификация горючих газов
23.Цепная реакция
Сложная реакция, в кот.происходит послед.повторение определ.превращений, описываемых простыми реакциями с участием актив.частиц, наз-ся цепной реакцией.
Для большинства реакций горения скорость рассчит-ая по числу молекул горючего и окислителя не совпадает с экспер-ми значениями.
Кинетика реакций основ-ая на столкновении молекул наз-ся макрокинетикой горения, кинетика, учитывающая участие в хим превращениях атомов, радикалов и др активных частиц наз-ся микрокинетикой горения.
В соот-ии с микрокинетикой горения, исходные вещ-ва превращаются в ходе реакции в конечные вещ-ва не сразу, а посредствам образования активных частиц, которые сравнительно легко вступают в дальнейшие соединения. В результате этих соединений получаются конечные продукты и одновременно образуется некоторое кол-во активных вещ-в. Акт-ые частицы могут вновь вступать в соединения, заново повторяя цикл превращений. Повторение цикла будет происходить до тех пор, пока не прекратится воссоздание активных вещ-в.
Сложная реакция, в которой происходит послед-ое повторение опред-ых превращений, описываемых простыми реакциями с участием активных частиц (звеньями) наз-ся реакцией цепочечного типа или цепной реакцией. После начального возбуждения такая реакция повт-ся несколько раз, не нуждаясь в подводе энергии из вне. Бывают неразветв-ые и раветв-ые цепные реакции.
24.Цепная неразветвлённая реакция
Цепная неразвет-ая реакция – цепная реакция, у которой с течением времени число звеньев не увеличивается.
Пример: Н2+Cl2= 2HCl
В соот-ии с микрокин образование конечного продукта происходит в результате чередования простых реакций с участием активных центров, т.е. атомов Н и Сl. Первичными акт-ми центрами явл-ся атомы, образующиеся при диссоц-ии молекул, при столкновениях с частицами вещ-ва, обладающих энергией (реакция зарождения цепи).
Cl2+M=Cl+Cl+M-13,6 кДж/моль. М – активная молекула, обладающая энергией и теряющей кинетич энергию после реакции. Н2+М=Н+Н+М-24,6 кДж/моль. В данном случае образованием атомарного Н можно пренебречь, т.к. молекула Н более прочная чем молекула Сl.
Два атома Сl могут при тройном столкновении рекомбинировать, т.е. превратиться в молекулу: Cl+Cl+M= Cl2+M+13,6 кДж/моль. Реакция такого типа, сопровождающаяся исчезновением своб-ой вален-ти наз-ся реакцией обрыва цепи.
В присутствии молек-ого Н атомы Cl могут реагировать другим путем: Н2+Cl= HCl+Н.
Эта реакция идет гораздо быстрее, чем бимолекулярная реакция Н с Сl, т.к. энергия активации реакции с участием атомарного Сl < чем при молек-ом Сl2. Это происходит из-за того, что при преобразовании НСl, возникает новый активный центр-атом Н, который далее реагирует с молекулой Cl2: Н+Cl2= HCl+ Cl – это и есть цепная реакция неразвет-ого типа.
обменивающейся
тепловой энергией с ОС, средняя
температура горения:
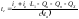 ,
,
где
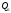 -
потеря тепловой энергии из горючей
системы в ОС;
-
потеря тепловой энергии из горючей
системы в ОС;
 -
химический недожог, вызванный
нестехиометричностью горения;
-
химический недожог, вызванный
нестехиометричностью горения;
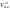 -
удельное количество продуктов горения
при нестехиометрических условиях
-
удельное количество продуктов горения
при нестехиометрических условиях
горения.
