
- •1.Горючая система. Осн. И доп. Компоненты.
- •2. Процессы, происходящие в гс.
- •3.Агрегатные состояния горючих веществ и окислителя.
- •4. Гетерогенная и гомогенная гс.
- •5. Диффузная и кинетическая гс.
- •6. Организованное и неорганизованное горение.
- •7. Классификация техногенных веществ, участвующих в горении.
- •8. Количественное представление о составе горючих веществ и окислителя.
- •9.Органическиё, сухой и горючий состав горючего вещества
- •10.Пересчет количества компонента от одного состава к другому.
- •11. Теплота сгорания. Высшая и низшая точка. Их соотношение
- •12. Определение теплоты сгорания вещества
- •13. Определение теплоты сгорания газовой смеси
- •14. Определение теплоты сгорания сложного вещества
- •15. Определение расхода окислителя
- •16. Определение состава продуктов горения
- •17. Тепловой баланс
- •18. Адиабатическая температура горения
- •19.Химическое равновесие в реакциях горения
- •20.Диссоциация продуктов горения
- •23.Цепная реакция
- •24.Цепная неразветвлённая реакция
- •25.Цепная разветвлённая реакция
- •26.Самовоспламенение. Термические условия
- •27.Нижний и верхний пределы самовоспламенения
- •28.Адиабатическое самовоспламенение
- •29.Температура самовоспламенения. Зависимость от условий
- •35.Экспериментальная скорость распространения пламени.
- •36. Определение нижнего концентрационного предела распространения пламени
- •37.Классификация горючих газов
12. Определение теплоты сгорания вещества
Теплота сгорания вещества зависит от его строения и агрегатного состояния.
По Закону Гесса: Q = ∑Qк - Qоб
Qк - сумма тепла сгорания компонентов, содержащихся в данном веществе
Qоб - теплота образования данного вещества в процессе горения
Пример:

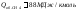 ;
;
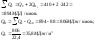
13. Определение теплоты сгорания газовой смеси
Теплота сгорания газовой смеси определяется как сумма теплот сгорания горючих составляющих
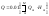 ,
где m
- номер горючего газа в составе смеси
,
где m
- номер горючего газа в составе смеси
Qm - теплота сгорания М-го горюч. газа
М - количество горючих газов в г.с.
Нm- процентное содержание Пример: Для смеси из Н2, окиси углерода, метана и сероводорода теплота сгорания составит:

14. Определение теплоты сгорания сложного вещества
Можно определять по сумме тепла сгорания отдельных элементарных компонентов.
Формула Д.И. Менделеева:

Qв - теплота сгорания высшая
О - содерж. кислорода
С - содержание углерода
W- содержание воды
Теплота сгорания горючего материала неизвестного состава определяется экспериментально в калориметрах.
В калориметре сжигается известное количество твердого, жидкого или газообразного вещества, тепловая энергия выделившаяся при этом практически полностью поглощается охлаждающей водой.
По количеству воду и повышению ее температуры из уравнения теплового баланса калориметра определяется значение теплоты сгорания.
Стехиометрическое уравнение горения
 ;
где m
ik
-число атомов K-го
элемента в i
-молекуле
;
где m
ik
-число атомов K-го
элемента в i
-молекуле
Ni - число i -ых молекул в горюч. системе
Вк - полное число атомов данного хим. элемента в смеси
Уравнение реакции горения в общем виде:
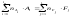
где Аi - химический символ i -го исходного вещества
Fi - химический символ j - го конечного вещества
nAi, nFj - стехиометрические коэффициенты
i0 - количество исходных веществ
j0 - количество конечных веществ
Горючая смесь называется стехиометрической, если исходные вещества взяты в таком соотношении, что химическое превращение полностью переводит их в продукты реакции.
Горючей системой стехиометрического состава называется система с необходимым для полного горения соотношением между количеством окислителя и горючего, котор. приводит к образованию продуктов не способных к последующему горению.

А1 - химический символ горючего вещества
А2 - химический символ окислителя
F - химический символ продуктов горения
nA1 - стехиометрический коэффициент
Удельный стехиометрический коэффициент реакции горения:
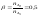 ,
,
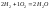 ;
;
 ,
,
где mC, mS, mH, …- число атомов углерода, серы, водорода в молекуле атома
mХ - число атом. галогенов (Cl, Br,…)
15. Определение расхода окислителя
Стехиометрический расход окислителя при горении горючего вещества можно определить преобразованием величины удельного стехиометрического коэффициента (β) в единицы массы или в единицы объема.
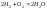 ,
β = 0,5
,
β = 0,5
О2 = 0,5
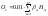 - удельный расход
- удельный расход
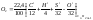
C, H, S, O - сод-е соотв. эл-та в вещ-ве
Удельный
стехиометрический расход воздуха на
горение:

Удельный
действительный расход воздуха на
горение:
 ,
α- коэффициент расхода воздуха. Коэффиц.
расхода воздуха α показывает отношение
удел. действ. расхода воздуха к удел.
стехиометрическому.
,
α- коэффициент расхода воздуха. Коэффиц.
расхода воздуха α показывает отношение
удел. действ. расхода воздуха к удел.
стехиометрическому.
При α <1 - горит богатая система, α >1 - бедная система, α =1 - смесь стехиометрич. состава
