
|
Глава XI Болезни щитовидной железы |
|
|
|
Заболевания щитовидной железы в эндокринологии после сахарного диабета занимают второе место. Классификация. По классификации, принятой на конференции социалистических стран в Софии (1961), официально используемой в СССР, различают следующие патологические процессы в щитовидной железе: 1. Токсический зоб (тиреотоксикоз). 2. Токсическая аденома. 3. Эндемический и спорадический зоб. 4. Гипотиреоз и микседема. 5. Воспалительные заболевания щитовидной железы: а) острые тиреоидиты (и струмиты) — негнойные и гнойные; б) хронические тиреоидиты — гигантоклеточный тиреоидит де-Кервена — Крайля, тиреоидит деревянистой консистенции (зоб Риделя), лимфоматозный тиреоидит (болезнь Хасимото); в) редкие воспалительные заболевания (туберкулез, сифилис и др.); грибковые и паразитарные (актиномикоз, эхинококк) заболевания. 6. Злокачественные опухоли щитовидной железы (рак, метастазирующая аденома, саркома и др.). 7. Повреждения щитовидной железы: а) открытые, б) закрытые. 8. Врожденные аномалии щитовидной железы: а) аплазия и гипоплазия (сопровождающиеся обычно гипотиреозом или микседемой); б) эктопии (способные давать начало аберрантным зобам); в) незаращение языкощитовидного протока, дающее начало кистам шеи (в том числе срединным кистам) и свищам (В. Г.Астапенко, 1976). Методы исследования щитовидной железы:
Функциональную активность щитовидной железы определяют для выявления эутиреоза, гипертиреоза или гипотиреоза по показателям скорости секреции и содержанию в крови тиреоидных гормонов. Исследование щитовидной железы радиоактивным йодом состоит в прослеживании метаболизма йода на основании степени его поглощения и задержки минимальной тестовой дозы. Накопление I131 в щитовидной железе в норме за 2 ч — 7—12%, за 24 ч — 20—29%. Йодом, связанным с белками сыворотки крови (СБЙ), более точно определяется функциональная активность щитовидной железы почти при всех ее патологических состояниях. Содержание СБЙ в сыворотке крови здоровых людей составляет 4—8 мкг %; уровень ниже 3,5 мкг % указывает на наличие гипотиреоза, выше 8,5 мкг % — гипертиреоза. Радиоизотопное скеннирование представляет собой объективный метод, который дает возможность судить о функциональной топографии различных участков щитовидной железы. Основной обмен, отражающий интенсивность энергетических процессов в организме в условиях покоя после 12-часового голодания и в норме у здорового человека, равен ±10—15%. Определение уровня холестерина в крови служит дополнительным показателем функции щитовидной железы. При гипотиреозе он повышается, при гипертиреозе снижается. Метод определения аутоантител к тиреоглобулину с помощью реакции пассивной гемоагглютинации в постановке Roitt и Doniach (1958) применяют для выявления аутоиммунного процесса в щитовидной железе. Интраоперационной многоточечной пункционной биопсией со срочным исследованием материала можно значительно расширить диагностические возможности цитологического метода и решить вопрос о диагнозе до выполнения основного момента операции (Б. 3. Любин, 1974). Воспалительные заболевания. Тиреоидит и струмит острый. Воспаление щитовидной железы (тиреоидит) или зобноизменной железистой паренхимы (струмит) возникает чаще после ангины, флегмоны, фурункулеза, сепсиса, пневмонии и других заболеваний в результате инфицирования лимфогенным или гематогенным путем. При этом щитовидная железа инфильтрируется полиморфноядерными лейкоцитами и лимфоцитами, однако функция ее существенно не изменяется. Заболевание начинается остро, общей слабостью, ознобами, высокой температурой (40° и выше), сильными болями в щитовидной железе, которые иррадиируют в уши, затылок, нижнюю челюсть, усиливаются при глотании и повороте головы. Отек и болезненная пальпация отмечаются преимущественно в пораженной доле щитовидной железы. Флюктуация появляется поздно и определяется при поверхностно сформировавшемся абсцессе. Лечение начинают с применения больших доз антибиотиков широкого спектра действия и сульфаниламидов. При подозрении на формирование абсцесса показано вскрытие в самые ранние сроки во избежание распространения гнойно-воспалительного процесса на смежные области шеи и средостение. Тиреоидит подострый (де Кервена) — негнойное воспаление щитовидной железы, по-видимому, вирусной этиологии. Болеют чаще женщины от 30 до 50 лет, встречается у 1 — 2% больных с тиреоидной патологией. Гистологически определяются деструкция фолликулов и фолликулярных клеток, характерные скопления гистиоцитов и гигантских клеток типа «инородное тело». Заболевание начинается с температуры (не выше 39°), болей в области щитовидной железы, которые отдают в затылок, ухо, надключичную область, сопровождается явлениями тиреотоксикоза. Щитовидная железа увеличена, уплотнена, болезненна при пальпации, значительно снижается поглощение I131. Лечение проводят преднизолоном — 20—30 мг в сутки или кортизоном — 100 мг в сутки, в более легких случаях назначают ацетилсалициловую кислоту — 2—4 г в сутки, на протяжении нескольких недель с последующим постепенным снижением доз глюкокортикоидов и салицилатов, с интервалами 4— 6 дней. Тиреоидные препараты (тиреоидин — 0,1—0,15, трийод-тиронин — 60—100 мкг, тироксин — 200—400 мкг в сутки) назначают после устранения острых явлений и восстановления эутиреоидного состояния. В случае рецидива заболевания повторяют медикаментозное лечение или применяют рентгенотерапию. Тереоидиты хронические. Тиреоидит аутоиммунный (лимфоматозный тиреоидит, болезнь Хасимото) — заболевание, в патогенезе которого аутоиммунный процесс служит основным фактором, приводящим к уменьшению функционирующей паренхимы щитовидной железы. Болеют чаще женщины. Заболеваемость нарастает с возрастом. Нарушается синтез тиреоид-ных гормонов, содержание йода в железистой паренхиме понижается, постепенно уменьшается объем функционирующей паренхимы и снижается функциональная активность щитовидной железы. Железа обычно увеличена в размерах, консистенция плотная, поверхность бугристая, на разрезе белесоватая из-за фиброза. При гистологическом исследовании на фоне гиперплазии железы определяется выраженная диффузная и очаговая инфильтрация лимфоцитами и плазматическими клетками. Заболевание начинается постепенно, появляется чувство сдавления и неприятного ощущения инородного тела в области шеи. У некоторых больных удается выявить «скрытые» симптомы пониженной функции щитовидной железы (ухудшение памяти, работоспособности, прибавки в весе, выпадение волос на голове, плохая переносимость холода и др.). По клиническому течению выделяют 4 формы аутоиммунного тиреоидита:
Дифференциальный диагноз аутоиммунного тиреоидита проводят с фиброзным тиреоидитом, эндемическим зобом и злокачественными опухолями щитовидной железы (см. соответствующие заболевания). Лечение проводят тиреоидными препаратами (тиреоидин 0,1—0,15 г, трийодтиронин — 60—100 мкг, тироксин — 300— 400 мкг в сутки). При выраженной воспалительной реакции назначают преднизолон или другие стероидные препараты с глюкокортикоидным эффектом. Хирургическое вмешательство со срочным цитологическим (гистологическим) исследованием применяют в диагностически неясных случаях для получения морфологического диагноза до выполнения основного этапа операции — экономной резекции макроскопически измененной паренхимы железы. Тиреоидит фиброзный (зоб Риделя) — стадия или форма аутоиммунного тиреоидита, проявляющаяся в разрастании соединительной ткани, приводящем к постепенной атрофии железистой паренхимы при эутиреоидном состоянии больных. Патологический процесс поражает долю или всю щитовидную железу. Последняя, увеличиваясь, приобретает дервянис-тую плотность, становится малоподвижной за счет фиброза, распространяющегося на близлежащие органы и ткани. Гистологически среди разросшейся соединительной ткани выявляются атрофированные фолликулы и небольшие скопления клеток тиреоидного эпителия. Выражена инфильтрация железы полиморфноядерными лейкоцитами, лимфоцитами и плазматическими клетками. Заболевание начинается постепенно и проявляется медленным ростом очень плотного, с неровной поверхностью, безболезненного зоба. Рано выявляются симптомы, связанные с вовлечением в патологический процесс тканей и органов шеи, — неподвижность железы при глотании, затрудненное дыхание, дисфагия, осиплость голоса и др. Температура тела нормальная. Гипотиреоз иногда развивается в поздних стадиях заболевания. Дифференциальную диагностику проводят с аутоиммунным гиреоидитом, при котором щитовидная железа имеет менее плотную консистенцию и подвижна при глотании; амилоидозом щитовидной железы, который появляется у больных с хроническими воспалительными процессами других органов; со злокачественными опухолями щитовидной железы, когда фиброзный процесс поражает одну долю (см. злокачественные опухоли щитовидной железы). Хирургическое лечение применяют при больших размерах зоба, выраженных компрессионных симптомах и диагностически неясных случаях. Срочный морфологический диагноз (цитологический или гистологический) позволяет сразу избрать правильный объем оперативного вмешательства. Гипотиреоз. Это синдром патологически пониженной функции щитовидной железы врожденного или приобретенного характера. Различают первичный, вторичный и третичный гипотиреоз. Первичный гипотиреоз связан с непосредственным поражением щитовидной железы и бывает при врожденных дефектах паренхимы, нарушении синтеза тиреоидных гормонов, резко выраженном дефиците йода в окружающей среде, аутоиммунном тиреоидите, после перенесенной тиреоидэктомии и как результат приема неадекватно большой дозы радиоактивного йода. Вторичный гипотиреоз развивается при деструктивных процессах в клетках гипофиза, продуцирующих тиреотропный гормон — ТТГ (хромофобная аденома, краниофарингиома и др.). Третичный гипотиреоз появляется при повреждении отделов гипоталамуса, ответственных за продукцию ТТГ. Для всех форм гипотиреоза характерен низкий уровень тиреоидных гормонов в крови, приводящий к нарушению обмена с изменением тканей и органов. Патологические изменения в щитовидной железе зависят от основного заболевания, вызвавшего гипотиреоз. Микседема — первичный гипотиреоз, для которого характерен слизистый отек, обусловленный экстрацеллюлярным накоплением полисахаридов в тканях и органах, повышающих их гидрофильность. Клиника гипотиреоза характеризуется заторможенностью больных, медлительностью движений, тугодумием, ослаблением памяти и умственных способностей. Температура тела понижена, больные плохо переносят холод. Расстроен сон, страдают запорами. У мужчин развивается импотенция. Лицо одутловатое, безразличное, взгляд неосмысленный, тупой. Глазные щели узкие, «мешки» под глазами. Нос и язык утолщены, постоянное слюнотечение из открытого рта. Часто имеется умеренное ожирение всего тела. Кожа бледная, с желтоватым оттенком, холодная, сухая, легко шелушится. Конечности утолщены, однако отек не сохраняет отпечатков пальцев при надавливании. Волосы на голове тонкие, редкие. Ногти тонкие, ломкие, с поперечной исчерченностью. Тоны сердца приглушены, часто наблюдается брадикардия. Артериальное давление колеблется, часто оно повышено. Снижен основной обмен (на 20—30%). У многих больных наблюдается анемия и ускоренная СОЭ. Гипотиреоидная кома — крайне утяжеленный гипотиреоз. Наступает у лиц преклонного возраста с нелеченным гиготи-реозом при хирургических вмешательствах, травмах, тяжелых инфекциях, приеме барбитуров или наркотиков. Постепенно нарастает слабость, сонливость, которая может перейти в сопор (терминальная стадия). При этом температура не превышает 34—35°, развиваются брадикардия, гипотония, редкое дыхание и олигурия. Лечение гипотиреоза основано на применении тиреоидных гормонов, которые компенсируют недостаточность щитовидной железы и нормализуют обменные процессы. Назначают малые дозы тиреоидина (0,05 г в сутки), которые повышают постепенно (0,025 г через 7—10 дней) до индивидуально переносимой (0,1—0,15 г в сутки), пока не будет достигнуто эутиреоид-ное состояние. При гипотиреоидной коме внутривенно вводят трийодтиронин 10—25 мкг 2 раза в сутки (необходим контроль пульса, артериального давления, дыхания, ректальной температуры). Одновременно назначают внутривенно 100 мг преднизолона или внутримышечно 100—300 мг гидрокортизона. Необходимо своевременно применять оксигенацию, сердечные гликозиды, антибиотики, внутривенное капельное введение 5% раствора глюкозы. Зоб — увеличение щитовидной железы при различных патологических процессах в ней. Форма, степень увеличения щитовидной железы и ее функциональное нарушение определяют клиническое проявление заболевания. По форме увеличения щитовидной железы различают: 1) диффузный зоб—равномерное увеличение одной или двух долей железы; 2) узловой зоб — на фоне редуцированной паренхимы железы определяются единичные или множественные узлы; 3) смешанный зоб — в щитовидной железе имеется диффузное и узловое ее увеличение. По степени увеличения щитовидной железы подразделяют: 1) 0 степень — щитовидная железа не видна при глотании и не пальпируется; 2) I степень — отчетливо польпируется увеличенный перешеек; 3) II степень — железа видна при глотании, кроме перешейка хорошо пальпируются обе доли; 4) III степень — щитовидная железа видна при осмотре передней поверхности шеи (так. называемая «толстая шея»); 5) IV степень — увеличенная железа, различная по своей форме, резко меняет конфигурацию шеи; 6) V степень — зоб огромных размеров, иногда висячий. I и II степень увеличения щитовидной железы не считается зобом, чаще носит функциональный характер и бывает у лиц юношеского возраста (особенно у девочек) в период полового созревания. По функциональным проявлениям различают зоб: 1) эутиреоидный; 2) гипертиреоидный; 3) гипотиреоидный. Зоб диффузный токсический (тиреотоксикоз, болезнь Базедова, Перри, Гревса, Флаяни) — заболевание, обусловленное гиперфункцией диффузно гипертрофированной и гиперплази-рованной щитовидной железы. Тиреотоксикоз у женщин встречается в 5—10 раз чаще, чем у мужчин. Наибольшая заболеваемость наблюдается в возрасте 20—40 лет. Психическая травма (80—85%), острое инфекционное заболевание (15—20%) и функциональное состояние половых желез являются основными этиологическими факторами возникновения тиреотоксикоза. Эти факторы вызывают расстройство нервно-эндокринной регуляции функции щитовидной железы и гиперсекрецию тиреоидных гормонов (тироксин — Т4, трийодтиронин — Тз), которые, действуя на различные ткани и органы, обуславливают клиническое проявление заболевания. Гистологически в паренхиме увеличенной щитовидной железы наблюдаются явления диффузной гиперплазии. Железистый эпителий разрастается, превращаясь в многослойный цилиндрический с папиллярными разрастаниями. Фолликулы богаты коллоидом. Соединительная ткань богато васкуляризирована и инфильтрирована лимфоидными элементами. На фоне диффузного увеличения железы иногда встречаются узлы — аденомы, преимущественно микрофолликулярного строения. Заболевание может начаться остро, обычно через несколько часов после психической травмы (острая форма), и постепенно, на протяжении нескольких недель или месяцев (хроническая форма). Клиническое проявление симптомов связано с изменением функции гипофиза (увеличение щитовидной железы, офтальмопатия, изменения кожи, в том числе претибиальная минседе-ма, мышечная слабость) и гиперфункцией щитовидной железы (нервная возбудимость, расширение глазных щелей, потливость, дрожание рук, тахикардия и др.). Увеличение щитовидной железы обычно небольшое (II—III ст.), консистенция мягкоэластичная, безболезненная, поверхность гладкая. Иногда на фоне диффузного увеличения могут определяться единичные или множественные узлы. Не существует параллелизма между величиной щитовидной железы и тяжестью тиреотоксикоза. У большинства больных тиреотоксикозом определяется в различной степени двусторонний экзофтальм, изредка он имеет преимущественно односторонний' характер. Обращает на себя внимание испуганное, гневное выражение лица, усиленный блеск глаз, широкое раскрытие глазной щели (симптом Дель-римпля), редкое мигание (симптом Штельвага), отставание верхнего века от радужки при движении глазного яблока сверху вниз (симптом Грефе) и противоположный ему симптом Кохера (при взгляде вверх расширяется участок склеры под радужкой). Наиболее ранним симптомом поражения мыпечного аппарата глазного яблока является нарушение конвергенции (симптом Мебиуса). Довольно часто можно отметить отечность верхнего века (симптом Зенгера) и пигментацию вокруг глаз (симптом Еллинека). Кожа у больных тиреотоксикозом «бархатная», влажная и горячая. Выражен красный дермографизм, обусловленный вазомоторными реакциями. В поздних стадиях заболевания может появиться утолщение и отек кожи на внутренней поверхности голеней (претибиальная микседема). В результате поражения нервной системы и психики больные тиреотоксикозом страдают бессоницей, сон тревожный, короткий. Отмечается также эмоциональное слабодушие, психолабильность, раздражительность, впечатлительность. Эмоциональные расстройства сочетаются с двигательно-волевыми нарушениями. Больные испытывают потребность находиться в движении, которые часто бывают нецелесообразными, — тиреотоксическая гиперкинезия. Разговор, жесты, мимика живые, резкие и быстрые. При этом наблюдается быстрая утомляемость, мелкий тремор пальцев рук, мышечная слабость, дрожание всего тела. Тахикардия, постоянный признак тиреотоксикоза (достигает до 150 и более ударов в мин), носит стойкий характер, не изменяется при перемене положения тела. Пульс очень лабилен, учащается при малейших психических и физических нагрузках. Пульсовое давление увеличено за счет повышения систолического и понижения диастолического давления. Минутный объем крови повышен соответственно частоте сердцебиений. При прогрессировании тиретоксикоза, особенно у лиц с сердечно-сосудистой патологией, наступает мерцательная аритмия. Вначале она носит параксизмальный характер, в далеко зашедших случаях переходит в стойкую форму мерцательной аритмии. При тиреотоксикозе повышены все виды обмена за счет воздействия тиреоидных гормонов на метаболизм. Основной обмен, как правило, вариабелен и прямо пропорционален тяжести тиреотоксикоза. Повышение окислительных процессов увеличивает теплопродукцию, что приводит к нарушению терморегуляции и субфебриллитету. Избыточная продукция тиреоидных гормонов приводит к усиленному распаду белков и жиров, из-за чего наступает прогрессивная потеря веса, несмотря на повышенный прием пищи. При токсическом зобе в патологический процесс вовлекаются желудочно-кишечный тракт и печень. В печени снижается содержание гликогена, нарушается антитоксическая, пигментообразовательная и другие функции. В более тяжелых случаях появляются участки некроза печеночных клеток и явления фиброза. Желтуха развивается при подострой и острой атрофии печени. Желудочная секреция имеет тенденцию к усилению. У некоторых больных кислотность понижается вплоть до полной ахилии. Усиление перистальтики кишечника и снижение функции поджелудочной железы приводят к периодически наступающим поносам. Иногда появляются желудочно-кишечные кризы. Локализация и интенсивность боли, при них могут симулировать острый аппендицит, прободную язву желудка, печеночную и почечную колики. У женщин тиреотоксикоз может сопровождаться различными типами нарушений менструального цикла вплоть до аменореи. У мужчин и женщин заторможено либидо, нередко развивается половая слабость. При тиреотоксикозе иногда отмечается лейкопения с относительным моноцитозом и лимфоцитоэом. Различают 3 степени тяжести тиреотоксикоза: Тиреотоксикоз I (СБЙ — 9,4±0,3 мкг%) — нерезко выраженная симптоматика (при опросе устанавливается небольшая потеря веса). Тахикардия умеренная, не более 100 ударов в I мин. Основной обмен не превышает+30%. Тиреотоксикоз II (СБЙ— 12,1 ±0,4 кгм%) —отчетливо выраженная симптоматика. Выраженное падение веса. Тахикардия— 100—120 ударов в 1 мин. Основной обмен — от +30 до +60%. Тиреотоксикоз III (СБЙ—16,3±1,7 мкг%)—резко выраженная симптоматика. Быстро прогрессирующее похудание со значительным дефицитом веса. Тахикардия — выше 120 ударов в 1 мин. Основной обмен превышает +60%. Независимо от интенсивности гипертиреоза к III степени относятся осложненные формы тиреотоксикоза — мерцательная аритмия, сердечная недастаточность, тиреотоксическое поражение печени и др. (В. Г. Баранов с соавторами, 1977). Тиреотоксический криз — предельно острое прогрессирующее ухудшение существующего тиреотоксикоза под влиянием психической или другой травмы. Усиление гипертиреоза и гиперактивность симпато-адрена-ловой системы являются основными факторами в патогенезе тиреотоксического криза. Внезапность развития кризов дала основание предположить, что в основе их лежат нарушения центральных нервных механизмов. При тиреотоксическом кризе появляются гипертермия (40° и выше), признаки нервного возбуждения, тахикардия (выше 150 ударов в 1 мин), пароксизмальная форма мерцания предсердий, желудочковая экстрасистолия, выраженный тремор конечностей и мышечная слабость, тошнота и неукротимая рвота, нарастают явления обезвоживания и сгущения крови, в выдыхаемом воздухе и моче определяется ацетон. В крайне тяжелых случаях больные находятся в бессознательном состоянии, с бульбарными парезами и параличами, может развиться острая сердечно-сосудистая или печеночная недостаточность. Летальность высокая, достигает 50% и наступает в первые часы или сутки. Дифференциальный диагноз диффузного токсического зоба приходится иногда проводить с неврозами. При неврозах эмоциональная лабильность, страх, беспокойство в большинстве случаев принимают грустный тон, больные предъявляют массу жалоб, которые не соответствуют данным объективного исследования. У больных неврозом кожа обычная, отмечается потливость ладонной поверхности кистей рук, подмышечных впадин, стоп, отсутствуют основные глазные симптомы и изменения со стороны сердечно-сосудистой системы. У больных с токсическим зобом кожа «бархатистая», влажная и горячая на ощупь, наблюдается потливость всего тела, имеются различной степени выраженности глазные симптомы, поражение сердечно-сосудистой системы и др. В диагностически неясных случаях нормальный уровень СБЙ, БЭЙ и Т4 в крови свидетельствует против наличия тиреотоксикоза. У некоторых больных с вегетоневрозами повышается захват щитовидной железой, однако, как правило, через 24 ч, в то время как при токсическом зобе— через 2 и 4 ч. Подострый тиреоидит может протекать с тиреотоксикозом, однако у этих больных отмечаются увеличенная болезненная щитовидная железа, ускоренная СОЭ и резкое снижение захвата I131 железистой тканью. Функция щитовидной железы может повышаться в начальных стадиях гипертонической болезни, при ревмокардите, но в данных случаях отсутствуют характерные для тиреотоксикоза тремор пальцев рук, патологические глазные признаки, падение веса тела и т. п. Аускультативно при ревмокардите определяются выраженная глухость тонов сердца, диастолические шумы, что нехарактерно для токсического зоба. На электрокардиограмме ревматический кардит часто дает удлинение интервала Р—Q. Длительная субфебрильная температура неясной этиологии может симулировать тиреотоксикоз. Повышение температуры наблюдается в клинически выраженных формах заболевания. Окончательную дифференциальную диагностику тиреотоксикоза и субфебрилитета неясной этиологии проводят по трийод-тесту подавления. При отсутствии токсического зоба поглощение I131 после введения трийодтиронина уменьшается больше чем на 50%. Лечение. В настоящее время излечение токсического диффузного зоба достигается созданием длительного эутиреоза за счет устранения гипертиреоза и тиреотоксикоза медикаментозными средствами, радиоактивным йодом и оперативным путем. Радиологический и хирургический методы лечения, направленные на уменьшение объема функционирующей железистой паренхимы, нужно применять только при максимально устраненном гипертиреозе, так ка они могут стать непосредственной причиной тиреотоксического криза. Всем больным с токсическим зобом создают физический и психический покой и проводят медикаментозную терапию антитиреоидными препаратами. Мерказолил — суточная доза 20—30 мг. Через 3—4 недели, когда наступает клиническое эутиреоидное состояние, дозу снижают до поддерживающей (5—10 мг в сутки) с интервалами в 10—14 дней. Перхлорат калия — эффективная доза 600—1000 мг в сутки (определяется захватом радиоактивного йода, не превышающим 10% от индикаторной дозы). Поддерживающая оптимальная доза, когда наступает эутиреоидное состояние, должна обеспечить захват радиоактивного йода в пределах 20—30%. Резерпин способствует устранению нервно-вегетативных проявлений тиреотоксикоза при лечении антитиреоидными препаратами. Начальную суточную дозу резерпина — 0,2— 0,3 мг — повышают с интервалом в 2—3 дня до 0,75—1,5 мг. Постепенное снижение препарата начинают через 1—2 недели после устранения тиреотоксикоза. В связи с тем, что антитиреоидные препараты могут оказывать токсическое действие на костномозговое кроветворение, весь период лечения необходимо контролировать периферическую кровь 1 раз в неделю и 1 раз в 2—3 недели при переходе на поддерживающие дозы. Метилтиоурацил — лечебная, доза 400—600 мг в сутки, поддерживающая— 50—100 мг в сутки. В настоящее время ограничено его применение из-за большей токсичности по сравнению с мерказолилом и перхлоратом калия. Неорганический йод (раствор Люголя, дийодтирозин) применяют в основном для предоперационной подготовки и лечения тиреотоксического криза. Раствор Люголя применяют по 5—15 капель 3 раза в день 20—30 дней, уменьшая дозу на 1 каплю при каждом приеме до достижения минимальной суточной дозы, перерыв 10 дней. Проводят 2—3 курса лечения. Дийодтирозин — суточная доза 0,2—0,3 г в течение полугода. Перерывы делать необязательно. Если в течение 4—6 месяцев медикаментозное лечение диффузного токсического зоба оказывается неэффективным, больному необходимо рекомендовать лечение хирургическое или радиоактивным йодом. Лечение радиоактивным йодом основано на избирательном свойстве паренхимы щитовидной железы накапливать I131, вызывающий ее местное повреждение без поражения окружающих тканей. Этот метод лечения применим у больных с диффузным токсическим зобом после 40—45 лет при осложненных формах тиреотоксикоза, рецидиве тиреотоксикоза после проведенной медикаментозной антитиреоидной терапии или хирургического лечения. Иногда применяют у лиц с тяжелыми сопутствующими заболеваниями, которым противопоказано хирургическое вмешательство. Лечение радиоктивным йодом противопоказано при максимально неустраненном тиреотоксикозе медикаментозными средствами, больших размеров диффузного токсического зоба, в детском возрасте (способствует развитию рака щитовидной железы) и у женщин в период беременности и лактации. Для предупреждения обострений тиреотоксикоза и тиреотоксического криза лечебную разовую дозу I131 (2—6 мКи) дают без отмены поддерживающих доз мерказолила или метилтиоурацила. Поддерживающую дозу нужно применять не менее 6 последующих месяцев. Противопоказано сочетание радиологического лечения с приемом перхлората калия, блокирующего механизм захвата йода паренхимой щитовидной железы. При лечении радиоактивным йодом могут появиться умеренная болезненность щитовидной железы, кожные аллергические реакции, артралгии и явления острого гастрита. Хирургическое лечение диффузного токсического зоба применяют во всех случаях, когда антитиреоидная медикаментозная терапия в течение 3 месяцев не дает эффекта и для своевременного и полного восстановления нарушенных функций организма. Операция показана также при больших размерах зоба и наличии опухоли в щитовидной железе. Оперативное вмешательство противопоказано после недавно перенесенного инфаркта миокарда, при остром расстройстве мозгового кровообращения. Острые воспалительные заболевания различных локализаций относятся к временным противопоказаниям. Успех хирургического лечения диффузного токсического зоба и профилактика послеоперационного тиреотоксического криза зависят от эффективности комплексной предоперационной подготовки индивидуально у каждого больного. Кроме подготовки психики и устранения или значительного снижения тиреотоксикоза люголевским раствором в сочетании с мерка-золилом, нейроплегическими, седативными и симпатолитиче-скими средствами обязательно проводят терапию, направленную на нормализацию нарушенных функций сердечно-сосудистой системы, печени, надпочечников и других органов. Противопоказан одновременный прием люголевского раствора с перхлоратом калия, который снимает антитиреоидный эффект йода. Субтотальной, субфасциальной струмэктомией по методике О. В. Николаева предусматривается оставление 2—6 г паренхимы железы, необходимых для поддержания дальнейшего длительного эутиреоидного состояния в организме. Лечением тиреотоксического криза предусматривается максимальное и быстрое устранение острого гипертиреоза и тиреотоксикоза. Для этого обычную суточную дозу мерказолила увеличивают до 60 мг, внутривенно вводят 5—10 мл люголевского раствора, в котором калий йод заменен на натрий йод, на 800 мл 5% раствора глюкозы. Каждые 6 ч внутривенно вводят 50—100 мг гидрокортизона (преднизолона). Резерпин дают в дозе 0,25—1 мг каждые 4 ч (при наличии рвоты — ректально). Назначают также барбитураты, сердечные средства (кордиамин, коргликон, строфантин), вдыхание увлажненного кислорода и общую гипотермию тела пузырями со льдом, вентиляторами. Зоб спорадический — заболевание, характеризующееся компенсаторным увеличением щитовидной железы в результате ферментативного дефекта синтеза тиреоидных гормонов, не связанного с определенной местностью. Этиология заболевания еще недостаточно выяснена. Предполагается, что частичные нарушения синтеза тиреоидных гормонов могут иметь место на различных этапах — захват йода железой, его органическое связывание, конденсация йодированных тирозинов, гидролиз тиреоглобулина, дейодинация (Staubury, 1966). Повышенная тиреотропная функция гипофиза приводит к компенсаторной гиперплазии и гипертрофии щитовидной железы, которая способствует формированию вторичной тиреоидной патологии — опухолей, кист, аутоимунного тиреоидита и др. (В. Г. Баранов и соавторы, 1977). Гистологически выявляют уплощение фолликулярного эпителия, накопление коллоида в фолликулах. Клиническое проявление заболевания очень медленное и зависит от формы увеличения щитовидной железы (диффузное, узловое, смешанное), которая может быть мягкой или умеренно плотной, как правило, безболезненная и подвижная при глотании. Состояние больных эутиреоидное, могут иногда наблюдаться легкие функциональные нарушения. Захват йода щитовидной железой умеренно повышен. Дифференциальную диагностику проводят со всеми заболеваниями, вызывающими увеличение щитовидной железы (см. тиреоидиты, диффузный токсический зоб, рак и др.). Лечение проводят тиреоидными препаратами (тиреоидин или Тз). После^ нормализации размеров железы больные принимают поддерживающие дозы препарата. Диффузная форма спорадического зоба больших размеров подлежит хирургическому лечению. Операция показана также при узловых формах зоба, независимо от его величины и функционального состояния железы. Зоб эндемический — заболевание всего организма, сопровождающееся увеличением щитовидной железы, которое встречается постоянно в определенных географических границах, поражает некоторое количество населения и имеет свои закономерности развития. Причиной заболевания служит йодная недостаточность в воздухе, воде, почве и продуктах питания эндемичных районов различных частей света. Недостаточное поступление йода в организм приводит к уменьшению выработки тиреоидных гормонов и снижению уровня белковосвязанного йода. Нарушение цикла обмена йода усиливает продукцию тиреотропного гормона гипофиза, что влечет за собой не только активизацию синтеза тиреоидных гормонов, но и компенсаторную гиперплазию щитовидной железы. Дефицит йода в среде часто сочетается с избытком солей кальция в ней, недостаточным количеством микроэлементов (цинка, меди, брома, магния и др.), с наличием струмогенов в некоторых продуктах растительного происхождения (тиоци-наты, тиоксизолидоны), а также гуминовых веществ, особенно в болотистых местностях, способствующих развитию эндемического зоба. В зависимости от патоморфологических изменений в щитовидной железе различают паренхиматозный и коллоидный зоб. Эндемия паренхиматозного зоба характеризуется наклонностью к образованию узлов микрофолликулярного строения и к гиперплазии паренхимы железы, содержащей большое количество новообразованных фолликулов с малым содержанием коллоида (Гималаи, Альпы и другие горные районы). Коллоидный зоб имеет крупные растянутые фолликулы, заполненные коллоидом. Фолликулярный эпителий уплощен, часто атрофичен. Встречается в районах со средней и легкой андемией (США, некоторые страны Европы). Клиническое проявление заболевания очень медленное, годами больной не знает о его существовании, и выявляют зоб случайно или массовыми профилактическими осмотрами. Нервное перенапряжение, перемена места жительства, роды, аборт и другие факторы могут ускорить развитие заболевания. У больных появляются жалобы на головную боль, слабость, нарушение памяти, плохой аппетит, нередко у женщин нарушается менструальный цикл. Основным симптомом проявления эндемического зоба является диффузное узловое или смешанное увеличение щитовидной железы (см. классификацию). Диффузное увеличение железы I—II степени не принято называть зобом. Этот диагноз устанавливают при III—V степенях гиперплазии (см. классификацию). В настоящее время высокие степени увеличения щитовидной железы встречаются редко. Огромный зоб может дать признаки сдавления трахеи, пищевода, нервов (осиплость голоса), сосудов шеи (одутловатость и синюшность лица) и даже привести к образованию «зобного сердца» (сердечная недостаточность по правожелудочковому типу с резким цианозом, одышкой, застойной печенью, отеками нижних конечностей). Симптомы механического характера могут проявляться и при загрудинном расположении зоба — расстройство дыхания, нарастание одышки при повороте головы. Если зоб находится в заднем средостении, довольно рано появляется дисфагия. По функциональным нарушениям эндемический зоб может быть только эутиреоидным и гипотиреоидным, так как патогенез заболевания связан с дефицитом тиреоидных гормонов. Кретинизм — выраженная форма гипотиреоза при эндемическом зобе. Встречается очень редко и протекает с нарушением интеллекта вплоть до идиотии, снижением физических потребностей, в тяжелых случаях может отсутствовать репродукция и членораздельная речь. В отличие от больных с гипотиреозом (см. гипотиреоз) при кретинизме пониженная функция щитовидной железы сопровождается глухонемотой, косоглазием, клинодактилией, складчатостью языка и другими симптомами, не поддающимися заместительной терапии тире-оидными гормонами. Дифференциальная диагностика наиболее трудна между диффузным токсическим зобом и диффузным эндемическим зобом, протекающим с явлениями вегетоневроза. При эндемическом зобе отсутствует прогрессивная потеря веса тела, постоянная тахикардия (исчезает через 20—30 мин), общая потливость (носит регионарный характер), мелкий тремор вытянутых пальцев рук (крупный, неравномерный), повышенное артериальное давление, глазные симптомы и др. Общим для обоих заболеваний является повышенный захват I131 щитовидной железой, но при эндемическом зобе высокий уровень радиоактивного йода держится долго (48—72 ч). Для тиреотоксикоза характерно быстрое его выведение, Эндемический зоб и аутоиммунный тиреоидит имеют сходную клиническую картину. Оба заболевания начинаются постепенно, без особых функциональных нарушений щитовидной железы, однако явления «скрытого» гипотиреоза и плотность железы наиболее характерны для аутоиммунного тиреоидита. Разграничению диагноза способствует выявление в крови больных лимфоматозным тиреоидитом аутоантител к тиреоидным гормонам. Если аутоиммунный тиреоидит протекает с неравномерным увеличением щитовидной железы в виде узлоподоб-ных образований или вызывает компрессию, дифференциальную диагностику с узловыми формами эндемического зоба целесообразно проводить срочным цитологическим (гистологическим) исследованием во время операции, до выполнения ее основного этапа. Дифференциальную диагностику рака щитовидной железы среди узловых форм эндемического зоба нужно проводить на ранних стадиях развития опухоли, т. е. тогда, когда клинические проявления заболеваний почти не отличаются друг от друга, но это сопряжено с определенными трудностями (см. рак щитовидной железы). Профилактика эндемического зоба состоит в проведении оздоровительных санитарно-гигиенических мероприятий (благоприятные условия труда и жизни) и восполнении недостатка йода в организме введением йодида калия («немая», групповая и индивидуальная профилактика). «Немая» профилактика в СССР — это обеспечение всех эндемичных районов йодированной солью (25 г йодистого калия в каждой тонне соли). Групповую профилактику проводят еженедельно дачей ан-тиструмина дошкольникам — '/2 таблетки, школьникам до 7 класса — 1 таблетку, старшим школьникам, беременным и кормящим женщинам — 2 таблетки (каждая таблетка содержит 1 мг йодистого калия). Индивидуальная йодная профилактика показана всем перенесшим струмэктомию по поводу эндемического зоба, больным зобом, которые отказываются от операции или последняя и гормональная терапия им противопоказаны, а также лицам, временно проживающим в эндемичном районе. Лечение независимо от стадии и формы заболевания начинают с консервативной терапии, которая может привести к полному выздоровлению больного. В случаях, где будет применено хирургическое 'лечение, медикаментозную терапию не более 2—3 месяцев используют как средство предоперационной подготовки. При диффузной форме эндемического зоба больные получают ежедневно 1 таблетку антиструмина в течение 3 месяцев. После достижения лечебного эффекта назначают поддерживающие дозы — 1—2 таблетки антиструмина в неделю. Если в щитовидной железе имеются кистозные или фиброзные дегенеративные изменения, геморрагии и небольшие мягкие узлы на фоне диффузной гиперплазии, лечение проводят тиреоидином (тироксином) под динамическим контролем СБЙ крови и состояния органа. Тиреоидин назначают 0,05 г в сутки, повышая дозировку на 0,05 г каждые 2 недели до максимально переносимой дозы, которая дает возможность сохранить эутиреоидное состояние больного до полного выздоровления, но не менее 6 месяцев. Если гормональная терапия приводит лишь к редукции ткани железы вокруг узла или с самого начала определяется хорошо инкапсулированный плотный узел, методом выбора нужно считать наиболее раннее хирургическое лечение. Операцией предусматривается удаление доброкачественного узла с параузловой тканью только после морфлогического исследования биопсийного материала. Такая тактика позволяет правильно выполнить объем и характер оперативного вмешательства при узловых формах эндемического зоба, аденомах и злокачественных опухолях щитовидной железы, своевременно выявленных в начальных стадиях развития. Лечение эндемического зоба радиоактивным йодом противопоказано, так как приводит к развитию тяжелой пострадиационной микседемы, не поддающейся медикаментозной терапии. Опухоли щитовидной железы. Щитовидная железа характеризуется многообразием структурных форм, определяющих морфологические особенности доброкачественных и злокачественных опухолей. Нарушение биосинтеза тиреоидных гормонов, повышенная тиреотропная стимуляция, гипертрофия и гиперплазия щитовидной железы, развитие в ней аденом и рака рассматривают как различные стадии единого патологического процесса. Опухоли щитовидной железы протекают крайне вариабельно, и поэтому клиническое и морфологическое понятие о злокачественности не всегда идентично. Аденомы щитовидной железы — инкапсулированные, условно доброкачественные опухоли, развивающиеся из тиреоидного эпителия, характеризующиеся самостоятельностью роста и функции. Гистологическая принадлежность аденом соответствует эмбриональным этапам развития щитовидной железы. Различают трабекулярные (эмбриональные), тубулярные (фетальные), микрофолликулярные и макрофолликулярные (коллоидные) аденомы щитовидной железы. Большинство аденом протекает с эутиреоидным состоянием больных, на скеннограмме определяются «холодные» узлы, и клиническая картина соответствует узловым формам эндемического зоба (см. эндемический зоб). Аденомы щитовидной железы меньше 1 см в диаметре почти не определяются пальпацией и не контурируются на скенограмме. Аденома токсическая состоит преимущественно из фолликулярных элементов, в различной степени синтезирует тиреоид-ные гормоны, контурируется на скенограмме в виде «горячих» или «теплых» узлов 4—5 см в диаметре. Клиническая карти-ria чаще соответствует тиреотоксикозу I (см. степени тяжести тиреотоксикоза). У пожилых больных может развиться мерцательная аритмия. Никогда не наблюдается офтальмопатия. Аденомы щитовидной железы подлежат хирургическому лечению на фоне эутиреоза. При токсической аденоме проводят предоперационную подготовку раствором Люголя, в некоторых случаях мерказолилом (см. лечение тиреотоксикоза). Операция — экономная резекция доли щитовидной железы на стороне аденомы после срочного цитологического (гистологического) исследования биопсийного материала. Лечение радиоактивным йодом у больных с токсической аденомой проводят при наличии общих противопоказаний к хирургическому вмешательству. Рак составляет 90% всех злокачественных опухолей щитовидной железы (саркома, злокачественная лимфома, геман-гиотелиома, злокачественная тератома и злокачественные метастазы внетиреоидного характера). Злокачественные опухоли щитовидной железы встречаются чаще у женщин (66—83%) от 40 до 60 лет, однако некоторые формы наблюдаются преимущественно в молодом, юношеском и детском возрасте. За последние десятилетия проблема рака щитовидной железы претерпела значительные изменения. Существующие классификации наряду с морфологическими признаками (многообразие структурных форм, множественность очагов, диффе-ренцировка клеток, критерии злокачественности, пути метаста-зирования) отражают клинические особенности рака железы, позволяющие хирургу избрать соответствующий вид лечения. Принято выделять: 1. Дифференцированные формы рака с относительно медленным ростом (папиллярный рак, фолликулярный рак). 2. Медуллярный рак (солидный рак с амилоидной стро-мой), обладающий «умеренной» злокачественностью. 3. Очень злокачественные анапластические формы рака. Папиллярный рак (папиллярная аденома, злокачественная папиллома, папиллярная цистаденома и др.) среди опухолей щитовидной железы составляет самую большую группу (40—60%), отличается низкой степенью злокачественности и относительно благоприятным течением. Папиллярные формы рака щитовидной железы имеют органоидное строение. При микроскопическом исследовании видны ветвящиеся папиллярные разрастания с васкуляризованной соединительнотканной основой, покрытые кубическим, местами цилиндрическим эпителием. Метастазы наблюдаются редко. Рост опухоли инвазивный, выражена наклонность к образованию кист и кальцификации. Лимфогенные метастазы папиллярного рака множественные как внутри щитовидной железы, так и вдоль сосудистого пучка шеи. Гистологическое строение метастазов такое же, как и основной опухоли. Папиллярный рак не захватывает радиоактивный йод и не продуцирует гормоны. В клиническом проявлении папиллярного рака щитовидной железы можно выделить два варианта. Первый вариант характеризуется медленно растущей, довольно плотной, безболезненной опухолью в щитовидной железе, которая поздно дает метастазы в регионарные лимфатические узлы. Рентгенологически можно выявить участки кальцификации. На скенограмме контурируется в виде «холодного» узла. Второй вариант этой группы — при небольших размерах первичной опухоли, как правило, не проявляющейся клинически, рано появляются метастазы в регионарных лимфатических узлах. Они могут быть первым и единственным признаком заболевания. Метастазы папиллярного рака растут медленно, в течение ряда лет, остаются инкапсулированными, смещаемыми, подвергаются склерозированию и даже обызвествлению. Фолликулярный рак (метастазирующая аденома, атипичная аденома, инкапсулированная ангиоинвазивная карцинома, злокачественная аденома и др.) составляет пятую часть злокачественных опухолей щитовидной железы. Встречается чаще у женщин пожилого возраста. Макроскопически представляет собой инкапсулированный плотный узел без кровоизлияний и некрозов. По гистологическому строению преобладает фолликулярная структура. Фолликулы мелкие, часто неправильной формы, содержат незначительное количество коллоида. Могут встречаться тубуляр-ные и папиллярные элементы, неравномерные по величине клетки и митозы. Опухоли свойственно метастазирование гематогенным путем — отдаленные метастазы, чаще множественные. Первичная опухоль и метастазы функционально активны, способны в различной степени связывать радиоактивный йод. Фолликулярный рак растет в щитовидной железе медленно, в виде плотного, подвижного при глотании узла. Тиреотоксикоз наблюдается редко, чаще имеется эутиреоидное состояние больных. Множественные метастазы в костях появляются рано, растут медленно, сопровождаются болями и патологическими переломами. На скенограмме первичная опухоль может контурироваться в виде «холодных», «теплых» и «горячих» узлов. Медуллярный рак (солитарный рак с амилоидной стромой, С-клеточный рак и др.) составляет 5—10% всех злокачественных эпителиальных опухолей щитовидной железы (возраст больных различный, чаще 40—50 лет), иногда носит семейный характер. Может сочетаться с феохромоцитомой или нейрофибромой слизистой рта, иногда с гиперплазией паращитовидных желез и, как исключение, с гиперплазией коры надпочечников. Опухоль с капсулой, консистенция различная, рост ин-фильтративный, метастазирует гематогенным и лимфогенным путем. Первичная опухоль и метастазы функционально не активны и не способны связывать радиоактивный йод. Медуллярный рак исходит из парафолликулярных клеток, способных продуцировать кальциотонин. Опухоль может развиваться из С-клеток. Гистологически в эозинофильной строме определяются густые клеточные поля, разделенные амилоидными массами. Клетки анаплазированы, полигональные и веретенообразные, протоплазма зернистая, ядра овальные. Митозы встречаются как исключение. Медуллярный рак развивается относительно медленно в виде узлового увеличения щитовидной железы. Плотность опухоли постепенно нарастает, присоединяется болезненность. Метастазы довольно ранние, в регионарные лимфатические узлы или отдаленные, которые поражают легкие, печень, кости и другие органы. На скенограмме контурируется в виде «холодного» узла. У некоторых больных наступает потеря веса из-за постоянных поносов. Кальциотонин в сыворотке крови повышается в 100—1000 раз. Синдром гиперкальциемии отсутствует. Анапластический рак составляет около 10% всех злокачественных эпителиальных опухолей щитовидной железы. Редко встречается у молодых, обычно — у лиц старше 50 лет. Обладает высокой степенью злокачественности, рано дает отдаленные метастазы и, как правило, прорастает капсулу железы, поражая окружающие ткани. Опухоль капсулы не имеет, быстро наступают в ней некрозы. Гистологически, в зависимости от клеточного состава, различают: полиморфно-клеточный, мономорфный (гиганто-клеточный и мелкоклеточный) и веретеноклеточный анапластический рак. Характерно обилие клеточных митозов. Метаплазированный плоскоклеточный рак, лимфосаркому и ретикуло-саркому гистологически трудно отличить от некоторых форм анапластического рака щитовидной железы, особенно в случаях, когда биопсийный материал получен из метастазов опухоли. Первичная опухоль и метастазы функционально не активны и не способны связывать радиоактивный йод. Анапластический рак поражает долю или всю щитовидную железу, которая становится болезненной, ограниченной в подвижности опухолью. Быстрый инфильтративный рост опухоли вовлекает в патологический процесс кожу, может вызвать парез возвратного нерва, затрудненное дыхание и глотание. Рано выявляются увеличенные регионарные лимфатические узлы и отдаленные метастазы. Дифференциальная и клиническая диагностика рака щитовидной железы в начальных стадиях развития представляет большие трудности. Это подтверждается тем, что около 10% удаленных доброкачественных зобов при гистологическом исследовании оказываются злокачественной опухолью. Несмотря на многообразие морфологических форм рака щитовидной железы, общим в клинике для диагностики является: быстрое увеличение ранее существовавшего узлового зоба, появление уплотнений в железе или бугристости неравномерной плотности, безуспешность лечения тиреоидными препаратами. Ограничение смещаемости опухоли, изменение голоса, нарушение дыхания, дисфагия и др. относятся уже к поздним симптомам и связаны с прорастанием рака в соседние ткани и органы. В этот период дифференциальный диагноз между узловым зобом (аденомой) и раком щитовидной железы относительно прост, но значительно затруднено проведение радикальных лечебных мероприятий. К поздним симптомам относится лимфагенное и гематогенное метастазирование даже в тех случаях, когда первичная опухоль в щитовидной железе клинически ничем себя не проявляет. При таком «скрытом» течении первичного очага хирургу необходимо решать еще вопрос, является ли обнаруженная опухоль метастазом рака или аберрантной щитовидной железой, так как дифференциальным диагнозом определяется выбор лечебной тактики. Выявление «холодного» очага на скенограмме, за исключением фолликулярных опухолей, при которых определяются «теплые» или «горячие» узлы, наиболее характерно для злокачественной опухоли щитовидной железы. Во всех диагностически неясных случаях показаны ранняя операция и срочные цитологические (гистологическое) исследования биопсийного материала, позволяющие избежать тактической ошибки. Наличие плотного зоба, ограниченная его подвижность, осиплость голоса, расстройство дыхания и глотания значительно затрудняют постановку дифференциального диагноза рака щитовидной железы и фиброзного тиреоидита. В таких случаях срочный морфологический диагноз, установленный до выполнения основного этапа операции, позволяет устранить компрессионные явления при фиброзном тиреоидите и расширить объем оперативного вмешательства при раке щитовидной железы. Аутоиммунный тиреоидит в отличие от рака щитовидной железы чаще встречается у женщин, характеризуется поражением обеих долей железы, компрессионные симптомы развиваются редко, в сыворотке крови имеются аутоантитела к ти-реоидным антигенам. В диагностически неясных случаях отсутствие заметного эффекта от пробного лечения тиреоидными препаратами (не более 2—4 недель) является показанием для оперативного вмешательства, позволяющего получить своевременный интраоперационный морфологический диагноз. Наибольшее распространение в настоящее время получило комбинированное, или сочетанное, «печение злокачественных опухолей щитовидной железы. При высокодифференцированных опухолях, с локализацией процесса в одной доле железы, показана гемитиреоидэктомия вместе с перешейком или субтотальная тиреоидэктомия. Если имеется поражение регионарных лимфатических узлов, операция дополняется радикальной или измененной шейной дессек-цией. В случаях, когда опухоль вышла за пределы капсулы железы или имеется низкодифференцированная форма рака, применяют расширенную операцию, которая не всегда обеспечивает радикализм. Послеоперационную лучевую терапию предпочтительно проводить на телегаммаустановках или установках для мега-вольтной терапии. Облучение обычно проводят со 2-го или 3-го тангенциальных полей. Разовая доза 150—200 рад. Суммарная доза на очаг 4000—5000 рад. Лучевую терапию как самостоятельный метод лечения злокачественных опухолей щитовидной железы применяют лишь в случаях, при которых операцию выполнить невозможно. Радиактивный йод используют при лечении рака щитовидной железы со множественными отдаленными метастазами (в легкие, кости и др.) после тотальной тиреоидэктомии или подавления гормональной функции неизмененной паренхимы железы другими методами (метилтиоурацил, I131). Гормональное лечение (тиреоидин — 2—3 г, трийодтиро-нин — 200—600 мкг в сутки) применяют длительно при распространенных формах рака щитовидной железы, когда оперативное лечение невыполнимо или явно необластично. Врачебно-трудовая экспертиза. При решении вопроса о трудоспособности больных с заболеваниями щитовидной железы необходимо учитывать характер, распространенность патологического процесса и выраженность наступивших осложнений в организме, зависящих от степени функциональных нарушений. При гипотиреозе (первичный, вторичный, третичный) вопрос о трудоспособности решают с учетом степени заболевания и возможности поддержания компенсации организма гормональными препаратами. При легких формах гипотиреоза трудоустройством по ВКК предусматривается ограничение значительного физического и умственного перенапряжения, общего охлаждения и действия токсических веществ. Больным с выраженным гипотиреозом устанавливают III группу инвалидности, так как им противопоказана работа, связанная с физической нагрузкой, длительной ходьбой, умеренным умственным напряжением, быстрыми предписанными темпами, неблагоприятными метеорологическими условиями труда и воздействием токсических веществ. При тяжелых формах гипотиреоза (микседема, кретинизм) устанавливают II группу инвалидности, так как больные не могут выполнять какой-либо труд. При диффузном токсическом зобе трудоспособность определяют с учетом степени тяжести тиреотоксикоза, если лечение не дает эффекта. При тиреотоксикозе I большинство больных трудоспособны по своей специальности. По решению ВКК, нужно ограничивать длительную ходьбу, действие токсических веществ и высоких температур. При тиреотоксикозе II устанавливают III группу инвалидности и укороченный рабочий день большинству лиц физического и умственного труда. Противопоказаны ночные смены, действие токсических веществ и высоких температур, ненормированный рабочий день и нервно-психическое напряжение. При тиреотоксикозе III устанавливают II группу инвалидности, так как больные не могут заниматься физическим и умственным трудом. При зобе эндемическом — эутиреоидном состоянии большинство больных остаются трудоспособными. При зобе IV—V степени не рекомендуется работа, связанная со значительным физическим напряжением, длительной ходьбой или вынужденным положением тела. Сдавление зобом жизненно важных органов, его загрудинное расположение в сочетании с выраженными сопутствующими заболеваниями, ограничивающими возможность выполнения операции, или злокачественное перерождение щитовидной железы являются показанием для установления II группы инвалидности. Трудоспособность при эндемическом зобе с функциональными нарушениями щитовидной железы решается соответственно выраженности гипотиреоза (см. гипотиреоз). Рак и другие злокачественные опухоли щитовидной железы являются показанием для установления II группы инвалидности. В ряде случаев, для реабилитации, больным разрешается работа с ограниченным рабочим днем, без значительного физического напряжения, ночных смен и воздействия токсических веществ. Тиреоидиты (аутоиммунный, острый, подострый и фиброзный) подлежат лечению. Если заболевание приводит к гипотиреозу, трудоспособность больных определяют соответственно его тяжести (см. гипотиреоз). |
Обследование щитовидной железы
Тиреотропный гормон
Тиреотропный гормон (ТТГ) — показатель, наиболее эффективно отражающий функцию щитовидной железы. ТТГ образуется в передней доле гипофиза и стимулирует выработку тиреоидных гормонов тироксина (Т4) и трийодтиронина (Т3) клетками щитовидной железы, при этом уровень этих гормонов по механизму отрицательной обратной связи контролирует его секрецию. Американская коллегия терапевтов рекомендует определять концентрацию ТТГ у всех женщин старше 50 лет, так как у них высока частота скрытого гипотиреоза [1]. Определение концентрации ТТГ у мужчин и женщин старше 35 лет каждые 5 лет — эффективный и недорогой метод выявления ранней недостаточности щитовидной железы. Его диагностическая значимость увеличивается с возрастом обследуемых и выше для женщин, чем для мужчин [2]. Однако у госпитализированных больных определение ТТГ часто дает ложноположительные результаты [3]. Ниже представлены состояния, ограничивающие диагностическую эффективность метода.
1. Центральный гипотиреоз. Определение ТТГ при этой патологии может давать ложные результаты. Центральный гипотиреоз следует подозревать, если концентрация свободного Т4 снижена, а концентрация ТТГ низкая, нормальная или недостаточно повышена для существующего уровня тиреоидных гормонов [4]. В этом случае у образующегося ТТГ снижена биологическая активность, но сохраняется иммунологическая, которая и определяется при проведении исследования [5].
2. Тиреотоксикоз в результате повышенной выработки ТТГ. Определение только ТТГ у больных с ТТГ-секретирующей аденомой гипофиза может приводить к ошибочным выводам. Диагноз помогают поставить выявление высоких концентраций свободных Т4 и Т3, нормальной или повышенной концентрации ТТГ, повышенного уровня α-субъединицы и обнаружение аденомы гипофиза при МРТ.
3. При лечении гипертиреоза уровень ТТГ может оставаться сниженным в течение 3 мес. и более после достижения клинической ремиссии. Из-за этой отсрочки в нормализации функции гипофиза ориентироваться в течение первых нескольких месяцев лечения следует на концентрацию свободных Т4 и Т3, по крайней мере до стабилизации гормональных показателей.
4. Концентрацию ТТГ могут изменять некоторые лекарственные средства. Дофамин подавляет секрецию ТТГ и может снижать уровень ТТГ у больных с гипотиреозом до нормальных значений. Глюкокортикоиды могут незначительно снижать уровень ТТГ до субнормальных значений. Кратковременная терапия амиодароном может временно повышать уровень ТТГ.
5. Патология другой локализации [6].
Свободный тироксин
Большая часть вырабатывающегося тироксина связывается с белками плазмы крови, и только его незначительная часть циркулирует в крови в свободном состоянии. Тем не менее именно уровень свободного гормона определяет его биологическую активность и достоверность измерения, так как общая концентрация гормона зависит от уровня связывающих его белков. Нарушения белкового состава плазмы могут изменять показатели тиреоидных гормонов, в то время как функция щитовидной железы будет нормальной. Хотя в настоящее время существует множество методик измерения концентрации ТТГ, ни одна из них, включая равновесный диализ, признанный достоверным стандартом диагностики, не позволяет определить истинный уровень влияния белков, конкурирующих с тироксин-связывающим глобулином за связывание Т4 [7].
Общие уровни тироксина и трийодтиронина
Общие уровни Т4 и Т3 в сыворотке крови отражают не только функцию щитовидной железы, но и уровень белков, их связывающих. Расхождение между нормальным уровнем свободных тиреоидных гормонов и высоким общим уровнем гормонов обычно свидетельствует о повышении концентрации связывающих белков. Это состояние известно как эутиреоидная гипертироксинемия. При нормальном уровне Т4 и низком уровне ТТГ следует определить концентрацию Т3 (Т3-токсикоз и скрытый гипертиреоз) [8]. Низкая концентрация Т3 у эутиреоидных больных при острой патологии может быть результатом снижения периферического превращения Т4 в Т3. Причиной гипертиреоза при высоком соотношении Т3/Т4 (> 20 нг/мкг) может быть болезнь Грейвса (диффузный токсический зоб).
Антитиреоидные антитела
Измерение уровня антител к йодидпероксидазе — наиболее чувствительный метод выявления аутоиммунных нарушений щитовидной железы. При использовании чувствительного метода уровень антител повышен у 95 % больных с тиреоидитом Хасимото и у 85 % — с болезнью Грейвса [8].
Антитела к рецепторам ТТГ повышены у большинства пациентов с болезнью Грейвса, хотя для подтверждения диагноза необходимости в этом исследовании, как правило, нет. Измерение уровня этих антител помогает определить риск рецидива гипертиреоза при болезни Грейвса после лечения антитиреоидными средствами [9]. Также их измеряют для определения риска нарушений функций щитовидной железы у плода и новорожденного при наличии у беременной аутоиммунного поражения щитовидной железы в анамнезе [10].
Антитела к тиреоглобулину измеряют дополнительно к определению концентрации тиреоглобулина в сыворотке крови при наблюдении за больными дифференцированным раком щитовидной железы. Даже очень низкий уровень этих антител может нарушать определение концентрации тиреоглобулина, что приводит к получению ложноповышенных или пониженных показателей [11]. Неожиданное повышение концентрации или появление антител к тиреоглобулину может быть первым признаком рецидива [8].
Тиреоглобулин
Тиреоглобулин — предшественник тиреоидных гормонов, который присутствует в крови здоровых людей. Его концентрация отражает три показателя: объем дифференцированной ткани щитовидной железы, физическое повреждение или воспаление щитовидной железы и уровень стимуляции рецепторов к ТТГ, так как большая часть этапов синтеза и секреции тиреоглобулина ТТГ-зависима [12]. Повышение уровня тиреоглобулина — неспецифичный признак нарушения функции щитовидной железы. Определение тиреоглобулина помогает отличить лекарственный гипертиреоз, возникающий при передозировке тиреоидных гормонов, от истинного эндогенного гипертиреоза, так как в первом случае его уровень обычно снижен, а во втором — повышен. Уровень тиреоглобулина прежде всего служит опухолевым маркером при наблюдении за больными с дифференцированным раком щитовидной железы после резекции щитовидной железы для выявления возможных рецидивов и метастазов. Определение концентрации тиреоглобулина на фоне стимуляции ТТГ (эндогенным ТТГ после отмены тиреоидных гормонов или рекомбинантным препаратом ТТГ) — более чувствительный метод для выявления дифференцированного рака щитовидной железы, чем определение базального уровня тиреоглобулина на фоне супрессивной терапии левотироксином [13].
Методы визуализации щитовидной железы
Ультразвуковое исследование
Ультразвуковое исследование (УЗИ) — метод выбора для определения размеров и морфологии щитовидной железы. Метод максимально чувствителен для выявления узлов щитовидной железы и позволяет определять поражения до 2–3 мм в диаметре. Также его используют для контроля проведения тонкоигольной аспирационной биопсии пальпируемых и непальпируемых узлов. Ультразвуковые признаки злокачественных узлов — гипоэхогенность, микрокальцификаты, широкое, неравномерное гало или его отсутствие, неравномерные края, поражение регионарных лимфоузлов и точечные кровоизлияния в ткани узла [14]. Однако УЗИ не позволяет точно отличить доброкачественные узлы от злокачественных, для этого необходимо провести тонкоигольную аспирационную биопсию. Также УЗИ проводят для обследования регионарных лимфоузлов при раке щитовидной железы как для предоперационной оценки их состояния, так и для контроля после операции. По результатам некоторых исследований, УЗИ — более чувствительный метод контроля, чем измерение концентрации тиреоглобулина и сцинтиграфия [15]. Основные недостатки УЗИ — высокая субъективность и невозможность выявлять поражения, расположенные за трахеей, ключицами и грудиной.
Сцинтиграфия
Сцинтиграфия с 99mТс — стандарт функциональной визуализации щитовидной железы. Обычно применяют один из двух радиоактивных изотопов: 123I или 99mТс-пертехнетат, при этом второй предпочтительнее из-за меньшей стоимости и большей доступности. Сцинтиграфия с 99mTс позволяет оценить функциональную способность тканей щитовидной железы и узла. Сцинтиграфию щитовидной железы проводят, чтобы:
— подтвердить, что крупное пальпируемое образование представляет собой скорее долю железы, чем узел;
— определить размер функционирующей части щитовидной железы;
— выявить причины гипертиреоза: гомогенное повышение захвата характерно для болезни Грейвса, а неравномерное — для многоузлового зоба или узлов щитовидной железы;
— определить функциональную активность узлов: горячие, или гиперфункциональные, узлы редко бывают злокачественными; выявление подобных узлов требует уточнения их природы с помощью тонкоигольной аспирационной биопсии;
— отследить эволюцию характеристик узлового зоба [16].
Компьютерная томография
Компьютерную томографию (КТ) применяют для выявления рецидива рака щитовидной железы, в частности для определения степени загрудинного роста опухоли и наличия метастазов в лимфоузлы, инвазии, сдавления или смещения трахеи, а также сосудистой инвазии. Также КТ помогает оценить опухоли, происхождение которых из щитовидной железы сомнительно, и массивные образования с возможной инвазией в соседние структуры. При выявлении образований в ткани щитовидной железы КТ менее чувствительна, чем УЗИ.
Исследование с радиоактивным йодом
Определение захвата радиоактивного йода предназначено для выявления гипертиреоза, дифференциальной диагностики подострого или скрытого тиреоидита и токсического зоба, определения целесообразности проведения терапии радиоактивным йодом и при ее необходимости — расчета дозы. Захват радиоактивного препарата отражает процессы поступления йода в фолликулярные клетки щитовидной железы, его окисление, йодирование гормонов и его высвобождение. Повышенный захват наблюдают при гипертиреозе, тиреоидите Хасимото, дефиците йода, подостром, скрытом или послеродовом тиреоидите в стадии восстановления, хориокарциноме и пузырном заносе, а также при лечении препаратами лития. Снижение захвата йода происходит при подостром, скрытом или послеродовом тиреоидите в тиреотоксической стадии, тиреоидите Хасимото с массивным разрушением паренхимы, агенезии щитовидной железы, после терапевтического разрушения щитовидной железы и при применении антитиреоидных средств [16].
Сцинтиграфия всего тела с 131I
Сцинтиграфию всего тела с 131I применяют для обследования пациентов с подозрением на рецидив или метастазирование рака щитовидной железы. По данным разных исследований, чувствительность метода значительно колеблется, составляя в среднем от 50 до 60 % в зависимости от дозы изотопа и локализации опухоли, будучи максимальной при метастазах в кости и легкие и минимальной при метастазах в лимфоузлы [17]. Специфичность метода достигает 90–100 % [18]. При комбинации с измерением тиреоглобулина после стимуляции ТТГ чувствительность метода значительно возрастает, составляя 93 % при ограничении образования ложем щитовидной железы и 100 % — при метастатическом поражении [13].
Позитронная эмиссионная томография с [18F]-фтордезоксиглюкозой
Позитронная эмиссионная томография (ПЭТ) с [18F]-фтордезоксиглюкозой помогает поставить диагноз в тех случаях подозрения на рецидив или метастазы рака щитовидной железы, когда другие исследования, например сцинтиграфия всего тела с 131I, не дали результатов [19]. Его чувствительность в этих случаях достигает 94 %, а специфичность — 95 % [20]. Этот метод особенно эффективен при раке из клеток Гюртле, при котором он также чувствительнее, чем сцинтиграфия всего тела [21].
Гипертиреоз
Определение
Гипертиреоз — синдром, развивающийся в результате реализации метаболических эффектов избыточного количества тиреоидных гормонов — Т4, Т3 или обоих сразу. При скрытом гипертиреозе ТТГ не определяется, а концентрация Т3 и Т4 сохраняется нормальной вне зависимости от наличия или отсутствия клинических проявлений.
Этиология
Гипертиреоз может быть эндогенного (повышенная выработка тиреоидных гормонов изолированно или в сочетании с их повышенным выделением) и ятрогенного (заместительная терапия тиреоидными гормонами или прием любых других препаратов, вызывающих тиреоидит) происхождения. Самые частые причины эндогенного гипертиреоза — болезнь Грейвса (диффузный токсический зоб), многоузловой токсический зоб, токсическая аденома и тиреоидит. Выделяют две формы подострого тиреоидита: болевую вирусного происхождения (гранулематозную) и безболевую, которая обычно встречается спорадически и чаще — в послеродовый период. В этом случае высокая частота обнаружения антител к йодидпероксидазе в сыворотке больных, лимфоцитарная инфильтрация ткани щитовидной железы, часто в сочетании с другими аутоиммунными заболеваниями, свидетельствуют об аутоиммунной природе патологии. Супрессивная терапия тиреоидными гормонами при раке и доброкачественных узлах щитовидной железы, избыточная заместительная гормональная терапия при гипотиреозе и злоупотребление препаратами тиреоидных гормонов также могут вызывать развитие клинически явного или бессимптомного гипертиреоза.
Эпидемиология
Болезнь Грейвса является причиной гипертиреоза примерно в 60–80 % случаев. Она встречается в 10 раз чаще у женщин, при этом риск заболевания выше в возрастной категории от 40 до 60 лет. Болезнь одинаково распространена среди представителей европеоидной и монголоидной рас и реже встречается среди лиц негроидной расы [22]. Автономные аденомы и токсический многоузловой зоб более распространены в странах Европы, а также в других регионах с дефицитом йода. Они также чаще встречаются у женщин и у пожилых (старше 60 лет) людей.
Патофизиология
При болезни Грейвса аутоантитела связываются и стимулируют рецепторы к ТТГ, что приводит к повышению уровня внутриклеточной цАМФ. Повышение цАМФ в свою очередь вызывает рост щитовидной железы с формированием зоба и увеличение выработки и выделения тиреоидных гормонов. С появлением высокочувствительных методов анализа эти антитела выявляют более чем у 90 % больных. Формирование токсического многоузлового зоба по-прежнему порождает больше вопросов для исследования, нежели ответов. Автономия щитовидной железы считается основным патогенетическим механизмом развития токсической аденомы и, вероятно, связана с соматическими мутациями, приводящими к активации каскада цАМФ. Подобные мутации подробно описаны [23], а в некоторых случаях многоузлового зоба описано сразу несколько мутаций у одного и того же пациента. Также в патогенезе токсического многоузлового зоба могут принимать участие факторы роста, повышенный захват йода и иммунные нарушения.
Диагностика
Основные клинические проявления гипертиреоза — нервозность, раздражительность, тремор, повышенная утомляемость, тахикардия или сердцебиение, непереносимость жары и снижение веса, часто несмотря на повышение аппетита. У больных более старшего возраста также наблюдаются мерцательная аритмия, сердечная недостаточность и общая слабость. При болезни Грейвса обычно обнаруживают плотный диффузный зоб (90 %), офтальмопатию (50 %) и локальную дермопатию переднелатеральной поверхности голени (1–2 %) [22]. При токсической аденоме во время физикального исследования часто обнаруживают пальпируемый узел щитовидной железы, в то время как для токсического многоузлового зоба более характерно плотное образование неоднородной консистенции различного размера. У некоторых больных с многоузловым зобом может отмечаться загрудинный рост зоба. Часто токсические аденомы и многоузловой зоб никак не проявляются клинически или проявляются слабо; диагноз в этом случае можно поставить только при обнаружении изменений лабораторных показателей. Подострый (гранулематозный) тиреодит может возникать после вирусной инфекции верхних дыхательных путей и характеризуется необычным размягчением щитовидной железы. Но чаще встречается его безболевая форма, развивающаяся в послеродовой период и характеризующаяся преходящим гипертиреозом с последующим развитием различного по продолжительности гипотиреоза и спонтанным самостоятельным разрешением. Лабораторная диагностика гипертиреоза представлена в табл. 1. Для явного гипертиреоза характерно снижение концентрации ТТГ и повышение концентрации Т4 и Т3, а при скрытом гипертиреозе концентрации тиреоидных гормонов обычно сохраняются нормальными. При подозрении на болезнь Грейвса рекомендуют определять уровень антител к рецепторам ТТГ. У больных с клиническими проявлениями гипертиреоза, повышением концентрации тиреоидных гормонов и нормальной или повышенной концентрацией ТТГ (неадекватная секреция ТТГ) следует исключить ТТГ-вырабатывающую опухоль гипофиза или избирательную резистентность клеток гипофиза к тиреоидным гормонам. Аналогичные лабораторные изменения без клинических проявлений гипертиреоза характерны для синдрома генерализованной резистентности к тиреоидным гормонам. В постановке диагноза значительную помощь могут оказать определение захвата радиоактивного йода и сцинтиграфия щитовидной железы. Повышенный гомогенный захват йода наблюдается при болезни Грейвса, в то время как при подостром тиреодите и гипертиреозе, вызванном гормональной терапией, захват будет снижен. Для токсических аденом характерно локальное повышение захвата радиоактивного препарата, а при многоузловом зобе общий захват йода может быть нормальным, но распределение будет неоднородным.
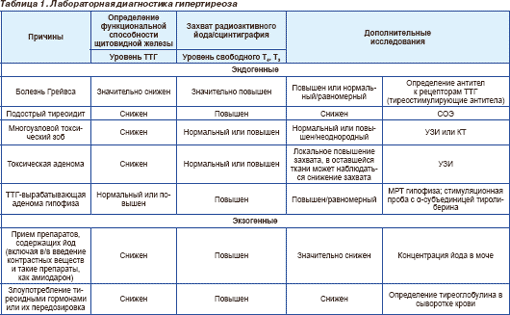
Лечение
Антитиреоидные препараты. Антитиреоидные средства — препараты выбора для лечения болезни Грейвса в большинстве стран мира. В США чаще всего применяют пропилтиоурацил в дозе от 100 до 150 мг каждые 8 ч и тиамазол в дозе от 10 до 40 мг 1 раз в сутки. При лечении гипертиреоза следует по возможности ограничиться минимальной дозой для поддержания эутиреоидного состояния, так как высокие дозы препаратов не снижают частоту рецидивов, но могут повышать частоту побочных реакций [24]. Тиамазол имеет преимущество однократного приема, что, безусловно, повышает комплайентность больных, однако пропилтиоурацил предпочтительнее во время беременности, так как он в меньшей степени проникает через плаценту. Основной недостаток лекарственной терапии — высокая частота рецидивов после прекращения лечения (приблизительно 60 %). Более длительное лечение позволяет несколько улучшить показатели ремиссии [25], хотя доказано, что увеличение продолжительности лечения более 18 мес. не приводит к достоверному улучшению результатов [26]. Длительная терапия, вероятно, показана и безопасна [27] только в том случае, если состояние больного можно контролировать низкими дозами препаратов. К основным побочным эффектам относят аллергические реакции, гепатит, артрит и агранулоцитоз.
Антитиреоидные препараты и левотироксин. Исследование, проведенное в Японии, показало, что значительно снизить частоту рецидивов (с 35 до менее чем 2 %) позволяет дополнительное назначение левотироксина после 6 мес. лечения тиамазолом с последующим его приемом в течение 3 лет после отмены тиамазола [28]. Однако другое исследование не подтвердило эти результаты [29]. Данные о целесообразности применения антитиреоидных средств при болезни Грейвса до терапии радиоактивным йодом противоречивы, не получено достоверного подтверждения того, что эти препараты предотвращают усугубление тиреотоксикоза, снижают время до достижения эффекта или частоту рецидивов [30].
Радиоактивный йод. Препараты радиоактивного йода применяют для лечения гипертиреоза более 60 лет. В США это средства выбора при болезни Грейвса, также они широко распространены во всем мире. Препараты радиоактивного йода показаны при болезни Грейвса, токсических узлах и многоузловом токсическом зобе [31]. Они эффективны, безопасны и позволяют уменьшать размеры щитовидной железы, хотя при крупных размерах зоба и тяжелом гипертиреозе могут потребоваться повторные курсы лечения [32]. Основной недостаток — развитие стойкого гипотиреоза у значительного числа пациентов, требующих пожизненной заместительной терапии тиреоидными гормонами. Некоторые исследователи считают, что применение радиоактивного йода временно усугубляет офтальмопатию при болезни Грейвса, для лечения которой назначают преднизолон [33].
Хирургическое лечение. При гипертиреозе хирургическое лечение показано больным с большими размерами зоба с признаками сдавления, с сопутствующими узлами щитовидной железы, при наличии противопоказаний или отказе от лекарственной терапии и лечения препаратами радиоактивного йода, беременным, а также при невозможности контролировать течение заболевания лекарственными средствами или развитии аллергических реакции на антитиреоидные препараты. Хирургическое лечение, как правило, безопасно и эффективно, общий уровень эффективности лечения достигает 92 % [34]. Осложнения включают гипопаратиреоз, паралич голосовых складок и гипотиреоз.
β-адреноблокаторы. β-адреноблокаторы используют для уменьшения адренергических проявлений гипертиреоза, поэтому их назначают в качестве предварительной дополнительной терапии и отменяют при достижении эффекта основной терапии антитиреоидными средствами и препаратами радиоактивного йода или хирургического лечения. β-адреноблокаторы также эффективно и безопасно применяются для предоперационного лечения. Доказано, что они быстрее приводят к облегчению проявлений гипертиреоза по сравнению с традиционной предоперационной подготовкой антитиреоидными препаратами [35].
Гипотиреоз
Определение
Гипотиреоз — клинический синдром, развивающийся при снижении выработки и выделения тиреоидных гормонов, чаще в результате поражения щитовидной железы (первичный гипотиреоз), и сопровождающийся повышением уровня ТТГ. Менее чем в 5 % случаев гипотиреоз имеет гипоталамическое или гипофизарное происхождение (вторичный гипотиреоз), в этом случае снижение концентрации тиреоидных гормонов будет сопровождаться нормальным или даже низким уровнем ТТГ. Для скрытого гипотиреоза характерно повышение концентрации ТТГ при нормальных показателях свободного Т4 и Т3, обычно на фоне бессимптомного течения.
Этиология
Ведущая причина гипотиреоза — тиреоидит Хасимото. Лечение тиреотоксикоза препаратами радиоактивного йода, резекция щитовидной железы, лекарственные средства (препараты лития и препараты, содержащие йод) или введение йодосодержащих контрастных веществ также могут вызывать гипотиреоз. Центральный гипотиреоз развивается при поражении гипоталамуса или гипофиза.
Эпидемиология и патофизиология
Гипотиреоз — одно из самых частых эндокринных нарушений. Его распространенность увеличивается с возрастом, и он чаще встречается у женщин, чем у мужчин. Около 2 % женщин в возрасте от 70 до 80 лет имеют клинически явный гипотиреоз. Частота бессимптомного гипотиреоза у женщин старше 50 лет несколько выше — 5–10 % [1]. Тиреоидит Хасимото — аутоиммунное поражение щитовидной железы, проявляющееся лимфоцитарной инфильтрацией ее тканей с последующей атрофией фолликулярных клеток и фиброзом. Примерно у 50–80 % больных со скрытым гипотиреозом обнаруживают антитела к йодид-пероксидазе.
Диагностика
Определение концентрации ТТГ — наиболее чувствительный метод для диагностики первичного гипотиреоза. Скрытый гипотиреоз обычно протекает бессимптомно и характеризуется нормальными показателями тиреоидных гормонов. При явном гипотиреозе отмечают низкий уровень тиреоидных гормонов и такие неспецифичные проявления, как непереносимость холода, увеличение веса, запоры, сухость кожи, повышенная утомляемость и периорбитальный отек. Необходимость массового обследования на скрытый гипотиреоз остается спорной, так как проведенные проспективные клинические испытания не подтвердили эффективность последующей терапии в этом случае. При центральном гипотиреозе отмечают снижение уровня тиреоидных гормонов, а также сниженный или нормальный уровень ТТГ. Для исключения поражения и опухолей гипоталамуса и гипофиза рекомендуется МРТ.
Лечение
Левотироксин. Левотироксин — препарат выбора при гипотиреозе. Обычная замещающая доза составляет от 1,6 до 4,2 мкг/кг в сутки, при этом дозу следует повышать до нормализации уровня ТТГ [36]. Оптимальной считают концентрацию ТТГ в сыворотке крови от 0,5 до 2 мМЕ/л [8]. Необходимость лечения скрытого гипотиреоза до конца не установлена. Некоторые исследования показали, что раннее назначение заместительной гормональной терапии уменьшает легкие проявления гипотиреоза [37] и улучшает показатели липидов сыворотки [38, 39], в то время как в других исследованиях не выявлено влияния лечения ни на общий уровень холестерина, ни на уровень холестерина ЛПНП [37].
Левотироксин и лиотиронин. Комбинация левотироксина и лиотиронина предложена в качестве альтернативы изолированному применению левотироксина, так как представляет собой более физиологичную форму заместительной терапии [40]. Однако следует отметить, что улучшение настроения и психоневрологических функций [40] не нашло подтверждения в последующих контролируемых испытаниях [41–43], несмотря на предпочтение больными в некоторых исследованиях именно этой комбинации препаратов [44].
Узлы щитовидной железы
Этиология
Автономно функционирующие (токсические) аденомы щитовидной железы могут развиваться в результате мутаций гена рецепторов к ТТГ или гена α-субъединицы белка G, приводящих к активации каскада цАМФ, а следовательно, к усилению ответа на стимуляцию ТТГ. Эти мутации вызывают рост и увеличение функциональной активности пораженных клеток, что, в свою очередь, приводит к образованию автономного узла, подавлению секреции ТТГ и снижению функции остальной части железы. При постепенном объединении автономных фолликулов различной степени активности формируется многоузловой токсический зоб.
Эпидемиология
Узлы щитовидной железы часто встречаются в клинической практике. Их распространенность в значительной степени зависит от используемого метода диагностики и характера обследуемой популяции. При пальпации, наименее чувствительном методе, их частота составляет примерно 4 % [45]. При УЗИ высокого разрешения показатель возрастает до 67 % [46]. По данным аутопсии больных без установленных заболеваний щитовидной железы в анамнезе, узлы обнаруживают в 50 % случаев [47]. Риск развития узлов щитовидной железы выше у лиц старшего возраста, женщин и больных, подвергавшихся лучевой терапии по поводу опухолей головы и шеи. По данным Фремингемского исследования, частота ежегодного выявления узлов при пальпации составляет 0,09 % [45].
Диагностика
Обычно узлы в щитовидной железе обнаруживают при пальпации области шеи во время стандартного физикального обследования. Диаметр большинства пальпируемых образований составляет как минимум 1 см. Также узлы могут случайно обнаруживаться при УЗИ шеи по поводу другой патологии. Определение концентрации ТТГ — лучший метод для определения функциональной активности узла. Если узел функционально активен, то ТТГ будет снижен. Для подтверждения диагноза показана сцинтиграфия.
Тонкоигольная аспирационная биопсия — наиболее значимый, эффективный и экономически оправданный метод определения злокачественности узла. Чувствительность и специфичность этого метода при раке щитовидной железы составляют соответственно 83 (65–98) и 92 (72–100)%, а общая диагностическая точность достигает 95 % [48]. К основным недостаткам исследования можно отнести сомнительные результаты и выявление неопределенных гистологических изменений, частота которых составляет соответственно 15 и 20 %. Повторная биопсия под контролем УЗИ может помочь преодолеть первый из недостатков, но в большинстве таких случаев для постановки точного диагноза все-таки необходимо хирургическое вмешательство. Случайно выявленные новообразования щитовидной железы встречаются довольно часто. Частота рака при обнаружении таких узлов колеблется от 6 до 9 % [14]. Такой же показатель отмечается при узлах больше или меньше 1 см. Независимыми признаками злокачественности считают неровные контуры образования, микрокальцификаты и точечные кровоизлияния в узел. В 87 % случаев при раке обнаруживают гипоэхогенное образование. При тонкоигольной аспирационной биопсии узлов при наличии хотя бы одного фактора риска частота выявления рака также достигает 87 % [14].
Лечение
Хирургическое лечение. Узлы при подозрении на их злокачественный характер или при получении сомнительных результатов тонкоигольной аспирационной биопсии необходимо удалять. Объем хирургического вмешательства остается спорным вопросом. Некоторые авторы считают целесообразным удалять щитовидную железу целиком или почти целиком, другие склонны ограничиться удалением только пораженной доли. Доброкачественные одиночные или множественные узлы не требуют хирургического лечения за исключением случаев сдавления соседних структур и гипертиреоза. Таким образом, хирургическое лечение показано больным с большими и/или гиперфункционирующими образованиями щитовидной железы [49].
Супрессивная терапия левотироксином. Данные об эффективности супрессивной гормональной терапии при узлах щитовидной железы противоречивы. В одном метаанализе показана эффективность супрессивной терапии левотироксином в подгруппе больных (20–23 %), при этом вероятность уменьшения узла как минимум на 50 % в 1,9–2,5 раза выше по сравнению с плацебо [50]. Однако, согласно данным другого исследования, достоверного эффекта терапии не выявлено [51]. Признаки возможного достижения эффекта не определены. Перед назначением терапии следует учитывать такие возможные побочные эффекты, как поражение сердечно-сосудистой и опорно-двигательной систем [52, 53]. Супрессивная терапия не показана при узлах с высокой функциональной активностью. Единственное контролируемое испытание эффективности супрессивной терапии при многоузловом нетоксическом зобе показало, что уменьшение объемов щитовидной железы происходит более чем на 13 % в 58 % случаев в группе левотироксина по сравнению с 5 % в группе плацебо [54].
Радиоактивный йод. Прием препаратов радиоактивного йода приводит к уменьшению объема щитовидной железы у 60 % больных с многоузловым нетоксическим зобом, а также у большинства из них уменьшает признаки сдавления [55]. Препараты эффективны примерно в 90 % случаев одиночной токсической аденомы, хотя необходимость назначения относительно высоких доз приводит к развитию отдаленного гипотиреоза у 10–20 % больных [49]. Также радиоактивный йод эффективен в 80–100 % многоузлового токсического зоба, хотя часто требуется проведение нескольких курсов терапии [56].
Чрескожная деструкция этанолом. Чрескожная деструкция этанолом показана больным, которые не могут пройти стандартное лечение или отказываются от него. Чрескожная деструкция этанолом не показана при солидных образованиях щитовидной железы из-за развития местного болевого синдрома, возможности повреждения возвратного гортанного нерва и необходимости проведения повторных курсов. В то же время при преимущественно кистозных узлах эту процедуру считают безопасной и эффективной. Ее проведение в данном случае вызывает выраженное уменьшение размеров узла, косметического дефекта и признаков сдавления (приблизительно до 80 % случаев) [57, 58].
Лазерная тепловая деструкция (лазерная вапоризация). Лазерная деструкция под контролем УЗИ — альтернативный способ лечения больных с доброкачественными гипофункциональными узлами щитовидной железы с признаками сдавления при наличии противопоказаний к хирургическому лечению или отказе от него. Этот метод приводит к уменьшению размеров узла на 45–60 % через 6 мес. после проведения процедуры [59, 60]. Лазерная деструкция требует особых навыков и должна проводиться только в специализированных медицинских центрах.
Рак щитовидной железы
Определение и классификация
Рак щитовидной железы — злокачественное новообразование, происходящее из эпителия щитовидной железы. Папиллярный и фолликулярный рак, входящий в группу дифференцированных раков щитовидной железы, формируется из эпителия фолликулов (фолликулярного эпителия). К другим злокачественным опухолям из фолликулярных клеток относят оксифильный рак (или рак из клеток Гюртле) и недифференцированный, или анапластический, рак. Медуллярный рак щитовидной железы образуется из парафолликулярных, кальцитонин-синтезирующих клеток (С-клетки). Чаще всего в США встречается папиллярный рак (его частота достигает 80 %), затем следует фолликулярный (10–15 %), медуллярный (5 %) и анапластический (5 %) рак. Примерно в 75 % случаев медуллярный рак носит спорадический характер, а в 25 % это наследственные или семейные формы (множественная эндокринная неоплазия типа 2А или 2В и семейный медуллярный рак).
Эпидемиология
Рак щитовидной железы обычно впервые обнаруживается как пальпируемый узел в ткани железы. Хотя узлы в щитовидной железе довольно распространены, рак встречается довольно редко, составляя только 1–2 % от всех злокачественных новообразований. Он встречается в 3 раза чаще у женщин. Ежегодно в мире выявляется 0,5–10 случаев на 100 000 населения. В CIIIA каждый год обнаруживают 18 000 новых случаев рака, являющихся причиной смерти в 1200 случаях в год [61]. В США частота скрытого рака щитовидной железы, выявляемого при аутопсии, колеблется от 0,5 до 13 %. В некоторых популяциях на развитие рака могут влиять генетические (отягощенный семейный анамнез) и внешние (воздействие ионизирующего излучения) факторы. К признакам высокой вероятности рака относят размер узла более 4 см, сращение с прилежащими структурами, увеличение регионарных лимфоузлов, паралич голосовых складок, быстрый рост узла и возраст больных младше 15 и старше 60 лет.
Диагностика
Исследование функции щитовидной железы. Уровень ТТГ определяют у всех больных с узлами щитовидной железы. При его повышении для исключения сопутствующего тиреоидита Хасимото показано определение антител к йодидпероксидазе. У больных с низкой концентрацией ТТГ и высокой концентрацией свободного Т4 может быть токсический узел. Так как риск озлокачествления в этом случае невелик, получение положительных результатов при сцинтиграфии требует проведения тонкоигольной аспирационной биопсии.
Тонкоигольная аспирационная биопсия. Большинство раков щитовидной железы протекают бессимптомно и обнаруживаются как уже пальпируемое образование при стандартном обследовании органов шеи. Тонкоигольная аспирационная биопсия остается единственным наиболее точным, достоверным и экономически оправданным методом диагностики рака щитовидной железы. Повторная тонкоигольная аспирационная биопсия под контролем УЗИ повышает диагностическую значимость биопсии и позволяет поставить диагноз. Однако получение сомнительных результатов при повторных аспирациях, особенно при больших солидных узлах или других признаках злокачественности, требует проведения тотальной биопсии. Подозрительные узлы почти всегда следует подвергать тотальной биопсии с учетом того, что вероятность их злокачественности может достигать 30 % [48, 62].
Опухолевые маркеры. Тиреоглобулин — гликопротеин, образующийся в щитовидной железе в ответ на действие ТТГ, — может использоваться как достоверный опухолевый маркер только после полной деструкции щитовидной железы, например после хирургического удаления или разрушения радиоактивным йодом (131I). В этих случаях определение тиреоглобулина на фоне отсутствия антител к нему — достоверный маркер местного рецидива рака или наличия регионарных или отдаленных метастазов. Чувствительность определения тиреоглобулина возрастает при стимуляции ТТГ, например при отмене Т4 или приеме рекомбинантного ТТГ, по сравнению с подавлением ТТГ [12, 63]. Выявление тиреоглобулина в смывах иглы после тонкоигольной аспирационной биопсии подозрительных лимфоузлов шеи у больного с раком щитовидной железы в анамнезе подтверждает развитие метастазов [64, 65]. Этот метод более чувствителен, чем цитологическое исследование образцов, полученных при биопсии лимфоузлов, к тому же при таком определении тиреоглобулина его уровень не зависит от антител сыворотки крови [65].
Кальцитонин, образующийся в парафолликулярных С-клетках, — наиболее чувствительный маркер диагностики и контроля медуллярного рака щитовидной железы, так как базальный уровень кальцитонина повышен у большинства больных медуллярным раком, при этом он может быть повышен и при бессимптомном течении заболевания. Введение стимуляторов секреции кальцитонина, например кальция и пентагастрина (последний в США больше не применяют), вызывает у больных медуллярным раком повышение концентрации кальцитонина, что позволяет выявлять гиперплазию С-клеток на ранних стадиях, иногда даже до развития самого рака. При наличии мутаций, характерных для семейных форм рака, стимуляционные пробы заменяются генетическим обследованием родственников первой линии больных медуллярным раком [66]. В 5 % случаев семейных форм рака выявить мутацию не удается, тогда у членов семьи определяют концентрацию кальцитонина после стимуляции его секреции. При этом пиковое значение кальцитонина будет превышать среднестатистические показатели. Умеренное повышение базальной или стимулированной секреции кальцитонина следует интерпретировать с особой осторожностью.
Раково-эмбриональный антиген сам по себе — малозначимый биохимический маркер при медуллярном раке. Его определение в сочетании с кальцитонином используют для контроля лечения больных с медуллярным раком. Так, сохранение высоких концентраций этих веществ после радикальной операции может говорить об остаточном раке или развитии метастазов. Уровни этих веществ, вероятно, зависят от размеров опухоли, будучи выше у больных с явными формами медуллярного рака по сравнению со скрытыми.
Лечение
Хирургическое лечение. Основное лечение рака щитовидной железы — полное удаление опухолевой ткани в пределах шеи. Объем удаления остается спорным вопросом. Никаких проспективных контролируемых исследований для его уточнения пока не проводилось. Так, некоторые авторы указывают на достаточность односторонней лобэктомии в большинстве случаев папиллярного или фолликулярного рака в группах низкого риска, приводя в качестве довода низкие показатели смертности и повышение частоты осложнений при увеличении объема операций [67]. Тем не менее большинство врачей считают целесообразным удалять всю или почти всю щитовидную железу [68–70], так как это снижает частоту местных рецидивов, регионарных метастазов и улучшает показатели выживаемости [70, 71]. Односторонняя лобэктомия связана с более высокой частотой отдаленных рецидивов (30 против 1 % при тотальном удалении щитовидной железы с последующей терапией 131I). К тому же папиллярные раки обычно многоочаговые и двусторонние [72].
Практически полное удаление щитовидной железы дополняют терапией радиоактивным йодом с последующим определением уровня тиреоглобулина и проведением сцинтиграфии всего тела для контроля развития рецидивов и метастазов. Изолированная лобэктомия показана при одиночном очаге папиллярной микрокарциномы, ограниченной пределами щитовидной железы и без сосудистой инвазии [69].
Полное удаление щитовидной железы с лимфаденэктомией центральной области шеи показано всем больным с подтвержденным или подозреваемым медуллярным раком, так как при семейных формах этого рака поражение обычно носит двусторонний многоочаговый характер. При этом следует учитывать тот факт, что примерно 10–20 % спорадических случаев в действительности имеют семейный характер.
Разрушение остатков ткани щитовидной железы радиоактивным йодом. Несмотря на то что применение радиоактивного йода в постоперационном периоде у больных с дифференцированным раком щитовидной железы широко распространено, показания к использованию радиоактивного йода для деструкции и последующих диагностических и терапевтических вмешательств до сих пор не определены. Причина этого — отсутствие контролируемых проспективных исследований. В большинстве ретроспективных исследований показано снижение частоты рецидивов и смертности, обусловленной опухолью, при раннем назначении дополнительной терапии радиоактивном йодом [69, 73]. По результатам обзора, включившего 1599 больных, проходивших лечение в онкологическом центре М.Д. Андерсона, терапия радиоактивным йодом была единственным значимым фактором прогноза развития безрецидивного периода и повышения уровня выживаемости [55]. Преимущества деструкции радиоактивным йодом следующие:
— разрушение остаточных тканей железы на фоне накопления радиоактивного йода местастазами в лимфоузлах шеи и легких;
— обеспечение высокой концентрации ТТГ, необходимого для усиления захвата йода тканями опухоли;
— вследствие разрушения любых остаточных тканей щитовидной железы можно использовать уровень тиреоглобулина как достоверный опухолевый маркер.
Также для выявления рецидивов и метастазов при наблюдении за больными с раком щитовидной железы применяют сцинтиграфию всего тела с 131I. В то время как назначение радиоактивного йода при рецидиве или метастазах, подтвержденных сцинтиграфией всего тела, является общепризнанным методом, эффективность и целесообразность применения радиоактивного йода у больных с отрицательными результатами сцинтиграфии и положительными анализами на тиреоглобулин остаются спорным вопросом. Назначение этой терапии может вызвать уменьшение размеров опухоли, но достоверного снижения смертности и частоты осложнений не выявлено. К тому же выраженность побочных эффектов может перевешивать любую пользу от лечения.
Супрессивная гормональная терапия (подавление выработки ТТГ тиреоидными гормонами). Прием левотироксина в качестве дополнительной терапии приводит к снижению частоты рецидивов по сравнению с группой больных, его не получавших [69, 73, 74]. По данным одного исследования, подавление уровня ТТГ до 0,05 мЕ/мл приводит к увеличению продолжительности безрецидивного периода по сравнению с уровнем ТТГ 1 мЕ/мл и более, а степень подавления ТТГ является независимым фактором прогноза рецидивов [75]. Однако пока не существует контролируемых исследований, посвященных определению оптимального уровня подавления ТТГ, соответствующего максимальной выживаемости при минимальных побочных эффектах от длительной супрессивной гормональной терапии.
Псевдодисфункция щитовидной железы
Определение и этиология
Псевдодисфункция щитовидной железы характеризуется нарушением функции щитовидной железы при тяжелых системных заболеваниях в отсутствие ее поражения. Чаще всего к развитию этого состояния приводят поражение гипоталамо-гипофизарной системы, нарушение связывания тиреоидных гормонов с белками плазмы крови, нарушение захвата тиреоидных гормонов в тканях и их метаболизма [76]. Обычно наблюдается снижение концентрации свободного Т3 и повышение концентрации его реверсивной формы, а при более тяжелых и затяжных заболеваниях снижается и уровень Т4, что усугубляет прогноз заболевания. Уровень ТТГ обычно в пределах нормы, но может быть умеренно или даже выражено снижен.
Патофизиология
Хотя механизмы развития патологии до сих пор до конца не изучены, выделяют несколько основных патогенетических факторов, включая снижение превращения Т4 в Т3 в периферических тканях, изменение концентрации белков, связывающих тиреоидные гормоны, снижение выделения ТТГ и ответа на него, низкий захват гормонов в тканях, нарушение метаболизма тиреоидных гормонов и повышение уровня цитокинов.
Диагностика
У больных с острой патологией прежде всего следует исключить заболевание щитовидной железы. При многих внутренних болезнях наблюдаются нарушения функции щитовидной железы, свойственные патологии самой железы. При псевдодисфункции щитовидной железы обычно снижен уровень Т3 на фоне нормальных показателей Т4 и ТТГ. Уровень ТТГ в пределах нормы или умеренно снижен у 80 % больных. Признаком истинного поражения щитовидной железы может быть наличие в анамнезе заболеваний щитовидной железы, внешнего облучения, зоба или обнаружение шрама по срединной линии шеи. Не следует ориентироваться только на однократное исследование функции щитовидной железы [76], лучше дождаться выздоровления или ремиссии, чтобы оценить ее состояние. Определение ТТГ у госпитализированных больных не отличается высокой точностью и дает небольшое число истинно положительных результатов при большем числе ложноположительных результатов [3]. По данным обследования 1580 больных, нарушение показателей ТТГ отмечалось у 17 % больных при поступлении, при последующем наблюдении и повторном измерении ТТГ (после достижения ремиссии основного заболевания) — у 63 % этих больных, при этом в 85 % случаев наблюдалось состояние эутиреоза [6]. Ложноположительные результаты обычно связаны с острыми заболеваниями и приемом лекарственных средств, в частности глюкокортикоидов.
Лечение
Заместительная терапия трийодтиронином. С учетом повышения смертности у больных с тяжелыми системными заболеваниями на фоне низких концентраций Т4 был поставлен вопрос о возможности и эффективности применения заместительной терапии тиреоидными гормонами. По данным одного контролируемого исследования, назначение Т3 больным, подвергшимся операции аортокоронарного шунтирования, привело к улучшению показателей гемодинамики сердца, а также к снижению постоперационной ишемии, необходимости в инотропных препаратах, уровня смертности и продолжительности пребывания в больнице [78]. Однако в другом исследовании эти результаты не нашли подтверждения [79].
|
КЛАССИФИКАЦИЯ ОПЕРАЦИЙ НА ЩИТОВИДНОЙ ЖЕЛЕЗЕ |
|
|
|
|
Комиссаренко И.В., Рыбаков С.И., Болгов М.Ю., Коваленко А.Е., Лысенко А.Г., Чернышев С.В.
Хирургический отдел Инстиута эндокринологии и обмена веществ им.В.П.Комиссаренко АМН Украины, г.Киев
Реферат. Представлена классификация операций на щитовидной железе по объему оставленной ткани, разработанная на основе анализа более чем 2 тысяч операций. Приведено обоснование и характеристика ее рубрик, использование которых позволяет адекватно учитывать объем вмешательства, что особенно важно при автоматизированной обработке больших массивов информации. Summary. The classification of operations on thyroid gland is presented. It is founded on detection of tissue which is left after operations. The main sections of classification are described. The autors consider it convenient and universal in practical work and processing of the large pieces of the information.
Ключевые слова: хирургия - операции на щитовидной железе.
Относительно недавно выделившись в самостоятельную дисциплину, хирургическая эндокринология является одним из прогрессивно развивающихся разделов хирургии. Тиреоидная патология занимает неоспоримое первое место среди оперативных вмешательств на эндокринных органах. Печальную лепту в увеличение количества больных с доброкачественными и злокачественными заболеваниями щитовидной железы в Украине внесла авария на Чернобыльской АЭС [3,6,8]. По данным нашей клиники, количество больных, нуждающихся в оперативном лечении по поводу заболеваний щитовидной железы, продолжает ежегодно расти. Все это объясняет повышенный интерес исследователей к этой проблеме, которая имеет много нерешенных вопросов, требующих дальнейшего изучения. Одним из них является разработка классификации операций на щитовидной железе. Попытка любого анализа результатов хирургического лечения неизбежно сталкивается с необходимостью дифференцированной оценки произведенных оперативных вмешательств. При лечении патологии щитовидной железы это имеет особое значение, так как объем оставленной ткани является одним из ключевых факторов, определяющих тактику послеоперационного ведения и необходимость заместительной терапии тиреоидными гормонами. Предупреждение рецидивов при операциях на щитовидной железе и определение адекватности первичной операции также, одним из основных критериев, включают степень резекции щитовидой железы. Таким образом, необходимость классификации операций на щитовидной железе, отражающей объем вмешательства, представляется очевидной. Обработка больших массивов информации просто немыслима без ее использования. В бывшем СССР вопросы классификации операций на щитовидной железе поднимали ленинградские авторы Е.С. Драчинская и И.С. Брейдо с 60-х годов. В книге “Хирургическое лечение заболеваний щитовидной железы” (1975 г)[2] выделяются следующие их типы: Удаление (экстирпация) щитовидной железы (тиреоидэктомия) Субтотальная резекция щитовидной железы Удаление левой, правой, боковой доли или перешейка Резекция какой либо доли (или долей) щитовидной железы Энуклеация узла (или узлов) с частичной резекцией доли Энуклеация узла (или узлов) При этом отмечается, что в практической деятельности часто используются сочетания этих основных типов, а все особенности, включая объем оставленной ткани отражаются дополнительно. Подобную классификацию приводит А.А.Нарычев при описании методик хирургического лечения заболеваний щитовидной железы (1971 г.)[5]. Работ, целенаправленно посвященных этому вопросу, в известной литературе нам найти не удалось. Иностранные авторы при описании операций на щитовидной железе используют градацию тиреоидэктомия-гемитиреоидэктомия-резекция [9,10,11,12]. Мы обратили внимание на важность рациональной классификации вмешательств на щитовидной железе при внедрении автоматизации ведения историй болезни, о чем уже сообщали [4]. Настоящая статья подводит итог исследований в этом направлении. Не предполагая принципиальной новизны, мы, напротив, старались учесть весь имеющийся опыт и существующие среди хирургов определения, видя своей целью свести их к единому и однозначно толкуемому перечню, пригодному для использования как в повседневной клинической деятельности, так и при последующем научном анализе накопленного опыта. Материалом для анализа послужили более 2 тысяч историй болезни пациентов, оперированных в клинике на щитовидной железе по поводу различных заболеваний и занесенных в базу данных. В течении последних трех лет мы неоднократно адаптировали имеющиеся данные к различным классификационным подходам, что стало возможным благодаря внедрению автоматизации ведения историй болезни [1]. Прежде всего необходимо остановиться на некоторых неоднозначных терминах, которые использовались и используются при наименовании операций на щитовидной железе. Одним из них является так называемая "расширенная резекция щитовидной железы" при узловых формах зоба. Данный термин подразумевает широкий захват здоровой ткани вокруг узлов. Такая методика выступает альтернативой энуклеации узлов, которая не обеспечивает необходимой степени радикальности и, поэтому, в настоящще время находит все меньше и меньше приверженцев. Однако, этот термин, как видно из его характеристики, отражая методику проведения операции, никак не отражает ее объем, который может быть как минимальным, так и составляющим более половины железы. Это обстоятельство заставило нас отказаться от использования названия "расширенная резекция" в классификации. Вместе с тем, любую резекцию доли мы выполняем по методике расширенной резекции в пределах здоровых тканей. Иными словами, так как все резекции являются расширенными, указание этого обстоятельства в наименовании операции теряет информационную ценность и может быть опущено. Термин “экономная резекция”, который продолжает еще употребляться, не выдерживает критики по тем же соображениям, что и “расширенная резекция”. Кроме того, он отражает менее радикальную тактику, что служит основанием к отказу от его использования. Еще одним широко используемым наименованием является "субтотальная резекция щитовидной железы". Среди хирургов он ассоциируется в основном с лечением тиреотоксического зоба. В контексте же объема резекции, этот термин подразумевает оставление “площадок” ткани (культей), рекомендуемый размер которых чаще всего составляет от 2 до 6 г. По методике О.В.Николаева они формируются на боковых поверхностях трахеи, по Е.С.Драчинской - в области верхних полюсов. Мы считаем, что понятие субтотальной резекции вполне может использоваться для отражения объема, если его не связывать только с лечением тиреотоксического зоба. Собственно техника операций при этой патологии безусловно имеет свои особенности, но, относительно объема оставляемой ткани, название “Субтотальная резекция щитовидной железы” вполне адекватно для операций, при которых послеоперационный объем культей щитовидной железы составляет около 5 г, что соответствует 1/3 веса нормальной доли. Наиболее целесообразным представляется классифицировать операции на щитовидной железе по объему оставленной ткани. При этом объем удаленной может быть весьма различным, информацию о чем должен содержать диагноз (в частности степень для доброкачественного зоба и TNM для злокачественных опухолей). Хотя некоторые наименования исторически тесно связаны с характером патологии, при котором они производятся, этот факт не должен доминировать. Для отражения заболевания и всех его особенностей служит диагноз, а названия операций на щитовидной железе рационально поставить в соответствие объему вмешательства. При этом избранные градации должны, равномерно распределяясь по объему оставленной ткани, иметь практическое клиническое значение. Приводим разработанную классификацию и описание ее рубрик.
Классификация операций на щитовидной железе по объему оставляемой ткани* Тиреоидэктомия Предельно субтотальная резекция щитовидной железы Субтотальная резекция щитовидной железы Гемитиреоидэктомия и субтотальная резекция контралатеральной доли Гемитиреоидэктомия и резекция контралатеральной доли Гемитиреоидэктомия Резекция обеих долей щитовидной железы Субтотальная резекция доли щитовидной железы Резекция доли щитовидной железы Удаление перешейка щитовидной железы (истмусэктомия) Вскрытие абсцесса щитовидной железы Открытая биопсия щитовидной железы * Удаление перешейка и пирамидальной доли производится при любом виде вмешательства кроме вскрытия абсцесса и открытой биопсии. Практическое использование указанных рубрик требует указания стороны (для несимметричных операций) и объема шейной диссекции (для операций при раке щитовидной железы).
Тиреоидэктомия. Данное вмешательство подразумевает удаление всей щитовидной железы. Технически это может быть выполнено экстра- и субфасциально. Выполнение первого типа вмешательства более опасно в связи с риском повреждения паращитовидных желез и возвратных гортанных нервов, однако обеспечивает необходимую онкологическую радикальность и возможность проведения радиойодной диагностики и лечения при высокодифференцированных карциномах. Напротив, при лечении доброкачественного многоузлового или рецидивного зоба нет необходимости тщательного удаления всей ткани щитовидной железы. В таких ситуациях обычно хирург стремится оставить макроскопически неизмененную ткань, если таковая имеется, а при необходимости тиреоидэктомии она выполняется субфасциально, как и при лечении хронических тиреоидитов. С точки зрения объема оставляемой ткани и последующей функции тиреоидэктомия остается операцией, при которой удаляется вся щитовидная железа. В практической деятельности используется еще термин “Окончательная тиреоидэктомия”, отражающий повторное вмешательство, необходимое после нерадикальных операций при раке щитовидной железы. Предельно субтотальная резекция щитовидной железы. Объем этой операции находится между субтотальной резекцией, при которой оставляются культи ткани около 5 г с каждой стороны и тиреоидэктомией, когда макроскопически определяемой ткани нет. Чаще всего такая ситуация возникает при многоузловых зобах с почти полным поражением щитовидной железы. В этом случае, когда у хирурга нет оснований предполагать озлокачествление, там, где это возможно, оставляются, минимальные кусочки ткани на капсуле железы (их размер обычно не превышает 0,5 см). Субтотальная резекция щитовидной железы. По объему вмешательства этот тип операции подразумевает формирование культей с общим объемом около 10 г (обычно две по 5). Безусловно, большинство субтотальных резекций производятся при диффузном тиреотоксическом зобе, но это не аксиома. Так, например, наличие злокачественной опухоли или многоузловое поражение могут послужить основанием к выполнению тиреоидэктомии при тиреотоксикозе, а иногда субтотальный объем резекции необходим при эутиреоидных формах зоба. Гемитиреоидэктомия. Собственно гемитиреоидэктомия тоже может быть выполнена по экстра- или субфасциальной методике, но в подавляющем большинстве оказывается субфасциальной, так как экстрафасциальное ее проведение не может иметь смысла ввиду наличия противоположной доли. Редким исключением являются ситуации, когда, из-за невозможности окончательно подтвердить или опровергнуть наличие злокачественного роста во время операции, приходится допускать возможность повторного вмешательства (окончательной тиреоидэктомии). Тогда при выполнении гемитиреоидэктомии ее совершают экстрафасциально. На практике же оказывается, что сам факт наличия злокачественного процесса обычно выясняется при получении результата экспресс-гистологического анализа, то есть после проведения гемитиреоидэктомии, а значит тип ее определяется дооперационной настроенностью хирурга. Так или иначе, относительно объема оставляемой ткани, эти операции могут считаться идентичными. Гемитиреоидэктомия и субтотальная резекция контралатеральной доли. Как следует из названия этот термин соответствует полному удалению одной доли и резекции противоположной с оставлением около 5 г ткани железы, что соответствует половинному объему субтотальной резекции. Гемитиреоидэктомия и резекция контралатеральной доли. В отличие от предыдущего типа вмешательства, в данном случае подразумевается удаление меньшего количества ткани контралатеральной доли. Следуя логике он должен быть более 5 г. Резекция обеих долей щитовидной железы. Обычно эта операция выполняется при наличии доброкачественных узлов в обеих долях, когда с обеих сторон хирург оставляет более 5 г (1/3 нормального объема доли). Субтотальная резекция доли щитовидной железы. Результатом этой операции (на одной доле) является оставление с одной стороны культи около 5 г. Резекция доли щитовидной железы. Как менее обширное вмешательство на одной доле щитовидной железы, этот тип операции обозначает, что объем оставленой ткани превышает 5 г. Удаление перешейка щитовидной железы. Эта операция выделена как самостоятельная единица для тех случаев, когда только в перешейке определяется небольшой узел и объем резекции каждой из долей не превышает 1/3 (5 г). Вскрытие абсцесса щитовидной железы и открытая биопсия приведены для полноты описания возможных вмешательств и не являются предметом дискуссии. Приведенная классификация, как и любая классификация вообще, конечно не может учесть всех возможных особенностей, но должна позволять, в данном случае, любую операцию однозначно отнести в ту или иную группу. Кроме того, что важно для автоматизированной обработки, смешение типов является плохой практикой, тогда как дополнение к основному наименованию операции позволяет отразить все необходимые детали. Но компьютерная обработка такого (произвольной формы) дополнения весьма проблематична. Именно поэтому основные типы вмешательств на щитовидной железе должны быть представлены рубриками. Использование нашей классификации делает наименование операции одним из содержательных критериев при проведении аналитических исследований. |
Классификация заболеваний щитовидной железы Синдром гипертиреоза (тиреотоксикоза)
1. Гипертиреоз, обусловленный повышенной продукцией гормонов щитовидной железы: 1.1. диффузный токсический зоб (ДТЗ, болезнь Грейвса, Базедова болезнь) 1.2. узловой (многоузловой) токсический зоб, токсическая аденома 1.3. йод-индуцированный гипертиреоз 1.4. гипертиреоидная фаза аутоиммунного тиреоидита 1.5. ТТГ-обусловленный гипертиреоз 1.5.1. ТТГ-продуцирующая аденома гипофиза 1.5.2. синдром неадекватной секреции ТТГ (резистентность тиреотрофов к гормонам щитовидной железы 1.6. трофобластический гипертиреоз 2. Гипертиреоз, обусловленный продукцией тиреоидных гормонов вне щитовидной железы: 2.1. struma ovarii 2.2. метастазы рака щитовидной железы, продуцирующие тиреоидные гормоны 3. Тиреотоксикоз, не связанный с гиперпродукцией гормонов щитовидной железы: 3.1. медикаментозный тиреотоксикоз (передозировка препаратов гормонов щитовидной железы) 3.2. тиреотоксикоз как стадия подострого тиреоидита де Кервена 3.3. тиреотоксикоз вследствии повышенной чувствительности тканей к гормонам щитовидной железы
Синдром гипотиреоза
1. Первичный гипотиреоз: 1.1. гипотиреоз, обусловленный уменьшением количества функционирующей ткани щитовидной железы 1.1.1. гипотиреоз,обусловленный нарушением эмбрионального развития щитовидной железы (врожденный гипотиреоз) 1.1.2. послеоперационный гипотиреоз 1.1.3. пострадиоционный гипотиреоз 1.1.4. гипотиреоз, обусловленный аутоиммунным поражением щитовидной железы (атрофическая форма аутоиммунноготиреоидита исход диффузно-токсического зоба в гипотиреоз) 1.1.5. гипотиреоз, обусловленный вирусным поражением щитовидной железы 1.1.6. гипотиреоз, на фоне новообразований щитовидной железы 1.2.гипотиреоз, обусловленный нарушением синтеза гормонов щитовидной железы: 1.2.1. эндемический зоб с гипотиреозом 1.2.2. спорадический зоб с гипотиреозом (дефекты биосинтеза гормонов щитовидной железы) 1.2.3. медикаментозный гипотиреоз (прем тиреостатиков и ряда других препаратов) 1.2.4. зоб и гипотиреоз, развившиеся в результате потребления пищи, содержащей зобогенные вещества 2. Гипотиреоз центрального генеза: 2.1. гипотиреоз гипофизарного генеза (вторичный) 2.2. гипотиреоз гипоталамическогогенеза (третичный) 3. Гипотиреоз вследствии нарушения транспорта, метаболизма и действия гормонов щитовидной железы (периферический)
Заболевания щитовидной железы, протекающие без нарушения ее функции
1. Эутиреоидный зоб: 1.1. зоб, обусловленный нарушением синтеза гормонов щитовидной железы 1.1.1. эндемический зоб (диффузный, узловой) 1.1.2. спорадический зоб (диффузный, узловой) 1.1.3. ятрогенный (медикаментозный) зоб 1.1.4. зоб, обусловленный зобогенными веществами, содержащимися в пище 2. Тиреоидная неоплазия 2.1.доброкачественные опухоли щитовидной железы 2.1.1. аденома 2.1.2. тератома 2.2. злокачественные опухоли 2.2.1. папиллярная кацинома 2.2.2. фолликулярная карцинома 2.2.3. медулярная карцинома недифферинцируемая карцинома 2.2.5. другие злокачественные опухоли щитовидной железы (саркома, лимфома, эпидермоидная карцинома) 3. Тиреоидиты: 3.1. острый 3.1.1. гнойный 3.1.2. не гнойный 3.2. подострый (вирусный, де Кервена) 3.3. хронические 3.3.1. аутоиммунный тиреоидит 3.3.2. инвазивный фиброзный тиреоидит 3.3.3. скрытый (безболевой) тиреоидит
Классификация заболеваний щитовидной железы.
20 мая, 2011 Просмотров: 1 313
Щитовидная железа
Комментариев нет
Общей классификации заболеваний щитовидной железы нет. Наиболее простой принцип, который мог бы лечь в основу такой классификации — функциональный (синдромальный), т.е. в зависимости от функции щитовидной железы (гипертиреоз, гипотиреоз, эутиреоз). Вариант такой классификации можно представить ниже. Но перед этим лучше рассмотреть ряд терминологических вопросов.
Под термином тиреотоксикоз подразумевается клинический синдром, обусловленный избытком тиреоидных гормонов в организме, при этом патогенетически он подразделяется на три варианта:
-
Гипертиреоз — гиперпродукция тиреоидных гормонов щитовидной железы.
-
Деструктивный (тиреолитический) тиреотоксикоз, который представляет собой патологическую реакцию щитовидной железы на ряд внешних и внутренних факторов, заключающуюся в массированном разрушении тиреоидных фолликулов с выходом их содержимого (гормонов) в кровеносное русло. При этом варианте гиперфункция щитовидной железы отсутствует. Заболевания, протекающие с деструктивным тиреотоксикозом, например подострый и послеродовый тиреоидиты, сопровождаются значительно менее выраженным тиреотоксикозом, чем обусловленные гиперфункцией щитовидной железы (болезнь Грейвса). Кроме того, они, как правило, имеют хороший прогноз.
-
Медикаментозный тиреотоксикоз, связанный с передозировкой препаратов тиреоидных гормонов.
Теперь собственно функциональная (синдромальная) классификация заболеваний щитовидной железы
Синдром тиреотоксикоза
-
Тиреотоксикоз, обусловленный повышенной продукцией гормонов щитовидной железы
-
Болезнь Грейвса
-
Многоузловой токсический зоб
-
-
Тиреотоксикоз, обусловленный продукцией тиреоидных гормонов вне щитовидной железы (хорионэпителиома, struma ovarii).
-
Тиреотоксикоз, не связанный с гиперпродукцией гормонов щитовидной железы
-
Медикаментозный тиреотоксикоз
-
Тиреотоксическая фаза деструктивных тиреоидитов (подострый, послеродовый)
-
Синдром гипотиреоза (снижение продукции гормонов)
-
Первичный гипотиреоз
-
Гипотиреоз центрального генеза (вторичный)
-
Нарушение транспорта, метаболизма и действия тиреоидных гормонов
Заболевания щитовидной железы, протекающие без нарушения функции
-
Эутиреоидный зоб
-
Зоб, обусловленный нарушением синтеза тиреоидных гормонов
-
Зоб, обусловленный зобогенными веществами
-
-
Тиреоидная неоплазия
-
Доброкачественные опухоли
-
Злокачественные опухоли
-
-
Тиреоидиты
Недостаточность щитовидной железы подразделяется на первичную и вторичную. Под первичным гипотиреозом подразумевают дефицит тиреоидных гормонов в организме, обусловленный патологией (разрушением, удалением) самой щитовидной железы, а под вторичным гипотиреозом — дефицит тиреоидных гормонов, обусловленный снижением (отсутствием) трофических и секреторных эффектов ТТГ на щитовидной железы (гипоталамо-гипофизарный гипотиреоз).
Под зобом (струмой) подразумевается увеличение объема щитовидной железы выше установленных норм для женщин — 18 мл, для мужчин — 25 мл. По макроскопической характеристике он подразделяется на диффузный (увеличена вся щитовидная железа), узловой, многоузловой (два и более узловых образования) и смешанный (сочетание общего увеличения щитовидной железы с наличием одного или нескольких узловых образований). По функциональному состоянию щитовидной железы зоб бывает эутиреоидным, токсическим и протекающим со снижением функции щитовидной железы.
Несмотря на всю простоту и логику функциональной классификации заболеваний щитовидной железы , она имеет ряд недостатков. Основной из них заключается в том, что при большинстве заболеваний функция щитовидной железы не является постоянной. Это относится ко всем заболеваниям щитовидной железы, протекающим с деструктивным тиреотоксикозом. При хроническом аутоиммунном тиреоидите той или иной длительности эутиреоидная фаза может закончиться субклиническим, а затем явным гипотиреозом. При многоузловом зобе в регионах йодного дефицита по мере нарастания функциональной автономии тироцитов эутиреоз постепенно сменяется тиреотоксикозом. В связи с этим, в настоящее время целесообразнее подразделять заболевания щитовидной железы в зависимости от их этиологии.
Наиболее часто формированию зоба способствуют различные зобогенные факторы, самым распространенным среди которых является дефицит поступления йода в организм. Здесь следует отметить уникальную особенность тиреоидной патологии в целом: спектр, распространенность и прогноз большинства заболеваний щитовидной железы будет во многом зависеть о того, в регионе с каким потреблением йода (недостаточным, нормальным, избыточным) проживает пациент.
Этиологическая классификация заболеваний щитовидной железы
