
- •Нет однозначного ответа
- •Нужны дополнительные сведения
- •Нет однозначного ответа
- •Нет однозначного ответа
- •Нет однозначного ответа
- •Вещества, в молекулах которых содержатся гидрофильные и гидрофобные группы
- •Нельзя дать ответ.
- •Нельзя дать ответ.
- •Железо;
- •Нет однозначного ответа.
- •Нужны дополнительные сведения.
Для стоматологов Первый уровень
Модуль 1
1. В состав молекулы хлорофилла в качестве металла – комплексообразователя входит:
-
Магний.
-
Цинк.
-
Молибден.
-
Хром.
-
Железо.
-
5% - ный раствор глюкозы означает:
-
5 г глюкозы находится в 100 г раствора;
-
5 молей глюкозы находится в литре раствора;
-
5 г глюкозы находится в литре раствора;
-
5 г глюкозы находится в 100 г воды;
-
5 г глюкозы находится в 1000 г воды;
-
Основным минеральным компонентом костной ткани является:
-
Са3(РО4)5ОН
-
Ва3(РО4)3ОН
-
NaCI.
-
CaSO4 2H2O.
-
BaSO4 2H2O.
-
Какой элемент образует прочную ковалентную связь?
-
Углерод;
-
Железо;
-
Хлор;
-
Натрий;
-
Медь
-
Какую концентрацию ионов гидроксида имеет раствор гидроксида калия с концентрацией 0,2 моль/л?
-
0,2 моль/л;
-
0,4 моль/л;
-
2 моль/л;
-
4 моль/л
-
20 моль/л
-
Что такое алкалоз?
-
сдвиг рН крови в щелочную сторону;
-
потенциальная кислотность;
-
нейтральная реакция среды;
-
сдвиг рН крови в кислую сторону.
-
общая кислотность
-
Что такое ацидоз?
-
сдвиг рН крови в кислую сторону;
-
нейтральная реакция среды;
-
потенциальная кислотность;
-
сдвиг рН крови в щелочную сторону.
-
общая кислотность
-
Что такое осмос?
-
Односторонняя диффузия молекул растворителя через полупроницаемую мембрану в сторону более концентрированного раствора
-
Односторонняя диффузия молекул растворителя через полупроницаемую мембрану в сторону более разбавленного раствора
-
Односторонняя диффузия молекул растворенного вещества через полупроницаемую мембрану в сторону более концентрированного раствора
-
Односторонняя диффузия молекул растворенного вещества через полупроницаемую мембрану в сторону менее концентрированного раствора
-
Диффузия растворенного вещества
-
Из приведенных смесей выберите ту, что обладает буферным действием:
-
HHb + KHb.
-
CH3COOH + CH3COONH4.
-
HCl + NH4Cl
-
HNO3 + NaNO3.
-
NaOH + NaCl.
-
Назовите буферную систему организма, состоящую из двух кислых солей:
-
Фосфатный буфер.
-
Гидрокарбонатный буфер.
-
Аммиачный буфер.
-
Белковый буфер.
-
Ацетатный буфер.
-
Укажите состав оксигемоглобинового буфера:
-
HHbO2 + KHbO2.
-
CH3COOH + CH3COONa.
-
NH4OH + NH4Cl.
-
HHb + KHb.
-
NaH2PO4 + Na2HPO4.
-
Соединения, в составе которых существуют биогенные d- элементы в организме, относятся классу:
-
Комплексных соединений.
-
Оснований.
-
Кислот.
-
Оксидов.
-
Простых веществ.
-
Чему равно онкотическое давление крови в норме?
-
3,5-3,9 кПа
-
2,9-3,5 кПа
-
4-4,5 кПа
-
5-5,5 кПа
-
5,5-5,9 кПа
-
Плазмолиз происходит вследствие:
-
Движения молекул воды из клетки
-
Движения внутриклеточных ионов из клетки
-
Движения воды в клетку
-
Движения внеклеточных ионов в клетку
-
Двустороннего движения молекул воды
-
Какой элемент принимает участие в образование макроэргических связей:
-
Р
-
CI.
-
S.
-
H.
-
N.
-
Какой элемент участвует в синтезе гормона щитовидной железы – тироксина и является его незаменимым структурным компонентом?
-
Йод.
-
Сера.
-
Калий.
-
Кальций.
-
Хлор.
-
В состав витамина В12 в корриновом кольце находится:
-
Кобальт.
-
Железо.
-
Никель.
-
Медь.
-
Хром.
-
Укажите общую кислотность желудочного сока в титриметрических единицах, в норме:
-
40 – 60;
-
15 – 25;
-
25 – 38;
-
68 – 70;
-
70 – 72.
-
Известно, что для определения кислотности желудочного сока можно использовать объемный метод. Какой из приведенных растворов является рабочим в данном случае?
-
раствор едкого натра;
-
раствор щавелевой кислоты;
-
раствор серной кислоты.
-
раствор соляной кислоты;
-
раствор уксусной кислоты
-
Какое значение рН имеет кровь:
-
7,35 – 7,45;
-
6,35 – 6,85;
-
1,5 – 3,0;
-
7,5 – 8,0;
-
5,8 – 6,8.
-
Укажите условия, которые характеризуют понятие «гипертонический раствор» относительно крови:
-
раствора 0,9 % NaCl;
-
раствора = 0,9 % NaCl;
-
раствора 4,5 % глюкозы;
-
Р раствора= 780 кПа
-
Изоэлектрическая точка (ИЭТ) аминокислот наблюдается когда:
-
Количества
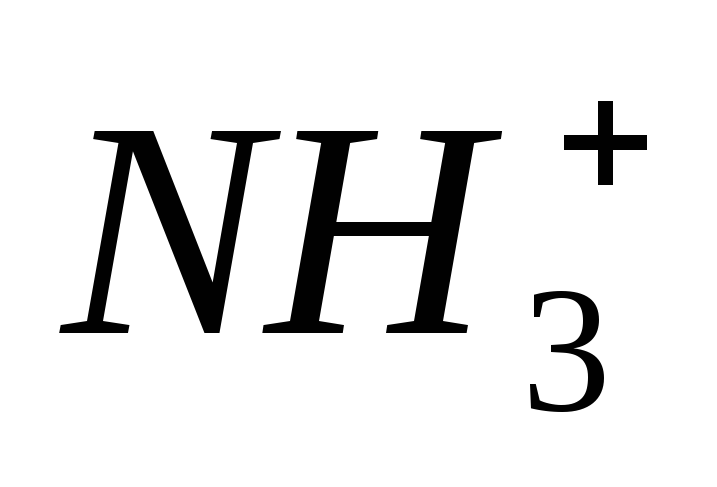 и
и
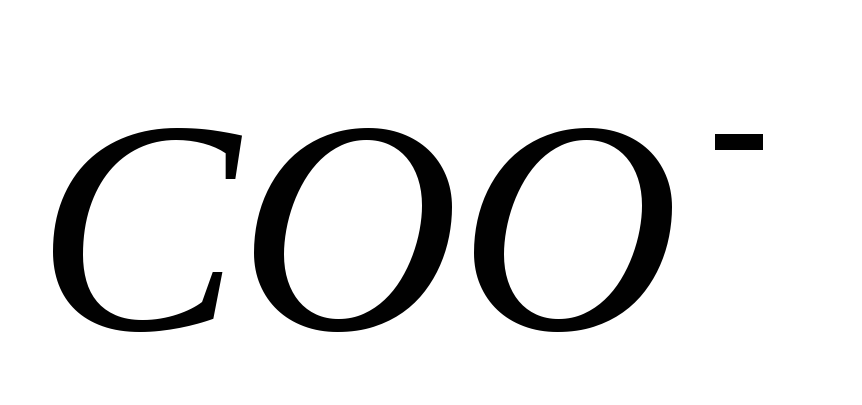 -групп
равны.
-групп
равны.
-
Количество групп
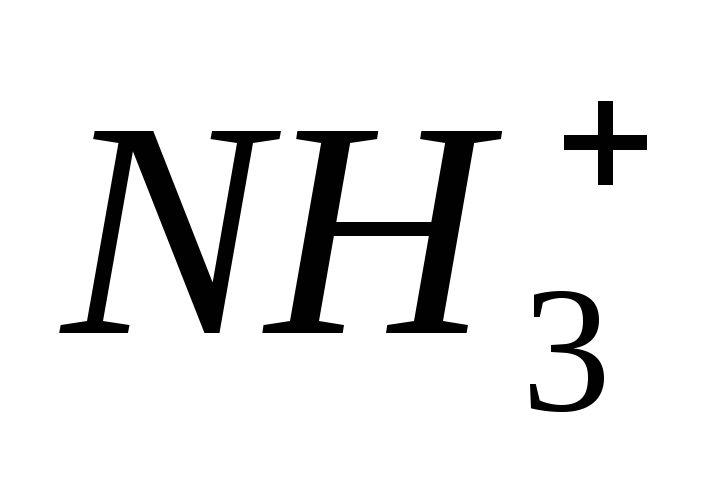 >
>
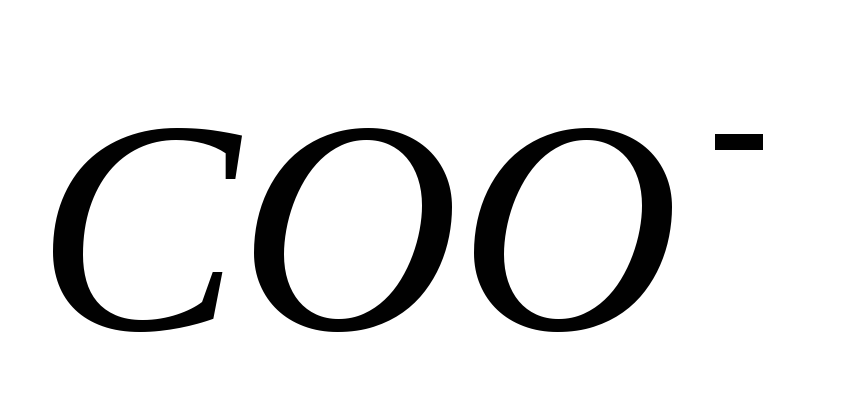 .
. -
Количество групп
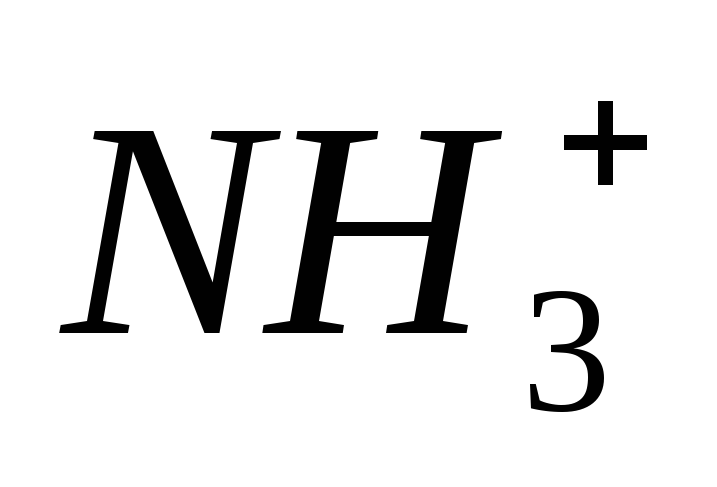 <
<
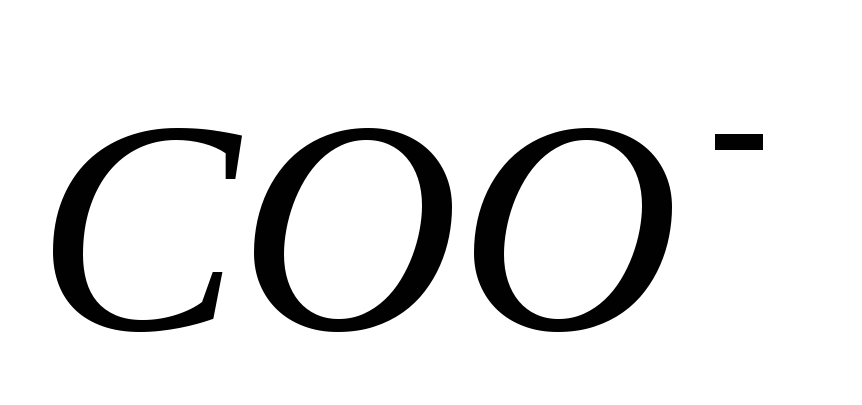 .
.
-
Количество ионов
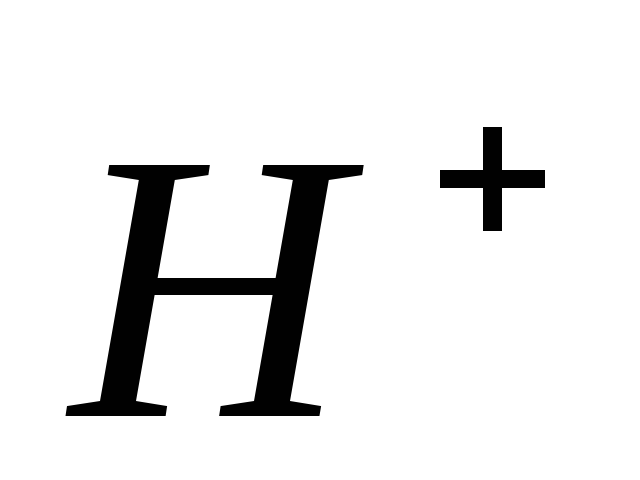 >
>
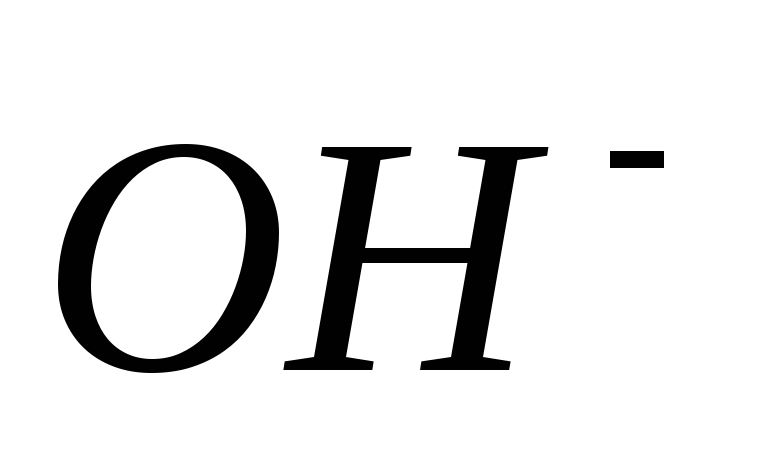 .
. -
Нет однозначного ответа
-
Что происходит с эритроцитом при помещении его в воду ?
-
Гемолиз;
-
Ничего не происходит;
-
Плазмолиз;
-
Нельзя дать ответ.
-
Нужны дополнительные сведения
-
Какова процентная концентрация раствора NaCl изотоничного крови?
-
0,85-0,9%
-
0,75-0,8%
-
0,8-0,85%
-
0,7-0,75%
-
1-1,2%
-
Гемолиз происходит при помещении эритроцитов в:
-
Гипотонический раствор
-
Гипертонический раствор
-
Физиологический раствор
-
Изотонический раствор
-
5% раствор глюкозы
-
Координационное число комплексообразователя в гемоглобине равно:
-
6 ;
-
4;
-
5;
-
2.
-
3
-
Укажите значение рН, в котором раствор более щелочной:
-
рН = 11;
-
рН = 5;
-
рН = 1;
-
рН = 7;
-
рН = 3
-
Алкалоз – это смещение кислотно-основного равновесия крови в направлении:
-
понижения
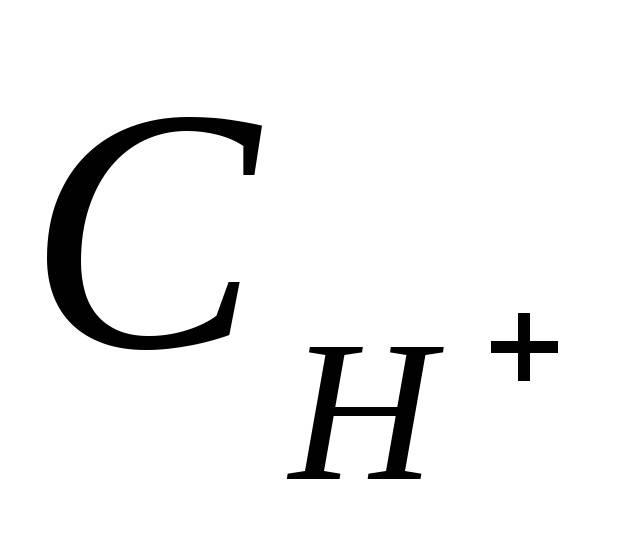 ;
;
-
повышения
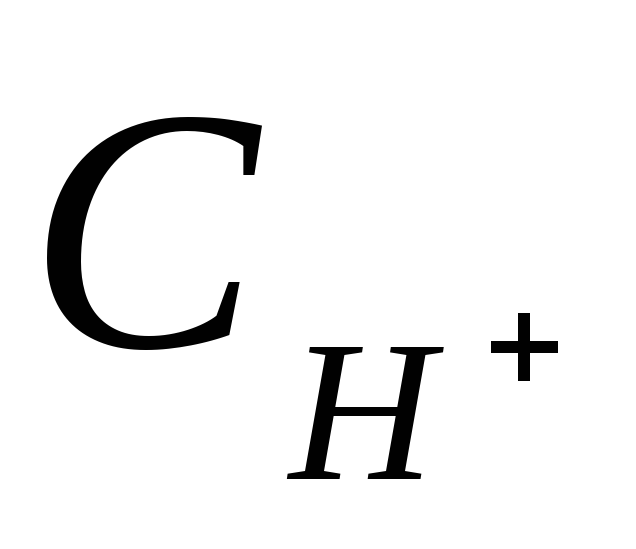 ;
;
-
уменьшения рН.
-
понижения СОН-
-
Нет однозначного ответа
-
Для коррекции кислотно-основного равновесия крови при ацидозе рекомендуют раствор:
-
NaHCO3
-
HCl
-
глюкозы
-
NaCl
-
уксусной кислоты
-
С наличием каких функциональных групп связан механизм буферного действия аминокислот:
-
Групп: -NH2 и -СООН.
-
Групп: -ОН и -СН3.
-
Групп: -SH и -СН3.
-
Гетероциклического кольца.
-
Бензольного кольца.
-
Смещение кислотно-основного равновесия крови в направлении снижения рН называют:
-
ацидозом
-
алкалозом
-
анабиозом
-
Из приведенных буферных смесей укажите буферную систему организма:
-
H2CO3 + NaHCO3.
-
NH4OH + NH4Cl.
-
H3BO3 + NaOH.
-
KH2PO4 + NaOH.
-
CH3COOH + CH3COONa.
-
Какова процентная концентрация раствора глюкозы, изотоничного крови?
-
3-3,5%
-
4-4,5%
-
4,5-5%
-
5,5-6%
-
6,5-7%
-
Что следует применять для промывания гнойных ран?
-
Гипертонические растворы
-
Гипотонические растворы
-
Изотонические растворы
-
Физиологические растворы
-
Дистиллированную воду
-
Плазмолиз происходит при помещении клетки в:
-
Гипертонический раствор
-
Гипотонический раствор
-
Физиологический раствор
-
Изотонический раствор
-
Дистиллированную воду
-
Электролиты классифицируются на сильные и слабые по:
-
степени диссоциации;
-
по растворимости;
-
по ионной силе раствора;
-
по активности
-
по рН
-
Укажите значение рН, в котором раствор более кислый:
-
рН = 1;
-
рН = 5;
-
рН = 3;
-
рН = 7;
-
рН = 11
-
Что является мерой активной кислотности среды?
-
рН
-
рКд
-
Р Kw
-
Kд
-
С
-
Укажите активную кислотность желудочного сока в титриметрических единицах, в норме:
-
20 – 40;
-
42 – 45;
-
12 – 17;
-
5 – 10;
-
45 – 50.
-
Что происходит с эритроцитом при помещении его в 0,7% раствор NаСl ?
-
Гемолиз;
-
Ничего не происходит;
-
Плазмолиз;
-
Нельзя дать ответ
-
Нет однозначного ответа
-
Какую концентрацию ионов водорода имеет раствор соляной кислоты с концентрацией 0,1моль/л?
-
0,1 моль/л;
-
1 моль/л;
-
2 моль/л;
-
0,2 моль/л
-
10 моль/л
-
Какие растворы называются изотоническими?
-
Растворы с равными осмотическими давлениями
-
Растворы с разными осмотическими давлениями
-
Растворы, содержащие одно и то же растворенное вещество
-
Растворы, имеющие одинаковые процентные концентрации разных растворенных веществ
-
Растворы, имеющие одинаковые моляльные концентрации разных растворенных веществ
-
Чему равен рН желудочного сока в норме ?
-
1,5 – 3,0;
-
0,2 – 1,5;
-
3,0 – 4,0;
-
4,0 – 5,0;
-
8,0 – 9,0
-
Буферные системы обладают свойством достаточно стойко сохранять постоянство:
-
Концентрации ионов водорода.
-
Концентрации ионов натрия.
-
Концентрации молекул углекислого газа.
-
Концентрации кислорода.
-
Концентрации ионов аммония.
-
Какой из приведенных растворов является буферной системой организма:
-
NаНСО3 + Н2СО3;
-
NаН2РО4 + (NН4)НРО4;
-
Nа2НРО4 + КН2РО4;
-
NН4НSО4 + Nа2НРО4.
-
CH3COOH + CH3COONa
-
Из приведенных буферных смесей укажите гидрокарбонатный буфер:
-
H2CO3 + NaHCO3.
-
CH3COOH + CH3COONa.
-
NH4OH + NH4Cl.
-
NaH2PO4 + Na2HPO4.
-
NH4OH + NaHCO3
-
Указать значение рН для случая «пониженной кислотности» желудочного сока:
-
3,5 – 4,5
-
1,5 – 3,0
-
1,0 – 1,5
-
2,0 – 2,5
-
рН=7
-
Константа нестойкости комплексних ионов составляет ниже приведенные значения. Укажите какой комплексный ион будет наиболее устойчив?
